Termodinamika Gas Ideal
Diunggah oleh
Dhevy Murti0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
24 tayangan7 halamanTermodinamika gas ideal dapat dijelaskan secara statistik dengan menggunakan fungsi partisi. Fungsi partisi merupakan jumlah dari semua kemungkinan status kuantum bagi suatu sistem. Dengan menggunakan fungsi partisi, hubungan antara tekanan, volume, dan temperatur pada gas ideal dapat diturunkan. Azas ekipartisi energi menyatakan bahwa energi rata-rata disumbangkan secara sama oleh energi kinetik dan potensial
Deskripsi Asli:
Hak Cipta
© © All Rights Reserved
Format Tersedia
PPTX, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniTermodinamika gas ideal dapat dijelaskan secara statistik dengan menggunakan fungsi partisi. Fungsi partisi merupakan jumlah dari semua kemungkinan status kuantum bagi suatu sistem. Dengan menggunakan fungsi partisi, hubungan antara tekanan, volume, dan temperatur pada gas ideal dapat diturunkan. Azas ekipartisi energi menyatakan bahwa energi rata-rata disumbangkan secara sama oleh energi kinetik dan potensial
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PPTX, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
24 tayangan7 halamanTermodinamika Gas Ideal
Diunggah oleh
Dhevy MurtiTermodinamika gas ideal dapat dijelaskan secara statistik dengan menggunakan fungsi partisi. Fungsi partisi merupakan jumlah dari semua kemungkinan status kuantum bagi suatu sistem. Dengan menggunakan fungsi partisi, hubungan antara tekanan, volume, dan temperatur pada gas ideal dapat diturunkan. Azas ekipartisi energi menyatakan bahwa energi rata-rata disumbangkan secara sama oleh energi kinetik dan potensial
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PPTX, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 7
B.
Termodinamika Gas ideal dalam Ungkapan
Statistik
•• Hukum termodinamika lazimnya dituliskan untuk besaran terukur pada
skala makroskopik. Misalnya, pada energi internal keseluruhan .
• Besaran-besaran fisika nampaknya terkait secara linier dengan dengan
ln(). Maka kita menggunakan fungsi partisi Z = , sehingga ln(Z) = ().
• Atom-atom yang jumlahnya N diberi nomor 1 sampai N sebagai nomor
atom dan masing-masing atom punya indeks status kuantum-nya.
Untuk membedakan, nomor atom akan ditulis di antara tanda kurung.
• Jadi energi atom nomor-j yang berada pada status ke-i akan ditulis
sebagai (j).
• Fungsi Partisi dapat dituliskan sebagai:
• Jika
jumlah atomnya 2 dan jumlah status
kuantumnya 3, maka dapat ditulis lengkap Z
sebagai:
• Jika terdiri atas 2 atom, masing-masing dengan
3 status kuantum, maka E dapat ditulis dengan
dua indeks, dan untuk menunjukkan status
kuantum. Artinya .Sehingga,
• Artinya,
Kumpulan atom sejumlah N memiliki
energi total E, yang nilainya bergantung pada
status kuantum masing-masing atom. Pilihan
status kuantum bebas tapi tidak bergantung pada
pilihan status kuantum untuk atom lainnya.
• Fungsi partisi adalah jumlah eksponen [,...] untuk
semua nilai (,....) yang tersedia. Jadi, kita
membuat ruang-U yang dimensinya 6N, atau
dinamakan ruang-, atau ruang-fase.
• Setiap kotak dalam ruang-fase melukiskan kondisi
kumpulan atom dengan indeks status (,....),
dimana energi terkait yang besarnya .
• Energi
internal kumpulan atom kita mestinya
juga dapat dinyatakan sebagai:
• Pada kasus gas ideal fungsi partisi Z bergantung
juga pada volume V. Jika tulisan indeks (,....)
disingkat menjadi r, maka perubahan V sebanyak
+dV akan mengubah sebanyak:
• Perubahan tersebut adalah kerja yang dilakukan
oleh gas. Jadi dapat diasosiasikan dengan:
•• di mana p adalah tekanan. Jika itu diterapkan maka,
• dinyatakan dengan Z
• Jadi,
• berarti tekanan gas ideal dapat diperoleh dengan,
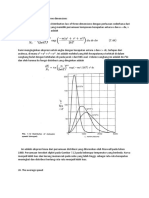
• Nilai Z yang telah dihitung, yaitu:
• Jika persamaan tersebut di atas diterapkan maka akan didapat:
• Dan kita peroleh hubungan yang sudah dikenal
3. Azas Ekipartisi Energi
•• untuk osilator harmonik fungsi Hamiltonnya
• Untuk osilator harmonik fungsi Hamiltoniannya
+
• Tapi kita dapat menuliskan fungsi Hamilton tersebut menjadi jumlah
dari fungsi Hamilton yang masing-masing hanya mengandung satu
variabel saja. Jadi untuk gas ideal kita dapat menuliskan
dengan , ,
• untuk zat padat kita dapat menuliskan dengan , ,
• Masing-masing dari sampai punya bentuk yang sama.
•• Ketika kita membuat hitungan fungsi partisi atom kita menggunakan
rumus yang sama, yaitu
• yang hasil integrasinya hanya bergantung pada konstanta a. Jadi pada
gas ideal masing-masing koordinat menyumbang nilai integral yang
sama. Ketika kita menghitung energi rata-ratanya, konstanta yang
mengandung massa partikel tidak muncul lagi. Energi rata-rata yang
diperoleh merupakan jumlah dari sumbangan 3 variabel koordinat,
sehingga energi rata-ratanya .
• Pada kasus zat padat gerak harmonik energinya disumbangkan dari
energi kinetik dan energi potensial dan masing-masing menyumbang
• Artinya energi rata-rata disumbangkan dalam jumlah yang sama dari
energi kinetik maupun oleh energi potensial, yaitu . Itulah yang
dijadikan semacam asas sumbangan yang sama atau azas ekipartisi
energi.
Anda mungkin juga menyukai
- Toaz - Info Vibrasi Kisi Dalam Kristal PRDokumen12 halamanToaz - Info Vibrasi Kisi Dalam Kristal PRsayyafpatoBelum ada peringkat
- Fistat Kel 6-Dikonversi-DikompresiDokumen18 halamanFistat Kel 6-Dikonversi-DikompresiAzaaBelum ada peringkat
- Vibrasi Kisi Dalam KristalDokumen12 halamanVibrasi Kisi Dalam Kristalwidyaiswari100% (2)
- Kapasitas Kalor KristalDokumen10 halamanKapasitas Kalor KristalZaenal T. ArifinBelum ada peringkat
- PEMICU 2 Bagian Hana 2,6,9Dokumen13 halamanPEMICU 2 Bagian Hana 2,6,9Hana Safira YudantiBelum ada peringkat
- Aplikasi Statistik Bose Einstein Teori Einstein Kapasitas Panas Zat PadatDokumen10 halamanAplikasi Statistik Bose Einstein Teori Einstein Kapasitas Panas Zat PadatAfdatul ZikriBelum ada peringkat
- Jawaban 1 & 10Dokumen6 halamanJawaban 1 & 10BadzlinaKhairunizzahraBelum ada peringkat
- CBR Gaya SentralDokumen26 halamanCBR Gaya SentralRahmaNasutionBelum ada peringkat
- Energi Rata-Rata PartikelDokumen17 halamanEnergi Rata-Rata PartikelDimas Fadili RohmanBelum ada peringkat
- Mutiara Dier - Aplikasi Maxwell Boztman Kapasitas Panas Spesifik Zat PadatDokumen10 halamanMutiara Dier - Aplikasi Maxwell Boztman Kapasitas Panas Spesifik Zat PadatMutiara DierBelum ada peringkat
- Group CDokumen21 halamanGroup CMei Dita AsriBelum ada peringkat
- Tugas 8Dokumen27 halamanTugas 8Hamda shoufi nadiahBelum ada peringkat
- BAB I Termo Pemicu 2 FixDokumen28 halamanBAB I Termo Pemicu 2 FixIrma PrihartiniBelum ada peringkat
- Kimia Dasar IDokumen60 halamanKimia Dasar IEkho Virgho GeminiBelum ada peringkat
- Kapasitas Panas Dan Konsep FononDokumen12 halamanKapasitas Panas Dan Konsep FononKartika Andria PertiwiBelum ada peringkat
- Entropi Dan Bobot StatistikDokumen16 halamanEntropi Dan Bobot StatistikJeliana Veronika Sirait100% (2)
- Pert 2. STRUKTUR ATOMDokumen26 halamanPert 2. STRUKTUR ATOMYusup SetiawanBelum ada peringkat
- PropertyDokumen16 halamanPropertyMetalwing Skyterror Azaazil100% (1)
- Kapsel StoikiometriDokumen16 halamanKapsel StoikiometriyunitaBelum ada peringkat
- Fisika IntiDokumen6 halamanFisika IntiSinta ParameswariBelum ada peringkat
- Rangkuman Struktur Inti Dan RadioaktivitasDokumen5 halamanRangkuman Struktur Inti Dan RadioaktivitasWinda AgustinaBelum ada peringkat
- Kerapatan IntiDokumen14 halamanKerapatan Intiritasilabannatalie100% (1)
- Contoh Soal Relasi Termo-Statistik AwalDokumen1 halamanContoh Soal Relasi Termo-Statistik AwalArdiana Ilham NurrohmanBelum ada peringkat
- Tugas Fungsi PartisiDokumen15 halamanTugas Fungsi Partisidewi asaningsihBelum ada peringkat
- Teori Elektron BebasDokumen27 halamanTeori Elektron BebasFatinBelum ada peringkat
- Sistem Dengan Komposisi BervariasiDokumen29 halamanSistem Dengan Komposisi BervariasiAprizalBelum ada peringkat
- Ensembel KanonikDokumen15 halamanEnsembel KanonikDwie Koerniawan0% (2)
- Atom HidrogenDokumen29 halamanAtom HidrogenEva MeutiaBelum ada peringkat
- Kimfis Translate BukuDokumen4 halamanKimfis Translate BukuadhelaBelum ada peringkat
- Thermal FononDokumen32 halamanThermal FononSatria Auffa Dhiya UlhaqueBelum ada peringkat
- Persamaan KeadaanDokumen13 halamanPersamaan KeadaanKomang SuardikaBelum ada peringkat
- Putri Ramadhani - Tugas Resume Fismod Teori Atom HidrogenDokumen9 halamanPutri Ramadhani - Tugas Resume Fismod Teori Atom Hidrogenputri ramadhaniBelum ada peringkat
- Makalah KimiaDokumen8 halamanMakalah KimiaAhlul NazriBelum ada peringkat
- Sifat Thermal Zat Padat KristalDokumen18 halamanSifat Thermal Zat Padat KristalmalikBelum ada peringkat
- Fisika Modern Kelompok 5Dokumen15 halamanFisika Modern Kelompok 5Mirdan0063PEND.FISIKA ABelum ada peringkat
- Tugas Kelompok Fisika Inti Bab 2 Subbab 2Dokumen30 halamanTugas Kelompok Fisika Inti Bab 2 Subbab 2Bimantara YudaBelum ada peringkat
- Osilator Linear TerkuantisasiDokumen9 halamanOsilator Linear TerkuantisasiInnes AndrianiBelum ada peringkat
- Dinamika Kristal 2Dokumen64 halamanDinamika Kristal 2immaammBelum ada peringkat
- Pert 1 Struktur - Dan - Sifat - IntiDokumen26 halamanPert 1 Struktur - Dan - Sifat - IntiYusmanila HanahBelum ada peringkat
- Aisyah Luthfi Wardani - 10-RESUME PENGANTAR FISIKA STATISTIKDokumen5 halamanAisyah Luthfi Wardani - 10-RESUME PENGANTAR FISIKA STATISTIKAisyah LuthfiBelum ada peringkat
- Makalah Statistik Maxwell BoltzmanDokumen14 halamanMakalah Statistik Maxwell Boltzmannurrahmah syahrir50% (2)
- Kel 10 Fisika Statistika Fungsi Partisi Dan Energi BebasDokumen14 halamanKel 10 Fisika Statistika Fungsi Partisi Dan Energi Bebassurya k hutabaratBelum ada peringkat
- Paper KFL FixDokumen48 halamanPaper KFL FixNur MultiawatiBelum ada peringkat
- HandBook UAS Kimia Dasar IADokumen25 halamanHandBook UAS Kimia Dasar IASalman HanifBelum ada peringkat
- Pelatihan Olimpiade Termodinamika Dan Fisika StatistikDokumen2 halamanPelatihan Olimpiade Termodinamika Dan Fisika StatistikTIARA SABRINA IVADABelum ada peringkat
- Pelatihan Olimpiade Termodinamika Dan Fisika Statisti - HIMAFI ITERADokumen2 halamanPelatihan Olimpiade Termodinamika Dan Fisika Statisti - HIMAFI ITERATIARA SABRINA IVADABelum ada peringkat
- Phonons II. Ciri-Ciri Thermal FixDokumen28 halamanPhonons II. Ciri-Ciri Thermal FixIMade Oka Guna AntaraBelum ada peringkat
- Teori Model Debye (Kapasitas Kalor Zadat)Dokumen12 halamanTeori Model Debye (Kapasitas Kalor Zadat)UmiKasanahBelum ada peringkat
- Tugas IntiDokumen7 halamanTugas IntiFebsen DenastaBelum ada peringkat
- Resume Jurnal Kuantum A Nonlinier ShrodingerDokumen9 halamanResume Jurnal Kuantum A Nonlinier ShrodingerNiLuhLindAyuBelum ada peringkat
- Model Tetesan CairanDokumen8 halamanModel Tetesan CairanKiki Ayu ManizzBelum ada peringkat
- Inti AtomDokumen13 halamanInti AtomMeiniaBelum ada peringkat
- Bobot Statistik Dan Contoh PerhiotungannyaDokumen5 halamanBobot Statistik Dan Contoh PerhiotungannyaArko Alfathar TumanggorBelum ada peringkat
- 14-Model Atom Mekanika KuantumDokumen5 halaman14-Model Atom Mekanika KuantumMaida KhoirinaBelum ada peringkat
- Tugas FisikaDokumen10 halamanTugas FisikaNovi Kurnianta Karina BintangBelum ada peringkat