Annissa Fauzia Hasqa Anhbal - Tugas 1 - B
Diunggah oleh
Annissa Fauzia Hasqa Anhbal0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
6 tayangan1 halamanJudul Asli
05201017_Annissa Fauzia Hasqa Anhbal_Tugas 1_B (1)
Hak Cipta
© © All Rights Reserved
Format Tersedia
PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
6 tayangan1 halamanAnnissa Fauzia Hasqa Anhbal - Tugas 1 - B
Diunggah oleh
Annissa Fauzia Hasqa AnhbalHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 1
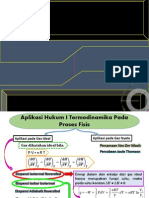
Entalpi (H)/ Heat content Nama Kelompok
Entalpi dipakai untuk Pengukuran Perubahan Entalpi
perubahan-perubahan pada Annisa Fauzia Hasqa Anhbal - 05201017
1. Perubahan entalpi mengikuti perubahan kimia
tekanan tetap H = U + PV dan Fitriani Jaya Saputra - 05201032 dan fisika.
PV hanya tergantung keadaan Shalma Rachmawati - 05201083 2. Diukur dengan kalorimeter
awal dan akhir sistem. a. kalorimeter api bertekanan tetap d'H = q
b. kalorimeter bom, pada volume tetap, melelui d'U dimana d'U=q
c. untuk reaksi yang tidak menghasilkan gas d'H = d'U
d. Untuk reaksi yang menghasilkan gas
Besarnya perubahan entalpi dari sistem H = U + PV = U +nRT
H2 –H1 = d'H
d'H = d'U + d'(PV) = d'U + d'n gas RT
(U2 + P2V2) - (U1 + P1V1) = d'H
dengan d'n = n gas produk = n gas reaktan
(U2-U1) + (P2V2 - P1V1) = d'H
HUKUM TERMODINAMIKA 1 e. Besarnya perubahan entalpi pada tekanan konstan setara dengan panas yang
pada P tetap
diserap.
d'U + P(V2-V1) = d'H
d'U + P d'V = d'H "Dalam sebuah sistem tertutup, perubahan
energi dalam sistem tersebut akan sama
Perubahan Energi pada Berbagai Keadaan
dengan banyaknya kalor yang masuk ke 1. Perubahan energi pada volume konstan dV = 0
Jika dihubungkan dengan hukum dalam sistem dikurangi usaha yang dilakukan dW = - PdV =0
termodinamika pertama pada oleh sistem tersebut." dUv = dqV
tekanan tetap berlalu q = d'H atau
d' U = qv ; terjadi kalorimeter bom
2. Perubahan energi pada tekanan konstan dP = 0
Apa Itu Entalpi ? Entalpi adalah jumlah energi yang
dimiliki oleh sebuah sistem termodinamika sebagai Secara Sistematis dapat dituliskan
contoh dalam reaksi kimia perubahan entalpi sistem
adalah panas reaksi. Dalam perubahan fasa dari cair ke dU = dq + dw
gas, perubahan entalpi sistem adalah panas laten
penguapan. Secara sederhana perubahan suhu,
d'U = q + w
perubahan entalpi dengan masing - masing derajat
adalah kapasitas panas sistem pada tekanan konstan. U2 - U1 = qp - p(V2 - V1)
Fisikawan Jerman Rudolf J. E. Clausius (U2 + PV2) - (U1 + PV1) =qp
Dengan kata lain, perubahan H2 - H1 = qp
energi dalam sistem (U) setara d'H = qp
dengan panas yang diberikan
pada sistem (q) dan kerja yang
Secara matematis, entalpi H diidentifikasi sebagai U +PV , dilakukan terhadap sistem (w)
dimana U adalah energi internal, P adalah tekanan, dan V
adalah Volume. H diukur dengan joule atau Unit Termal Inggris
(BTU).
ENCARTA 2007
Jika Hanya diberikan panas, berlaku
d'U = q
Jika hanya dilakukan kerja berlaku
d'U = W
Anda mungkin juga menyukai
- Hukum Termod Nol Dan Pertama 09Dokumen26 halamanHukum Termod Nol Dan Pertama 09anita sukarini100% (1)
- Hukum Termod Nol Dan Pertama 09Dokumen26 halamanHukum Termod Nol Dan Pertama 09yudhaBelum ada peringkat
- Lecture - Note - No. - 2 - Konsep - Dasar - Hukum - I - Thermodinamika (New Version)Dokumen8 halamanLecture - Note - No. - 2 - Konsep - Dasar - Hukum - I - Thermodinamika (New Version)andro sihombingBelum ada peringkat
- MATERI 2A. Hukum Termodinamika I MetalurgiDokumen12 halamanMATERI 2A. Hukum Termodinamika I Metalurgirajadwaa daffaBelum ada peringkat
- Pertemuan 4Dokumen84 halamanPertemuan 403Ahmad Risqiansyah PurwantoBelum ada peringkat
- 2 Hukum Termodinamika 1 RevisiDokumen28 halaman2 Hukum Termodinamika 1 RevisiMusyarrofBelum ada peringkat
- Pertemuan 5 - Energi Dalam, Termokimia, Dan Kapasitas KalorDokumen19 halamanPertemuan 5 - Energi Dalam, Termokimia, Dan Kapasitas KalorSabilaria TisaBelum ada peringkat
- Lecture 4 (Thermo I) (w#6)Dokumen28 halamanLecture 4 (Thermo I) (w#6)Indri AnisaBelum ada peringkat
- Energetika Kimia Dan Wujud ZatDokumen29 halamanEnergetika Kimia Dan Wujud ZatRina septiyaBelum ada peringkat
- EnergetikaDokumen38 halamanEnergetikaputriBelum ada peringkat
- HK Pertama Termodinamika SajaDokumen19 halamanHK Pertama Termodinamika Sajafarqimkajian2Belum ada peringkat
- Termodinamika Kel 1Dokumen24 halamanTermodinamika Kel 1IraBelum ada peringkat
- Pertemuan 5-6Dokumen23 halamanPertemuan 5-6M RamadanaBelum ada peringkat
- Kelompok 5. Energi Internal, Transaksi Kerja Kalor & EntalpiDokumen11 halamanKelompok 5. Energi Internal, Transaksi Kerja Kalor & EntalpiMochamad Rifli Al RahmanBelum ada peringkat
- Tugas 3 - Resume Hukum 1 TermodinamikaDokumen10 halamanTugas 3 - Resume Hukum 1 TermodinamikaIndah PuspitaBelum ada peringkat
- TermodinamikaDokumen68 halamanTermodinamikaJihan ZaniraBelum ada peringkat
- Hukum TermodinamikaDokumen22 halamanHukum TermodinamikahighynitaBelum ada peringkat
- Hukum 1 TermodinamikaDokumen10 halamanHukum 1 Termodinamikaputri rahmaBelum ada peringkat
- TermodinamikaDokumen8 halamanTermodinamikaYihuuBelum ada peringkat
- 71 - 80, Thermodinamika, Noverio Suwartono, 22321021Dokumen17 halaman71 - 80, Thermodinamika, Noverio Suwartono, 22321021noverio suwartonoBelum ada peringkat
- 6 Hukum-Termodinamika-I TM3Dokumen16 halaman6 Hukum-Termodinamika-I TM3Lutfiah BerliantiBelum ada peringkat
- Ringkasan Bab Kimia Fisik Bab 14Dokumen2 halamanRingkasan Bab Kimia Fisik Bab 14antonia putriBelum ada peringkat
- Hukum Pertama Termodinamika (Autosaved)Dokumen64 halamanHukum Pertama Termodinamika (Autosaved)Supia SianaBelum ada peringkat
- Termodinamika: Pertemuan 4 Dan 5Dokumen30 halamanTermodinamika: Pertemuan 4 Dan 5Ricard AbieBelum ada peringkat
- TermodinamikaDokumen33 halamanTermodinamikaAnis Nadhira0% (2)
- Pertemuan 2 KF 2Dokumen21 halamanPertemuan 2 KF 2RamaBelum ada peringkat
- Materi Tambahan Termodinamika1Dokumen12 halamanMateri Tambahan Termodinamika1Kamil HidayatBelum ada peringkat
- TermodinamikaDokumen29 halamanTermodinamika13putrirahmaBelum ada peringkat
- Termodinamika PDFDokumen0 halamanTermodinamika PDFIbnu HamdunBelum ada peringkat
- Rizka Fitriana Ayundari - Materi Hukum I TermodinamikaDokumen10 halamanRizka Fitriana Ayundari - Materi Hukum I TermodinamikaRizka Fitriana ABelum ada peringkat
- Kelompok 14-Aplikasi HK 1 TermodinamikaDokumen10 halamanKelompok 14-Aplikasi HK 1 TermodinamikaRatih NoviyantiBelum ada peringkat
- Termodinamika Kimia HK 1Dokumen26 halamanTermodinamika Kimia HK 1lidyaBelum ada peringkat
- Kimia Kapasitas Panas Dan Hukum I Termodinamika (Proses Fisis)Dokumen3 halamanKimia Kapasitas Panas Dan Hukum I Termodinamika (Proses Fisis)IrmairmairmaBelum ada peringkat
- Materi Tambahan Termodinamika1Dokumen12 halamanMateri Tambahan Termodinamika1Kamil HidayatBelum ada peringkat
- Bab 5 - Proses Reversibel Gas Nyata Dan Ideal Tanpa AliranDokumen27 halamanBab 5 - Proses Reversibel Gas Nyata Dan Ideal Tanpa AliranAngelina FebrianaBelum ada peringkat
- Hukum I, II Dan III TermodinamikaDokumen53 halamanHukum I, II Dan III TermodinamikaCirry Suciati UtamiBelum ada peringkat
- Makalah Farmasi Fisika IDokumen44 halamanMakalah Farmasi Fisika IarguarBelum ada peringkat
- Makalah Entalpi Hukum 2 Termodinamika enDokumen7 halamanMakalah Entalpi Hukum 2 Termodinamika enJumi PermatasyariBelum ada peringkat
- Kimia Hukum 1 Termodinamika BaruDokumen15 halamanKimia Hukum 1 Termodinamika BaruNur AzizahBelum ada peringkat
- Hukum 1 TermodinamikaDokumen22 halamanHukum 1 TermodinamikaEka WiranathaBelum ada peringkat
- Tugas KimfisDokumen32 halamanTugas KimfisAndikageorgiaBelum ada peringkat
- Konsep Hukum 1 TermodinamikaDokumen6 halamanKonsep Hukum 1 TermodinamikaAlfiya RahmaBelum ada peringkat
- Materi Tambahan TermodinamikaDokumen20 halamanMateri Tambahan TermodinamikaKamil HidayatBelum ada peringkat
- B2-Termodinamika Dan Perpindahan Panas 2Dokumen16 halamanB2-Termodinamika Dan Perpindahan Panas 2Brasilia Septya AyuBelum ada peringkat
- Materi Tambahan TermodinamikaDokumen20 halamanMateri Tambahan TermodinamikaKamil HidayatBelum ada peringkat
- Tugas Kimia Fisika Bu AuliaDokumen8 halamanTugas Kimia Fisika Bu AuliaMuhammad HarisBelum ada peringkat
- RPP 3.12 JunDokumen22 halamanRPP 3.12 JunJun Hidayat100% (2)
- TermodinamikaDokumen33 halamanTermodinamikaLukman HakimBelum ada peringkat
- Energetika 1Dokumen23 halamanEnergetika 1AzuraEarthlings Exo-lBelum ada peringkat
- Mekanika Fluida 4Dokumen13 halamanMekanika Fluida 4Hermawan -Belum ada peringkat
- Hukum I TermodinamikaDokumen12 halamanHukum I TermodinamikaOktaviani SurbaktiBelum ada peringkat
- EnergetikaDokumen33 halamanEnergetikaSeptiaBelum ada peringkat
- Bab 2 (Lanjutan Materi)Dokumen18 halamanBab 2 (Lanjutan Materi)sitiBelum ada peringkat
- Hukum Pertama TermodinamikaDokumen25 halamanHukum Pertama TermodinamikaAhmad NawwaafBelum ada peringkat
- Hukum I TermodinamikaDokumen14 halamanHukum I TermodinamikaMuhammad RipandiBelum ada peringkat
- Resume Kimfis UTSDokumen17 halamanResume Kimfis UTSElok FaikhatulBelum ada peringkat
- Termodinamika: Pertemuan 4 Dan 5Dokumen77 halamanTermodinamika: Pertemuan 4 Dan 5Ricard AbieBelum ada peringkat
- TermodinamikaDokumen53 halamanTermodinamikaolpi olaBelum ada peringkat