Bab 3 Laju Reaksi
Diunggah oleh
Annisa RuwaidaJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Bab 3 Laju Reaksi
Diunggah oleh
Annisa RuwaidaHak Cipta:
Format Tersedia
Bab 3 Laju Reaksi
LAJU REAKSI
Setelah mempelajari Laju Reaksi diharapkan siswa dapat :
1. Menjelaskan pengertian kemolaran dan penggunaannya
2. Menuliskan ungkapan laju reaksi ( v )
3. Menjelaskan persamaan laju reaksi dan tingkat reaksi serta penentuannya
4. Menentukan orde reaksi berdasarkan data hasil eksperimen
5. Menjelaskan faktor-faktor yang mempengaruhi laju reaksi
6. Menjelaskan peranan katalisator dan energi pengaktifan dalam teori tumbukan
7. Menerapkan peranan laju reaksi dalam industri.
1. Kemolaran /Konsentrasi (M )
n
M = ---- n = mol zat terlarut
V V = volume larutan ( L )
%x x 10 = massa jenis
M = ------------------ % = kadar larutan
Mr Mr = massa molekul
Pengenceran Larutan
1 = keadaan sebelum pengenceran
2 = keadaan setelah pengenceran
V1M1 = V2M2 V = volume larutan
M = molaritas larutan
Molaritas Campuran
V1M1 + V2M2
M campuran = ------------------
V1 + V2
Contoh Soal :
1. Hitunglah kemolaran dari :
a. 12 gram asam cuka,CH3COOH (60 gram/mol) dilarutkan dlm air sehingga
volumenya 500 mL.
b. Asam klorida pekat ( 36,5 gram/mol ) kadar 36,5 % massa jenis 1,19 gram/mL.
Jawab :
a. M CH3COOH = x = 0,4Molar
b. M HCl = = 11,9 Molar
2. Tersedia asam sulfat pekat (98gr/mol) berkadar 18% massa jenis 1,8 gr/mL, sebanyak
2 mL asam sulfat pekat diencerkan dengan air sehingga volumenya 1000 mL . Kemudian
diambil 100 mL dicampur dengan 100 mL asam sulfat 0,1 M . Hitunglah molaritas
campuran asam tersebut !
Jawab :
98 x 1,8 x 10
M H2SO4 pekat ( M1 ) = ------------------- = 18 M
98
V1M1 = V2M2 2 .18 = 1000 . M2
M2 = 0,036 (M2 dianggap M1 pada pencampuran )
V1M1 + V2M2
M camp = ------------------
V1 + V2
100. 0,036 + 100 . 0,1
= ------------------------------- = 0,068 Molar
100 + 100
LKS Kimia Kelas X1 MAN Kupang
Bab 3 Laju Reaksi
LKS Non Eksperimen
Nama
Kelas
Kemolaran ( M )
1. Tuliskan rumus kemolaran suatu larutan !
2. Hitunglah kemolaran larutan berikut !
a. 7,4 gram Ca(OH)2 dilarutkan dalam air sehingga volumenya 2 L. ( Ca=40,)=16,H=1 ).
b. 100 mL HCl 0,1 M dicampur dengan 200 mL HCl 0,1 M
3. Asam sulfat pekat mengandung 98% massa H2SO4 ( H=1, S=32, O=16 ) dan massa jenis 1,8
gr/mL .
a. Hitunglah kemolaran asam sulfat tersebut !
b. Berapa mL asam ini yang diperlukan untuk membuat 500 mL larutan H2SO4 0,1 M ?
4. Kedalam 500 mL larutan NaCl 0,1 M dimasukkan 58,5 gram NaCl dan air sehingga volumenya
menjadi 1 Liter. Hitunglah kemolaran sekarang ! ( Na=23, Cl=35,5 )
5. Sebanyak 24,6 gram MgSO4.7H2O dilarutkan dalam air dan volum larutan tepat 500 mL.
a. Hitunglah kemolaran larutan itu ! ( Mg=24, S=32, O=16, H=1 )
b. Sebanyak 10 mL diambil dalam gelas kimia. Berapa kemolaran larutan dalam gelas kimia ?
c. Hitunglah massa MgSO4 dalam 10 mL larutan itu !
d. Hitunglah mL air yang harus ditambah kedalam 100 mL larutan itu sehingga molaritasnya
menjadi 0,1 M !
6. 4 gram NaOH ( 40gr/mol ) dilarutkan dalam air sehingga volumenya 400 mL dicampur dengan
600 mL Ca(OH)2 0,2 M.
Hitunglah :
a. kemolaran campuran NaOH dan Ca(OH)2
b. massa Ca(OH)2 ( 74gr/mol ) dalam larutan 600 mL Ca(OH)2 0,2 M
Diperiksa pada tanggal Parap Guru
2. Pengertian dan Ungkapan Laju Reaksi
a. Pengertian Laju Reaksi
[Na]
P
R P
t (waktu)
Jika R adalah zat pereaksi (Reaktan) dan P zat produk, maka Laju reaksi adalah perubahan
konsentrasi zat pereaksi dan konsentrasi zat produk per satuan waktu. Berarti konsentrasi zat
pereaksi (R) makin berkurang dan konsentrasi zat produk (P) makin bertambah tiap satuan
waktu.
Satuan laju reaksi Molar per satuan waktu, karena umumnya reaksi kimia berlangsung
dalam detik maka satuan laju reaksi adalah Molar/dt ( M/dt ).
b. Ungkapan Laju Reaksi
R P
[ R ] [ P ]
v = - -------- atau v = + --------
t t
Keterangan :
tanda + berarti konsentrasi P makin bertambah persatuan waktu.
Tanda - berarti konsentrasi R makin berkurang persatuan waktu.
LKS Kimia Kelas X1 MAN Kupang
Bab 3 Laju Reaksi
Misalnya :
1. Pembentukan gas N2O5 menurut reaksi : 4NO2(g) + O2(g) 2N2O5 (g)
Tentukan perbandingan VNO2 , VO2 ,VN2O5
Jawab :
V=- =- =+
VNO2 = VO2 = VN2O5
VNO2 : VO2 : VN2O5 = 4 : 1 : 2
2. Pada penguraian 0,1 M gas amonia terbentuk 0,01 M gas nitrogen setiap 10 detik
menurut reaksi :
2 NH3(g) N2(g) + 3 H2(g) .
Tentukan :
a. Laju pembentukan N2(g)
b. Laju penguraian NH3(g)
c. laju pembentukan H2(g)
Jawab :
VNH3 = VN2 = VH2
a. VN2 = 0,01 M/ 10 dt = 0,001 M/dt
b. VNH3 = 2VN2 = 2. 0,001 M/dt = 0,002 M/dt
c. VH2 = 3VN2 = 3. 0,001 M/dt = 0,003 M/dt
LKS Non Eksperimen
Nama
Kelas
Pengertian dan Ungkapan Laju Reaksi
1. Jelaskan pengertian laju reaksi !
2. Jika zat pereaksi A, dan zat hasil B menurut reaksi : A B
a. Bagaimana pengertian laju reaksinya !
b. Tuliskan persamaan ungkapan laju reaksinya !
3. Untuk reaksi : 2 SO2 (g) + O2 (g) 2 SO3 (g)
a. Tuliskan ungkapan laju reaksi untuk SO2, O2 , SO3 dengan VSO2,VO2,VSO3 !
b. Bagaimana hubungan antara VSO2 denganVO2 maupun denganVSO3 !
4. Untuk reaksi : 2 SO2 (g) + O2 (g) 2 SO3 (g)
Pada P dan T tertentu laju pembentukan SO 3 sebesar 5,0 x 10-3 M/dt. Hitunglah laju
berkurangnya SO2 dan O2 !
5. Sebanyak 2,4 gram pita Mg ( Mg=24 ) dilarutkan dalam larutan HCl berlebihan. Reaksi
selesai dalam 20 detik. Nyatakan laju rata-rata reaksi dalam mol/dt !
6. Kedalam 1 L wadah dimasukkan x mol gas P, y mol gas Q. Setelah t detik sebagaian
membentuk z mol gas R, menurut reaksi : P (g) + 2 Q (g) 3 R (g). Nyatakan laju reaksi
rata-rata gas P, Q dan R !
7. Sejumlah serbuk pualam , CaCO3 direaksikan ke dalam larutan asam klorida berlebihan.
Volume gas CO2 yang terbentuk dicatat menurut tabel di bawah ini :
Waktu ( menit ) 0 1 2 3 4 5 6 7
Volume CO2 ( mL ) 0 10 18 24 28 30 30 30
a. Berapakah volume CO2 yang terbentuk pada menit ke-1 ?
b. Berapakah laju rata-rata reaksi selama menit ke-1 dan ke-2 ?
c. Berapa menitkah reaksi selesai ?
d. Berapakah laju rata-rata reaksi tersebut ?
e. Buatlah grafik reaksi tersebut !
Diperiksa pada tanggal Parap Guru
LKS Kimia Kelas X1 MAN Kupang
Bab 3 Laju Reaksi
3. Faktor-faktor yang mempengaruhi laju reaksi
1. Luas Permukaan Sentuh
Jika a gram serbuk logam A dan a gram keping zat B karena zat A mempunyai luas
permukaan sentuh lebih besar dari zat B. Bila zat A dan zat B direaksikan dengan 100 mL
larutan HCl 0,1 M maka laju reaksi zat A lebih cepat dari zat B. Mengapa ?
2. Konsentrasi Pereaksi
Sebanyak a gram logam besi direaksikan dengan 100 mL larutan H2SO4 0,1 M dan 100 mL
larutan H2SO4 0,2 M maka besi akan lebih cepat bereaksi dengan 100 mL larutan H2SO4 0,2
M. Mengapa demikian ?
3. Suhu
Logam Mg direaksikan dengan 100 mL larutan H 2SO4 0,1 M pada suhu 20oC dan 100 mL
larutan H2SO4 0,1 M pada suhu 30 oC, reaksi akan lebih cepat pada suhu 30 oC. Hal ini karena
pada suhu 30oC energi kinetik partikel-partikelnya lebih besar dari semula sehingga molekul-
molekulnya telah memiliki energi aktivasi ( Ea = energi minimum untuk dapat
melangsungkan reaksi ) yang berakibat laju reaksi lebih cepat. Pada umumnya setiap
kenaikan 10 oC laju reaksi dua kali lebih cepat. Semakin tinggi suhu semakin banyak molekul
yang mencapai energi aktifasi.
Contoh :
a. Suatu reaksi berlangsung 8 detik pada suhu 25 oC dan setiap kenaikan 10 oC laju reaksi
dua kali lebih cepat. Tentukan kecepatan reaksi pada suhu 55 oC.
b. Pada suhu 60oC laju reaksi berlangsung 27 x 10 -2 M/dt dan setiap kenaikan 10 oC laju
reaksi tiga kali lebih cepat. Tentukan laju reaksi pada suhu 20 oC.
Jawab :
a.
Suhu 25oC 35oC 45oC 55oC
Waktu (dt) 8 4 2 1
b.
Suhu 60oC 50oC 40oC 30oC 20 oC
Laju Reaksi
(M/dt) 27x10-2 9x10-2 3x10-2 1x10-2 0,33x10-2
4. Tekanan
Tekanan diperbesar berarti volume mengecil yang mengakibatkan konsentrasi senyawa
bertambah maka laju reaksi bertambah.
5. Katalisator
Katalis merupakan zat yang mempercepat reaksi, karena katalis akan menurunkan energi
aktifasi reaksi yang berlangsung sehingga laju reaksi akan bertambah cepat.
E E
Ea
R
P
Ea
P R
R. Eksoterm Reaksi Endoterm Waktu
= tanpa katalis
= dengan katalis
Faktor-faktor yang mempengaruhi laju reaksi
1. Sebutkan faktor-faktor yang mempengaruhi laju reaksi !
2. Jelaskan mengapa konsentrasi larutan dapat mempengaruhi laju reaksi !
3. Mengapa zat yang berbentuk serbuk lebih cepat laju reaksinya dari zat yeng berbentuk kristal!
4. Jelaskan mengapa pada reaksi pembentukan amonia menurut proses Haber-Bosch lebih optimal
pada suhu 500oC ,reaksi ini digunakan katalis serbuk besi !
Reaksinya :
N2 (g) + 3 H2 (g) 2 NH3 (g) H = - 92 kJ
5. Jelaskan pengaruh katalis pada laju reaksi !
LKS Kimia Kelas X1 MAN Kupang
Bab 3 Laju Reaksi
6. Suatu reaksi berlangsung dua kali lebih cepat setiap kenaikan suhu 10oC. Jika laju reaksi pada
suhu 20 oC adalah 8 M/dt. Hitunglah laju reaksi pada suhu 50 oC !
7. Suatu reaksi berlangsung tiga kali lebih cepat setiap kenaikan suhu 10oC. Jika laju reaksi pada
suhu 25 oC adalah 4 menit. Tentukan laju reaksi pada suhu 55 oC !
Diperiksa pada tanggal Parap Guru
4. Persamaan Laju Reaksi
pA + q B r C + s D
Maka persamaan laju reaksi dapat ditulis :
V = laju reaksi dalam M/dt
V = k Ax By k = tetapan laju reaksi
x = orde/tingkat reaksi terhadap A
y = orde/tingkat reaksi terhadap B
x dan y dicari dari data eksperimen
Contoh :
1. Pada reaksi : 2 P + Q P2Q diperoleh data sebagai berikut :
NO. [ P ] (M) [ Q ] (M) Laju Reaksi (V)
(M/dt)
1 0,1 0,1 0,1
2 0,1 0,2 0,2
3 0,2 0,2 0,4
Tentukanlah orde reaksi total dan persamaan laju reaksinya !
Jawab :
V = k [P]x[Q]y
Orde reaksi terhadap P adalah x diperoleh data 2 dan 3 : = ( )x( )y
x=1
Orde reaksi terhadap Q adalah y diperoleh data 1 dan 2 : = ( )x( )y
y=1
Orde reaksi total = x + y = 2
Persamaan laju reaksinya : V = k[P] .[Q]
2. Pada reaksi : A + 3B AB3 diperoleh data sebagai berikut :
NO. [A](M) [B](M) Waktu (dt)
1 0,1 0,2 16
2 0,2 0,4 8
3 0,8 0,8 2
Tentukan :
a. Laju reaksi terhadap zat A
b. Laju reaksi terhadap zat A
c. Laju reaksi total
d. Persamaan laju reaksi
e. Satuan tetapan k pada orde reaksi tersebut
Jawab :
V = k [A] x . [B] y
Orde reaksi zat A = x dicari dari data 1 dan 2 :
0,2 x 0,4 y
x y
--- . ----- . = ----- 2 .2 =2 x + y = 1 …………. ( 1 )
0,1 0,2
Orde reaksi zat B = dicari dari data 2 dan 3 :
0,8 x 0,8 y
LKS Kimia Kelas X1 MAN Kupang
Bab 3 Laju Reaksi
----- ----- . = ----- 22x . 2 y
=4 2x + y = 2 …………. ( 2 )
0,2 0,4
sehingga : x+y=1
2x + y = 2
-
x =1
y =0
a. Orde reaksi terhadap zat A = 1
b. Orde reaksi terhadap zat B = 0
c. Orde reaksi terhadap zat A dan B ( orde total ) = 1 + 0 = 1
d. Persamaan laju reaksi : V = k [A]
e. Satuan k orde reaksi di atas ( orde 1) : k = = = dt-1
Latihan Soal Persamaan Laju Reaksi
1. Tuliskan persamaan laju reaksi untuk reaksi :
a. N2 (g) + 3 H2 (g) 2 NH3 (g)
b. 2 NH3 (g) N2 (g) + 3 H2 (g)
2. Suatu reaksi : A(g) + B(g) AB(g) mempunyai persamaan laju reaksi V = k [ A ]2 [ B ]3
Tentukan :
a. orde reaksi terhadap gas A
b. orde reaksi terhadap gas B
c. orde reaksi total
3. Pada reaksi : 2 V + W V2W
Diperoleh data sebagai berikut :
Jika [ V ] dinaikkan dua kali dan [ W ] tetap laju reaksi menjadi dua kali dan jika [ V ] dinaikkan
dua kali dan
[ W ] dinaikkan dua kali laju reaksi menjadi empat kali.
Tentukanlah orde reaksinya !
4. Pada reaksi : 2A(g) + 3B(g) A2B3(g) diperoleh data sebagai berikut :
No [A]M [B]M Laju reaksi (M/dt)
1 0,1 0,1 2 x 10-2
2 0,1 0,4 4 x 10-2
3 0,2 0,1 8 x 10-2
Tentukan :
a. Persamaan laju reaksi
b. Orde reaksi total
c. Tetapan laju reaksi
d. Laju reaksi jika [ A ] = 0,5 M dan [ B ] = 0,5 M
e. Gambarkan grafik laju reaksi terhadap gas A dan gas B
5. Pada reaksi : X2(g) + 2Y(g) 2XY(g) diperoleh data sebagai berikut :
No [X]M [Y]M Laju Reaksi (M/dt)
1 0,1 0,1 1
2 0,2 0,4 2
3 0,4 0,8 8
Tentukan :
a. Persamaan laju reaksi
b. Orde reaksi total
c. Tetapan laju reaksi
d. Laju reaksi jika [ X ] = 0,5 M dan [ Y ] = 0,5 M
6. Pada reaksi : P + 3 Q PQ3 diperoleh data sebagai berikut :
No [P](M) [Q](M) Waktu ( dt )
1. 1 1 32
2. 2 4 16
3. 4 8 4
Tentukanlah :
a. Orde reaksi total
b. Persamaan Laju Reaksi
c. Satuan k laju reaksi di atas
7. Pada reaksi : A + B + C D diperoleh data sebagai berikut :
No [A](M) [B](M) [C](M) Laju Reaksi ( M/dt )
LKS Kimia Kelas X1 MAN Kupang
Bab 3 Laju Reaksi
1. 0,1 0,1 0,2 1 x 10-1
2. 0,1 0,2 0,2 2 x 10-1
3. 0,2 0,2 0,4 4 x 10-1
4. 0,2 0,4 0,8 8 x 10-1
Tentukanlah :
a. Orde reaksi total
b. Persamaan Laju Reaksi
LKS Non Eksperimen
5. Teori tumbukan
Setiap tumbukan antara partikel belum tentu menghasilkan reaksi hanya tumbukan yang
efektiflah yang menghasilkan reaksi. Tumbukan efektif hanya terjadi jika partikel tersebut
memiliki energi minimal yang disebut energi aktivasi ( Ea).
Energi aktifasi dipengaruhi oleh
- konsentrasi
- luas permukaan sentuh
- suhu
- katalisator.
Jawablah pertanyaan berikut ini !
1. Mengapa tidaklah setiap tumbukan menghasilkan reaksi. Jelaskan !
2. Sebut faktor-faktor pada tumbukan yang dapat menghasilkan reaksi !
3. a. Jelaskan pengertian energi aktivasi !
b. Mengapa energi aktivasi dapat mempercepat reaksi ?
Mengapa bensin pada suhu kamar tidak terbakar ?
4. Gambarkan dengan diagram fungsi katalisator pada reaksi eksoterm dan endoterm !
5. Gambarkan dengan diagram letaknya energi aktivasi pada reaksi eksoterm dan endoterm !
Diperiksa pada tanggal Parap Guru
LKS Non Eksperimen
Nama
Kelas
No Absen
6. Peranan Laju Reaksi dalam Industri
- Proses Haber Bosch (Pembuatan Amonia)
N2 (g) + 3 H2 (g) 2 NH3 (g) H = - 92 kJ
Untuk mengoptimalkan hasil amonia maka :
- menggunakan katalisator serbuk besi
- suhu 500 0C
- tekanan tinggi ( 250 atm )
- Proses Kontak ( Pembuatan Asam Sulfat )
2 SO2 (g) + O2 (g) 2 SO3 (g) H = - 98 kJ
SO3 (g) + H2O (l) H2SO4 (aq)
Untuk mengoptimalkan hasil SO3 maka :
- menggunakan katalisator Vanadium pentaoksida, V2O5
- suhu 500 0C
- tekanan normal (1 atm).
Jawablah pertanyaan berikut ini !
1. Berilah contoh katalis yang digunakan dalam industri !
2. Jelaskan pengertian dari :
a. katalis homogen
b. katalis heterogen
c. inhibitor
LKS Kimia Kelas X1 MAN Kupang
Bab 3 Laju Reaksi
3. Mengapa pada proses Haber Bosch ( Pembuatan Amonia )
N2 (g) + 3 H2 (g) 2 NH3 (g) H = - 92 kJ
Untuk mengoptimalkan hasil amonia :
a. menggunakan katalisator (serbuk besi)
b. berlangsung pada suhu 500 0C padahal reaksinya eksoterm
c. berlangsung pada tekanan tinggi ( 250 atm )
4. Jelaskan mengapa pada proses Kontak ( Pembuatan Asam Sulfat )
2 SO2 (g) + O2 (g) 2 SO3 (g) H = - 98 kJ
SO3 (g) + H2O (l) H2SO4 (aq)
Untuk mengoptimalkan hasil SO3 maka :
a. menggunakan katalisator (Vanadium pentaoksida, V2O5)
b. berlangsung pada suhu 500 0C
Diperiksa pada tanggal Parap Guru
PROSEDUR EKSPERIMEN LAJU REAKSI
PENGARUH SUHU TERHADAP LAJU REAKSI
1. ALAT DAN BAHAN
a. Alat :
- Gelas ukur 10 mL
- Gelas kimia 100 mL
- Pipet tetes
- Kakitiga dan kasa porselin
- Pembakar spritus
b. Bahan :
- Na2S2O3(aq) 0,1 M
- HCl(aq) 1 M
2. LANGKAH KERJA
a. Buatlah tanda silang pada kertas putih
b. Isilah gelas kimia dengan Na2S2O3(aq) 0,1 M sebanyak 50 mL dan ukur suhunya
c. Letakkan di atas kertas yang sudah diberi tanda silang kemudian tuangkan 5 mL HCl(aq) 1 M
dan catat waktunya sampai tanda silang tersebut hilang
d. Ulangi percobaan tersebut dengan Na2S2O3(aq) 0,1 M dipanaskan sampai suhunya ( t + 10oC)
dan tuangkan 5 mL HCl(aq) 1 M dan catat waktunya sampai tanda silang hilang.
3. PENGAMATAN
Waktu yang diperlukan sejak penambahan HCl sampai tanda silang tidak terlihat :
No. Percobaan Suhu Waktu
1 ………………… …………………..
2 ………………… …………………..
3 ………………… …………………..
4. PERTANYAAN
1. Bagaimanakah pengaruh suhu terhadap kecepatan reaksi antara larutan Na2S2O3 dengan
larutan HCl ? Jelaskan sebabnya.
2. Banyak reaksi yang berlangsung dua kali lebih cepat jika suhu dinaikkan 10oC. Apakah seperti
itu berlaku untuk reaksi larutan Na2S2O3 dengan larutan HCl?
5. KESIMPULAN
ULANGAN HARIAN LAJU REAKSI ( A )
I. Pilihlah jawaban yang benar dengan menuliskan a, b, c, d dan e disertai alasannya pada lembar
jawab !
Volume asam sulfat 98% massa jenis 1,8 gram/mL yang diperlukan untuk membuat 180 mL larutan
H2SO4 0,5 M adalah ….
A. 2,5 mL B. 5 mL C. 9 mL D. 10 mL E. 18 mL
LKS Kimia Kelas X1 MAN Kupang
Bab 3 Laju Reaksi
1. Untuk membuat 500 mL larutan NaOH 0,2 M diperlukan 4 gram diperlukan kristal NaOH murni.
Penyedian larutan melalui langkah-langkah sebagai berikut :
1. menimbang 4 gram kristal NaOH
2. menyiapkan alat & bahan
3. mengisi labu ukur dengan air hingga tepat 500 mL
4. melarutkan NaOH kira-kira 400 mL air dalam labu ukur
5. menambah air ke dalam labu ukur hingga tepat 50 mL
Urutan langkah kerja yang benar adalah ….
A. 1, 2, 3 dan 5 D. 2, 1, 4 dan 5
B. 2, 1, 3 dan 5 E. 2, 1, dan 5
C. 1, 2, 4 dan 5
2. Sebanyak 0,8 mol sulfur trioksida (SO 3) dipanaskan dal ruang 10 L sehingga terurai membentuk
sulfur dioksida (SO2) dan gas oksigen (O2) menurut reaksi : 2 SO3 (g) 2 SO2(g) + O2(g)
Dalam 10 detik pertama terbentuk 0,2 mol gas oksigen, maka penguraian gas SO3 adalah ….
A. 0,02 M/dt D. 0,08 M/dt
B. 0,04 M/dt E. 0,16 M/dt
C. 0,06 M/dt
3. Perhatikan reaksi berikut : 2 Fe(s) + 6 HCl(aq) 2 FeCl3(aq) + 3 H2(g)
Apakah pengaruhnya terhadap laju reaksi dan volume gas hidrogen jika logam besi diganti
serbuk besi ….
Laju reaksi Volume gas hidrogen
A. bertambah bertambah
B. bertambah tetap
C. bertambah berkurang
D. berkurang tetap
E. berkurang berkurang
4. Dari reaksi berikut yang diharapkan bereaksi paling cepat adalah ….
A. 20 mL HCl 0,1 M + 20 mL Na2S2O3 0,1 M pada suhu 30oC
B. 20 mL HCl 0,1 M + 20 mL Na2S2O3 0,1 M pada suhu 40oC
C. 20 mL HCl 0,1 M + 20 mL Na2S2O3 0,1 M + 10 mL air pada suhu 30oC
D. 20 mL HCl 0,1 M + 20 mL Na2S2O3 0,1 M + 10 mL pada suhu 40oC
E. 20 mL HCl 0,1 M + 20 mL Na2S2O3 0,1 M + 20 mL pada suhu 30oC
6. Data percobaan A + B C adalah
Percobaan Massa/bentuk Zat A Konsentrasi B (M) Waktu (detik) Suhu (oC)
1. 5 gram serbuk 0,1 2 2
2. 5 gram larutan 0,1 3 25
3. 5 gram padat 0,1 5 25
4. 5 gram larutan 0,2 1,5 25
5. 5 gram larutan 0,1 1,5 35
Berdasarkan percobaan 2 dan 5 maka untuk kenaikan suhu sebesar 10oC, laju reaksi akan …
A. sama dengan semula D. menjadi 2 kali semula
B. menjadi lebih lambat E. menjadi 4 kali semula
C. menjadi kali semula
7.Diagram tingkat energi untuk reaksi R P adalah sebagai berikut :
Energi aktifasi reaksi tersebut ….
100 A. 10 kJ
B. 20 kJ
C. 30 kJ
20 D. 50 kJ
10 E. 80 kJ
8.Satuan tetapan laju reaksi orde ke dua adalah ….
A. M-1dt-1 B. M-2dt-1 C. M-2dt-1 D. Mdt-1 E. M-1dt-1
9. Untuk reaksi A + B C diperoleh data sebagai berikut :
Jika konsentrasi A dinaikkan dua kali dan konsentrasi B tetap laju reaksi menjadi dua kali,
Jika konsentrasi A tetap dan konsentrasi B dinaikan dua kali laju reaksi menjadi empat kali,
Maka orde reaksinya adalah ….
LKS Kimia Kelas X1 MAN Kupang
Bab 3 Laju Reaksi
A. 1 B. 2 C. 3 D. 4 E. 5
10.Untuk reaksi : P + 2Q PQ2 diperoleh data sebagai berikut :
Percobaan [P](M) [Q](M) Waktu (dt)
1 0,1 0,1 16
2 0,1 0,2 8
3 0,2 0,2 2
Maka persamaan laju reaksinya adalah ….
A. V = k[P][Q]2 D. V = k[P][Q]2
2
B. V = k[P] [Q] E. V = k[P]2[Q]3
2 2
C. V = k[P] [Q]
II. Jawablah soal berikut dengan singkat dan benar !
11. Sebanyak 24,6 gram MgSO4.7H2O dilarutkan dalam air dan volum larutan tepat 500 mL.
A. Hitunglah kemolaran larutan itu ! ( Mg=24, S=32, O=16, H=1 )
B. Sebanyak 10 mL diambil dalam gelas kimia. Berapa kemolaran larutan dalam gelas kimia ?
C. Hitunglah massa MgSO4 dalam 10 mL larutan itu !
D. Hitunglah mL air yang harus ditambah kedalam 100 mL larutan itu sehingga molaritasya
menjadi 0,1 M !
12. Pada reaksi : X2(g) + 2Y(g) 2XY(g) diperoleh data sebagai berikut :
No [X]M [Y]M Laju Reaksi M/dt)
1 0,1 0,1 1
2 0,2 0,4 2
3 0,4 0,8 8
Tentukan :
A. Persamaan laju reaksi
B. Orde reaksi total
C. Tetapan laju reaksi
13. Suatu reaksi berlangsung dua kali lebih cepat setiap kenaikan suhu 10oC. Jika laju reaksi pada
suhu 20 oC adalah 8 M/dt. Hitunglah laju reaksi pada suhu 50 oC !
14. Gambarkan dengan diagram energi fungsi katalisator pada reaksi eksoterm dan endoterm !
-o-
ULANGAN HARIAN LAJU REAKSI ( B )
Pilihlah jawaban yang benar dengan menuliskan a, b, c, d dan e disertai alasannya pada lembar
jawab !
1. Sebanyak 4 gram NaOH ( 40 gram/mol ) dilarutkan ke dalam air hingga 500 mL dicampur
dengan 500 mL larutan KOH 0,2 M maka konsentrasi capuran sebesar ….
A. 0,1 M B. 0,15 M C. 0,2 M D. 0,25 M E. 0,3 M
2. Laju reaksi Mg(s) + 2 HCl(aq) MgCl2(aq) + H2(g) dapat dinyatakan sebagai ….
A. laju bertambahnya [HCl] persatuan waktu
B. laju bertambahnya [Mg] persatuan waktu
C. laju bertambahnya [MgCl2] persatuan waktu
D. laju berkurangnya [MgCl2] persatuan waktu
E. laju berkurangnya [H2] persatuan waktu
3. Dalam ruang 5 L telah terurai 0,5 mol amonia menjadi gas nitrogen dan gas hidrogen
menurut reaksi :
2 NH3(g) N2(g) + 3 H2(g)
Setelah 10 detik terbentuk 0,1 mol gas nitrogen, maka pernyataan yang benar tentang laju
reaksi ….
A. VNH3 = 0,5 M/dt D. VH2 = 0,03 M/dt
B. VNH3 = 0,05 M/dt E. VH2 = 1,5 M/dt
C. VN2 = 0,25 M/dt
4. Reaksi penguraian padatan KClO3 sebagai berikut : 2 KClO3(s) 2 KCl(s) + 3 O2(g)
Kurva A ( lihat gambar ) menunjukkan volume gas oksigen hasil reaksi yang dilangsungkan
pada suhu 50oC Manakah diantara aksi berikut :
1. digunakan katalis MnO2
LKS Kimia Kelas X1 MAN Kupang
Bab 3 Laju Reaksi
2. tanpa menggunakan katalis MnO2 B
3. reaksi berlangsung pada suhu 50oC A
4. reaksi berlangsung pada suhu 70oC
Yang akan menghasilkan kurva B adalah ….
A. 1, 2, 3 dan 4 D. 1 dan 4
B. 1, 2 dan 3 E. 2, 3 dan 4
C. 2 dan 3
5. Data percobaan A + B C adalah
Percobaan Massa/bentuk Konsentrasi B Waktu Suhu (oC )
Zat A (M) (detik)
1. 5 gram serbuk 0,1 2 2
2. 5 gram larutan 0,1 3 25
3. 5 gram padat 0,1 5 25
4. 5 gram larutan 0,2 1,5 25
5. 5 gram larutan 0,1 1,5 35
Pada percobaan 1 dan 3 laju reaksi dipengaruhi faktor ….
A. Konsentrasi D. luas permukaan
B. sifat-sifat E. katalis
C. suhu
6. Setiap kenaikan suhu 20oC laju reaksi menjadi 3 kali lebih cepat dari semula. Jika pada suhu
20oC laju reaksi berlangsung 243 detik, maka laju reaksi pada suhu 80oC adalah …
A.27 detik B. 9 detik C. 3 detik D. 1 detik E. detik
7. Diagram tingkat energi untuk reaksi R P adalah sebagai berikut :
Perubahan entalpi reaksi tersebut ….
100 A. 10 kJ
B. 20 kJ
C. 30 kJ
20 D. 50 kJ
10 E. 80 kJ
0
8. Satuan tetapan laju reaksi orde ke tiga adalah ….
A. M-1dt-1 D. M-2dt-1
B. M-2dt-1 E. Mdt-1
C. M-1dt-1
9. Untuk reaksi A + B C diperoleh data sebagai berikut :
Jika konsentrasi A dinaikkan tiga kali dan konsentrasi B tetap laju reaksi menjadi tiga kali,
Jika konsentrasi A tetap dan konsentrasi B dinaikan tiga kali laju reaksi menjadi sembilan kali,
Maka orde reaksinya adalah ….
A. 1 B. 2 C. 3 D. 4 E. 5
10. Untuk reaksi : X + 3Y XY3 diperoleh data sebagai berikut :
Percobaan [X](M) [Y](M) Waktu (dt)
1 0,1 0,1 27
2 0,1 0,3 9
3 0,3 0,1 3
Maka persamaan laju reaksinya adalah ….
A. V = k[P][Q] D. V = k[P][Q]2
2
B. V = k[P] [Q] E. V = k[P]2[Q]3
2 2
C. V = k[P] [Q]
Jawablah soal berikut dengan singkat dan benar !
11. Sebanyak 4 gram NaOH ( 40gr/mol ) dilarutkan dalam air sehingga volumenya 400 mL
dicampur dengan
600 mL Ca(OH)2 0,2 M.
Hitunglah :
a.kemolaran campuran NaOH dan Ca(OH)2
b. massa Ca(OH)2 ( 74gr/mol ) dalam larutan 600 mL Ca(OH)2 0,2 M
12. Pada reaksi : P + 3 Q PQ3 diperoleh data sebagai berikut :
No [P](M) [Q](M) Waktu ( dt )
LKS Kimia Kelas X1 MAN Kupang
Bab 3 Laju Reaksi
1. 1 1 32
2. 2 4 16
3. 4 8 4
Tentukanlah :
A. Orde reaksi total
B. Persamaan Laju Reaksi
C. Satuan k laju reaksi di atas
13. Suatu reaksi berlangsung tiga kali lebih cepat setiap kenaikan suhu 10oC. Jika laju reaksi pada
suhu 25 oC adalah 4 menit. Tentukan laju reaksi pada suhu 55 oC !
14. Gambarkan dengan diagram letak energi aktivasi pada reaksi eksoterm dan endoterm !
-o-
LKS Kimia Kelas X1 MAN Kupang
Anda mungkin juga menyukai
- Laju Reaksi 1: Kelas Xi Semester 1Dokumen40 halamanLaju Reaksi 1: Kelas Xi Semester 1RAIHAN. APBelum ada peringkat
- Laju Reaksi - 1Dokumen36 halamanLaju Reaksi - 1Dinda Saharani RBelum ada peringkat
- Laju Reaksi LitbangDokumen18 halamanLaju Reaksi LitbangAna FitrianaBelum ada peringkat
- Laju Reaksi Litbang NewDokumen16 halamanLaju Reaksi Litbang NewAna FitrianaBelum ada peringkat
- Bab 3 Laju Reaksi KimiaDokumen16 halamanBab 3 Laju Reaksi KimiaApa BenarBelum ada peringkat
- 2021 XI Laju ReaksiDokumen11 halaman2021 XI Laju ReaksiAnnisaBelum ada peringkat
- Bab 3 Laju ReaksiDokumen16 halamanBab 3 Laju ReaksiRhahil BluesBelum ada peringkat
- 5 Bab 3 Laju Reaksi NewDokumen28 halaman5 Bab 3 Laju Reaksi Newneneng rohayatiBelum ada peringkat
- Laju ReaksiDokumen49 halamanLaju Reaksierna ferikaBelum ada peringkat
- Stoikiometri 2Dokumen48 halamanStoikiometri 2wiracanaBelum ada peringkat
- 04 Bab 3Dokumen28 halaman04 Bab 3RiskyKaIshiBelum ada peringkat
- XI 4 MIPA JK 5 Menentukan V Jumat 22102021Dokumen3 halamanXI 4 MIPA JK 5 Menentukan V Jumat 22102021Anisa Nurhuda UtamiBelum ada peringkat
- Stoikimometri Dan Reaksi KimiaDokumen34 halamanStoikimometri Dan Reaksi KimiaRifdahTsabitaBelum ada peringkat
- Praktik LAJU REAKSI XI 2022Dokumen5 halamanPraktik LAJU REAKSI XI 2022ebenezer.sinaga20Belum ada peringkat
- Laju Reaksi - 1Dokumen5 halamanLaju Reaksi - 1I MADE SRI SAMHITABelum ada peringkat
- Sifat KoligatifDokumen14 halamanSifat KoligatifDavinSantikaWardhanaBelum ada peringkat
- Pertemuan 1 Konsep Laju ReaksiDokumen23 halamanPertemuan 1 Konsep Laju ReaksiLittle AyuBelum ada peringkat
- Stokiometri BogiDokumen53 halamanStokiometri BogiRicki KurniawanBelum ada peringkat
- 11.3. Laju ReaksiDokumen4 halaman11.3. Laju ReaksiDar Sono TursinBelum ada peringkat
- Laju Reaksi (Kemolaran)Dokumen21 halamanLaju Reaksi (Kemolaran)esmarmangalikBelum ada peringkat
- Laju ReaksiDokumen4 halamanLaju ReaksiMelin GintingBelum ada peringkat
- Kimia 3 OktoDokumen14 halamanKimia 3 Oktoafra mudrikahBelum ada peringkat
- Kinetika KimiaDokumen24 halamanKinetika KimiaaudrefthyahBelum ada peringkat
- 4.LAJU DAN ORDE REAKSI 13 1011 PowerpointDokumen31 halaman4.LAJU DAN ORDE REAKSI 13 1011 Powerpointanon_753584013Belum ada peringkat
- KecepatanreaksiDokumen19 halamanKecepatanreaksiYuliati SipahutarBelum ada peringkat
- Laju ReaksiDokumen14 halamanLaju ReaksiFerdinandus Laki NuwaBelum ada peringkat
- Bab 4 Laju ReaksiDokumen32 halamanBab 4 Laju ReaksiRyanBelum ada peringkat
- Soal Soal Kimia AnalitikDokumen11 halamanSoal Soal Kimia AnalitikRusda SelviaBelum ada peringkat
- Laju RaksiDokumen27 halamanLaju Raksizhafirah radhwaBelum ada peringkat
- Laju Reaksi Nadia AltaffaDokumen2 halamanLaju Reaksi Nadia AltaffaNadia. AltaffaBelum ada peringkat
- Persamaan Laju ReaksiDokumen50 halamanPersamaan Laju ReaksiBabetan SonyeondadBelum ada peringkat
- Kon Sent RasiDokumen11 halamanKon Sent Rasisandia widianiBelum ada peringkat
- Bahan Ajar Ujian PPLDokumen6 halamanBahan Ajar Ujian PPLmesi nubatonisBelum ada peringkat
- Stokiometri LarutanDokumen13 halamanStokiometri LarutanvgestantyoBelum ada peringkat
- Laju ReaksiDokumen21 halamanLaju ReaksiEddy Pengen Jadi HokageBelum ada peringkat
- Sifas Hantaran Larutan ElektrolitDokumen31 halamanSifas Hantaran Larutan ElektrolitRizky Mutiara AyuBelum ada peringkat
- III Laju ReaksiDokumen28 halamanIII Laju ReaksiDian PurnamaBelum ada peringkat
- Laju Reaksi SoalDokumen8 halamanLaju Reaksi SoalNisaBelum ada peringkat
- Stoikiometri LarutanDokumen26 halamanStoikiometri LarutanSiskaBelum ada peringkat
- 213 LajuDokumen1 halaman213 LajuNovita RamadhaniBelum ada peringkat
- Laju Reaksi Kimia TPDokumen36 halamanLaju Reaksi Kimia TPSuriani anyekBelum ada peringkat
- Jenis Konsentrasi Zat Dan PerhitungannyaDokumen24 halamanJenis Konsentrasi Zat Dan PerhitungannyaSatriyani Hastuti RahayuBelum ada peringkat
- Lembar Kerja Siswa Laju ReaksiDokumen3 halamanLembar Kerja Siswa Laju ReaksiJunathan NjotoBelum ada peringkat
- Laju Reaksi IDokumen23 halamanLaju Reaksi IShella NilambumalaBelum ada peringkat
- Laju ReaksiDokumen35 halamanLaju ReaksiZatmika PutuBelum ada peringkat
- Kimia - Stoikiometri Reaksi SederhanaDokumen11 halamanKimia - Stoikiometri Reaksi SederhanaYusha Camilla MasyitaBelum ada peringkat
- Stoikiometri IIDokumen38 halamanStoikiometri IIZaenab SyukriadiBelum ada peringkat
- Konsep Mol Kelompok 7Dokumen27 halamanKonsep Mol Kelompok 7Liiea ChevlovestupidblackeyepeasBelum ada peringkat
- 3.4 Laju ReaksiDokumen16 halaman3.4 Laju ReaksiMailanmailaniBelum ada peringkat
- Bab 1 Konsep MolDokumen7 halamanBab 1 Konsep Moliwan60Belum ada peringkat
- STOIKIOMETRIDokumen23 halamanSTOIKIOMETRIM SyukurdiBelum ada peringkat
- Laju Reaksi MateriDokumen20 halamanLaju Reaksi MateriFebi AdityaBelum ada peringkat
- Pertanyaan PKNDokumen2 halamanPertanyaan PKNAnnisa RuwaidaBelum ada peringkat
- PPKN KLMPK LLDokumen10 halamanPPKN KLMPK LLAnnisa RuwaidaBelum ada peringkat
- Makalah Karya Ilmiah Bahasa IndonesiaDokumen6 halamanMakalah Karya Ilmiah Bahasa IndonesiaAnnisa RuwaidaBelum ada peringkat
- Latihan Soal Akidah Akhlak Kelas X PatDokumen13 halamanLatihan Soal Akidah Akhlak Kelas X PatAnnisa RuwaidaBelum ada peringkat
- Annisa Ruwaidah AdangDokumen1 halamanAnnisa Ruwaidah AdangAnnisa RuwaidaBelum ada peringkat
- Zahra Tugas SBKDokumen4 halamanZahra Tugas SBKAnnisa RuwaidaBelum ada peringkat
- Materi TIK Mengenal Dan Menggunakan InternetDokumen8 halamanMateri TIK Mengenal Dan Menggunakan InternetAnnisa RuwaidaBelum ada peringkat
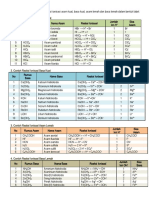
- Tabel Unsur Dan Senywa - AsbasDokumen1 halamanTabel Unsur Dan Senywa - AsbasAnnisa RuwaidaBelum ada peringkat
- TLObladiladaDokumen3 halamanTLObladiladaAnnisa RuwaidaBelum ada peringkat
- Daftar Menari & SinopsisDokumen2 halamanDaftar Menari & SinopsisAnnisa RuwaidaBelum ada peringkat
- Penilai TerbaruDokumen1 halamanPenilai TerbaruAnnisa RuwaidaBelum ada peringkat
- Nama Unsur Dan SenyawaDokumen2 halamanNama Unsur Dan SenyawaAnnisa RuwaidaBelum ada peringkat
- LKPD Protista Mirip HewanDokumen3 halamanLKPD Protista Mirip HewanRendi Yuntara100% (3)