Termo 1 Bab 2
Diunggah oleh
Azhar UmamJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Termo 1 Bab 2
Diunggah oleh
Azhar UmamHak Cipta:
Format Tersedia
9
Yosef Agung Cahyanta : Termodinamika I
BAB II
SIFAT-SIFAT ZAT MURNI
ZAT MURNI (PURE SUBSTANCE)
Merupakan zat yang mempunyai komposisi kimia yang tetap (stabil), misalnya :
air (water) , nitrogen, helium, dan CO2.
Zat murni bisa terdiri dari satu elemen kimia (N2 ) maupun campuran
(udara).Campuran dari beberapa fase zat murni adalah zat murni, contohnya
campuran air dan uap air. Tetapi campuran dari udara cair dan gas bukan zat murn
karena susunan kimianya berubah atau berbeda.
N2
Udara
Vapor
Vapor
Liquid
H2O
Zat murni
Udara
Liquid
Bukan zat murni
FASE dari ZAT MURNI
Diidentifikasi berdasarkan susunan molekulnya.
Solid (padat) : jarak antar molekul sangat dekat sehingga gaya tarik antar
molekul sangat kuat, maka bentuknya tetap. Gaya tarik antara molekulmolekul cenderung untuk mempertahankannya pada jarak yang relatif
konstan.Pada temperatur tinggi molekul melawan gaya antar molekul dan
terpencar.
Liquid (cair) : Susunan molekul mirip dengan zat padat , tetapi terhadap
yang lain sudah tidak tetap lagi. Sekumpulan molekul akan mengambang
satu sama lain.
Gas : Jarak antar molekul berjauhan dan susunannya acak. Molekul
bergerak secara acak.
Yosef Agung Cahyanta : Termodinamika I
10
PERUBAHAN FASA dari ZAT MURNI
Semua zat murni mempunyai mempunyai kelakuan umum yang sama. Sebagai
contoh air (water).
State 1 : Pada state ini disebut compressed liquid atau subcooled
liquid. Pada state ini penambahan panas hanya akan menaikkan
temperatur tetapi belum menyebabkan terjadi penguapan (not
about to vaporize)
State 2 : Disebut saturated liquid (cairan jenuh). Pada state ini
fluida tepat akan berubah fasenya. Penambahan panas sedikit saja
akan menyebabkan terjadi penguapan (about to vaporize). Akan
mengalami sedikit penambahan volume.
State 3 : Disebut Saturated liquid - vapor mixture (campuran
uap - cairan jenuh). Pada keadaan ini uap dan cairan jenuh berada
dalam kesetimbangan. Penambahan panas tidak akan menaikkan
temperatur tetapi hanya menambah jumlah penguapan.
State 4 : Campuran tepat berubah jadi uap seluruhnya, disebut
saturated vapor (uap jenuh). Pada keadaan ini pengurangan
panas akan menyebabkan terjadi pengembunan (about to
condense).
State 5 : Disebut superheated vapor (uap panas lanjut).
Penambahan panas akan menyebabkan kenaikkan suhu dan
volume..
Gambar 2.1 Pemanasan Air
pada tekanan konstan
Yosef Agung Cahyanta : Termodinamika I
11
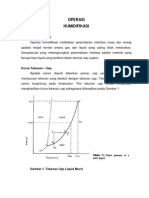
Proses-proses tersebut di atas dapat digambarkan dalam diagram T - v. Diagram
ini menggambarkan perubahan-perubahan temperatur dan volume jenis.
Gambar 2.2 Diagram T-v proses perubahan fase air pada tekanan konstan
Proses 1-2-3-4-5 adalah pemanasan pada tekanan konstan
Proses 5-4-3-2-1 adalah pendinginan pada tekanan konstan
.
PROPERTY DIAGRAM ( DIAGRAM SIFAT)
Diagram T - v
Gambar 2.3 Diagram T- v perubahan fase zat murni (air) pada
berbagai variasi tekanan
Yosef Agung Cahyanta : Termodinamika I
12
Dari gambar 2.3 dapat dilihat bahwa semakin tinggi tekanan air maka semakin
tinggi pula titik didihnya. Tsat merupakan fungsi dari Psat ,(Tsat = f Psat)
Tsat = Saturation temperature , temperatur saat zat murni berubah phase
pada tekanan tertentu.
Psat = Saturation pressure , tekanan saat zat murni berubah phase pada
temperatur tertentu.
Garis yang menghubungkan keadaan cair jenuh dan uap jenuh akan semakin
pendek jika tekanannya makin besar. Pada tekanan tertentu (22,09 MPa) keadaan
cair jenuh dan uap jenuh berada pada satu titik. Titik ini disebut titik kritis
(critical point). Untuk air (water) : Tcr = 374,14oC ; Pcr = 22,09 MPa. ; vcr =
0,003155 m3/kg. Jika titik-titik pada keadaan cair jenuh dihubungkan maka
diperoleh garis cair jenuh. Jika titik-titik pada keadaan uap jenuh dihubungkan
maka diperoleh garis uap jenuh. Kedua garis ini bertemu di titik kritis.
Gambar 2.4 Diagram T- v zat murni
Di atas titik tekanan kritis proses perubahan dari cair menjadi uap tidak lagi
terlihat jelas/nyata. Terjadi perubahan secara spontan dari cair menjadi uap.
Yosef Agung Cahyanta : Termodinamika I
13
Diagram P - v
Gambar 2.5 Diagram P- v zat murni
Bentuk dari diagram P-v mirip dengan diagram T- v. Pada diagram P-v
garis temperatur konstan mempunyai trend menurun sedangkan pada diagram T-v
garis tekanan konstan mempunyai trend menaik.
Diagram P - v dan P-T fase padat, cair dan gas
Mengecil sewaktu membeku
Kebanyakan zat murni akan menyusut saat membeku.
Gambar 2.6 Diagram P- v zat murni yang menyusut saat membeku
Yosef Agung Cahyanta : Termodinamika I
14
Mengembang sewaktu membeku
Gambar 2.7 Diagram P- v zat murni yang mengembang saat
membeku (contohnya adalah air)
Pada kondisi tertentu fase padat, cair dan gas berada dalam
kesetimbangan. Pada diagram P-v dan T-v keadaan ini akan membentuk suatu
garis yang disebut Triple line. Dalam diagram P-T keadaan ini nampak sebagai
suatu titik dan disebut Triple point. Triple point air adalah TTR = 0,01 oC dan PTR
= 0,06113 kPa.
Gambar 2.8 Diagram P- T zat murni (diagram fase)
15
Yosef Agung Cahyanta : Termodinamika I
Diagram P-T sering disebut sebagai diagram fase karena dalam diagram PT, antar tiga fase dipisahkan secara jelas, masing-masing dengan sebuah garis.
Ketiga garis bertemu di triple point. Garis penguapan (vaporisation) berakhir di
titik kritis karena tidak ada batas yang jelas antara fase cair dan fase uap. Tidak
ada zat yang berada pada fase cair jika tekanannya berada di bawah tekanan
Triple point. Ada dua cara zat padat berubah menjadi uap Pertama melalui proses
mencair kemudian menguap dan kedua fase padat berubah langsung menjadi fase
gas (disebut menyublim). Menyublim hanya dapat terjadi pada tekanan di bawah
tekanan Triple point.
Diagram P - v - T
a. Menyusut saat membeku
b. Mengembang saat membeku
Gambar 2.8 Diagram P- T zat murni (diagram fase)
PROPERTY TABEL (TABEL SIFAT-SIFAT THERMODINAMIKA)
Sebagai contoh akan dibahas tabel air (water), untuk zat yang lain analog.
Tabel jenuh air (saturated water table) :
Pada proses perubahan fase temperatur dan tekanan merupakan variabel yang
saling tergantung (dependent variable). Oleh karena itu disusun dua tabel yaitu
tabel dengan temperatur sebagai variable bebas dan tabel dengan tekanan sebagai
variabel bebas.
Yosef Agung Cahyanta : Termodinamika I
Tabel Temperatur
Tabel Tekanan
16
17
Yosef Agung Cahyanta : Termodinamika I
Volume jenis
untuk fase
cair jenuh
Volume jenis
untuk fase
uap jenuh
indeks f = fluid : cairan jenuh ( vf , uf , hf , sf )
g = gas : uap jenuh (vg , ug , hg , sg )
fg = fluid - gas : selisih antara harga uap jenuh dan cairan jenuh
( vfg = vg - vf ; ufg = ug - uf ; hfg = hg - hf ; sfg = sg - sf )
hfg
= entalpi penguapan(latent heat of vaporisation) yaitu jumlah energi yang
diperlukan untuk menguapkan satu satuan massa cairan pada suatu temperatur dan
tekanan tertentu. Jika tekanan dan temperatur bertambah maka hfg akan
berkurang, dan pada titik kritik harganya nol ( hfg = 0 ). Enthalpy merupakan
gabungan antara energi dalam, tekanan dan volume.
H = U + P V atau h = u + P v
Campuran uap dan cairan jenuh (saturated liquid vapor mixture)
Pada proses penguapan zat cair dan uap berada pada kesetimbangan atau
zat berada pada fase cair dan fase uap secara bersama-sama. Untuk melakukan
analisa pada fase ini dimunculkan suatu besaran yang disebut kualitas uap (fraksi
uap).
X=
m vapor
m total
X = kualitas uap (quality)
18
Yosef Agung Cahyanta : Termodinamika I
Gambar 2.9 Campuran cair jenuh dan uap
mtotal = mliq + mvapor = mf + mg
m = massa
liq = cair
vapor = uap
V = Vf + Vg
V = m v av ; Vf = m f .v f ; Vg = m g .v g
m v av = m f .v f + m g .v g
v av =
m f .v f m g .v g
+
m
m
mf m - mg
=
m
m
mg
= 1
m
= 1 X
v av = (1 X ) v f + X v g
= v f + X (v g v f )
= v f + X v fg
Sifat-sifat termodinamika suatu campuran cair jenuh dan uap dengan kualitas X :
u = uav = uf + X ufg
h = hav = hf + X hfg
s = sav = sf + X sfg
secara umum y = yf + X yfg
Yosef Agung Cahyanta : Termodinamika I
Gambar 2.10 Kualitas (fraksi) uap
Fraksi uap dapat dinyatakan
X=
y - yf
y fg
Superheated vapor (uap panas lanjut)
Daerah di sebelah kanan garis uap jenuh.
19
20
Yosef Agung Cahyanta : Termodinamika I
Compressed liquid
Daerah di sebelah kiri garis cair jenuh.
Apabila tabel Compressed liquid tidak dijumpai maka nilai properti didekati
sebagai properti pada keadaan cair jenuh berdasarkan temperatur y yf @ T
Atau untuk entalpi didekati dengan
Tabel Karakteristik tiap fase
Given
T
Compressed
liquid
P > Psat
Saturated
liquid
P = Psat
Liquid - vapor
mixture
P = Psat
Saturated
vapor
P = Psat
superheated
vapor
P < Psat
T < Tsat
T = Tsat
T = Tsat
T = Tsat
T > Tsat
P, T
v < vf
v = vf
vf < v <vg
v = vg
v > vg
P, T
u < uf
u = uf
uf < u <ug
u = ug
u > ug
P, T
h < hf
h = hf
hf < h <hg
h = hg
h > hg
P, T
s < sf
s = sf
sf < s <sg
s = sg
s > sg
Cara Menggunakan Tabel
Untuk membaca nilai properti
gunakan tabel sesuai fasenya. Fase suatu zat
ditentukan dengan cara membandingkan properti yang diketahui dengan properti
pada keadaan jenuh (lihat karakteristik tiap fase).
21
Yosef Agung Cahyanta : Termodinamika I
PERSAMAAN GAS IDEAL
Persamaan keadaan (equation of state) : persamaan yang menghubungkan
tekanan, temperatur dan volume jenis suatu zat.
fase uap suatu zat disebut gas jika berada di atas temperatur kritis.
vapor (uap) : gas yang tidak jauh dari keadaan kondensasi
Robert Boyle (Inggris, 1662)
P~
1
v
J. Charles dan J. Gay Lussac (Perancis 1810)
Pv=RT
P=R
T
v
Persamaan gas ideal
= Tekanan absolut : Tekanan terukur + tekanan atmosfir
= Temperatur absolut ( K atau R)
= Volume jenis
= konstante gas
R=
udara
R = 287 J/(kg K)
helium
R = 2077 J/(kg K)
argon
R = 208 J/(kg K)
nitrogen
R = 296 J/(kg K)
RU
M
RU = konstanta gas umum
= 8,314 kJ/(k mol K)
= 1,986 Btu/(lb mol R)
M = molar mass (berat molekul)
massa sistem : m = M N
; N = jumlah molekul
V=mv
PV=mRT
m R = M N R = N RU
P V = N RU T
V=Nv
P v = RU T
v = volume jenis molekul
( volume tiap satuan mole )
Untuk fixed mass system :
P1 V1
PV
= 2 21 = m R
T1
T2
Yosef Agung Cahyanta : Termodinamika I
22
Gambar 2.11 Penyimpangan nilai volume jenis dengan asumsi
steam sebagai gas ideal dibanding tabel
Percent error =
vtabel videal
x 100%
vtabel
Pada tekanan rendah dan temperatur tinggi gas dapat dianggap sebagai gas ideal.
Awas :
Uap air bukan gas ideal. Untuk uap air jangan gunakan persamaan gas ideal.
Di sekitar garis uap jenuh kesalahan besar.
FAKTOR KOMPRESIBILITAS (Z)
Merupakan tolok ukur penyimpangan terhadap sifat gas ideal.
23
Yosef Agung Cahyanta : Termodinamika I
Pv
RT
Pv= ZR T
v
Z = actual
v ideal
Z
; v ideal =
RT
P
Variable kunci :
* Reduced Pressure (tekanan tereduksi)
* Reduced Temperature (suhu tereduksi)
PR =
P
PCR
TR =
T
TCR
Z untuk semua gas sama pada PR dan TR yang sama ( Principle of corresponding
states)
Catatan :
1. PR << 1 (regardless temperatur) : mendekati gas ideal
2. Temperatur tinggi ( TR > 2 ) : mempunyai ketelitian yang baik tanpa
memperhatikan tekanannya, kecuali untuk PR >> 1.
3. Deviasi dari gas ideal akan semakin besar bila dekat dengan titik kritis.
Gambar 2.12 Perbandingan nilai-nilai Z dari berbagai gas
24
Yosef Agung Cahyanta : Termodinamika I
PERSAMAAN KEADAAN YANG LAIN
1. Persamaan Van Der Waals (1873)
P + 2 (v b ) = R T
v
2
27 R 2 TCR
a =
64 PCR
b =
R TCR
8 PCR
a
= pengaruh gaya - gaya antar molekul.
v2
b = pengaruh volume ruang yang ditempati molekul gas.
2. Persamaan Beeattie - Bridgeman (1928)
Disusun dari grafik yang diperoleh dari data eksperimen
P =
R U T (1 - )
v
( v + B) -
A
v
a
A = A o (1 - )
v
b
B = B o (1 - )
v
c
=
v T3
Persamaan Beattie - Bridgeman digunakan untuk massa jenis kurang dari
massa jenis pada titik kritis. Untuk massa jenis yang lebih besar dapat
digunakan persamaan Benedict - Webb - Rubin .
3. Persamaan Benedict - Webb - Rubin (1940)
P=
R UT
v
C 1 bR T a
+ Bo RU T Ao o2 2 + U 3
+ 6 +
T v
v
v
1 + 2
3 2
vT v
v2
e
25
Yosef Agung Cahyanta : Termodinamika I
Gambar 2.14 Penyimpangan nilai volume jenis Nitrogen dengan
menggunakan persamaan dibanding tabel
Percent error =
vtabel v persamaan
vtabel
x 100%
Anda mungkin juga menyukai
- Zat Murni Kelompok 3 Termodinamika TeknikDokumen17 halamanZat Murni Kelompok 3 Termodinamika TeknikSyadad Algany Faras ArkhanBelum ada peringkat
- Kelompok 3 Zat MurniDokumen18 halamanKelompok 3 Zat MurniSyadad Algany Faras ArkhanBelum ada peringkat
- Fasa Zat MurniDokumen9 halamanFasa Zat MurniTrixie WoworBelum ada peringkat
- Chapter03 en IdDokumen56 halamanChapter03 en IdAngga QurniawanBelum ada peringkat
- Pemicu 1 - Kelompok CDokumen74 halamanPemicu 1 - Kelompok CDanar AdityaBelum ada peringkat
- Makalah Pemicu 1Dokumen33 halamanMakalah Pemicu 1Abubakar Adeni100% (1)
- Sifat Zat MurniDokumen16 halamanSifat Zat Murniaokta5Belum ada peringkat
- Tugas Termodinamika 2Dokumen8 halamanTugas Termodinamika 2Yulius ApolonarisBelum ada peringkat
- Kuliah Ke 3. Zat MurniDokumen39 halamanKuliah Ke 3. Zat MurniKhusus DownloadBelum ada peringkat
- Diagram Fase Zat MurniDokumen16 halamanDiagram Fase Zat Murnilisa andrianiBelum ada peringkat
- Sistem Satu KomponenDokumen6 halamanSistem Satu KomponenGunk Putri PuspaBelum ada peringkat
- Zat Murni Proses Perubahan Fase Dan Tabel UapDokumen30 halamanZat Murni Proses Perubahan Fase Dan Tabel UapFadel AshariBelum ada peringkat
- LTM Termo - Kesetimbangan Uap-Cair PDFDokumen4 halamanLTM Termo - Kesetimbangan Uap-Cair PDFj0haNN3sBelum ada peringkat
- Zat Murni Dan Karakteristik Gas IdealDokumen21 halamanZat Murni Dan Karakteristik Gas IdealKevinBelum ada peringkat
- Operasi HumidifikasiDokumen8 halamanOperasi HumidifikasiDwi ApriansyahBelum ada peringkat
- R.kesetimbangan FaseDokumen41 halamanR.kesetimbangan FaseAde RahmaniaBelum ada peringkat
- Translate Termo - Bab 9Dokumen25 halamanTranslate Termo - Bab 9Fregita UbattaBelum ada peringkat
- BAB II Tekanan UapDokumen7 halamanBAB II Tekanan UapYustinus Selis ToronBelum ada peringkat
- Rangkuman Termodinamika 1Dokumen12 halamanRangkuman Termodinamika 1Arnold Thamrin van LutteranBelum ada peringkat
- Hukum Fase For PrintDokumen43 halamanHukum Fase For Printlilik supriantiBelum ada peringkat
- Menentukan Sifat-Sifat System (Part I)Dokumen46 halamanMenentukan Sifat-Sifat System (Part I)Roda TeknikBelum ada peringkat
- Muhammad Dzikrillah Fahuda - Peralatan Destilasi SederhanaDokumen14 halamanMuhammad Dzikrillah Fahuda - Peralatan Destilasi SederhanaGogon SantosoBelum ada peringkat
- Bab 18 Sifat Thermal MaterialDokumen25 halamanBab 18 Sifat Thermal MaterialMufid Hadi RaharjoBelum ada peringkat
- 6708S1TKCE30432018 - Termodinamika Teknik Kimia - Pertemuan 6 - Materi Tambahan PDFDokumen43 halaman6708S1TKCE30432018 - Termodinamika Teknik Kimia - Pertemuan 6 - Materi Tambahan PDFAlifia PangestiBelum ada peringkat
- Diagram Fase Yang Paling Sederhana Adalah Diagram TekananDokumen5 halamanDiagram Fase Yang Paling Sederhana Adalah Diagram TekananNur RachmanBelum ada peringkat
- Pert 03 - Karakteristik Zat MurniDokumen30 halamanPert 03 - Karakteristik Zat MurniSyawal IbrahimBelum ada peringkat
- Kelompok 4a Indralaya - PPT Tugas 3 Termodinamika DasarDokumen56 halamanKelompok 4a Indralaya - PPT Tugas 3 Termodinamika DasarM.rangga PerdanaBelum ada peringkat
- Kimia AnalitikDokumen3 halamanKimia AnalitikElfa NofiaBelum ada peringkat
- Bab I PendahuluanDokumen18 halamanBab I PendahuluanMelany AdeliaBelum ada peringkat
- Diagram Fase DagulDokumen46 halamanDiagram Fase DagulFresz Ddoraemon'sBelum ada peringkat
- Entalpi Dan EntropiDokumen10 halamanEntalpi Dan EntropiRahmad Hidayat Boli100% (1)
- Bab 3 Mengevaluasi SifatDokumen10 halamanBab 3 Mengevaluasi SifatBlackArmy88Belum ada peringkat
- Perubahan FasaDokumen25 halamanPerubahan FasaKatarina fransiscaBelum ada peringkat
- Terjemahan Hal 4-5Dokumen2 halamanTerjemahan Hal 4-5anan zahraBelum ada peringkat
- Kesetimbangan FasaDokumen19 halamanKesetimbangan Fasadwi nurmalasariBelum ada peringkat
- Rangkuman Materi Persamaan Keadaan Kelompok 2 MUTIDokumen16 halamanRangkuman Materi Persamaan Keadaan Kelompok 2 MUTImutiaBelum ada peringkat
- Diagram BinnerDokumen39 halamanDiagram BinnerDevi Murtiya NingsihBelum ada peringkat
- Rangkuman Termodinamika FarhanDokumen8 halamanRangkuman Termodinamika FarhanelridhanieldaBelum ada peringkat
- Diagram Fasa CairDokumen6 halamanDiagram Fasa CairVictorBelum ada peringkat
- Kesetimbangan Fasa (Power Point)Dokumen31 halamanKesetimbangan Fasa (Power Point)Asriandy Ramadhan100% (3)
- Kelompok 5 Ganjil-PPT Neraca Massa Dan Energi-Sistem MultifasaDokumen39 halamanKelompok 5 Ganjil-PPT Neraca Massa Dan Energi-Sistem MultifasaRetta Emelda 2007110685Belum ada peringkat
- Transformasi Zat Murni - Fisika KimiaDokumen22 halamanTransformasi Zat Murni - Fisika KimiaFauzan Van Isnanda LfcBelum ada peringkat
- Sifat ThermoDokumen17 halamanSifat ThermoFaizaBelum ada peringkat
- Diagram Fase Zat MurniDokumen19 halamanDiagram Fase Zat Murnilisa andrianiBelum ada peringkat
- Hukum FaseDokumen42 halamanHukum Faselilik suprianti100% (4)
- Kesetimbangan Fasa Satu Komponen (Air Dan Karbondioksida)Dokumen20 halamanKesetimbangan Fasa Satu Komponen (Air Dan Karbondioksida)Nikke Ardilah0% (1)
- 3 Perubahan Keadaan 1Dokumen36 halaman3 Perubahan Keadaan 1alifia aisyBelum ada peringkat
- Keseimbangan FasaDokumen33 halamanKeseimbangan FasaNadia TrianaBelum ada peringkat
- Kesetimbangan Fasa 2Dokumen34 halamanKesetimbangan Fasa 2Mira Homsatun100% (1)
- Laporan BMDokumen18 halamanLaporan BMvinaBelum ada peringkat
- DestilasiDokumen18 halamanDestilasijeonlix 13Belum ada peringkat
- Ringkasan TermodinamikaDokumen90 halamanRingkasan TermodinamikaFajar Satrio SatrioBelum ada peringkat