Ringkasan Termodinamika
Diunggah oleh
Fajar Satrio SatrioDeskripsi Asli:
Judul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Ringkasan Termodinamika
Diunggah oleh
Fajar Satrio SatrioHak Cipta:
Format Tersedia
http://riyanto04.wordpress.
com
BAB I
PENDAHULUAN
Termodinamika mempelajari energi dan perubahannya. Sifat-sifat zat dan
perubahannya karena transformasi energi.
Energi : - kemampuan untuk melakukan kerja atau perubahan
- tidak dapat diciptakan atau dihilangkan, hanya dapat dirubah bentuknya
(Hukum Utama I)
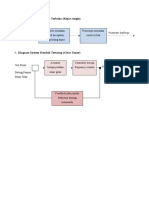
Engineering
Thermodynamics :
- First law
- Second law
- Properties of matter
Engineering Design of Thermodynamics
Process Devices & Systems
Other Engineering
Sciences :
- Heat Transfer
- Mass Transfer
- Momentum Transfer
- Chemical Kinetics
SOCIAL SCIENCES
HUMANITIES
Contoh : pembuatan listrik tenaga uap, sistem pendinginan
Energy : - stored energy
Energi kinetik
Energi potensial
Energi dalam (internal energy)
Energi kimia, ..dsb
- energy in transition
Panas (heat), kalor
Kerja (work)
http://riyanto04.wordpress.com
SISTEM dalam termodinamika merupakan daerah yang ditinjau perubahan
energinya.
sekitar / surrounding
Heat transfer
work
SISTEM
Boundary
(lapis batas)
Medium
(fluida kerja)
masa transfer
ISOLATED
SISTEM
NOT ISOLATED - INTERACTION
CLOSED
(m = konst.)
OPEN
Contoh : gas dalam tangki (c), holier (o).
BOUNDARY
FIXED
ELASTIC
Contoh : gas dalam tangki, silinder + torak
MEDIUM /
WORKING FLUID
Material yang menyerap/membuang/membawa energi selama terjadi proses.
Sifat-sifat Fisis Medium
Massa/mass
= kg
Gaya/force
= N (Newton)
Berat/Weight
= N (Newton)
Tekanan/pressure = Pa (N/m2)
http://riyanto04.wordpress.com
Cara menyatakan tekanan :
1. Absolut (Pabs)
2. Terukur/relative (Pgage)
Pgage = Pabs - Patm
Pvac = Patm Pabs
Tekanan di atas atm
Skala
Tekanan
Pabs
Prel
Tekanan atm
Pvacum
Patm
Tek.di bawah nol
Pabs
Massa jenis/density ()
= kg/m3
Berat jenis/specific weight
= N/m3
Volume jenis/specific volume
= m3/kg
Nol. abs
(Volume dari 1 satuan massa)
Temperatur indeks/ukuran dari aktivitas molekul.
P1 (rel) = ?
P1 (abs) = ?
A = Luas penampang pipa
Pengaruh gravitasi dari gas diabaikan; tekanan di setiap titik dalam tangki,
termasuk titik 1 adalah sama.
P1 = P2
(mendatar)
A . P1 = A. Patm + W
W
= m.g = Agh
P = P1 Patm = gh
P1 = Patm + gh
http://riyanto04.wordpress.com
h
Mercury h = ?
Mercury h = ?
T(K)
T(C)
-273,15
P (kPa)
ABSOLUTE
VACUM
V = Konstant
T (K)
= T ( C) + 273,15
T (R)
= T ( F) + 459, 67
T (R)
= 1,8 (K)
T ( F) = 1,8 ( C) + 32
C
100
K
373,15
C
212,0
K
671,67
0,01
273,16
32,02
491,69
-273,15
-459,67
Titik didih air pada
tek. 1 atm
TRIPLE POINT
OF WATER
Nol absolut
2
3
Jika T1
= T3
Dan T2
= T3
Maka T1 = T2
http://riyanto04.wordpress.com
SATUAN TERMODINAMIKA DALAM SI
Besaran
1. Panjang
2. massa
3. suhu
4. waktu
5. jumlah zat
6. jumlah kalori
7. gradien suhu
8. arus kalor
9. entropi
10. kapasitas kalori
11. kapasitas kalori spesifik
12. kapasitas kalori molar
13. koefisien konduksi
14. koefisien difusi
15. koefisien muai
16. konstanta boltzmann
17. konstanta gas umum
18. konstanta Stefan
19. konstanta wien
20. bilangan avogadro
Btu
Btu/1bm
Btu/1bm
1bf
1bm
1bf/m2
ft3/1bm
hp
R
kJ
kJ/kg
kJ/kgK
N
kg
kPa
m3/kg
kw
K
Lambang
l
m
t
T
Q
T
S
C
c
cm
a
,
k
R
c
NA
x 1,005056
2,326
4,1868
4, 448222
0, 453592
x 6, 894757
0, 062428
0, 7457
1/1,8
Nama satuan SI
Meter, m
Kilogram, kg
Sekon, detik
Kelvin, K
Mola, mol
Joule, J
K m-1
J s-1
J K-1
J K-1
J kg-1 K-1
J K-1 mol -1
J S-1 m -1 K-1
m2 s-1
K-1
J K-1
J K-1 mol -1
W m2 K-4
mK
-
http://riyanto04.wordpress.com
22
BAB II
SIFAT-SIFAT ZAT MURNI
(Properties of pure Substances)
1. Zat murni
2. Fase
3. Diagram sifat - diagram p.v.T
(P = tekanan, v = volume jenis, T = temperatur)
4. Tabel
5. Gas ideal
6. Faktor kompresibilitas .
1. ZAT MURNI ("pure substance"), zat yang mempunyai komposisi kimiawi
tertentu (tetap): water, nitrogen, helium dan CO2
N2
Vapor
AIR
Vapor
LIQUID
LIQUID
H2O
AIR
(a)
(b)
Nitrogen dan udara, zat murni
(a) Campuran dari air & uap adalah zat murni.
Campuran dari beberapa fase zat murni =
zat murni.
(b) Tetapi campuran dari air dan udara bukan
zat murni.
Catatan :
- udara terdiri dari beberapa gas, tetapi sering dianggap sebagai zat murni karena
mempunyai komposisi kimia "uniform"
- tetapi campuran oli dan air bukan zat murni
- campuran 2 atu 3 fase dari zat murni masih merupakan zat murni masih
merupakan zat murni : es + air
- tetapi cairan udara & gas (udara) bukan campuran zat murni
http://riyanto04.wordpress.com
22
2. FASE dari ZAT MURNI
SOLID
- padat
LIQUID
- cair
GAS
- gas
Identifikasi fase berdasarkan susunan molekulnya.
Padat
: Jarak antar molekul sangat dekat, gaya tarik antar molekul
sangat kuat, bentuk tetap.
Cair
: susunan molekul tidak berbeda jauh dengan zat padat, tetapi
posisi terhadap yang lain sudah tidak tetap lagi
Gas
: berjauhan - acak
Posisi tetap (solid)
: gaya tarik antara molekul-
molekul cenderung untuk mempertahankan
pada jarak yang relative konstan.
Pada temperatur tinggi : molekul melawan gaya
antar dan terpencar.
Liqiud
Sekumpulan
molekul-molekul
mengambang (float) satu sama lain.
Gas : Molekul-molekulnya berjauhan satu sama
yang lain (bergerak terhadap yang lain).
http://riyanto04.wordpress.com
22
PERUBAHAN FASE dari bahan murni
Contoh : "water" (tetapi untuk semua zat murni mempunyai kelakuan umum yang
sama), berlaku untuk zat yang lain.
v COMPRESSED LIQUID : Not about to vaporize
(SUBCOOLED LIQUID)
v SATURATED LIQUID : Is about to vaporize
(Cairan Jenuh)
v SATURATED LIQUID VAPOR
MIXTURE :
Liquid and vapor phases co exist in
equilibrium
v SATURATED VAPOR : Is about to condense
(Uap jenuh)
(kondensasi
mengembun)
v SUPERHEATED VAPOR : Not about to condense
(Uap panas lanjut)
http://riyanto04.wordpress.com
22
Bila selama proses-proses tersebut digambarkan perubahan-perubahan temperatur
& volume jenisnya "diagramT-v"
1-2-3-4-5 : Pemanasan, P=c
5-4-3-2-1 : Pendinginan, P=c
(P=c : Isobaris)
Tsat = saturation temperature, temperatur dimana zat murni mulai mendidih
Psat = saturation pressure, tekanan, zat murni (boil)
Tsat = f(Psat)
untuk air (water) :
= 1 N/m2
Psat = 101,35 kPa
1Pa
Tsat = 100 C
1bar = 105 Pa = 0,1 MPa = 100 kPa
1 atm = 101.325 Pa = 1.01325 bar
http://riyanto04.wordpress.com
"liquid - vapor saturation curve" : untuk air
"pressure cooker" : memasak dengan tekanan yang lebih tinggi daripada tekanan
atmosfer, Tsat > 100C
3. DIAGRAM SIFAT, untuk perubahan fase
1. diagram T - v
T : temperatur
2. diagram P - v
v : volume jenis
3. diagram P - T
P : tekanan
4. diagram P - v T
DIAGRAM T - v :
angka-angka tersebut berlaku untuk air
http://riyanto04.wordpress.com
22
Di atas temperature kritik, zat dianggap
sebagai Superheated vapor
http://riyanto04.wordpress.com
DIAGRAM P v :
Untuk air : Tar = 374,14 C
Par = 22,09 MPa
Var = 0,003155 m3/kg
22
http://riyanto04.wordpress.com
22
Diagram P v fase padat
Mengecil sewaktu
membeku
Mengembang
sewaktu membeku
http://riyanto04.wordpress.com
22
Diagram P - T
Pada PTR dan TTR; fase gas, cair dan
VAPOR
padat berada dalam keseimbangan.
(untuk air : TTR = 0,01o C
LIQUID
SOLID
PTR = 0,6113 kPa)
http://riyanto04.wordpress.com
22
PERMUKAAN P v - T
http://riyanto04.wordpress.com
22
4. TABEL SIFAT-SIFAT TERMODINAMIKA
Sebagai contoh akan dibicarakan tabel uap untuk zat lain "analog"
entalpi :
H = U + PV
(kJ),
atau
h = u + Pv
(kJ/kg) entalpi jenis
Cairan jenuh dan uap jenuh :
(Saturated liquid and saturated vapor)
indeks f = cairan jenuh (vf, hf ...)
g = uap jenuh (vg, hg , ...)
fg = beda antara harga cairan jenuh & uap jenuh
(vfg = vg - hf ; hfg = hg - hf; ...)
hfg = entalpi penguapan, jumlah energi yang diperlukan untuk menguapkan satu
satuan massa cairan pacta suatu temperatur & tekanan tertentu
P, T
hfg
dan pada titik kritis hfg = 0
http://riyanto04.wordpress.com
22
Cairan jenuh - campuran uap :
X : kualitas (quality)
X =
m Vapor
m Total
= massa
liq
= cair
vapor = uap
untuk campuran jenuh : campuran dari uap jenuh & cairan jenuh
m v = X.m t = X(m f + m g )
v = v f + x(v g v f )
= v f + x(v g f )
Suatu campuran di dalam tangki dengan kualitas X :
Uav = Uf + XUfg = U
hav = hf + Xhfg = h
y
= yf + Xyfg
5. PERSAMAAN KEADAAN GAS IDEAL
Persamaan keadaan: persamaan yang menghubungkan tekanan, temperatur dan
volume jenis dari suatu zat (sederhana/rumit)
gas vapor
- fase uap dari suatu zat biasanya disebut GAS jika berada diatas temperatur
kritis
- vapor (uap) : gas yang tidak jauh dari keadaan kondensasi
http://riyanto04.wordpress.com
22
* 1662 - Robert Boyle (Inggris), p
1
v
T
* 150 tahun kemudian - J. Charles & J. Gay Lussac (Prancis), P = R
V
Pv = RT (persamaan keadaan gas ideal)
P
: tekanan absolute tekanan terukur (tekanan relatif) + tekanan atmosfer
: temperatur absolut T(K) = T(oC) + 273;
T(R) = T(oF) + 460; T(R) = T(K) .1,8
: volume jenis
: konstante gas: udara,
R = 287 J/(kg.K)
helium, R = 2077 J/(kg.K)
argon,
R = 208 J / ( kg. K)
nitrogen, R = 296 J/(kg.K)
R=
Ru
M
Ru = konstanta gas umum = 8,314 kJ/(k.mol.K)
M = berat molekul (massa molekul)
m = MN
m
: massa
: jumlah molekul
= mv ,
PV = mRT
mR = (MN)R = NRu ,
PV = NRuT
V = Nv ,
Pv = RuT
v : volume jenis molekul (volume/sat.mol)
P1 V1 P2 V2
=
T1
T2
Pada tekanan rendah dan temperatur tinggi, rapat jenis gas dapat dianggap sebagai
gas ideal.
http://riyanto04.wordpress.com
22
V Videal
Percent error = tabel
x 100%
Vtabel
6. FAKTOR KOMPRESIBILITAS ( )
=
Pv
RT
Pv = RT
Atau =
v actual
,
v ideal
v ideal =
RT
P
Z = 1 (gas ideal)
PR =
P
; tekanan tereduksi
Per
TR =
T
; temperatur tereduksi
Ter
http://riyanto04.wordpress.com
22
Catatan :
1. PR << 1 (regardless temperature) : mendekati gas ideal
2. Temperatur tinggi (TR > 2) : mempunyai ketelitian yang baik tanpa
memperhatikan tekanannya, kecuali untuk PR >>1
3. Deviasi dari gas akan semakin besar, bila dekat dengan titik kritis.
http://riyanto04.wordpress.com
22
FAKTOR Z
http://riyanto04.wordpress.com
22
7. PERSAMAAN KEADAAN
1. VAN DER WAALS (1873)
(p +
a
) (v b) = RT
v2
27R 2 T 2 er
64Per
RTer
b=
8Per
a=
2. Beattie Bridgeman :
p=
RuT
c
A
(1
)(
v
+
B)
v2
vT 3
v2
a
A = Ao(1 )
v
B = Bo(1
B
);
v
Ao, Bo, a, b, c tabel 299
3. Benediet Webe rubin genedik
RuT
Co 1 bRuT a a 2
+ ( BoRuT Ao 2 ) +
+ 6
v
T v
v3
v
C
2 2
+ 3 2 (1 + 2 )e / v
vT
v
P=
http://riyanto04.wordpress.com
BAB III
HUKUM PERTAMA TERMODINAMlKA - SISTEM TERTUTUP
A. Pendahuluan
Hukum Pertama merupakan suatu pernyataan dari prinsip kekekalan
energi. "Energi tidak dapat diciptakan atau dirusak; tetapi hanya berubah bentuk".
Selama interaksi antara sistem dan sekelilingnya (surrounding) jumlah energi
yang didapat oleh sistem sama dengan jumlah energi , yang hilang dari
sekelilingnya. Energi dapat melintasi lapis batas (boundary) dari suatu sistem
tertutup berupa panas (heat) dan kerja (work); ini sangat penting untuk
membedakan dua hal tersebut :
Lapisan batas
(bourdary)
panas
Sistem tertutup
(m const)
kerja
1. Panas
Panas didefinisikan sebagai bentuk energi yang berpindah antara dua
sistem (atau suatu sistem dan sekelilingnya) yang dikarenakan perbedaan
temperatur. Arti dari istilah "panas (heat)" berbeda dengan yang dipergunakan
sehari-hari. Di dalam kehidupan kita sehari-hari panas sering digunakan untuk
mengartikan tenaga dalam (internal energy): kandungan panas dari bahan
bakar, kenaikan panas, burung menyimpan panas di badannya, ... dsb.
Di dalam termodinamika, panas dan tenaga dalam adalah dua hal yang
berbeda; energi adalah suatu sifat tetapi panas bukan sifat. Suatu benda
mengandung energi tetapi bukan panas. Energi berhubungan dengan suatu
keadaan; panas berhubungan dengan proses.
23
http://riyanto04.wordpress.com
24
Panas adalah suatu energi dalam transisi; hal ini dikenal hanya bila energi
melintasi suatu lapis batas sistem. Misalkan dalam gambar di atas ini (kentang
bakar yang panas); kentang ini mengandung energi dan energi ini disebut panas
hanya hila energi ini melintasi kulit kentang (sebagai lapis batas sistem) untuk
mencapai udara di sekitarnya. Ketika mencapai sekelilingnya, panas ini
menjadi bagian dari tenaga dalam dari sekelilingnya. Maka dalam
termodinamika istilah panas berarti heat transfer.
Dalam suatu proses dimana tidak ada perpindahan panas disebut proses
adiabatis.
Ada 2 cara untuk mendapatkan proses adiabatis : pertama, sistem diisolasi
sehingga jumlah panas yang dapat melewati lapis batas bisa diabaikan; kedua,
sistem dan sekeliling mempunyai temperatur yang sama sehingga tidak ada
gaya gerak (driving force) untuk memindahkan panas. Meskipun dalam proses
ini tidak ada perpindahan panas, kandungan energi dan temperatur dari . sistem
masih dapat berubah oleh hal yang lain misalnya karena kerja.
Karena panas adalah salah satu bentuk dari energi, maka satuannya adalah
satuan energi kJ (atau Btu). Panas yang masuk ke sistem adalah positif dan
yang keluar negatif. Sehingga setiap perpindahan panas yang menaikkan energi
dari suatu sistem adalah positif dan yang mengurangi energi dari suatu sistem
adalah negatif.
2. Kerja Kerja, seperti panas, adalah interaksi energi antara suatu sistem dan
sekelilingnya. Seperti telah disebutkan sebelumnya bahwa energi dapat
melintasi lapis batas sistem dalam bentuk panas dan tenaga. Sehingga jika
http://riyanto04.wordpress.com
25
energi yang melintasi lapis batas sistem bukan panas maka energi tersebut
berupa kerja.
Pengenalan panas adalah mudah: gaya geraknya adalah perbedaan temperatur
antara sistem dan sekelilingnya. Maka dapat dikatakan bahwa suatu interaksi
energi yang tidak disebabkan oleh perbedaan temperatur antara sistem dan
sekelilingnya adalah kerja.
Kerja adalah suatu bentuk tenaga seperti panas, maka satuannya adalah satuan
energi, seperti kJ. Kerja tiap satuan waktu disebut power (kJ,/s atau kW). Kerja
yang dihasilkan oleh suatu sistem dipandang sebagai sesuatu yang diharapkan,
berakibat positif, dan konsumsi kerja oleh suatu sistem dipandang sebagai
suatu yang tidak diharapkan, berakibat negatif. Berdasarkan filosofi ini maka
aturan pemberian tanda untuk kerja adalah sebagai berikut : Kerja yang
dilakukan oleh sistem adalah positif dan yang diberikan pada sistem adalah
negatif. Tenaga dari suatu sistem berkurang bila ia melakukan kerja dan
bertambah bila kerja dikenakan pada sistem.
Panas dan kerja adalah interaksi antara suatu sistem dan sekelilingnya, dan
diantara keduanya ada kemiripan antara lain:
- Keduanya teramati pada lapis batas dari sistem sewaktu merekamelewatinya.
Sehingga keduanya disebut fenomena lapis batas (boundary phenomena)
- Sistem mempunyai energi, tapi bukan panas atau kerja. Sehingga panas dan
kerja, adalah fenomena transisis (transient phenomena)
- Keduanya berhubungan dengan suatu proses, bukan pada suatu keadaan
(state).
Tidak seperti sifat-sifat (properties), panas dan kerja tidak mempunyai arti
pada suatu keadaan.
-
Keduanya merupakan fungsi lintasan, yaitu "besarnya" tergantung pada
lintasan yang dilalui selama proses berlangsung.
Fungsi lintasan mempunyai diferensial tak tentu yang diberi simbol dengan ;
maka penulisan Q dan W sebagai pengganti dQ dan dW.
http://riyanto04.wordpress.com
26
Sifat-sifat adalah fungsi titik (point function), yaitu hanya tergantung pada
keadaannya saja, dan tidak tergantung bagaimana suatu sistem mencapai
keadaan tersebut; mereka mempunyai diferensial tertentu dengan simbol d.
Misalkan perubahan kecil dari volume adalah dV dan perubahan total volume
selama proses antara keadaan 1 dan 2 adalah
dv = v 2 v1 = v
(perubahan volume selama proses 1-2 adalah volume pada keadaan 2 dikurangi
volume pada keadaan 1, tanpa memperhatikan lintasan prosesnya; lihat gambar
di bawah ini)
Tetapi kerja total selama proses 1-2 adalah :
w = w 12
(bukan W); di sini kerja total didapat dengan mengikuti lintasan dari proses.
Integral dari dari W tidak sama dengan W2 W1 (kerja pada keadaan 2
dikurangi kerja pada keadaan 1), yang tidak mempunyai arti karena kerja
bukanlah suatu sifat (property) dan sistem tidak mempunyai kerja pada suatu
keadaan.
3. KEADAAN SEIMBANG : suatu sistem dalam keadaan seimbang bila tidak ada
kecenderungan dari sistem untuk berubah secara
mendadak
http://riyanto04.wordpress.com
27
"internal equilibrium" : untuk sistem terisolasi
"external equilibrium": untuk "closed system"
B. Proses: perubahan sistem dari suatu keadaan ke keadaan yang lain
-
Reversible
Ir-Reversible
Proses
: perubahan keadaan, perubahan sifat fisis, tidak tergantung dari
cara perubahannya, dihitung berdasar titik-titik pada ujungnya, "PATHFUNCTION".
Jumlah kerja/work clan panas/heat, tergantung dari prosesnya atau lintasan
proses "PATH FUNCTION".
Proses sederhana pada sistem tertutup (massa konstan), antara lain:
PROSES VOLUME KONSTAN (isovolume / isokoris) :
vol. spesifik terakhir = vol. spesifik awal proses misalnya:
- Pendinginan uap air jenuh di dalam sebuah tangki tertutup
T
200 C
200 C
- Pemanasan udara di dalam ruangan tertutup
udara
v2 = v1
Cv konstan
V2 = V1
http://riyanto04.wordpress.com
28
- Pemanasan air jenuh di dalam sebuah tangki tertutup
T
2
v2 = v1
1
PROSES TEKANAN KONSTAN :
tekanan akhir sistem = tekanan mula-mula (ISOBARIS)
misalnya :
- ekspansi gas nitrogen di dalam silinder berpiston
P 1 = P2
N2
1
- Pendinginan campuran air dan uap air sehingga menjadi air jenuh
T
P=k
2
1
P2 = P1
http://riyanto04.wordpress.com
29
PROSES TEMPERATUR KONSTAN (ISOTERMIS)
Tawal = Takhir
misalnya :
ekepansi/kompresi gas di dalam silinder berpiston
T
P2
P1
PROSES ADIBATIS : tidak ada perpindahan panas melewati batas sistem
(tioundary)
Misalnya :
~ ekspansi/kompresi gas di dalam silinder yang berpiston
1-2 : isentropis (adiabatis reversibel)
1-2 : isotermis
W(kerja) 1-2 > W 1-2
http://riyanto04.wordpress.com
30
PROSES ENERGI DALAM KONSTAN : proses perubahan keadaan
sistem tanpa per pindahan panas & tanpa kerja.
P Vn = konstan
U2 =U1
- proses isotermis, T = c, n = 1
- proses isobaris, p = c
- proses isovolum, v = c
- proses adiabatis. n = k =
cp
cv
- proses politropis, n = n
- luasan di bawah proses reversibe 1 pada diagram p-v adalah kerja
- luasan di bawah proses reversibel pada diagram T-e adalah panas
C. Hukum I Termodinamika (sistem tertutup)
Transfer energi total yang kenaikan/penurunan dari/ke sistem yang berupa =
energi total dari panas & kerja system.
Q W = E (kJ)
q - W = e (kJ/kg)
q w = de (kJ/kg)
Q = transfer panas total yang melewati lapis batas (boundaries)
= (Qin - Qout )
W = kerja total dalam segala bentuk
= (wout win )
E = perubahan energi dari sistem = E2 E1
http://riyanto04.wordpress.com
31
E = U + KE + PE
U
= internal energy
KE = kinetik energy
PE = Potensial energy
E = U + KE + PE
sehingga :
Q W = U + KE + PE
U
= m(u2 u 1 )
KE =1/2m (v 22 v12 )
PE = mg(Z2 Z1 )
~ Untuk stationary closed system :
Z1 Z2 PE = 0
V1 V2 KE = 0
E = U
Sehingga :
Q W = U
~ Untuk Cyclic Process: (kondisi akhir = kondisi awal)
E2 = E1
E = E2 - E1= 0
Sehingga :
Q-W=O
(kJ)
http://riyanto04.wordpress.com
32
Qnet = Wnet
Contoh-contoh :
2 kJ
2 kJ
1 kJ
Qin = 20 kJ
- jumlah panas yang masuk :
Qin = 20 kJ
- jumlah panas yang keluar
Qout = (1 + 1 + 2) kJ
- kerja : W = 0
Jadi perubahan energi dari sistem :
E = Q W = Qin Qout
= 16 kJ
http://riyanto04.wordpress.com
33
Sebuah tangki yang kaku, volumenya dibagi dua sama besar dan diberi pemisah.
Volume bagian bawah berisi air dengan tekanan 200 kPa, 25C sebanyak 5 kg.
Bagian atas kosong. Kemudian pemisah dihilangkan sehingga air tersebut
berekspansi ke atas. Karena ada perpindahan panas dengan seke1ilingnya.,
temperatur air kembali menjadi 25C.
Tentukan :
a. volume tangki
b. tekanan tangki
c. perpindahan panasnya
Penyelesaian:
a. - Kondisi awal dari air, compressed liquid karena tekanan 200 kPa > tekanan
jenuh pada 25 C (3.169 kPa)
- v1 v f pada 25oC = 0,001003 m3 /kg
http://riyanto04.wordpress.com
34
(vf : volume jenis pada cairan/air jenuh)
sehingga
volume awal, V1= mv1 = 5 x 0,001003 = 0,005 m3
volume tangki keseluruhan = 2 x 0.005 = 0.01 m3
b. Kondisi akhir : v 2 =
v 2 0,01 m 3
=
= 0,002 m 3 /kg
m
5 kg
pada 25C : vf = 0,001003 m3/kg
vg = 43,36 m3/kg
vf < v2 < vg : kondisi akhir berupa campuran jenuh air uap air.
Sehingga tekanannya (tekanan akhir) = tekanan jenuhnya
P2 = Psat pada 25C = 3,169 kPa.
c. Q W = U + KE + PE
(perubahan energi kinetik & energi potensial diabaikan)
Q = m (u 2 u1)
u1 u f t = 25C = 104,88 kJ/kg
x2 =
v 2 v f 0,002 0,001
=
= 2,3 x 10 5
v fg
43,36 0,001
u 2 = u f + x 2 u fg
= 104,88 kJ/kg + (2,3 x 10 -5 ) (2304,9 kJ/kg)
= 104,93 kJ/kg
Q = (5 kg) (104,93 - 104,88) kJ/kg = 0,25 kJ
(+ ) : panas ditransfer ke air
D. Panas Jenis (spesifik heat)
membutuhkan jumlah panas yang berbeda, tergantung bahannya "energy
storage capabilities" sifat bahan.
http://riyanto04.wordpress.com
35
spesific heats : heat capacity
(kapasitas air 1)
Energi yang dibutuhkan untuk menaikkan temperatur 1 derajat oleh 1
satuan massa zat
(m = 1 & AT = 1).
Tergantung prosesnya
Proses volume konstan
Proses tekanan konstan
Cv
Cp
Panas jenis untuk sistem tertutup
volume konstan kerja "boundary" (Wb = 0)
Hukum Utama I Termodinamika :
q Wo = dU
(Wo : kerja selain Wb )
( Wo ) : jumlah energi dan panas yang ditransfer ke system, dan dari definisi
( Wo ) : Cv dT.
sehingga
Cv dT = du
(v konstan ), atau
http://riyanto04.wordpress.com
36
u
Cv =
T v
Tekanan konstan identik
h
Cp =
T p
(Wb + U = h)
u
Cv =
T v
: perubahan internal energy terhadap temperatur pada volume
konstan.
h
Cp =
T p
Satuan
: Perubahan entalpi terhadap temperatur pada tekanan konstan
: kJ/(kgoC) atau kJ/kg.K
identik karena T(oC) = T(K)
Cv , Cp
: molar : kJ/(kmolC), kJ/(kmol.K)
Cv , Cp
: berubah terhadap tekanan dan temperatur, tetapi biasanya harganya
tidak benar.
U, h, c dari Gas Ideal
Gas Ideal
: Pv = RT
Joule, 1843 (eks)
: u = u(T)
h = u + RT
Definisi
: h - u + Pv
karena R : konstan, maka; u = u(T)
h = h (T) Cp = Cp (T)
u = u (T) Cv = Cv (T)
hanya fungsi T
: du = cv (T) dT
dh = cp (T) dT
Proses 1 2
: u = u 2 u 1 = C v (T) dT
2
h = h 2 h 1 = C p (T) dT
2
Dicari dulu Cv, Cp fungsi
T
http://riyanto04.wordpress.com
37
Pada tekanan rendah : sifat gas riil mendekati gas ideal, panas jenis hanya
tergantung dari temperature dan disebut ideal gas specific heats atau zero
pressure specific heats
(Cpo & Cvo)
tersedia tabel/grafik/persamaan analitisnya
Penggunaan data panas jenis gas ideal dibatasi pada tekanan rendah. Tetapi
dapat juga pada tekanan menengah dengan memperhatikan ketelitiannya, sifatsifat gas belum menyimpang jauh dari gas ideal.
Panas jenis dari gas dengan susunan mol.kompleks (molekulnya mempunyai 2
atau lebih atom) mempunyai harga yang lebih tinggi dan bertambah besar
terhadap temperatur.
Penentuan harga rata-rata dari C :
u 2 u1 = cv,av (T2 T1)
h2 h1 = cv,av (T2 T1)
http://riyanto04.wordpress.com
38
Tabel gas ideal, OK (zero Kelvin) sebagai kondisi acuan (reference)
U (0) = h (0) = 0
u = Cv.av. T
berlaku untuk semua jenis proses.
h = Cp.av. T
Entalpi : h = u + pv
H2 h1 = (u 2 u1) + v (P2-P1), V2 = V1 = V
h = u + Vp
(kJ/kg)
Biasanya Vp << u Vp dapat diabaikan.
Pada proses T = konstan (T = 0) : u = 0, maka
h2 h1 + V(P2 - P1)
Bila kondisi 1
2
: cairan jenuh (saturated liquid)
: compressed liquid.
Pada T yang sama
maka entalpi dari compressed liquid :
h p,T h f, T + Vf,T (P Psat )
http://riyanto04.wordpress.com
BAB IV
HUKUM PERTAMA TERMODINAMlKA (Sistem terbuka)
Pada sistem tertutup tidak ada aliran massa
yang melewati
"boundary"/batas. Dalam sistem terbuka dimungkinkan adanya aliran massa
tersebut.
C.V.
: Control volume
C.S.
: Control surface
* Water heater
* Car radiator
* Turbin
* Kompresor,
Fixed (bentuk + ukuran)
C.V
Moving (berubah)
- Steady
: tidak berubah terhadap waktu >< unsteady, transient
- Uniform
: tidak breubah terhadap tempat
39
http://riyanto04.wordpress.com
40
KEKEKALAN ENERGI (hukum 1)
Energi total
lewat boundary
sebagai panas &
kerja.
Energi total dari
massa yang
masuk C.V.
Energi total
dari massa
yang keluar
C.V.
Perubahan
energi di
dalam C.V.
P = tekanan fluida
F = gaya untuk mendorong fluida
A = luasan
L = jarak
V = Volume
V = volume jenis
F = P. A
W flow = F. L = ALP = PV
(kJ)
Wflow = Pv
* Hukum utama (I) untuk sistem terbuka, akan dibicarakan lebih lanjut pada
steady flow process.
http://riyanto04.wordpress.com
41
FLOW WORK: energi yang diperlukan untuk mendorong fluida masuk atau
keluar dari G.V. disebut flow work/flow energy, energi ini merupakan bagian dari
energi yang dibawa oleh fluida.
Dm = Vn dA
m = A . Vn dA
(kg/s)
m : laju aliran massa (mass flow rate)
p
: density .
Vn : komponen normal kecepatan terhadap dA
dA : luasan
m = p Vav A
(kg/B)
Vav : kecepatan rata-rata A
masa flow ratenya
sama.
laju aliran volum : V = A Vn dA = Vav A (m3/s)
m = v& =
&
V
V
sederhana; V : penampang & rata-rata
A : aliran
untuk aliran stedi, min = mout
(pVA)in. = (pVA)out
pVA = konstan
http://riyanto04.wordpress.com
42
P = tekanan fluida
F = gaya untuk mendorong
fluida
A = luasan
L = jarak
V = volume
v = volume jenis
F = P.A
Wflow = F . L = ALP = PV (kJ)
Wflow = Pv
- Hukum Utama (I) untuk sistem terbuka, akan dibicarakan lebih lanjut pada
"steady flow process".
http://riyanto04.wordpress.com
V. HUKUM II TERMODINAMIKA
Hukum I
: energi terkonservasi selama proses
Hukum II
: proses terjadi pada arah tertentu
Suatu proses tak akan terjadi bila tidak memenuhi kedua; hukum tersebut.
Contoh:
-
air panas diletakkan dalam ruangan dingin
akan menjadi dingin.
Proses ini memenuhi Hukum I karena
energi yang hilang dari air panas akan
sama dengan energi yang diterima oleh
udara dingin sekelilingnya.
- bila proses dibalik, air panas menjadi semakin panas karena ada energi dari
udara dingin.
Hal ini memenuhi hukum I, jumlah energi yang diterima oleh air panas sama
dengan yang diberikan oleh udara. Tetapi hal ini tidak mungkin terjadi.
Proses terjadi pada arah tertentu (Hukum II)
Terdapat banyak pernyataan-pernyataan tentang Hukum II Termodinamika, tetapi
di sini hanya akan diberikan beberapa pernyataan yang ada hubungannya dengan
peralatan yang beroperasi secara siklus (Kelvin Planck dan Clausius).
Sebelumnya akan dibicarakan lebih dulu tentang :
- THERMAL ENERGY RESERVOIR
- HEAT ENGINES
- REFRIGERATORS & HEAT PUMPS
43
http://riyanto04.wordpress.com
44
THERMAL ENERGY RESERVOIR: benda yang mempunyai kapasitas energi
panas (massa x panas jenis) relatif besar
yang
mampu
menyerap/memberikan
sejumlah energi panas tanpa mengalami
perubahan temperatur.
misalnya:
* air dalam jumlah yang sangat besar : laut, danau, sungai
* udara atmosfer
* two-phase system : dapat menyerap/melepaskan panas dengan T = konstan
* industrial furnace
SOURCE
: reservoir yang memberikan energi
SINK
: reservoir yang menyerap energi
Contoh sebuah heat engine (steam power plant)
P : pompa
B : boiler
T : Turbin
C : kondensor
Win
Qin
Wout
Qout
(kJ)
http://riyanto04.wordpress.com
45
Secara keseluruhan : - closed system
- siklus u = 0, sehingga
W net, out= Qin. - Qout
Efisiensi termal = th =
Wnet,out
Q in
= 1
Qout
Q in
HEAT ENGINES: mesin yang mengubah panas menjadi kerja
kerja panas (mudah)
panas kerja (sulit)
Karakteristiknya:
- mesin menerima panas dari sumber/source bertemperatur sangat tinggi (solar
energy, oil furnace. nuclear reactor, ...)
- mesin mengkonversi sebagian panas menjadi kerja, biasanya dalam bentuk
putaran poros.
- membuang sisa panas ke reservoir bertemperatur rendah (sink, misalnya :
atmosfer, sung ai, ...)
- beroperasi secara siklus
http://riyanto04.wordpress.com
46
"Cyclic devices such as steam power plants cannot run continously unless the
cycle is completed"
(1) gas dipanaskan 100 kJ dari reservoir pacta 100C
(1) (2) : gas berekspansi
(2) piston sampai di atas, beban dihilangkan Temperatur gas diamati 90C
Kerja ekspansi : untuk menaikkan energi potensial (misalnya 15 kJ)
Jumlah panas yang diberikan ke gas lebih besar daripada jumlah kerja karena
sebagian panas dipakai untuk menaikkan temperatur gas.
Untuk proses selanjutnya, mungkinkah memindahkan kelebihan panas (85
kJ). pada temperatur 90~C ke dalam reservoir pada temperatur 100C?
Bila mungkin, efisiensi termis 100 % tidak mungkin (panas dari
temperatur yang tinggi ke yang rendah)
(3) Panas harus dibuang ke reservoir dengan temperatur lebih rendah "waste
energy".
Every heat engine must waste some energy by transfering it to a low
temperature reservoir in order to complete the cycle, even under idealized
conditions.
http://riyanto04.wordpress.com
47
Hukum II Termodinamika :
pernyataan dari Kelvin Planck:
"it is impossible for any device that operate on a cycle to recieve heat from a
single reservoir and produce an equivalent amount of work"
"no heat engine can have a thermal efficiency of 100 percent", atau
"for a power plant to operate, the working fluid must exchange heat with the
environment as well as the furnace" .
REFRIGERATOR & HEAT PUMPS
- Panas berpindah dari T >> ke T << (alami)
- hila Q dari T << ke T >> (perlu alat, misal : refrigerator, fluida kerja/refrigerant)
http://riyanto04.wordpress.com
48
1 2 : Proses
2 3 : .
3 4 : .
4 1 : .
- magnitudenya:
QL : dari TL
QH : ke TH
COP = coefficient of performance (efisiensi)
COPR.: refrigerator
COPHP : heat pump
- refrigerator: mengambil panas {QL) dari ruang yang diinginkan dan
mempertahankan ruangan dingin
- heat pump: mempertahankan ruangan hangat
(keduanya mempunyai siklus yang sama).
(desired)
output
QL
COPR =
=
input
Wnet,in
(required)
COPR =
QL
Wnet,in
Konservasi energi :
Wnet,in = QH QL
sehingga COPR =
( kJ )
QL
1
=
QH Q L Q H
1
QL
(COPR dapat > 1) bila panas yang diserap dari ruangan dingin dapat > daripada
kerja yang diberikan.
http://riyanto04.wordpress.com
49
SIKLUS CARNOT (sadi CARNOT, 1824)
"heat power cycle"
proses-proses (reversible), fluida kerja gas
1 2 : komprewsi kemitropik
2 3 : panas masuk
3 4 : ekpansi kemotropik
4 1 : panas keluar
=
Q H - QL
QH
QH : panas yang diterima pada temperatur TH
QL : panas yang dikeluarkan pada temperatur TL
Proses-proses tersebut Reversibel, siklus Carnot dapat dibalik menjadi siklus heatpump/Refrigerasi dari Carnot.
COP =
QL
QH - QL
http://riyanto04.wordpress.com
50
Skala temperatur dari Kelvin (1848) :
dari siklus Carnot ;
TH Q H
=
TL
QL
Ketidaksamaan Clausius ; =
=
Q H - QL
QH
TH - TL
TH
Ketidaksamaan Clausius
Dari pers.
TH Q H
=
, ditulis sebagai
TL
QL
- QL QH
=
;
TL
QH
(-) = panas yang keluar
QH
Q
+ L = 0 perubahan
TH
QL
Q
T dalam siklus Reversibel carnot 0
Clasius, untuk setiap proses siklus berlaku :
= 0 siklus reversible
Q
< 0 <
T
< 0 Irrevesibel
Q
Q
Karena jumlah dari untuk siklus ini reversibel = 0, maka adalah
T
T
sama untuk setiap proses reversible antara 1 s/d 2 dari sebuah sistem.
Q
T adalah "property of the system"
Sifat ini disebut dengan entropi (perbandingannya antara panas yang di-transfer
selama proses reversibel dibagi dengan temperatur absolut dari sistem.
Q
ds =
T REV
Q
s =
T
REV
Tds = Q : luasan dalam diagram T-s dari proses reversibel menunjukkan
besarnya panas yang ditransfer selama proses.
Bila prosesnya IRReversibel, tidak menunjukkan besarnya panas.
http://riyanto04.wordpress.com
51
pada sistem 27C, Q = 60 kJ
s sistem =
60.000 J
= 200 J/k
300 K
SSURRoundin g =
+ 60.000 J
= 0,2 kJ/K
300 K
Suniverse = Ssistem + Ssur = -0,2 kJ/K + 0,2 kJ/K
Suniverse = 0
Clausius
Suniv 0
<
= untuk proses reversibel
> untuk proses IRReversibe
"Unavailable energy" .
Qs = Qa + Qu
Qs : panas yang diberikan
Qa : "available energy" yang dikonversi menjadi kerja
Qu : "unavailable energy"/energy rejected
Dari skala Kelvin:
Q u Qs
=
Tu
Ts
Q u = Tu
atau
Qs
Ts
Tu : temperatur dimana panas dibuang
Ts : temperatur dimana panas diberikan
Q u = Tu
Qs
Ts
Q u = Tu .s
Panas yang
dibuang
Index of unavailable
energy
http://riyanto04.wordpress.com
VI. THERMODYNAMIC PROPERTY RELATIONS
How some unknown properties can be determined from limited
available data.
t
V
m
v
u
h
g
dapat diukur langsung
ditentukan dengan persamaan sederhana
tidak dapat diukur langsung
1. PERSAMAAN MAXWELL
Hubungan P
v
Untuk zat yang mampu mampat dalam bentuk diferensial
t
parsial, didapatkan dari 4 persamaan Gibbs :
s
du = Tds - Pdv
. . . . . .. (1)
dh = Tds + vdP
. . . . . .. (2)
a = u Ts
. . . . . .. (3)
g = h Ts
. . . . . .. (4)
persamaan 3 & 4
da = du - Tds - sdT
dg = dh - Tds - sdT
persamaan 1 & 2
da = - sdT - p. dv
. . . . . .. (5)
dg = - sdT - v - dp
. . . . . .. (6)
Persaman tersebut analog dengan bentuk :
dZ = M dx + N dy
. . . . . .. (7)
M
N
dengan
=
y x x y
. . . . . .. (8)
52
http://riyanto04.wordpress.com
53
Berdasarkan analogi bentuk persamaan 7 & 8. maka dari persamaan:
T
P
(1) =
v s
s v
. . . . . . (9)
T
(2) =
P s
v
s
P
. . . . . ..(10)
s
(3) =
v T
P
T
v
. . . . . ..(11)
s
v
(4) =
P T
T v
. . . . . ..(12)
PERSAMAAN MAXWELL: -limited to simple compressible system
-menentukan
perubahan
entropi
dengan mengukur perubahan p,v,T.
2. PERSAMAAN CLAPEYRON
Menentukan perubahan entalpi.
Dari persamaan ke-3 Maxwell (persamaan 11) yang digunakan pada perubahan
fase
P
dP
Psat = f (Tsat ) =
T v dT sat
P
T : - konstan pada P & T yang konstan
sat
- tidak tergantung pada v
http://riyanto04.wordpress.com
54
dP
Persamaan 11 dapat diintegralkan dengan harga konstam
dT sat
antara 2 kondisi jenuh (misal f & g) pada temperatur yg sama.
dP
S g S f = (v g v f )
dT sat
S fg
P
T = V
sat
fg
atau
. . . . . ..(13)
. . . . . ..(14)
dh = T ds + v dP = 0
dh = T ds
g
hf g
P
T = Tv
sat
fg
hf g = T Sf g
dari persamaan (14)
. . . . . ..(15)
(persamaan Clapeyron)
atau:
h 12
dP
dT = Tv
sat
12
. . . . . ..(16)
3. PERSAMAAN CLAPEYRON CLAUSIUS
Pendekatan:
Pada p rendah Vg >> Vf
Vapor dianggap gas ideal
dimasukkan ke persamaan 15 :
Ph f g
dP
dT = RT 2
sat
atau
h f g dT
dP
=
dT
R T 2 sat
sat
Untuk T kecil
hf g 1
P
1
in 2 =
R T1 T2
P1 sat
sat
(persamaan Clapeyron-Clausius)
- vapor - solid hfg hig
. . . . . ..(16)
http://riyanto04.wordpress.com
55
4. PERUMUSAN du, dh, ds, Cv & Cp
a. Perubahan Internal Energi (du)
Diferensial total dari internal energi yang fungsi dari temperatur dan volume
jenis dapat ditulis sebagai berikut :
u
u
du = dT +
T v
v T
dari definisi Cv,
u
du = C v dT + dv
v T
. . . . . .. (18)
Sedangkan diferensial total dari entropi mempunyai bentuk:
s
s
ds = dT + dv
T v
v T
. . . . . .. (19a)
Persamaan ini disubstitusikan ke persamaan internal energi :
du = T ds - P dv
s
s
du = T dT + T P dv
T
v T
. . . . . .. (19b)
persamaan (18) = (19)
Cv
s
T = T
v
. . . . . (20)
u
s
T = T v P
T
T
. . . . . .. (21)
persamaan (21) dimasukkan ke persamaan Maxwell (ke-3) :
u
P
v = T T P
T
v
. . . . . .. (22)
kemudian dimasukkan ke persamaan (18) menjadi :
P
du = C v dT + T P dv
T v
. . . . . .. (23)
http://riyanto04.wordpress.com
56
Perubahan energi dalam dari sebuah sistem kompresibel (18) sederhana,
T2
v 2 P
u 2 u 1 = C v dT + T P dv
T1
v1
T v
. . . . . .. (23)
b. Perubahan entalpi dh
Dengan cara yang sarna dengan perubahan internal energi dipilih entalpi
merupakan fungsi dari T dan P dan bentuk diferensial totalnya adalah :
h
h
dh = dT + dP
T P
P T
dari definisi CP persamaan tersebut menjadi.
h
dh = C P dT + dP
P T
. . . . . .. (24)
dipilih entropi fungsi dari temperatur dan tekanan, maka :
s
s
ds = dT + dP
T P
P T
. . . . . .. (25)
persamaan (25) disubstitusikan ke persamaan perubahan entalpi didapatkan :
s
s
dh = T dT + T - v dP
T P
P T
. . . . . .. (26)
persamaan (24) = (26)
CP
s
T = T
P
. . . . . .. (27)
h
P = P - v
T T
. . . . . .. (28)
dari persamaan Maxwell ke-4 dan persamaan. (28) :
h
v
P = v T T
T
P
disubstitusikan ke persamaan (24) :
v
dh = C P dT + v T dP `
T P
. . . . . .. (29)
http://riyanto04.wordpress.com
57
"simple compressible system"
T2
P2
v
h 2 h 1 = C P dT + v - T dP
T1
P1
T P
. . . . . .. (30)
Bila (U2 - U1) sudah diketahui, maka : h = u + Pv
h2 h1 = (u2 u1 ) + (P2 v2 P2 v2 )
. . . . . .. (31)
C. PERUBAHAN ENTROPI
"simpel compressible system"
Cara 1 :
s
s
Persamaan 19 a : ds = dT + dv
T v
v T
disubstitusikan ke persamaan Maxwell ke-3 :
ds =
Cv
P
dT + dv
T
T v
dan s 2 s1 =
T2
T1
v 2 s
Cv
dT + dP
v1
T
T T
. . . . . .. (32)
. . . . . .. (33)
Cara 2 :
s
s
persamaan 25 : ds = dT + dP
T P
P T
disubstitusikan ke persamaan Maxwell ke-4 :
ds =
CP
v
dT dP
T
T P
s 2 s1 =
T2
T1
P2 v
CP
dT + dP
P1
T
T P
d. SPECIFIC HEAT CV & CP
Untuk gas ideal, C = C (T) ;
pure substance C = C (v, P, T)
pada tekanan rendah, gas dapat berkelakuan seperti gas ideal.
Cvo
Zero pressure specific heat
Cpo
. . . . . .. (34)
. . . . . .. (35)
http://riyanto04.wordpress.com
58
pada tekanan yang lebih tinggi ?
dZ = M dx + N dy
N
M
=
persamaan 8 :
x y y x
persamaan 32 : ds =
Cv
P
dT + dv
T
T v
persamaan 34 : ds =
CP
v
dT dT
T
T P
dari persamaan-persamaan tersebut menghasilkan :
dan
C v
2P
=
T
v
T 2
v
T
. . . . . .. (36)
C p
2v
= T 2
T p
P T
. . . . . .. (37)
Untuk menghitung deviasi Cp dari Cpo terhadap temperatur digunakan
persamaan 37 :
p 2v
(C p C po ) T = T 2 dP
o T
. . . . . .. (38)
HUBUNGAN Cp & Cv
persamaan 32 : ds =
Cv
P
dT + dv
T
T v
persamaan 34 : ds =
CP
v
dT dP
T
T P
dT =
T (v/T) p
T (P/T) v
dv +
dp
Cp Cv
Cp Cv
. . . . . .. (39)
http://riyanto04.wordpress.com
59
dipilih temperatur fungsi dari tekanan dan volume jenis,
T
T
dT = dv + dP
v p
P v
. . . . . .. (40)
persamaan 39 = 40
v
C p C v = T
T p
P
T
v
. . . . . .. (41)
atau :
P T v
dari persamaan = 1
T v v p P T
P
v
T = T
v
p
P
v
T
disubstitusikan ke persamaan (41) didapat,
v
C p C v = T
T p
2
P
v
T
. . . . . .. (42)
atau :
definisi : = volume expansivity =
1 v
4 T p
= isothermal compressibility =
1 v
4 P T
. . . . . .. (43)
. . . . . .. (44)
substitusi persamaan (43) & (44) ke persamaan (42) :
Cp Cv =
v T 2
. . . . . .. (45)
http://riyanto04.wordpress.com
60
Beberapa hal yang dapat disimpulkan dari persamaan 45 :
Cp Cv =
v T 2
1. > 0 (untuk semua benda, fase)
< 0 (untuk benda.tertentu) , 2 > 0
T>0
sehingga: Cp Cv 0
Cp Cv
2. (Cp Cv ) 0 bila T 0
3. Cp dan Cv identik untuk ,. incompressible" karena v konstan
diagram T - P
fluida masuk : P1 ,T1 (tetap)
fluida keluar : P2 ,T2 (berubah) dengan cara mengganti ukuran "porons-plug".
diukur
http://riyanto04.wordpress.com
61
- supaya temperatur menurun selama proses throttling, maka proses harus
berlangsung di sebelah kiri inversion line.
- tidak ada efek pendinginan bila proses throttling berlangsung di atas "maximum
inversion temperature"
JOULE - THOMSON COEFFICIENT
Koefisien Joule-Thomson:
T
=
P h
<0:T
=0:T=k
<0:T
(perubahan temperatur terhadap tekanan selama proses h = tetap)
"slope dari lengkung h = konstan dalam diagram T - P = ?
Perubahan entalpi (persamaan 29) :
v
dh = Cp . dT + v T dP
T p
http://riyanto04.wordpress.com
62
throttling dh = 0,
1
T
P = = C
h
p
v
v T
T p
. . . . . .. (46)
h
u
GAS RIIL
s
Gas P rendah : - mendekati gas ideal
- u = u (T) ; Cv = Cv (T)
h = h (T) ; Cp = Cp (T)
P tinggi : - Pv = ZRT
h
u
s
a. h :
h = h (P,T)
T2
p2
v
persamaan 30 : h 2 h 1 = C p .dT + v T dP
T1
p1
T p
h property point function h tidak tergantung pada lintasan
proses.
http://riyanto04.wordpress.com
63
Perubahan dari keadaan 1 ke 2 dapat ditempuh lewat proses:
(1) 1 2
(2) 1 1* (isotermis)
1* 2* (isobaris)
2* 2 (isotermis)
p2
v
h 2 h 2 = 0 + v T
dP
p 2
T p T =T
p2
v
dP
= v T
0
T p T =T2
. . . . . .. (47)
h 2 h 1 = C p .dT + 0 = C po (T) dT
. . . . . .. (48)
T2
T2
T2
T1
p1
v
h 1 h 1 = 0 + v T dP
p1
T p T =T
1
p1
v
= v T dP
p0
T p T = T
(h2 h1) = (h2 h2 )+ (h2* - h1*) + (h1* - h1)
(h* - h)
. . . . . .. (49)
. . . . . .. (49a)
: - enthalpy departure
- perubahan entalpi gas terhadap tekanan pada temperatur tetap.
disubstitusikan ke persamaan 49 :
p1 ZRT
ZR Z T 2 R
T
(h * h) T =
dP
0
P T P P
P
p1 Z dP
= RT 2
0
T p P
Bila TR =
PR =
T
Tc r
P
Pc r
http://riyanto04.wordpress.com
Zh =
(h * - h) T
= TR2
R u Tc r
64
pR
d (in PR )
TR P R
. . . . . .. (50)
Zh = enthalpy departure factor
Persamaan 50 dapat dipresentasikan secara grafis (generalized enthalpy
departure chart) atau secara numeris.
Dengan mengganti h* dengan hideal, persamaan 50 dapat untuk menghitung h
selama proses 1 2 :
h 2 h 1 = R u Tcr (Z h1 Z h2 ) + (h 2 h 1 ) ideal
. . . . . .. (51)
h 2 h 1 = RTc r (Z h1 Z h2 ) + (h 2 h 1 ) ideal
. . . . . .. (52)
atau
RTc r (Z h1 Z h2 ) = 0 (gas ideal)
b. u :
Dicari dari h
u 2 u 1 = (h 2 h 1 ) - R u (Z 2T2 Z1T1 )
. . . . . .. (53)
c. s :
persamaan 35 : s 2 s1 =
T2
T1
P2 v
CP
dT + dP
P
1 T
T
P
cara integral seperti pada entalpi tidak dapat dilakukan (T1 = C P = 0 T2
= c) karena entropi P = 0 .
Dipakai cara berikut :
http://riyanto04.wordpress.com
65
s2 s1 = (s2 sb*) + (sb*- s2*) +(s2*- s1*) + (s1*- s2*) + (sa*- s1)
state
. . . . . .. (54)
1*
in the imagination: gas dianggap ideal
2*
1 & 1* identik (T1 = T1*)
2 & 2* identik (T2 = T2*)
Untuk mencari deviasi entropi pada kondisi (P, T) dapat dimisalkan proses
isotermal dari kondisi aktual (P*,T*) :
(sp sp*) T = (sp so*) T + (so*- sp*) T
p v
0 v
= dP dP
0 T
p T
p
p
dimana :
v=
ZRT
P
v* = v ideal
RT
P
atau :
p1 (1 - Z)R
RT Z
(s p s p *) T =
dP
0
P T P
P
bila T = TCR TR
P = PCR PR
"entropy departure factor" dapat di tulis
Zs =
PR
(s * s ) T.P
= Z 1 + TR
0
Ru
d(in PR )
TR PR
. . . . . .. (55)
( s * s ) T.P : "entropy departure"
Harga Zs "generalized entropy departure chart", yang dipakai untuk
menentukan besarnya deviasi dari entropi gas terhadap entropi gas ideal pada
(P,T) yang sama.
S* Sideal :
maka perubahan entropi selama proses 1 2 :
s 2 s1 = R u (Z s 1 Z s2 ) + (s 2 s1 ) ideal
. . . . . .. (56)
s 2 s1 = R u (Z s 1 Z s2 ) + (s 2 s1 ) ideal
. . . . . .. (57)
http://riyanto04.wordpress.com
BAB VII
CAMPURAN DARI GAS IDEAL & VAPOR
CAMPURAN GAS IDEAL :
Pada tekanan relatif rendah, gas murni yang terdiri dari suatu campuran
dapat dianggap sebagai gas ideal; sehingga dapat diperlakukan sebagai gas ideal
tunggal.
Pada persamaan-persamaan di bawah ini, indeks A, B, C, ...
menunjukkan jenis gas A, B, C, . dan seterusnya.
1. Hukum tekanan parsial dari Dalton:
Tekanan campuran dari gas A, B, C, ... merupakan jumlah dari masing-masing
tekanan, sehingga :
Pcamp = PA + PB + PC + .
(1)
Pcamp = tekanan campuran
PA, PB, PC, ...= tekanan parsial dari gas A, B, C. ... Tekanan parsial ini dihitung
pada volume dan temperatur carnpuran.
2. Hukum volume dari Amagat :
Volume campuran dari berbagai macam gas, merupakan jumlah dari masingmasing volume gas tersebut.
Vcamp = VA + VB+ VC + ..
(2)
Volume parsial VA, VB, VC, .. dihitung berdasarkan temperatur dan tekanan
dari campuran.
3. Massa (berat) carnpuran sarna dengan jumlah dari massa masing-masing
komponennya.
Wcamp = WA + WB + WC + .....
(3)
4. Jumlah molekul campuran sama dengan jumlah molekul masing-masing gas.
ncamp = nA + nB + nC +..
(4)
definisi:
ni
n mix
= xi
Xi = mole fraction dari komponen i
(camp)
66
http://riyanto04.wordpress.com
67
XA + XB + XC + .= 1
XA =
nA
n camp
XB =
nB
.dst
n camp
5. Berat molekul ekivalen dari campuran :
Mcamp = XA MA + XB MB + XC MC + ....
6. Konstante gas ekivalen dari campuran :
R camp =
Ro
M camp
Ro = konstanta umum gas
7. Dari persamaan (1), (2). dan (4) dapat ditulis :
Pi = Xi Pcamp
Vi = XiVcamp
8. Sifat-sifat lain dari campuran gas dapat dituliskan :
1. kapasitas panas:
C PCamp = C PA
WC
WA
WB
+ C PB
+ C PC
+ ....
Wcamp
Wcamp
Wcamp
2. entalpi :
h camp = h A
WC
WA
WB
+ hB
+ hC
+ ....
Wcamp
Wcamp
Wcamp
3. internal energy :
u camp = u A
WC
WA
WB
+ uB
+ uC
+ ....
Wcamp
Wcamp
Wcamp
ANALISA GRAVIHETRI & VOLUMETRI
Analisa campuran gas dapat berdasarkan volume atau beratnya. Jika
tekanan totalnya relatif rendah sehingga campuran gas dapat dianggap sebagai gas
ideal, maka persentasi volume dari masing-masing komponen ekivalen dengan
persentase "mole fraction" (Xi).
http://riyanto04.wordpress.com
68
CAMPURAN UDARA & UAP AIR
Pada tekanan rendah uap air mempunyai sifat-sifat seperti gas ideal,
sehingga pada tekanan ini uap air dapat dianggap sebagai gas ideal.
Pada umumnya uap di dalam campuran berupa uap panas lanjut (superheated) dan
untuk uap air entalpinya dimisalkan sama dengan entalpi uap air jenuh (saturated
water vapor) pada temperatur yang sama.
Jika uap air di dalam campuran keadaannya jenuh (saturated) maka campurannya
disebut campuran jenuh (saturated mixture).
Beberapa definisi untuk campuran udara dan uap air adalah:
* kelembaban relatif (Relatif humidity) :
=
tekanan parsial uap air
tekanan jenuh uap air pd temp. yang sama
Pw
Psat T
atau Pw = Psat
atau Vw =
Vsat
,
V = Volume jenis
* kelembaban jenis (specific humidity) = W atau perbandingan kelembaban
(humidity ratio) = HR
HR =
massa uap air
atau
massa udara kering pada volume yang sama
W =
kg uap air
1 kg udara kering
* "Dew point" : jika campuran uap air panas lanjut (superheated) dan udara
didinginkan pada tekanan total konstan (tekanan parsial uap air
konstan) sampai mencapai kondisi jenuhnya maka campuran
tersebut mencapai "dew point".
Kelembaban relatif pada "dew point" = 100 %, karena pada titik ini tekanan parsial
uap air (pw) = tekanan jenuhnya (psat).
=
pw
p
= sat = 1
p sat p sat
http://riyanto04.wordpress.com
69
* "wet bulb temperature" (temperatur bola basah) : untuk menentukan kandungan
uap air di dalam campuran uap air - udara dipakai alat "wet-bulb psychrometer".
Alat ini terdiri dari dua buah termometer. Satu disebut bola kering (dry-bulb), yang
lain disebut bola basah (wet-bulb) karena ditutupi oleh kain basah.
Proses ini disebut "adiabatic saturation".
W1 =
0,24 (t 2 t 1 ) + W2 h f g 2
h g1 h f 2
Indeks :
(1) : temperatur bola kering
(2) : temperatur bola basah
http://riyanto04.wordpress.com
BAB VIII
STEADY FLOW PROCESS
STEADY FLOW PROCESS: analisa teknik dari proses untuk sistem terbuka.
Proses-proses yang dijumpai dalam teknik sangat bervariasi, mulai dari
yang sangat sederhana sampai yang rumit. Dalam beberapa hal, proses yang rumit
dapat disederhanakan atau diuraikan menjadi bagian-bagian yang sederhana
(dengan pengandaian-pengandaian).
Hal yang perlu diketahui dalam steady flow process :
- selama proses, sifat-sifat fluida dalam volume kontrol (G.V) dapat berbeda
terhadap posisi, tetapi tetap konstan terhadap waktu.
- selama proses, kandungan massa & energi dari volume kontrol tidak berubah
terhadap waktu.
- selama proses, sifat-sifat fluida di inlet & outlet tidak berubah terhadap waktu.
70
http://riyanto04.wordpress.com
71
proses dengan perubahan sifat-sifat fluida secara periodis dapat dianalisa
sebagai "steady flow process".
Ad. 4
Konservasi massa :
m in m out =
dm
Laju perubahan massa dalam C.V
dt
Untuk sistem terbuka dengan kondisi "steady-state - steady-flow" :
m in m out
dm
dt = 0
Bila hanya 1 aliran masuk dan 1 aliran keluar :
(pVA)in = (pVA)out
atau :
pVA = konstan
= densitas
V = kecepatan rata-rata pada luasan A
(dalam mekanika fluida persamaan ini biasa disebut persamaan kontinuitas)
http://riyanto04.wordpress.com
72
"STEADY-STATE STEADY-FLOW DEVICES:
Sistem-sistem dalam bidang teknik yang menyangkut aliran antara lain:
- power plants: PLTU. PLTG.
- refrigeration plants
- air separation plants
- gas-liquefaction paints
- water-desalination paints
Sistem-sistem ini terdiri dari komponen-komponen dimana fluida akan mengalir.
Komponen-komponen inilah apa yang disebut dengan "steady-state steady-flow
devices".
Peralatan ini dapat dikelompokkan menjadi 6 kelompok :
1. Peralatan yang menyerap kerja / tenaga : pompa, kompresor,.
2. Peralatan yang menghasilkan kerja : turbin, mesin, ekspansi,..
3. Nosel dan difuser
4. Peralatan pemindah panas (HE) : ketel uap, kondenser, . . . .
5. Throttling devices: "expansion valves, control valves"
6 Perpipaan / "piping".
Unjuk kerja dari sistem-sistem tersebut di atas tergantung dari unjuk kerja masingmasing peralatan yang dipakai pada sistem tersebut.
Pada peralatan nomor 1 & 2, pada umumnya kerja diberikan atau dihasilkan oleh
peralatan melewati sebuah poros; kerja ini disebut kerja poros (shaft work).
Berapa besarnya kerja poros ini ? (paros pompa, poros kompresor, poros turbin)
Bila
: - proses Reversibel
- hanya 1 saluran masuk & 1 saluran keluar
- perubahan energi kinetik & patensial diabaikan (KE, PE, 0)
maka:
- dari Hukum I, steady-state steady-flow, untuk satu satuan laju aliran :
dq = dh + dWshaft
- untuk proses Reversibel, Hukum II; steady - state steady flow:
dq = T ds
http://riyanto04.wordpress.com
73
- kedua persamaan digabung, didapatkan
T ds = dh + dWshaft
- dari "property relation" untuk fluida kompresibel sederhana :
T ds = dh + - v dp
sehingga:
dWshaft = - v dp
Untuk peralatan nomor 1 dWshaft = kerja minimum yang diberikan.
Untuk peralatan nomor 2 dWshaft = kerja maksimum yang dihasilkan.
Supaya kerja poros dapat dihitung makan harus diketahui hubungan antara v dan p
untuk proses reversibel yang dipakai.
Apakah isotermis Reversibel, adiabatis Reversibel, atau politropis Reversibel ?
PERSAMAAN YANG DIGUNAKAN
Pada contoh-contoh di depan, proses terjadi pada sistem tertutup atau sistem
dengan massa konstan.
Analisa proses akan lebih tidak sederhana lagi bila dalam sistem tersebut selain
kalor, ada sejumlah massa (flow) yang masuk atau keluar melewati "boundary"
dari sistem. Sehingga dalam analisa proses ini perlu menambahkan prinsip
kekekalan massa.
Atau secara lengkap persamaan-persamaan yang digunakan meliputi :
1. Persamaan keseimbangan energi
(energy-balance equation), yang tidak lain adalah Hukum I Termodinamika)
2. Persamaan Perubahan entropi (Hukum II Termodinamika)
3. "Property Relation" / "State postulate"
4. Persamaan Keseimbangan massa (conservation of mass)
ad. 1 (Hukum I) :
"Energy" tidak dapat diciptakan dan tidak dapat dimusnahkan, tetapi hanya dapat
dirubah bentuknya.
Perubahan energi dalam sistem = energi yang masuk energi yang keluar
Change in stored energy = energy input energi output
http://riyanto04.wordpress.com
74
Sehingga Hukum I, dapat ditulis :
Qcv = (E2 + E1)cv + Ws + mout (u + pv +
m in (u + pv +
v2
+ Z)out
2
v2
+ Z) in
2
definisi entalpi : h = u + pv
Qcv = (E2 + E1)cv + Ws + mout (h +
m in (h +
v2
+ Z)out
2
v2
+ Z)in
2
Dalam bentuk diferensial terhadap waktu, dapat ditulis
2
2
& = E& + W
& + m (h + v + Z) m (h + v + Z)
Q
cv
cv
cv
out
out
in
in
2
2
Tetapi dalam aplikasinya (di Bidang Teknik), beberapa sistem terbuka dapat
dimodelkan sebagai sistem yang bekerja pada "STEADY-STATE STEADYFLOW CONDITIONS".
Kondisi ini mempunyai sifat sebagai berikut :
1. Laju aliran kalor melewati C.S. konstan
2. Laju kerja melewati C.S. konstan
3. Keadaan & kecepatan pada setiap aliran masuk konstan
4. Keadaan & kecepatan pada setiap aliran keluar konstan
5. Laju aliran massa pada setiap aliran masuk konstan
6. Laju aliran massa pada setiap aliran keluar konstan
7. Laju aliran massa TOTAL yang masuk clan keluar adalah sama
Pada kondisi ini pula cv 0
Sehingga Hukum I untuk kondisi ini :
2
2
& =W
& - m(h + v + Z) m(h + v + Z)
Q
cv
s
in
out
2
2
( m = min = mout)
q w = h + pe + ke
http://riyanto04.wordpress.com
75
atau
(E2 E1 )cv = Ein Eout + Qcv Wcv
(E2 E1 )cv
: perubahan "stored energy" di dalam C.V.
Ein
: energi yang ditambahkan ke dalam C.V. karena aliran pada
kondisi "inlet".
Eout
: energi yang dikeluarkan dari C.V. karena aliran pada kondisi
"outlet".
Qcv
: perpindahan kalor yang melewati C.S.
Wcv
: kerja yang melewati C.S.
Dapat juga ditulis : Wcv :
Wcv = Ws + mout (pv)out min (pv)in.
Ws
= kerja yang lewat C.S. kecuali "flow work"
mout
= massa aliran keluar
min
= massa aliran masuk
E in = m in (u +
v2
+ Z) in
2
E out = m out (u +
v2
+ Z) out
2
http://riyanto04.wordpress.com
76
Aliran stedi
P1 = 80 kPa
T1 = 10C
V1 = 200 m/s V2 << V1
A1 = 0,4 m2
a = mass flow rate dari udara
b = T2 ?
untuk udara (gas ideal), (Tcr = -147 C, Pcr = 3390 kPa)
a. v1
RT1 [0,287 kPa . m 3 / (kg . K)] (283 K)
=
= 1,015 m 3 /kg
P2
80 kPa
1
m = 1 V1 A 1 = V1 A1
v1
1
m
kg
200 [0,4 m 2 ] 78,8
=
3
g
s
1,015 m /kg
Karena aliran stedi, m sama di semua penampang.
b. W = 0
Q =0
Z1 Z2 Pe = 0
Q W = h + Ke + Pe satuan massa
0 = (h 2 h 1 ) +
V22 V12
2
V2 << V12
h1 = 283,14 kJ/kg (tabel)
h2 = 283.14 kJ/kg =
0 (200 m/s) 2 1 kJ / kg
1000 m 2 /s 2
2
h2 = 303, 14 kJ/kg T2 = 303,1 K
= 30,1 C
http://riyanto04.wordpress.com
77
ad. 2 :
Hukum II Termodinamika (open system)
Untuk "steady-state steady flow" dalam bentuk laju kecepatan :
&
Q
S& total = S& gen = mS mS K 0
TK
out
in
dS
dt = 0
gen = "Rate of entropy generation for the process"
(Reversibel S& gen = 0)
( S& gen < 0 impossible process)
( S& gen > 0 IRReversible process)
actual process
ad. 3 :
"Property relation" / "state postulate" : any eguation that relates one property to
other properties may be called a property equation.
misalkan :
- "state postulate of a simple compressible substance"
s = s (u, v)
u = u (s, v)
h = h (s, p) .
http://riyanto04.wordpress.com
78
KEKEKALAN MASSA
Massa (m) seperti energi (E), tidak dapat diciptakan dihilangkan; massa dan
energi dapat saling dikonversikan (Einstein) :
E = m c2
(c = kecepatan cahaya)
massa dari suatu sistem akan berubah hila energinya berubah.
Tetapi pada semua konversi (interaksi) energi yang dijumpai dalam praktek
(kecuali energi nuklir) perubahan massanya sangat kecil (tidak dapat dideteksi).
misalnya : pembentukan 1 kg air dari oksigen & hidrogen, terlepas energi sebesar
yang ekivalen dengan massa sebenar 1.76 x 10-10 kg.
- sistem tertutup : massa konstan selama proses
- sistem terbuka :
massa total masuk C.V. = massa total keluar C.V. = perubahan massa dalam C.V.
i : inlet/masuk
out/e : exit/keluar
C.V. : control volume
persamaan dalam waktu,
in
m out =
dm
laju perubahan massa dalam C.V.
dt
III.1. POMPA DAN KOMPRESOR
- untuk menaikkan tekanan
- pompa untuk "liquid" .
- kompresor untuk "vapor/gas"
Pada kompresor, bila tidak ada usaha untuk mendinginkan gas selama kompresi,
maka proses kompresi dapat dianggap adiabatis.
http://riyanto04.wordpress.com
79
Karena :
- permukaan yang memindahkan kalor relatif kecil dan
- proses kompresi berjalan dengan cepat
Maka proses ideal untuk kompresi adalah adiabatis reversibel/isentropis.
" Untuk membadingkan kerja ideal dan aktual efisiensi adiabatis dari
kompresor.
c
Wrev
Wact
Wrev = kerja kompresi isentropis
Wact = kerja kompresi aktual/sesungguhnya
Untuk pompa: p
Wrev
Wact
Contoh soal :
Work in - efisiensi adiabatic 0,70
- steady-state steady-flow pump.
-
air/water
saturated
t = 40C
20 MPa
actual pump work ? (kerja sesungguhnya ?)
http://riyanto04.wordpress.com
80
Penyelesaian :
Penyederhanaan yang dilakukan :
- air sebagai fluida tidak mampat.
- Perubahan tenaga kinetik diabaikan
- Perubahan tenaga potensial juga diabaikan
Wrev
W
Wact = rev
Wact
p
Dari definisi p =
Wrev = v dp
2
Karena air dianggap sebagai fluida tidak mampat (pengaruh kompresibilitas
diabaikan).
Wrev = v dp
2
Dari tabel air/uap,
P1 = tekanan jenuh pada 40 C
= 7,375 kPa
v
= Vf pada 40 C
= 0,0010078 m3/kg
maka :
Wrev = - 0010078 (20 x 1000 7,375) kJ/kg
= - 20, 15 kJ/kg
Wact =
20,15
= 28,79 kJ/kg
0,70
Catatan :
Pada penyelesaian tersebut pengaruh kompresibilitas diabaikan (V1 = V2 = V3
pada 40C). Bila pengaruh ini tidak diabaikan, maka kita juga dapat menggunakan
persamaan berikut untuk menghitungnya : Wrev = - (h2s h1)
h2s dicari pada p2s = 20 MPa dan
S2s = S1 = Sf pada 40C
Untuk ini harus digunakan data air yang cukup teliti.
http://riyanto04.wordpress.com
81
III-2. TURBIN
Mesin yang menghasilkan kerja pada putaran yang sangat tinggi
Sehingga dengan turbin, yang berukuran relatif kecil dapat dihasilkan tenaga yang
besar, perpindahan panas dari permukaan turbin ke sekelilingnya biasanya sangat
kecil dibanding dengan tenaga yang dihasilkan.
Pada umumnya, proses ekspansi di dalam turbin dapat dimodelkan
sebagai proses adiabatis. Sedangkan proses ideal sebagai pembanding adalah
proses adiabatis reversibel/isentropis.
Efisiensi adiabatis (dari turbin) :
T =
Wact
Wrec
Wact = kerja ekspansi adiabatis sesungguhnya, dari keadaan awal ke tekanan akhir.
Wrev = kerja ekspansi isentropis dari keadaan awal ke tekanan akhir yang sama.
III-3. HEAT EXCHANGERS I pemindah kalor : peralatan yang memungkinkan
terjadinya pemindahan kalor, antara :
-
suatu fluida dengan fluida yang lain
Suatu fluida dengan sebuah sumber panas atau penyerap panas.
atau suatu bagian dengan bagian yang lain
HE ini merupakan komponen yang sangat penting di dalam sistem teknik,
penggunaannya sangat luas. Mulai dari pendinginan sirkuit elektronik sampai ke
reaktor nuklir.
Nama peralatan pemindah kalor ini, disesuaikan dengan.
fungsinya, misalnya :
- dalam "steam power plant", pemindah panas ini dikenal dengan nama "boiler,
condenser & feed water heater".
- dalam "internal combustion engine", dikenal dengan "water-jacket, radiator"
- dalam "gas-liquefaction plant", dikenal dengan "evaporator, regenerator"
(Dipelajari lebih mendalam dalam mata kuliah Perpindahan Kalor).
Dilihat dari prosesnya,
- tidak ada kerja poros
- KE & PE << panas yang dipindahkan.
http://riyanto04.wordpress.com
82
Maka persamaan Hukum I, dapat ditulis sebagai berikut :
Q = mh mh
out
in
III-4. SISTEM TERBUKA dengan lebih dari satu aliran stedi
Dalam penggunaan persamaan Hukum I yang perlu diperhatikan adalah aliran
yang masuk ("in") dan keluar ("out").
Contoh:
Hitunglah jumlah air panas yang harus dimasukkan bila diinginkan hasil uap
jenuh sebesar 1000 kg/jam.
Dari tabel: h1 = h pada t - 160C & p = 1000 kPa
h2 = 675,7 kJ/kg
h3 = hg pada p = 350 kPa = 2731,6 kJ/kg
h4 = hf pada p = 350 kPa = 584,3 kJ/kg
Diasumsikan : - PE
- KE
diabaikan
- Perpindahan kalor diabaikan
Dari Hukum I :
http://riyanto04.wordpress.com
83
& h m
&h
0 = m
out
in
0 = m 3 h 3 + m 4 h 4 m 1h 1
Dari persamaan kontinuitas
&1 =m
& 3 +m
&4
m
maka
&1=
m
& 3 (h3 h4 )
m
h1 h4
&1 =
m
1000 (2731,6 584,3)
= 23,493,4 kg/jam air panas
675,7 584,3
atau
http://riyanto04.wordpress.com
BAB IX
SIKLUS IDEAL DARI GAS
SIKLUS IDEAL DARI GAS
- menghitung efisiensi dari siklus-siklus
- dengan pengandaian-pengandaian sebagai berikut :
- sifat-sifat dari fluida kerja mengikuti hukum-hukum gas ideal
- panas jenis konstan
- proses-proses dari siklus adalah proses Reversible
- jumlah fluida kerja konstan selama proses, penambahan dan pengurangan panas
disebabkan karena perpindahan panas
SIKLUS YANG DIBICARAKAN
* SIKLUS CARNOT (1824)
* SIKLUS OTTO (1876)
* SIKLUS BRAYTON (1872 - 1874)
* SIKLUS STIRLING (1827)
* SIKLUS ERICSSON (1850)
* SIKLUS DIESEL (1892)
* SIKLUS DUAL
1. SIKLUS CARNOT
84
http://riyanto04.wordpress.com
85
Proses
Panas masuk
Kerja keluar
12
- cv (T2 T1)
23
cv (T3 T2)
34
- cv (T4 T3)
41
cv (T1 T4)
Wnet = cv (T3 T4 + T1 T2)
1
W
= net = 1
Q in
rv
Qin = cv (T3 T2)
rv =
k 1
V4
V3
3. SIKLUS BRAYTON
Proses
Panas masuk
Kerja keluar
12
- Cv (T2 T1)
23
Cv (T3 T2)
34
41
Cv (T1 T4)
P3V3 P2V2
- Cv (T4 T3)
P1V1 P4V4
http://riyanto04.wordpress.com
86
k 1
W
T T1
= net = 1 4
Q in
T3 T2
atau
1
=1
rp
rp =
P2
P1
4. SIKLUS STIRLING
Proses
Panas masuk
Kerja keluar
12
Cv (T2 T1)
RT2 in
23
34
V3
V2
- Cv (T2 T1)
- RT1 in
41
V4
V1
RT2 in
V3
V2
0
- RT1 in
V4
V1
REGENERASI : panas yang dikeluarkan dari proses 3-4 (luas c-4-3-d-c) ke fluida
kerja dalam proses 1-2 (luas a-1-2-b-a).
Regenerator effectiveness 100 % bila kedua besaran tersebut
sama.
http://riyanto04.wordpress.com
87
p
Wnet
T
= 1 1 = 1 rv 4
Q in
T2
p2
(untuk regenerator effectiveness 100 %)
5. SIKLUS ERICSOON
Proses
Panas masuk
Kerja keluar
12
CP (T2 T1)
P2 (V2 V1) = R (T2 T1)
23
34
41
RT2 in
p2
p3
- Cv (T2 T1)
- RT1 in
p1
p4
Untuk regenerator effectiveness 100%.
RT2 in
p2
p3
P3 (V4 V3) = R (T1 T2)
- RT1 in
p1
p4
http://riyanto04.wordpress.com
88
= 1
T1
v
= 1 rp 2
T2
v3
p
Wnet = R (T2 T1 ) in 1
p4
p
, Q in = RT2 in 1
p4
6. SIKLUS DIESEL
Proses
Panas masuk
Kerja keluar
12
- Cv (T2 T1)
23
Cp (T3 T2)
P2 (V3 V2) = R (T3 T2)
34
- Cv (T3 T4)
41
Cv (T1 T4)
Wnet
Qin
= 1
cv (T4 T1 )
1 (T4 T1 ) atau
=1
cp (T3 T2 )
K (T 3 T2 )
1
= 1
rv
rv =
k 1
=1
1 (T4 T1 ) dimana
K (T 3 T2 )
v1
: Volumetric compression Ratio
v2
http://riyanto04.wordpress.com
89
rv =
v1
: fuel c.v. - off Ratio
v2
7. SIKLUS DUAL
Siklus ini adalah gabungan dari siklus OTTO dan DIESEL
Proses
Panas masuk
Kerja keluar
12
- Cv (T2 T1)
23
Cv (T3 T2)
34
Cp (T4 T3)
Cp (V4 V3)
45
- Cv (T5 T4)
51
Cv (T1 T5)
PERBANDINGAN DARI SIKLUS-SIKLUS DI ATAS :
Siklus-siklus tersebut dapat dibuat dengan membandingkan kerja output dari panas
masuk dalam diagram T-s dan p-v.
http://riyanto04.wordpress.com
90
Perbandingan - perbandingan dapat diberikan dengan berdasarkan hal-hal sebagai
berikut :
1. Batas temperatur : karena temperatur minimum dibatasi oleh temperatur
sekitarnya dan temperatur maksimum dibatasi oleh sifat-sifat bahan yang
digunakan.
Anda mungkin juga menyukai
- TERMODINAMIKADokumen47 halamanTERMODINAMIKAWillybrordus PramudhitaBelum ada peringkat
- WUJUD ZATDokumen34 halamanWUJUD ZATrantanBelum ada peringkat
- THERMODINAMIKADokumen17 halamanTHERMODINAMIKAFaizaBelum ada peringkat
- Materi Suhu Kalor Dan TermodinamikaDokumen10 halamanMateri Suhu Kalor Dan TermodinamikaDilla OktantiaBelum ada peringkat
- Rangkuman Termodinamika 1Dokumen12 halamanRangkuman Termodinamika 1Arnold Thamrin van LutteranBelum ada peringkat
- Wujud ZatDokumen82 halamanWujud ZatPpyongpyong Puing100% (1)
- Memposting StatusDokumen19 halamanMemposting StatusIntan Putri AmandaBelum ada peringkat
- Pertemuan 16 A, GasDokumen87 halamanPertemuan 16 A, GasFahrul TandraBelum ada peringkat
- 3 Wujud Zat dan SifatnyaDokumen50 halaman3 Wujud Zat dan SifatnyaNovia Dwi CahyantiBelum ada peringkat
- Fisika II Kegiatan Belajar 3Dokumen19 halamanFisika II Kegiatan Belajar 3Ida Bagus Gede Yamuna C.N.Belum ada peringkat
- PENCAIRAN GASDokumen51 halamanPENCAIRAN GASAdlan Baqi100% (1)
- TERMOKIMIADokumen19 halamanTERMOKIMIADinanti PratiwiBelum ada peringkat
- Sifat ThermoDokumen33 halamanSifat ThermoErdi CiplukBelum ada peringkat
- 6. wujud zat_gas (1)Dokumen37 halaman6. wujud zat_gas (1)Wina Septia UtariBelum ada peringkat
- Wujud ZatDokumen50 halamanWujud ZatTiara SalsabilaBelum ada peringkat
- Wujud Zat dan PerubahannyaDokumen50 halamanWujud Zat dan PerubahannyaTiara SalsabilaBelum ada peringkat
- GAYADokumen9 halamanGAYAQory JuliandoBelum ada peringkat
- Kuliah1 Kimia FisikDokumen37 halamanKuliah1 Kimia FisikFariz IzzanBelum ada peringkat
- BAB II. Kosep Dasar Thermodinamika Dalam Teknik Pendingin Dan Pengkosnisian UdaraDokumen24 halamanBAB II. Kosep Dasar Thermodinamika Dalam Teknik Pendingin Dan Pengkosnisian UdaranafizBelum ada peringkat
- Sistem Fasa 1 PTA 2023-2024Dokumen47 halamanSistem Fasa 1 PTA 2023-2024Syafira Aliyah FitriBelum ada peringkat
- Zat Murni Proses Perubahan Fase Dan Tabel UapDokumen30 halamanZat Murni Proses Perubahan Fase Dan Tabel UapFadel AshariBelum ada peringkat
- Azas BlackDokumen8 halamanAzas BlackMonika UrsulaBelum ada peringkat
- Laporan BMDokumen18 halamanLaporan BMvinaBelum ada peringkat
- Persamaan Keadaan Dan TemperaturDokumen41 halamanPersamaan Keadaan Dan TemperaturRobi'atul AdawiyahBelum ada peringkat
- WUJUD ZAT DAN PERUBAHANNYADokumen45 halamanWUJUD ZAT DAN PERUBAHANNYAFranco Wadi MoreBelum ada peringkat
- Sistem Fasa 1 (Bab 4)Dokumen47 halamanSistem Fasa 1 (Bab 4)Saskhia GomezBelum ada peringkat
- BAB 1 Gas Dan Sifat-SifatDokumen19 halamanBAB 1 Gas Dan Sifat-SifatIke Dayi FebrianaBelum ada peringkat
- Farmasi Fisika, Sifat AlirDokumen26 halamanFarmasi Fisika, Sifat AlirLina Nurfadhila0% (1)
- Suhu Dan KalorDokumen12 halamanSuhu Dan KalorGaluh Vita RespatiBelum ada peringkat
- Wujud ZatDokumen28 halamanWujud ZatMentari R. MuktiBelum ada peringkat
- Kimfis 1Dokumen37 halamanKimfis 1Gilbert SunaryoBelum ada peringkat
- Persamaan KeadaanDokumen16 halamanPersamaan KeadaanDewi Fairuz ZulaikhaBelum ada peringkat
- 3 WUJUD ZAT-gas-2021Dokumen26 halaman3 WUJUD ZAT-gas-2021Aesyah FadhilahBelum ada peringkat
- Wujud Zat Dan Kesetimbangan FaseDokumen47 halamanWujud Zat Dan Kesetimbangan FaseTinaBelum ada peringkat
- Komsep Dadar Ipa Kelompok 5Dokumen28 halamanKomsep Dadar Ipa Kelompok 5Sucita WulandariBelum ada peringkat
- REAKSI_EKSODokumen11 halamanREAKSI_EKSOTheodorus Garry Putra GanaBelum ada peringkat
- GASPERBEDAANDokumen25 halamanGASPERBEDAANAesyah FadhilahBelum ada peringkat
- Kenaikan Titik DidihDokumen21 halamanKenaikan Titik DidihBainatuljannabBelum ada peringkat
- Farfis IDokumen25 halamanFarfis IAkhmad RidhaniBelum ada peringkat
- Konsep DasarDokumen81 halamanKonsep DasarGanda NugrohoBelum ada peringkat
- Tugas TPBBDokumen9 halamanTugas TPBBJoe GoparBelum ada peringkat
- TERMODINAMIKADokumen21 halamanTERMODINAMIKALia Simanullang15Belum ada peringkat
- Wujud Zat-2Dokumen79 halamanWujud Zat-2WIKA YUVENTABelum ada peringkat
- Fasa Zat MurniDokumen9 halamanFasa Zat MurniTrixie WoworBelum ada peringkat
- VOLUMEN MOLARDokumen17 halamanVOLUMEN MOLARTutuzz Ithu AniJugazakiaBelum ada peringkat
- SuhuDokumen24 halamanSuhuIRENE NABILABelum ada peringkat
- Suhu Gas dan PemuaianDokumen7 halamanSuhu Gas dan PemuaiankokoBelum ada peringkat
- Fluida Kerja Dan Proses Evaporasi SalinanDokumen13 halamanFluida Kerja Dan Proses Evaporasi SalinanWanda HayatiBelum ada peringkat
- GgdukdfkgfDokumen97 halamanGgdukdfkgfkhafifah nanda permata sari100% (2)
- PERPINDAHAN PANAS KONVEKSIDokumen37 halamanPERPINDAHAN PANAS KONVEKSIMarfizalBelum ada peringkat
- Termodinamika KimiaDokumen29 halamanTermodinamika KimiapaktanigamsBelum ada peringkat
- Kuliah ThermodinamikaDokumen55 halamanKuliah Thermodinamikalevonavon50Belum ada peringkat
- GASDokumen19 halamanGASRindi Septiani DepariBelum ada peringkat
- 1 Wujud ZatDokumen21 halaman1 Wujud Zathorale88Belum ada peringkat
- BAB II Mekanika Fluida Sifat-Sifat Fluida 1997-2003Dokumen17 halamanBAB II Mekanika Fluida Sifat-Sifat Fluida 1997-2003DerikRiyantoBelum ada peringkat
- 11suhu Dan KalorDokumen15 halaman11suhu Dan KalorIntan Cahyani SariBelum ada peringkat
- File Ap1 2016Dokumen3 halamanFile Ap1 2016Aden Sii AriffBelum ada peringkat
- Tugas Sistem KendaliDokumen1 halamanTugas Sistem KendaliFajar Satrio SatrioBelum ada peringkat
- SAE 304 Stainless SteelDokumen4 halamanSAE 304 Stainless SteelFajar Satrio SatrioBelum ada peringkat
- Elemen MesinDokumen16 halamanElemen MesinClinton Banua Betlehem HutajuluBelum ada peringkat
- Bab I PendahuluanDokumen9 halamanBab I PendahuluanFajar Satrio SatrioBelum ada peringkat
- Buku Ajar MEH FixDokumen115 halamanBuku Ajar MEH FixFajar Satrio SatrioBelum ada peringkat
- Makalahtermodinameeeika 131002101133 Phpapp02Dokumen13 halamanMakalahtermodinameeeika 131002101133 Phpapp02Nita Murtia HandayaniBelum ada peringkat
- Sistem Pengukuran Teknik1Dokumen23 halamanSistem Pengukuran Teknik1Sadeli JWBelum ada peringkat
- 6.B. Sistem Bahan BakarDokumen47 halaman6.B. Sistem Bahan BakarMuch Abdulah NurhidayatBelum ada peringkat
- BAB 2 Fix Heat ExchangerDokumen17 halamanBAB 2 Fix Heat ExchangerFajar Satrio SatrioBelum ada peringkat
- IHP dan BHPDokumen11 halamanIHP dan BHPFajar Satrio SatrioBelum ada peringkat
- Presentation 9 Sistem Bahan BakarDokumen17 halamanPresentation 9 Sistem Bahan BakarFajar Satrio SatrioBelum ada peringkat