Tugas Bahan Ajar Aristha SMK Kesehatan Airlangga
Diunggah oleh
Aristha ArsyHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Tugas Bahan Ajar Aristha SMK Kesehatan Airlangga
Diunggah oleh
Aristha ArsyHak Cipta:
Format Tersedia
MODUL SIFAT PERIODIK UNSUR 1
DAFTAR ISI
HALAMAN SAMPUL ............................................................................................................... 1
DAFTAR ISI............................................................................................................................... 2
PETUNJUK SISWA ................................................................................................................... 3
SIFAT PERIODIK UNSUR ....................................................................................................... 4
LATIHAN SOAL ..................................................................................................................... 17
RANGKUMAN ........................................................................................................................ 18
UJI KOMPETENSI .................................................................................................................. 20
DAFTAR PUSTAKA ............................................................................................................... 25
MODUL SIFAT PERIODIK UNSUR 2
Petunjuk Siswa:
Agar siswa berhasil menguasai dan memahami materi dalam modul ini, lalu dapat
mengaplikasikannya dalam kehidupan sehari-hari, maka bacalah dengan cermat dan ikuti petunjuk
berikut dengan baik, antara lain:
1. Bacalah doa terlebih dahulu sesuai dengan keyakinanmu, agar diberikan kemudahan dalam
mempelajari materi ini.
2. Bacalah materi ini dengan seksama, sehingga isi materi ini dapat dipahami dengan baik.
3. Buatlah catatan kecil mengenai istilah atau rumus yang belum dipahami, untuk ditanyakan
kepada guru mata pelajaran.
4. Kerjakan lembar kegiatan siswa dan soal-soal yang sudah disediakan dengan sungguh-
sungguh.
5. Ulangi sampai kamu memahami materi modul.
MODUL SIFAT PERIODIK UNSUR 3
SIFAT PERIODIK UNSUR
Materi kemiripan sifat unsur dan keperiodikan unsur merupakan materi kimia SMA,
pada Kurikulum 2013 disajikan di kelas X semester 1 dengan Kompetensi Dasar (KD)
aspek pengetahuan dan aspek keterampilan:
3.4 Menganalisis kemiripan sifat unsur dalam golongan dan keperiodikannya
4.4 Menyajikan hasil analisis data-data unsur dalam kaitannya dengan kemiripan dan
sifat keperiodikan unsur.
A. Tujuan
Setelah belajar dengan modul ini diharapkan Anda dapat menjelaskan tentang kemiripan sifat-
sifat unsur dalam satu golongan dan menganalisis hubungan antara nomor atom dengan sifat
keperiodikan unsur (jari-jari atom, energi ionisasi, afinitas elekton, dan keelektronegatifan)
berdasarkan data sifat keperiodikan unsur.
B. Indikator Pencapaian Kompetensi
Indikator pencapaian kompetensi yang diharapkan dicapai melalui modul ini adalah:
1. Menjelaskan tentang kemiripan sifat-sifat unsur dalam satu golongan
2. Menganalisis hubungan antara nomor atom dengan sifat keperiodikan unsur (jari-jari atom,
energi ionisasi, afinitas elekton, dan keelektronegatifan) berdasarkan data sifat
keperiodikan unsur.
C. Uraian Materi
Unsur dikelompokkan dalam tabel periodik unsur. Tabel Periodik Unsur digambarkan
sebagai “the chemist’s best friend.” Sifat-sifat unsur berkorelasi dengan posisi mereka padai
tabel periodik. Kimiawan menggunakan tabel periodik sebagai petunjuk yang sangat berharga
MODUL SIFAT PERIODIK UNSUR 4
dalam penelitian material baru yang berguna. Pada tabel periodik yang sekarang digunakan
atau tabel periodik modern, unsur-unsur dikelompokkan dalam satu golongan dan periode.
Dalam satu golongan unsur-unsur umumnya memiliki sifat yang sama, dalam satu periode
memiliki sifat yang berbeda secara periodik. Kecenderungan sifat unsur dalam satu golongan
dan periode dikenal dengan istilah keperiodikan sifat unsur atau sifat periodik unsur yang
meliputi jari jari atom, enegi ionisasi, afinitas elektron dan keelektronegatifan.
Tabel sistem periodik unsur
Pengelompokkan unsur-unsur dalam sistem periodik modern menghasilkan golongan yang
memuat unsur-unsur dengan sifat yang mirip dan sepiriode, dimana terjadi pengulangan sifat
secara berkala atau periodik. Sifat-sifat unsur yang berhubungan dengan letak unsur dalam
tebel periodik disebut sifat periodik. Sifat periodik unsur dibedakan menjadi berikut.
MODUL SIFAT PERIODIK UNSUR 5
Sifat periodik yang akan dibahas disini adalah sifat atomik, meliputi jari-jari atom, energi ionisasi,
afinitas elektron, keelektronegatifan, serta titik didih dan titik leleh.
1. Jari-jari atom
Jari-jari atom adalah jarak yang dihitung dari inti atom hingga lintasan paling luar suatu atom.
Nilai jari jari atom dari unsur unsur dalam sistem periodik dapat dilihat pada grafik berikut:
Grafik hubungan jari-jari atom dengan nomer atom
Dari grafik tersebut, terdapat suatu keteraturan nilai jari-jari atom baik dalam periode maupun
golongan, hal ini dapat ditunjukkan dalam gambar berikut.
MODUL SIFAT PERIODIK UNSUR 6
Dalam satu periode, jari-jari atom berkurang dari kiri ke kanan, hal ini dikarenakan muatan
inti bertambah positif, sedangkan elektron-elektron valensi masih menempati kulit yang
sama. Keadaan ini menyebabkan gaya tarik-menarik inti terhadap elektron semakin kuat.
Akibatnya jari-jari atom semakin kecil
Dalam satu golongan, jari-jari atom bertambah dari atas ke bawah, hal ini dikarenakan
meskipun muatan inti bertambah positif, tetapi jumlah kulit semakin banyak, keadaan ini
menyebabkan gaya Tarik inti terhadap elektron semakin lemah. Akibatnya jari-jari atom
bertambah besar
Contoh Soal:
Dari Kedua unsur berikut Na dan Mg yang masing-masing mempunyai nomor atom
11 dan 12. Tentukan unsur yang memiliki jari – jari atom paling kecil.
Jawab:
11Na: 1s2, 2s2, 2p6, 3s1 → Na terletak pada golongan I A dan periode 3
12Mg: 1s2, 2s2, 2p6, 3s2 → Mg terletak pada golongan II A dan periode 3
Na dan Mg terletak pada periode yang sama yaitu 3.
Kedua unsur tersebut harus diurutkan ke samping kanan, yaitu: Na – Mg
(Mg disebelah kanan karena memiliki nomor golongan yang lebih besar yaitu II A)
Ingat: Sifat jari – jari atom dari kiri ke kanan makin kecil
Jadi unsur Mg memiliki jari – jari atom paling kecil
MODUL SIFAT PERIODIK UNSUR 7
Jari-jari atom diukur dalam berbagai satuan, diantaranya dengan picometer (pm) dan amstrong
(Å). Jari-jari atom terbesar adalah fransium (87Fr) dan terkecil adalah helium (2He)
2 Energi Ionisasi
Energi ionisasi adalah energi yang diperlukan untuk melepaskan elektron dari suatu atom
netral dalam keadaan gas.
Energi + X(g) → X+ (g) + e
Nilai energi ionisasi dipengaruhi oleh faktor berikut:
a. Jari-jari atom, yaitu semakin besar jari-jari atom, semakin kecil nilai energi ionisasi
b. Muatan inti positif, yaitu semakin besar muatan inti, semakin besar nilai energi ionisasi
c. Jumlah elektron kulit dalam, yaitu semakin banyak jumlah elektron di kulit dalam, semakin
kecil nilai energi ionisasi.
Perhatikan grafik yang memuat nilai energi ionisasi dari atom unsur-unsur sistem periodik
berikut.
Grafik energi ionisasi dari unsur terhadap nomor atom dalam tabel periodik unsur
Dalam satu periode, energi ionisasi bertambah dari kiri kekanan. Hal ini dikarenakan
muatan inti bertambah positif dan jari-jari atom berkurang. Keadaan ini menyebabkan gaya
tarik-menarik inti terhadap elektron terluar semakin kut. Akibatnya, energi ionisasi semakin
bertambah.
MODUL SIFAT PERIODIK UNSUR 8
Dalam satu golongan, Energi ionisasi berkurang dari atas kebawah. Hal ini karena gaya
Tarik-menarik inti terhadap elektron terluar semakin lemah
Contoh Soal:
Dari Ketiga unsur berikut:
3Li (nomor atom 3)
11Na (nomor atom 11)
19K (nomor atom 19)
Urutkan ketiga unsur tersebut berdasarkan sifat energi ionisasinya.
Jawab:
3Li: 1s2, 2s1 → Li terletak pada golongan IA dan periode 2
11Na: 1s2, 2s2, 2p6, 3s1 → Na terletak pada golongan I A dan periode 3
19K: 1s2, 2s2, 2p6, 3s2, 3p6, 4s1 →K terletak pada golongan I A dan periode 4
Li, Na, dan K terletak pada golongan yang sama yaitu IA
Ketiga unsur tersebut harus diurutkan ke bawah, yaitu:
Li (Li paling atas karena memiliki nomor periode paling kecil yaitu 2)
Na
K ( K paling bawah karena memiliki nomor periode paling besar yaitu 4)
Sifat energi ionisasi dari bawah ke atas makin besar.
Jadi energi ionosasi: K < Na < Li.
Li memiliki energi ionisasi paling besar.
Perbandingan energi ionisasi dalam saru periode (kiri) dan satu golongan (kanan)
MODUL SIFAT PERIODIK UNSUR 9
Pengecualian:
Unsur-unsur golongan IIA memiliki energi ionisasi lebih besar dari unsur-unsur golongan IIIA.
Unsur-unsurngolongan VA memiliki energi ionisasi lebih besar dari unsur-unsur golongan
VIA. Pengecualian ini terjadi karena unsur-unsur golongan IIA, VA, dan VIIIA mempunyai
konigurasi elektron yang relatif stabil sehingga elektron sukar dilepaskan.
Energi Ionisasi dinyatakan menggunakan satuan kJ mol-1 atau elektronVolt (eV). Energi
Ionisasi terbesar dimiliki helium (2He), dan terkecil dimiliki cesium (55Cs).
Uji Kemampuan Diri
1. Hidrogen (H) mempunyai energi ionisasi sebear 1.312 kJ mol-1. Apakah artinya?
2. Diantara Na dan Cl, manakah yang mempunyai energi ionisasi lebih besar? Jelaskan.
3 Afinitas Elektron
Afinitas elektron adalah besarnya energi yang dibebaskan dan diserap untuk menerima
elektron dari luar atom netral agar menjadi ion negatif. Unsur yang memiliki afinitas elektron
bertanda negatif, berarti mempunyai kecenderungan lebih besar dalam menyerap elektron
daripada unsur yang afinitas elektronnya bertanda positif. Makin negatif nilai afinitas elektron,
maka makin besar kecenderungan unsur tersebut dalam menyerap elektron (kecenderungan
membentuk ion negatif). Afinitas Elektron dinyatakan menggunakan satuan kJmol-1 atau
elektronVolt (eV). Afinitas elektron terbesar dimiliki klor (17Cl), dan terkecil dimiliki berilium
(4Be).
Beberapa hal berikut perlu diperhatikan untuk memahami afinitas elektron.
Penyerapan elektron ada yang disertai pelepasan energi, ada pula yang disertai penyerapan
energi.
Jika penyerapan elektron disertai dengan pelepasan energi, afinitas elektronnya dinyatakan
dengan tanda negatif
Contoh:
MODUL SIFAT PERIODIK UNSUR 10
Afinitas elektron klorin = -349 kJ mol-1, berarti penyerapan elektron oleh atom klorin
membentuk ion Cl- disertai pelepasanenergi sebanyak 349 kJ mol-1
Jika penyerapan elektron disertai penyerapan energi, afinitas elektronnya dinyatakan
dengan tanda positif
Contoh:
Afinitas elektron berilium = 240 kJ mol-1. Berarti terjadi penyerapan elektron oleh atom
berilium, sehingga membentuk ion Be- disertai penyerapan energi. Dalam hal ini, elektron
baru dapat memasuki atom berilium jika diberi tambahan energi sebanyak 240 kJ mol-1
Unsur yang mempunyai afinitas elektron bertanda negatif mempunyai daya tarik atau
afinitas elektron yang lebih besar daripada unsur yang afinitas elektronnya bertanda positif.
Dengan kata lain, makin negatif nilai afinitas elektron, makin besar kecendrungannya
menarik elektron membentuk ion negatif
Contoh:
Afinitas elektron korin = -349 kJ mol-1, berarti ion Cl- lebih stabil daripada atom Cl-
Unsur yang mempunyai afinitas elektron bertanda negatif, akan membentuk ion negatif
yang lebih stabil daripada atom netralnya.
Contoh:
Afinitas elektron berilium = 240 kJ mol-1, menunjukkan ion Be- kurang stabil dibandingkan
atom Be
Sebaliknya, unsur yang afinitas elektronnya bertanda positif akan membentuk ion negatif
yang kurang stabil daripada atom netralnya.
Dalam satu periode, afinitas elektron cenderung bertambah dari kiri kekanan. Hal ini
karena muatan inti bertambah positif dan nilai jari-jari atom berkurang. Keadaan ini
menyebabkan gaya Tarik menarik inti terhadap elektron yang ditambahkan akan semakin
kuat. Akibatnya, afinitas elektron semakin bertambah.
MODUL SIFAT PERIODIK UNSUR 11
Dalam satu golongan, afinitas elektron cenderung berkurang dari atas ke bawah. Hal ini
karena meski muatan inti bertambah positif, namun jumlah elektron di kulit dalam semakin
banyak. Keadaan ini menyebabkan gaya tarik-menarik inti terhada elektron yang
ditambahkan semakin lemah. Akibatnya afinitas elektron semakin berurang.
Uji Kemampuan Diri
1. Apakah afinitas elektron itu? Berikan contohnya.
2. Diketahui afinitas elektron magnesium = 230 kJ mol-1 dan fluorin = -328 kJ mol-1
a. Manakah yang lebih mudah menyerap elektron, atom magnesium atau atom
fluorin?
b. Manakah yang lebih stabil, ion Mg- atau atom Mg?
c. Manakah yang lebih stabil, atom F atau ion F-?
4 Kelektronegatifan
Keelektronegatifan atau elektronegativitas adalah ukuran kemampuan atau kecenderungan
suatu atom untuk menarik elektron dalam ikatan kimianya. Semakin besar keelktronegatifan
suatu atom, semakin besar kecendrungannya untuk menarik elektron dari atom lain yang terikat
secara kimiawi dengan atom tersebut.
MODUL SIFAT PERIODIK UNSUR 12
Skala keelektronegatifan yang dipakai sampai sekarang adalah yang dikembangkan oleh
Pauling ia berhasil menghitung nilai keelektronegatifan dari rumus matematis yang digunakan
untuk menghitung energi ikayan kimia. Pauling memberikan skala keelektronegatifan 4 untuk
unsur yang memiliki energi ionisasi dan energi afinitas elektron tinggi, yaitu pada unsur florin,
sedangkan unsur-unsur lainnya di bawah nilai 4.
Jika dilihat sekilas terdapat kemiripan antara keelektronegatifan dan afinitas elektron,
Persamaan keelektronegatifan dan afinitas elektron adalah sama-sama membahas tentang
bagaimana suatu atom menarik elektron dari luarnya. Perbedaan keelektronegatifan dan
afinitas elektron adalah, keelektronegatifan hanya mengukur kemampuannya saja, sedangkan
afinitas elektron mengaitkannya dengan jumlah energi dan pembentukan ion
Dalam satu periode, keelektronegatifan bertambah dari kiri ke kanan. Hal ini dikarenakan
muatan inti bertambah positif dan jari-jari atom berkurang. Keadaan ini menyebabkab gaya
trik menarik inti terhadap elektron semakin kuat. Akibatnya, kemampuan atom untuk
menark elektron semakin besar.
Dalam satu golongan, keelektronegatifan berkurang dari atas ke bawah. Hal ini terjadi
karena meski muatan initi bertanbah poitif, tetapi jumlah elektron didalam kulit dalam
semakin banyak. Akibatnya jari-jari atom bertambah besar dan kemampuan inti untuk
menarik elektron menjadi lemah.
MODUL SIFAT PERIODIK UNSUR 13
Contoh Soal:
Dari kedua unsur berikut: O (no atom 8) dan F (no atom 9), manakah yang mempunyai
keelektronegatifan paling besar
Jawab: Unsur O dan unsur F merupakan unsur-unsur yang berada dalam satu periode ke
2. Unsur F mempunyai keelektronegatifan lebih besar dari O karena dalam satu periode
bertambahnya nomor atom, keelektronegatifan makin besar.
Uji Kemampuan Diri
Tanpa melihat daftar keelektronegatifan, tentukan unsur mana yang mempunyai
keelektronegatifan yang lebih besar dari unsur-unsur berikut.
1. Boron (Z = 5) atau oksigen (Z = 8)? Jelaskan
2. Fluorin (Z = 9) atau bromin (Z = 35)? Jelaskan
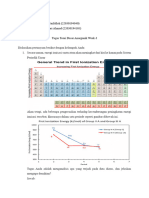
5 Titik Leleh dan Titik Didih
Titik leleh adalah suhu ketika tekanan uap zat padat sama dengan tekanan ap zat cairnya,
sedangkan titik didih adalah suhu saat tekanan uap zat cair sama dengan tekanan uap
disekitarnya. Keteraturan titik didih dan titik leleh unsur-unsur dalam tabel periodik untuk
unsur-unsur dengan Z ≤ 18 dapat dilihat pada grafik berikut.
MODUL SIFAT PERIODIK UNSUR 14
Berdasarkan grafik tersebut, keteraturan titik leleh dan titik didihmuntuk unsur-unsur dengan
Z ≤ 18 adalah sebagai berikut:
a. Dalam satu periode, titik leleh dan titik didih awalnya bertambah dari kiri ke kanan
sampai golongan IVA, kemudian berkurang mencapai nilai terendah untuk golongan VIIIA
b. Dalam satu golongan, titik leleh dan titk didih unsur logam berkurang dari atas ke bawah.
Sementara itu, titk leleh dan titik didih unsur nonlogam bertambah dari atas ke bawah
Titik leleh dan titik didih terbesar dimiliki karbon (6C), dan terkecil dimiliki helium (2He).
6 Sifat Logam Dalam Periodik
Sifat logam dalam sistem periodik terkait dengan dua sifat atomic, yaitu energi ionisasi dan
afinitas elektron.
a. Unsur logam memiliki energi ionisasi kecil sehingga mudah melepaskan elektron
membentuk ion positif
b. Unsur non logam memiliki afinitas elektron yang besar sehingga mudah menarik elektron
membentuk ion negatif
Dalam satu periode, sifat logam unsur berkurang dari kiri kekanan. Nilai energi ionisasi unsur
meningkat dari kiri kekanan. Oleh karena itu, semakin ksulit bagi unsur untuk melepas elektron
sehingga sifat logam unsur akan berkurang. Demikian pula, nilai afnitas elektron unsur
MODUL SIFAT PERIODIK UNSUR 15
semakin meningkat dari kiri ke kanan. Jadi semakin mudah bagi unsur menarik elektron
sehingga sifat non logam bertambah.
Dalam satu golongan, sifat logam unsur bertambah dari atas kebawah.
Uji Kemampuan Diri
1. Diantara unsur kalium dan natrium, unsur manakah yang memiliki sifat logam yang
paling kuat?
2. Diantara unsur fosforous dan klorin, unsur manakah yang memiliki sifat non logam
yang paling kuat?
.
7 Tren Periodik
Secara keseluruhan tren/kecendrungan periodik dapat digambarkan sebagai berikut
MODUL SIFAT PERIODIK UNSUR 16
LATIHAN SOAL
Untuk mengetahui pemahaman kalian tentang materi ini silahkan kerjakan latihan soal berikut ini.
Jawablah pertanyaan-pertanyaan dibawah ini dengan benar.
1. Mengapa jari – jari atom dalam satu periode semakin ke kanan semakin kecil?
2. Jelaskan apa yang dimaksud dengan afinitas elektron?
3. Bagaimana energi ionisasi atom – atom dalam satu golongan dan periode?
4. Jelaskan apa yang dimaksud dengan keelektronegatifan?
5. Mengapa unsur – unsur golongan halogen mempunyai afinitas elektron terbesar?
MODUL SIFAT PERIODIK UNSUR 17
Rangkuman
1. Sifat-sifat unsur yang berhubungan dengan letak unsur dalam tabel periodik disebut sifat
periodik. Sifat periodik unsur dibedakan menjadi sifat atomik, sifat fisis dan sifat kimia
2. Jari-jari atom: jarak elektron terluar ke inti.
- Dalam satu periode: dari kanan ke kiri makin besar
- Dalam satu golongan: dari atas ke bawah makin besar.
Searah panah makin besar dan sebaliknya
3. Keeletronegatifan: besaran kecendrungan atom dalam menerima elektron untuk
membentuk ion negatif.
- Dalam satu periode: dari kiri ke kanan makin besar.
- Dalam satu golongan: dari bawah ke atas makin besar.
Searah panah makin besar dan sebaliknya
4. Energi Ionisasi (Potensial ionisasi) : besarnya energi yang diperlukan suatu atom untuk
melepaskan elektron yang terikat paling lemah (pada kulit terluar).
- Dalam satu periode : dari kiri ke kanan makin besar.
- Dalam satu golongan : dari bawah ke atas makin besar
Searah panah makin besar dan sebaliknya
5. Afinitas Elektron : besarnya energi yang dilepaskan oleh suatu atom untuk dapat menerima
sebuah elektron.
- Dalam satu periode : dari kiri ke kanan makin besar.
- Dalam satu golongan : dari bawah ke atas makin besar.
Searah panah makin besar dan sebaliknya
MODUL SIFAT PERIODIK UNSUR 18
6. Titik leleh dan titik didih: titik dimana suatu unsur mulai berubah wujud menjadi wujud
lain
Golongan IA – IVA:
- Dalam satu periode : dari kiri makin ke kanan dalam satu periode makin bertambah
sampai puncaknya pada IVA (TL dan TD tertinggi).
- Dalam satu golongan : dari atas Makin ke bawah dalam satu golongan makin
berkurang.
7. Sifat logam: kemampuan suatu atom untuk melepas elektron dan menjadi bermuatan
positif.
- Dalam satu periode: dari kanan ke kiri makin besar
- Dalam satu golongan: dari atas ke bawah makin besar
Searah panah makin besar dan sebaliknya
MODUL SIFAT PERIODIK UNSUR 19
UJI KOMPETENSI
Pilihlah satu jawaban yang paling tepat.
1. Pernyataan yang benar tentang sifat – sifat keperiodikan unsur dalam satu periode dari kiri ke
kanan adalah …
a. sifat logam bertambah
b. jari – jari atom berkurang
c. energi ionisasi berkurang
d. keelektronegatifan berkurang
e. sifat asam berkurang
2. Unsur – unsur yang mempunyai kemiripan sifat ditempatkan dalam …
a. periode yang sama
b. golongan yang sama
c. blok yang sama
d. kulit yang sama
e. wujud yang sama
3. Di antara sifat periodik unsur berikut, yang benar dalam satu golongan dari atas ke bawah
adalah …
a. jari – jari atom makin pendek
b. elektronegativitas makin besar
c. energi ionisasi makin besar
d. afinitas elektron makin kecil
e. sifat logam makin berkurang
4. Pernyataan yang tidak benar dari sifat keperiodikan sistem periodik unsur adalah… .
a. Sepanjang periode semakin besar nomor atom semakin panjang jari-jari atomnya
b. Dalam satu golongan semakin besar nomor atom semakin pendek jari-jari atomnya
c. Sepanjang periode dari kiri ke kanan semakin mudah melepaskan elektron valensinya
d. Untuk periode yang sama afinitas unsur golongan ia lebih besar daripada unsur iia
e. Untuk unsur segolongan atom unsur periode 2 lebih mudah melepaskan elektron daripada
atom unsur periode 4
5. Pernyataan di bawah ini yang tidak sesuai dengan bertambahnya nomor atom adalah… .
MODUL SIFAT PERIODIK UNSUR 20
a. Jari-jari atom dalam satu periode semakin kecil
b. Jari-jari atom dalam satugolongan semakin besar
c. Energi ionisasi dalam satu periode cenderung semakin kecil
d. Afinitas elektron dalam satu golongan semakin kecil
e. Keelektronegatifan dalam satu golongan semakin kecil
6. Faktor yang menyebabkan jari-jari atom semakin besar dalam satu golongan adalah… .
a. Bertambahnya jumlah proton
b. Bertambahnya jumlah kulit
c. Bertambahnya nomor atom
d. Bertambahnya nomor massa
e. Bertambahnya elektron valensi
7. Di antara unsur-unsur berikut yang jari-jari atomnya paling besar adalah… .
a. 6C
b. 9F
c. 8B
d. 7N
e. 10Ne
8. Di antara unsur-unsur di bawah ini yang energi ionisasinya paling besar adalah… .
a. 11Na
b. 1H
c. 9F
d. 10Ne
e. 2He
9. Unsur A, B, dan C merupakan unsur-unsur yang terdapat dalam satu golongan. Jika energi
ionisasi unsur-unsur tersebut berturut-turut 419, 403, dan 496. Urutan unsur tersebut dari atas
ke bawah adalah… .
a. A-B-C
b. C-A-B
c. A-C-B
d. C-B-A
e. B-A-C
MODUL SIFAT PERIODIK UNSUR 21
10. Di antara atom-atom di bawah ini yang mempunyai afinitas elektron terbesar adalah… .
a. 9F
b. 17Cl
c. 11Na
d. 19K
e. 13Al
11. Dalam periode yang sama bila dibandingkan dengan unsur golongan alkali tanah, maka unsur
alkali mempunyai sifat-sifat… .
a. Energi ionisasinya lebih besar
b. Afinitas elektronnya lebih besar
c. Jari-jari atomnya lebih panjang
d. Keelektronegatifannya lebih besar
e. Kurang reaktif
12. Jika jari-jari atom (angstrom) unsur-unsur Li, Na, K, Be, dan B secara acak adalah: 2,03; 1,23;
1,57; 0,80; dan 0,89 maka jari-jari atom Li adalah… .
a. 2,03 angstrom
b. 0,89 angstrom
c. 1,57 angstrom
d. 0,80 angstrom
e. 1,23 angstrom
13. Elektronegativitas atau keelektronegatifan suatu atom adalah sifat yang menyatakan… .
a. Besarnya energi yang dilepaskan apabila atom menangkap sebuah elektron dan menjadi
ion negatif
b. Besarnya kecenderungan untuk menarik elektron dalam pembentukan ion negatif
c. Besarnya energi yang diperlukan apabila atom melepaskan sebuah elektron dan menjadi
ion positif
d. Besarnya kecenderungan untuk melepaskan sebuah elektron dalam pembentukan ion
positif
e. Besarnya kecenderungan satu atom untuk menarik elektron
14. Bertambahnya kereaktifan unsur-unsur alkali menurut urutan Li, Na, dan K disebabkan oleh
bertambahnya … .
MODUL SIFAT PERIODIK UNSUR 22
a. Jumlah elektron
b. Nomor atom
c. Jari-jari atom
d. Jumlah proton
e. Massa atom
15. Dalam urutan unsur 8O, 9F, dan 10Ne, jari-jari atom akan … .
a. Bertambah
b. Bekurang
c. Sama besar
d. Bertambah lalu berkurang
e. Berkurang lalu bertambah
16. Konfigurasi elektron dari unsur yang memiliki keelektronegatifan terbesar adalah …
a. 2, 5
b. 2, 7
c. 2, 8
d. 2, 8, 1
e. 2, 8, 8
17. Sifat logam yang paling kuat di antara unsur-unsur berikut dimiliki oleh … .
a. Aluminium
b. Natrium
c. Magnesium
d. Kalsium
e. Kalium
18. Energi ionisasi terbesar dimiliki oleh … .
a. Helium
b. Neon
c. Natrium
d. Argon
e. Kalium
MODUL SIFAT PERIODIK UNSUR 23
19. Diketahui beberapa energi ionisasi untuk X = 520; Y = 419; Z = 496; A = 376; B = 403 (dalam
kJ/mol). Urutan yang benar dari unsur logam alkali berdasarkan harga energi ionisasi dari atas
ke bawah adalah …
a. X – Y – Z – A – B
b. B – A – Z – Y – X
c. Z – Y – X – B – A
d. A – B – X – Y – Z
e. X – Z – Y – B – A
20. Di antar deret unsur halogen, atom yang memiliki keelektronegatifan paling besar adalah …
a. 9F
b. 17Cl
c. 35Br
d. 53I
e. 85At
MODUL SIFAT PERIODIK UNSUR 24
DAFTAR PUSTAKA
Anonim. (2013, Juni). Sifat Tabel Periodik. Diakses 31 Juni 2019
https://materi78.files.wordpress.com/2013/06/sperio_kim1_5.pdf
Anonim. (2011, Juni). Latihan Soal Sifat Periodik Unsur. Diakses 01 Juli 2019
http://chemistry35.blogspot.com/2011/06/latihan-soal-sifat-periodik-unsur.html#!/tcmbck
Anonim. (2014). Soal Pembahasan Sifat Keperiodikan Unsur. Diakses 01 Juli 2019
https://smpsma.com/soal-pembahasan-sifat-keperiodikan-unsur.html 2014
Johari, J.M.C. dan Rachmayani,M. 2017. Kimia Untuk SMA/MA Kelas X. Jakarta: Erlangga
Saidah, Aan dan Darmayani, Tiara. 2018. Kimia C1 Untuk SMK/MAK Kelas X. Jakarta: Erlangga
Silviakimangela. (2015, September). Sistem Periodik Unsur. Diakses 31 Juni 2019
https://silviakimangela.files.wordpress.com/2015/10/sistem-periodik-unsur.pdf
Susianto., Nirwan. (2019). Sistem Periodik Unsur. Diakses 01 Juli 2019
https://www.studiobelajar.com/sistem-periodik-unsur/
MODUL SIFAT PERIODIK UNSUR 25
Anda mungkin juga menyukai
- LKPDDokumen14 halamanLKPDAristha ArsyBelum ada peringkat
- Materi Struktur Atom 5Dokumen8 halamanMateri Struktur Atom 5Arty ItsnaBelum ada peringkat
- Makalah Sistem PeriodikDokumen19 halamanMakalah Sistem PeriodikRina AngrianiBelum ada peringkat
- Makalah Unsur Dan SenyawaDokumen16 halamanMakalah Unsur Dan SenyawaDarmawan Setiadi100% (1)
- Pemb. 6 Sifat Sifat Periodik Unsur Klas XDokumen9 halamanPemb. 6 Sifat Sifat Periodik Unsur Klas XnurwindaBelum ada peringkat
- LKPD Sifat Periodik UnsurDokumen7 halamanLKPD Sifat Periodik UnsurFTC •IqbalBelum ada peringkat
- Makalah Kimia Dasar Siap PrintDokumen22 halamanMakalah Kimia Dasar Siap PrintDio Irsyad0% (1)
- Atom 3Dokumen18 halamanAtom 3Agus SanzdingerBelum ada peringkat
- Sifat Atom Dan Tabel BerkalaDokumen13 halamanSifat Atom Dan Tabel BerkalaRangga BuanaBelum ada peringkat
- Spu 10 MaDokumen29 halamanSpu 10 MaAris SanwaniBelum ada peringkat
- Sifat Periodik UnsurDokumen16 halamanSifat Periodik UnsurFriska HilmaBelum ada peringkat
- LKPD SpuDokumen9 halamanLKPD Spusuci indah sariBelum ada peringkat
- Susunan Tabel BerkalaDokumen9 halamanSusunan Tabel BerkalaRyan R. EzraBelum ada peringkat
- Sistem Periodik UnsurDokumen20 halamanSistem Periodik UnsursariBelum ada peringkat
- Kuliah #2 B Tabel+PeriodikDokumen15 halamanKuliah #2 B Tabel+PeriodikMondesHutapeaBelum ada peringkat
- Sistem PeriodikDokumen30 halamanSistem PeriodikHengky FirmansyahBelum ada peringkat
- 6 LKS SpuDokumen4 halaman6 LKS SpuNadya RianasariBelum ada peringkat
- Bahan Ajar Sifat Periodik UnsurDokumen8 halamanBahan Ajar Sifat Periodik UnsurFadilla Qinthara ZahraniBelum ada peringkat
- Pengertian Sistem Periodik Unsur Dan SifatDokumen8 halamanPengertian Sistem Periodik Unsur Dan SifatDiela GrimoniaBelum ada peringkat
- Bab I Kimia PDFDokumen25 halamanBab I Kimia PDFDavid Julianto SiraitBelum ada peringkat
- Tabel PeriodikDokumen28 halamanTabel PeriodikfrenaldoBelum ada peringkat
- Kelompok AldiDokumen11 halamanKelompok AldiIkhwan Kosong DelapanBelum ada peringkat
- Materi Sifat Periodik UnsurDokumen10 halamanMateri Sifat Periodik UnsurtanzilataqiaBelum ada peringkat
- Sifat Periodik UnsurDokumen9 halamanSifat Periodik UnsurGusdwi DwipaBelum ada peringkat
- SPU KesatuDokumen4 halamanSPU KesatuFawzia AuliaBelum ada peringkat
- Tugas 1 Kimia Dasar Teknik GeologiDokumen6 halamanTugas 1 Kimia Dasar Teknik GeologiMOH.SUDANDIBelum ada peringkat
- Makalah SpuDokumen24 halamanMakalah SpuDhita LinchBelum ada peringkat
- RESUME IKATAN KIMIA Yuliarnol G30122048Dokumen8 halamanRESUME IKATAN KIMIA Yuliarnol G30122048Yuliarnol Alik KarurukanBelum ada peringkat
- Materi Olimpiade KimiaDokumen9 halamanMateri Olimpiade KimiaDummy CipawBelum ada peringkat
- Sistem Periodik UnsurDokumen5 halamanSistem Periodik UnsurFatihah al MustanirohBelum ada peringkat
- Makalah Gol7aDokumen17 halamanMakalah Gol7aRucita KailaBelum ada peringkat
- Inisiasi 2 (KIMD)Dokumen6 halamanInisiasi 2 (KIMD)Asmaningrum SetyawatiBelum ada peringkat
- Sistem Periodik UnsurDokumen8 halamanSistem Periodik UnsurWahdiantiputri MunirBelum ada peringkat
- Materi Kimia Kelas XDokumen6 halamanMateri Kimia Kelas XYokoSimanjuntakBelum ada peringkat
- KimiaDokumen11 halamanKimiaLa TempoBelum ada peringkat
- Sifat UnsurDokumen30 halamanSifat UnsursamuelexaudyBelum ada peringkat
- X - Kimia - KD 3.4 - SIFAT-SIFAT PERIODIK UNSURDokumen12 halamanX - Kimia - KD 3.4 - SIFAT-SIFAT PERIODIK UNSURRima MelatiBelum ada peringkat
- X Kimia KD-3.4 FinalDokumen7 halamanX Kimia KD-3.4 FinalRizki SetiawanBelum ada peringkat
- Sistem Periodik Unsur - KIMIA KELAS XDokumen6 halamanSistem Periodik Unsur - KIMIA KELAS XTabitha Maudy Charoline Ginting100% (1)
- Sifat Keperiodikan UnsurDokumen9 halamanSifat Keperiodikan UnsurRhine ArdiBelum ada peringkat
- Keperiodikan UnsurDokumen58 halamanKeperiodikan UnsurNur FadiaBelum ada peringkat
- Tugas Periodik UnsurDokumen6 halamanTugas Periodik UnsurmahesBelum ada peringkat
- Makalah Kimia Kelompok 6Dokumen9 halamanMakalah Kimia Kelompok 6safrilBelum ada peringkat
- KIMIA - Contoh Makalah Sistem Priodik Unsur154409Dokumen6 halamanKIMIA - Contoh Makalah Sistem Priodik Unsur154409NurlailiBelum ada peringkat
- Sistem Periodik Unsur (Kelompok 8)Dokumen18 halamanSistem Periodik Unsur (Kelompok 8)Andi Isna YunitaBelum ada peringkat
- Sistem Periodik UnsurDokumen40 halamanSistem Periodik UnsurFajrian FaridhoBelum ada peringkat
- Bahan Ajar Sistem Periodik UnsurDokumen16 halamanBahan Ajar Sistem Periodik UnsurNita NurBelum ada peringkat
- 2..sistem Periodik UnsurDokumen20 halaman2..sistem Periodik UnsurALL PURNAWARMANBelum ada peringkat
- (PDF) Sifat Periodik UnsurDokumen20 halaman(PDF) Sifat Periodik Unsuryuni hartati eliya rosaBelum ada peringkat
- Sistem Periodik Unsur STPDokumen20 halamanSistem Periodik Unsur STPladestamBelum ada peringkat
- SIFATDokumen9 halamanSIFATLinda Dwi ApecawatiBelum ada peringkat
- Sistem Periodik UnsurDokumen34 halamanSistem Periodik UnsurKumpulan soalBelum ada peringkat
- 040 - Moh Threewahyu Saifulloh - Tugas TDA Week-3 - PKB22Dokumen6 halaman040 - Moh Threewahyu Saifulloh - Tugas TDA Week-3 - PKB22Egi 100PKB22Belum ada peringkat
- Makalah SpuDokumen11 halamanMakalah SpuCarlos Thomas100% (1)
- Sifat Keperiodikan Unsur Kelompok 3Dokumen14 halamanSifat Keperiodikan Unsur Kelompok 3MulyawatiBelum ada peringkat
- Sifat KimiaDokumen12 halamanSifat KimiaTiara PutrianaBelum ada peringkat
- Bab 1Dokumen41 halamanBab 1givvaBelum ada peringkat
- Pdfslide - Tips - Rincian Tugas Panitia UkkDokumen2 halamanPdfslide - Tips - Rincian Tugas Panitia UkkAristha Arsy50% (2)
- Cover PerangkatDokumen2 halamanCover PerangkatAristha ArsyBelum ada peringkat
- SKL KimiaDokumen38 halamanSKL KimiaAristha Arsy100% (1)
- Bahan Ajar Gas MuliaDokumen9 halamanBahan Ajar Gas MuliaAristha ArsyBelum ada peringkat
- RPP Kimia Unsur Alkali Sma 54 OkDokumen21 halamanRPP Kimia Unsur Alkali Sma 54 OkAristha ArsyBelum ada peringkat
- Lembar Kerja Peserta Didik GAS MULIADokumen2 halamanLembar Kerja Peserta Didik GAS MULIAAristha Arsy100% (1)
- Materi 1 Kompetensi GuruDokumen19 halamanMateri 1 Kompetensi GuruJuwita AgustinBelum ada peringkat
- Contoh Pengisian Evaluasi Diri Guru Untuk Pengembangan Keprofesian BerkelanjutanDokumen13 halamanContoh Pengisian Evaluasi Diri Guru Untuk Pengembangan Keprofesian BerkelanjutanAristha ArsyBelum ada peringkat