MODUL KIMIA
Diunggah oleh
Asyari Nurul FitriDeskripsi Asli:
Judul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
MODUL KIMIA
Diunggah oleh
Asyari Nurul FitriHak Cipta:
Format Tersedia
MODUL KIMIA
SMA IPA Kelas 12
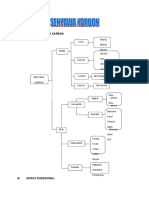
A. GUGUS FUNGSI
1. Gugus fungsi adalah gugus pengganti yang memiliki peranan besar terhadap sifat suatu senyawa
karbon.
2. Beberapa gugus fungsi yang akan dibahas sebagai berikut :
Gugus Fungsi Rumus umum Nama
R–X Haloalkana
R–OH Alkohol
R–O–R’ Eter
R–CHO Aldehid
R–CO–R’ Keton
R–COOH Asam karboksilat
R–COO–R’ Ester
Pada rumus diatas, R adalah gugus alkil, R = CnH2n+1.
B. HALOALKANA
1. Tata nama haloalkana
Aturan penamaan haloalkana :
a. Rantai induk (utama) harus mengandung halogen.
b. Atom C yang mengikat halogen diberi nomor serendah mungkin.
c. Nama halogen berakhiran O kemudian diikuti nama alkana rantai utama.
d. Bila terdapat lebih dari 1 jenis halogen, prioritas penomoran berdasarkan kereaktifan (F, Cl, Br,
I).
e. Halogen yang sejenis dinyatakan dengan awalan di, tri, tetra, dst.
2. Isomer haloalkana
Haloalkana dapat memiliki isomer rantai dan isomer posisi.
Contoh : isomer C4H9Cl
CH3-CH2-CH2-CH2-Cl 1 kloro butana
CH3-CH2-CH-CH3 2 kloro butana
Cl
E-book ini hanya untuk kalangan sendiri
tidak untuk dijualbelikan
1
MODUL KIMIA
SMA IPA KELAS 12
CH3-CH-CH2 1 kloro 2 metil propana
CH3 Cl
Cl
CH3-C-CH3 2 kloro 2 metil propana
CH3
3. Sifat-sifat haloalkana
a. Bereaksi dengan basa kuat menghasilkan alkohol.
b. Dengan pemanasan bersama alkoksida terjadi eliminasi.
4. Kegunaan haloalkana
a. Metilendiklorida (CH2Cl2) digunakan sebagai pelarut zat-zat organik dan sebagai pendingin.
b. Etilen dibromida ditambahkan ke dalam bensin agar timbal dalam TEL menjadi PbBr2 yang
mudah menguap dan mudah dikeluarkan bersama asap.
c. Kloroform dahulu digunakan sebagai zat anestesi tetapi sekarang tidak, kegunaan kloroform
sekarang untuk pelarut, sebagai zat anestesi digunakan 2 bromo 2 kloro 1,1,1 trifluoro etana
(halothane), dll.
C. ALKOHOL
1. Tata nama alkohol
a. Rantai C terpanjang yang merupakan nama alkananya harus mengikat gugus OH.
b. Atom C yang mengikat OH harus diberi nomor serendah mungkin.
c. Rantai C cabang harus diberi nomor sedekat mungkin terhadap C yang mengikat OH.
d. Urutan penamaan : nomor cabang, nama cabang, nomor letak gugus OH diikuti nama alkanol
rantai utama.
2. Jenis-jenis alkohol
a. Alkohol primer
Adalah alkohol yang gugus –OH nya terikat pada atom C primer.
Contoh : CH3-CH2CH2-OH
Rumus umum : R-CH2-OH
b. Alkohol sekunder
Adalah alkohol yang gugus –OH nya terikat pada atom C sekunder.
Contoh : CH3-CH2-CH-CH3
OH
Rumus umum : R-CH-R’
OH
c. Alkohol tersier
Adalah alkohol yang gugus –OH nya terikat pada atom C tersier.
Contoh : CH3
CH3-C-CH3
OH
E-book ini hanya untuk kalangan sendiri
2 tidak untuk dijualbelikan
MODUL KIMIA
SMA IPA Kelas 12
Rumus umum : R’
R-C-R’’
OH
3. Keisomeran alkohol
a. Isomer posisi
Adalah isomer yang terjadi karena perbedaan letak gugus –OH dalam molekul alkohol. Isomer
pposisi juga dapat didefnisikan sebagai senyawa yang mempunyai rumus molekulsama, gugus
fungsi sama, tetapi posisi gugus fungsinya berbeda.
Contoh : 1-propanol dan 2-propanol
b. Isomer optic
Adalah atom C yang terikat pada 4 gugus yang berbeda (atom C asimetrik).
Contoh : 2-butanol
c. Isomer fungsi
Adalah isomer yang terjadi karena perbedaan gugus fungsi di antara dua senyawa yang
mempunyai rumus molekul sama. Alkohol berisomer fungsi dengan eter.
4. Sifat-sifat alkohol
a. Sifat fisis
i. Bersifat polar karena memiliki gugus –OH.
ii. Mempunyai titik didih lebih tinggi dari eter. Hal ini disebabkan antara molekul alkohol
terjadi ikatan hidrogen.
iii. Metanol, etanol, dan propanol mudah larut, alkohol lainnya hanya sedikit larut.
b. Sifat kimia
i. Reaksi dengan natrium
Alkohol dapat bereaksi dengan logam Na membentuk alkoksida dan gas hidrogen.
2C2H5OH(aq) + 2Na(s) 2C2H5ONa(aq) + H2(g)
ii. Reaksi oksidasi
Alkohol primer dioksidasi akan menghasilkan aldehis. Jika dioksidasi lebih lanjut
akan menjadi asam karboksilat.
Alkohol sekunder dioksidasi akan menghasilkan keton.
Alkohol tersier tidak dapat dioksidasi.
iii. Reaksi esterifikasi
Alkohol dengan asam karboksilat dapat menghasilkan ester.
C2H5OH(aq) + CH3COOH(aq) CH3COOC2H5(aq) + H2O(l)
iv. Reaksi dengan asam sulfat pekat
Jika alkohol direaksikan dengan asam sulfat pekat, maka hasil reaksinya bergantung dari
suhu reaksi. Pada suhu ±180℃ akan dihasilkan alkena, sedangkan pada suhu ±140℃ akan
dihasilkan eter.
v. Reaksi dengan hidogen halide
Jika alkohol direaksikan dengan hidrogen halida akan terbentuk haloalkana dan air.
C2H5OH(aq) + HCl(aq) C2H5Cl(aq) + H2O(l)
5. Kegunaan alkohol
a. Metanol digunakan untuk pelarut dan bahan pembuat ester serta sebagai bahan bakar alternatif.
b. Etanol digunakan sebagai pelarut, desinfektan, bahan pembuatan ester dan sebagai bahan bakar.
c. Glikol juga digunakan sebagai bahan baku dalam industri serat sintesis dan pelarut.
E-book ini hanya untuk kalangan sendiri
tidak untuk dijualbelikan
3
MODUL KIMIA
SMA IPA KELAS 12
D. ETER
1. Tata nama eter
a. CH3-O-CH2-CH3
IUPAC : metoksi etana
Trivial : etil metil eter
b. CH3-O-CH2-CH2-CH3
IUPAC : 1-metoksi propane
Trivial : metil propil eter
2. Isomer fungsi antara eter dan alcohol
Alkohol dengan rumus umum R-OH dan eter dengan rumus umum R-O-R’ mempunyai isomer fungsi.
Alkohol dan eter mempunyai rumus molekul sama tetapi gugus fungsinya berbeda.
Contoh : 1-propanol dengan metoksi etana
3. Sifat-sifat eter
a. Sifat fisis
i. Berupa zat cair (kecuali metil eter(, brbau harum dan mudah menguap.
ii. Titik didihnya rendah karena tidak mempunyai ikatan hidrogen.
iii. Sukar larut dalam air.
b. Sifat kimia
i. Tidak bereaksi dengan logam Na dan PCl3 (reaksi ini dapat digunakan untuk membedakan
alkohol dengan eter).
ii. Bereaksi dengan PCl5, tetapi tidak membebaskan HCl (reaksi ini dapat digunakan untuk
membedakan alkohol dengan eter).
iii. Eter mudah terbakar membentuk gas CO2 dan uap air.
4. Kegunaan eter
a. Eter digunakan sebagai pelarut senyawa organik.
b. Dalam bidang kesehatan, eter banyak digunakan untuk obat pembius atau anestetik.
c. MTBE (metil tersier butil eter) ditambahkan ke dalam bensin untuk meningkatkan bilangan oktan.
E. ALDEHIDA
1. Tata nama aldehida
a. Nama sebagai alkanal (IUPAC).
b. Nama alkanal seperti alkana dengan mengganti akhiran ana dengan anal serta nomor 1 dimulai
dari gugus fungsi .
2. Isomer pada aldehida
Aldehida tidak mempunyai isomer posisi karena gugus fungsi aldehida terletak diujung rantai C.
Aldehida memilki isomer struktur yang terjadi karena adanya cabang dan letak cabang. Isomer aldehida
mulai terdapat pada suku ke-4 yaitu butanal.
Contoh : isomer pentanal adalah 2-metilbutanal, 3-metilbutanal, 2,2-dimetilpropanal)
3. Sifat-sifat aldehida
a. Sifat fisis
Suku pertama aldehida pada suhu kamar berwujud gas yang berbau merangsang, sedangkan suku
berikutnya berwujud cair yang berbau harum dengan semakin panjang rantai karbonnya.
b. Sifat kimia
i. Bila direduksi menghasilkan alkohol.
ii. Bila dioksidasi menghasilkan asam karboksilat.
iii. Dapat mengadisi HCN.
E-book ini hanya untuk kalangan sendiri
4 tidak untuk dijualbelikan
MODUL KIMIA
SMA IPA Kelas 12
iv. Dapat mereduksi larutan fehling membentuk endapan merah dan mereduksi pereaksi tollens
membentuk endapan Ag. Pereksi tollens adalah larutan AgNO3 dalam larutan NH3 berlebih.
v. Reaksi aldehida dengan larutan fehling menghasilkan endapan merah bata dari Cu2O.
4. Kegunaan aldehida
a. Untuk membuat formalin, yaitu 40% larutan formaldehida dalam air. Formalin digunkan untuk
mengawetkan contoh biologi dan juga mengawetkan mayat.
b. Formaldehida untuk membuat damar buatan, plastik, dan insektisida.
F. KETON
1. Tata nama keton
a. Sistem IUPAC, seperti pada alkana hanya akhiran ana diganti anon.
b. Sistem trivial dengan menyebutkan alkil-alkil yang mengapit gugus sesuai urutan abjad dan
diakhiri dengan keton.
2. Isomer pada keton
Isomer alkanon disebabkan oleh cabang, letak gugus fungsional dan isomer fungsional dengan
aldehida.
3. Sifat-sifat keton
a. Sifat fisis
i. Keton dengan suku rendah pada suhu kamar berwujud cair, tidak berwarna, berbau harum
dan mudah larut dalam air. Suku yang lebih tinggi sukar larut dalam air, dan berwujud padat.
ii. Keton termasuk senyawa polar dan larut dalam air.
b. Sifat kimia
i. Reaksi membedakan aldehida dan keton.
Aldehida + fehling endapan merah bata
Aldehida + tollens cermin perak
Keton + fehling tidak bereaksi
Keton + tollens tidak bereaksi
ii. Dapat direduksi menjadi alkohol sekunder.
4. Kegunaan keton
a. Pelarut senyawa karbon (aseton).
b. Sebagai bahan pengering alalt-alat laboratorium.
G. ASAM KARBOKSILAT
1. Tata nama asam karboksilat
a. Sistem IUPAC, seperti pada alkana hanya akhiran ana diganti anoat.
b. Sistem trivial sama seperti aldehida, hanya akhiran aldehid diganti dengan akhiran at.
2. Isomer asam karboksilat
Asam karboksilat tidak mempunyai isomer posisi karena gugus fungsinya terletak diujung rantai C.
Asam karboksilat memilki isomer struktur yang terjadi karena adanya cabang dan letak cabang.
3. Sifat-sifat asam karboksilat
a. Sifat fisis
i. Mulai dari C1 sampai C4 mudah larut dalam air. Makin panjang rantai C-nya makin sukar
larut dalam air.
ii. Titik didih dan titik lelehnya tinggi, karena antara molekulnya terdapat ikatan hidrogen.
E-book ini hanya untuk kalangan sendiri
tidak untuk dijualbelikan
5
MODUL KIMIA
SMA IPA KELAS 12
iii. Asam karboksilat merupakan asam lemah, semakin panjang rantai karbon semakin lemah
sifat asamnya.
iv. Suku-suku rendah berupa zat cair, sedangkan suku-suku yang lebih tinggi berupa zat padat.
b. Sifat kimia
i. Direaksikan dengan alkohol membentuk ester. Reaksi ini disebut reaksi esterifikasi.
ii. Dapat bereaksi dengan basa membentuk garam. Reaksi ini disebut penetralan.
iii.
4. Kegunaan asam karboksilat
a. Asam formiat yaitu untuk mengumpulkan lateks, penyamakan kulit, dan pada proses pencelupan
tekstil.
b. Sebagai bahan pembuatan ester dengan cara mereaksikan dengan alkohol.
c. Asam asetat digunakan untuk pengasam makanan.
d. Asam salisilat untuk membuat aspirin dan minyak gondopuro.
H. ESTER
1. Tata nama ester
Ester diberi nama sesuai dengan nama asalnya dan diberi awalan alkil yang menggantikan atom H pada
asam.
2. Isomer ester
Ester selain berisomer dengan sesama esterlainnya juga berisomer fungsi dengan asam karboksilat.
3. Sifat-sifat ester
a. Sifat fisis
i. Ester suku rendah berupa zat cair yang berbau harum (beraroma buah-buahan).
ii. Ester mudah menguap dibandingkan dengan asam atau alkohol pembentuknya.
iii. Ester sedikit larut dalam air.
iv. Ester memiliki titik didih dan titik beku yang lebih rendah dari titik didih dan titik beku
asam karboksilat.
b. Sifat kimia
i. Ester dapat mengalami hidrolisis menjadi asam karboksilat dan alkohol. Reaksi ini dikenal
dengan reaksi hidrolisis ester.
ii. Ester bersifat netral dan tidak bereaksi dengan logam natrium maupun PCl3.
iii. Ester mudah direduksi oleh gas hidrogen menjadi alkohol.
iv. Hidrolisis ester suku tinggi dengan NaOH atau KOH menghasilkan sabun dan gliserol
(reaksi penyabunan).
4. Kegunaan ester
a. Ester memiliki bau yang harum (khas), sehingga banyak dipakai sebagai essens buah-buahan.
b. Bahan pembuat sabun.
c. Ester digunakan untuk pembuatan mentega.
d. Sebagai pelarut pada pembuatan cat, cat kuku, dan perekat.
E-book ini hanya untuk kalangan sendiri
6 tidak untuk dijualbelikan
MODUL KIMIA
SMA IPA Kelas 12
Pilihlah satu jawaban yang tepat dengan member tanda pada salah satu huruf A, B, C, D dan E.
1. Senyawa berikut yang dapat menghasilkan C. pati
endapan merah bata bila direaksikan dengan D. maltosa
pereaksi fehling adalah ... E. sukrosa
A. CH3-CH2-CH2-OH
B. CH3-CH2-O-CH3 7. Margarin adalah mentega sintesis yang dapat
C. CH3-CH2-COH dibuat dari proses ...
D. CH3-CH2-COOH A. hidrogenasi lemak
E. CH3-COCH3 B. hidrolisis ester
C. oksidasi ester
2. Gugus fungsi berikut yang menyatakan D. adisi H2 dan aldehida
gugus fungsi aldehid, keton dan asam E. pemanasan lemak
karboksilat adalah ...
A. –COOH, -CO-, -COO 8. Senyawa golongan eter dengan rumus
B. –COH, -CO-, -COO- molekul C4H10O memiliki jumlah isomer ...
C. –COH, -CO-, -COOH A. 2
D. –COH, -COOH, -CO- B. 3
E. –COOH, -CO-, -COOH C. 4
D. 5
3. Senyawa dengan rumus struktur E. 6
CH3CH(C2H5)CH(Cl)CH(F)CH3 memiliki
nama ...
A. 3-kloro-2-fluoro-4-metil-heksana
9. Senyawa dengan rumus struktur
B. 3-kloro-2-fluoro-4-etil-pentana
CH3CH(C2H5)COCH(C2H5)CH3
C. 3-kloro-4-fluoro-2-etil-pentana
mempunyai nama ...
D. 4-kloro-5-fluoro-4-metil-heksana
A. 2,3-dietil-3-pentanon
E. 5-kloro-4-fluoro-4-metil-heksana
B. 2-etil-4-metil-3-heksanon
C. 3,5-dimetil-4-heptanon
4. Reaksi antara karbit (CaC2) dengan air
D. 5-etil-3-metil-4-heksanon
menghasilkan gas X, kemudian gas X
E. dibutil-1-keton
direaksikan dengan gas klor dengan jumlah
mol yang sama menghasilkan gas Y.
10. Senyawa di bawah ini yang dapat
Senyawa X dan Y berturut-turut adalah ...
membentuk endapan merah bata dengan
A. etena dan 1,1-dikloro-etana
pereaksi fehling adalah ...
B. etuna dan 1,1-dikloro-etena
A. CH3C(CH3)2CH3
C. etuna dan 1,2-dikloro-etena
B. CH3COCH3
D. etuna dan 1,2-dikloro-etana
C. CH3COH
E. etena dan 1,2-dikloro-etena
D. CH3OCH3
E. CH3CH(CH3)COCH3
5. Oksidasi 2 propanol menghasilkan ...
A. CH3CH2COOH
11. Senyawa karbon yang rumus molekulnya
B. CH3OCH3
C3H8O adalah ...
C. CH3COOH
A. etil metil eter
D. CH3COCH3
B. aseton
E. CH3CHO
C. propenal
D. asam propionat
6. Cara membuat etanol yang paling ekonomis
E. metil asetat
adalah dari ...
A. tetes tebu
B. glukosa
E-book ini hanya untuk kalangan sendiri
tidak untuk dijualbelikan
7
MODUL KIMIA
SMA IPA KELAS 12
12. Rumus struktur beberapa senyawa sebagai A. 2
berikut : B. 3
1) CH3CH2CHO C. 4
2) CH3CHOHCH3 D. 5
3) CH3COCH3 E. 8
Gugus fungsi senyawa tersebut bertururt-
turut adalah ... 18. Senyawa 2-metil-2-propanol berisomer
A. –CO-, -OH, -COOH fungsi dengan ...
B. –OH, -COH, -CO- A. 2-butanol
C. –COH, -OH-, -CO- B. 2-metil-1-propanal
D. –O-, -COH, -COO- C. 1-butanol
E. –OH, -CO-, -COH D. dietil eter
E. asam propanoat
13. Oksidasi 2 propanol akan menghasilkan ...
A. CH3CH2COOH 19. Isomer dari butanal adalah ...
B. CH3OCH3 A. asam propanoat
C. CH3COCH3 B. metil propanoat
D. CH3COOH C. etil metil keton
E. CH3COH D. metil propil eter
E. metoksi propana
14. Suatu senyawa X dapat bereaksi dengan
logam Na menghasilkan gas H2. Jika 20. Asam karboksilat yang dapat mereduksi
senyawa tersebut direaksikan dengan larutan Fehling maupun larutan Tollens
KMnO4 akan manghasilkan senyawa adalah ...
bereaksi positif terhadap fehling dan oksidasi A. asam propanoat
lebih lanjut akan menghasilkan senyawa B. asam sitrat
bersifat asam. Senyawa X adalah ... C. asam format
A. aldehida D. asam asetat
B. alkohol primer E. asam laktat
C. alkohol sekunder
D. alkohol tersier 21. Pada oksidasi suatu alkohol dihasilkan
E. asam karboksilat aseton (propanon). Alkohol yang dioksidasi
...
15. Suatu senyawa alkohol dioksidasi kuat A. 1-propanol
menghasilkan asam butanoat. Rumus B. 1-butanol
struktur alkohol tersebut ... C. 2-metil-1-propanol
A. CH3CH2CH2CH2OH D. 2-propanol
B. CH3CH(OH)CH2CH3 E. 2-butanol
C. CH3CH2CH2COH 22. Senyawa organik dengan rumus molekul
D. CH3C(CH3OH)CH3 C5H12O yang merupakan alkohol tersier ...
E. CH3CH(CH3)COH A. 3-pentanol
B. 2-metil-2-butanol
16. Yang merupakan isomer isopropanol adalah C. 2-metil-3-butanol
... D. 3-metil-2-butanol
A. propanal E. trimetiil karbinol
B. etil metil eter
C. aseton 23. Oksidasi dari suatu alkohol menghasilkan 2-
D. propenal pentanon. Alkohol tersebut adalah ...
E. propanon A. CH3(CH2)3CH2OH
B. (CH3)2CHCH2CH2OH
17. Berapa isomer dari senyawa C5H12O yang C. CH3CH2CHOHCH2CH3
merupakan eter ... D. CH3(CH2)2CH(OH)CH3
E-book ini hanya untuk kalangan sendiri
8 tidak untuk dijualbelikan
MODUL KIMIA
SMA IPA Kelas 12
E. CH3C(CH3)2CH2OH E. 2-metil-2propanol
24. Di bawah ini beberapa struktur senyawa 27. Nama yang tepat untuk senyawa
hidrokarbon : CH3CH2CH(OH)CH(CH3)C2H5 adalah ...
1) CH3CH(OH)CH3 A. 2-sekunder butil-1-butanol
2) CH3CH2COOCH3 B. 2,3-dietil-1-butanol
3) CH3CH2COOH C. 2-etil-3-metil-1-pentanol
4) CH3OCH2CH3 D. 4-metil-3-heksanol
5) CH3COCH3 E. isookatanol
Yang merupakan senyawa golongan ester
dan eter adalah ... 28. Senyawa yang merupakan isomer fungsional
A. 1 dan 2 dari butanol adalah ...
B. 2 dan 3 A. C2H5OC2H5
C. 2 dan 4 B. CH3CH2CH2COH
D. 3 dan 5 C. CH3COCH2CH3
E. 4 dan 5 D. CH3CH(OH)CH2CH3
E. CH3CH2CH2COOH
25. Senyawa yang merupakan isomer fungsional
dari etoksi etana (dietil eter) adalah ... 29. Rumus empiris dari dihaloalkana adalah ...
A. CH3CH2CH2CH2OH A. CnH2n+2X2
B. CH3CH2CH2COH B. CnH2n+1X2
C. CH3CH2COCH3 C. CnH2n-1X
D. CH3CH2COOCH3 D. CnH2n-2X2
E. CH3CH2CH2CH(OH)CH3 E. CnH2nX2
26. Suatu alkohol dengan rumus molekul
C4H10O dioksidasi dengan kalium dikromat 30. Senyawa karbon yang digunakan untuk obat
dalam asam menghasilkan butanon, maka bius adalah ...
alkohol tersebut adalah ... A. CH2OH-CH2OH
A. n-butanol B. CHF2-CHCl2
B. 2-butanol C. CF3-CHClBr
C. tersier-butil-alkohol D. CH3CH2OH
D. 2-metil-1-propanol E. CH2OH-CHOH-CH2OH
E-book ini hanya untuk kalangan sendiri
tidak untuk dijualbelikan
9
Anda mungkin juga menyukai
- Tugas Kimia Sulthan, Yoga, Rafi, Dan DafaDokumen28 halamanTugas Kimia Sulthan, Yoga, Rafi, Dan DafaSuhaibi SuhaibiBelum ada peringkat
- Kunci Jawaban Soal Paket 2@Dokumen22 halamanKunci Jawaban Soal Paket 2@mina ajaBelum ada peringkat
- Pengetahuan Dan Pemahaman Umum 1 - 12Dokumen3 halamanPengetahuan Dan Pemahaman Umum 1 - 12ahtisa cutipieBelum ada peringkat
- Isi Praktikum KimiaDokumen14 halamanIsi Praktikum KimiaReyhan AhmadBelum ada peringkat
- Soal Kimia Unsur KelompokDokumen16 halamanSoal Kimia Unsur KelompokghinaBelum ada peringkat
- Laporan LiterasiDokumen13 halamanLaporan LiterasiYopi Amera PutriBelum ada peringkat
- Amir Nilai CerpenDokumen5 halamanAmir Nilai CerpentaufikBelum ada peringkat
- Dimensi Tiga dan KubusDokumen6 halamanDimensi Tiga dan KubusWilliam DoloksaribuBelum ada peringkat
- RedoksDokumen16 halamanRedoksdiksaBelum ada peringkat
- Berikut ini jawaban untuk soal-soal pilihan ganda di atas:1. C2. E 3. D4. B5. B6. D7. B 8. CDokumen7 halamanBerikut ini jawaban untuk soal-soal pilihan ganda di atas:1. C2. E 3. D4. B5. B6. D7. B 8. CWildana67% (3)
- ALKOHOL DAN ETERDokumen3 halamanALKOHOL DAN ETERRian ImantaBelum ada peringkat
- SOAL LATIHAN UN - UNBK - USBN SMA PROGRAM IPSDokumen18 halamanSOAL LATIHAN UN - UNBK - USBN SMA PROGRAM IPSManuel JonathanBelum ada peringkat
- Soal-Soal AldehidaDokumen12 halamanSoal-Soal AldehidaFriedrich Rabin SitumorangBelum ada peringkat
- OPTIMIZED TITLEDokumen15 halamanOPTIMIZED TITLEHafipBelum ada peringkat
- Soal To 3 Paket 02Dokumen16 halamanSoal To 3 Paket 02Firman M Ady100% (1)
- JAWABANDokumen9 halamanJAWABANTsabita AfaaninBelum ada peringkat
- SOAL US 2020 OceDokumen16 halamanSOAL US 2020 OceAddyeHanEunWookBelum ada peringkat
- Senyawa Karbon dan TurunannyaDokumen30 halamanSenyawa Karbon dan TurunannyaYulida erdaniBelum ada peringkat
- F1c020140-Kimia Pers ReaksiDokumen6 halamanF1c020140-Kimia Pers ReaksiTaja Purnama HandikaBelum ada peringkat
- ElastisitasDokumen9 halamanElastisitasYayu Sri Rahayu SardiBelum ada peringkat
- DuniaFayDokumen4 halamanDuniaFayramaersamBelum ada peringkat
- JUDULDokumen7 halamanJUDULFennika EllaBelum ada peringkat
- Bab 9 Alkana, Alkena, Dan AlkunaDokumen28 halamanBab 9 Alkana, Alkena, Dan AlkunaoveBelum ada peringkat
- Ade Novia AnggraeniDokumen26 halamanAde Novia AnggraeniNanna Arina KhairunisaBelum ada peringkat
- Senyawa Alkohol Struktur dan PenamaanDokumen3 halamanSenyawa Alkohol Struktur dan PenamaanGunBelum ada peringkat
- Soal PG FungiDokumen3 halamanSoal PG FungiSiti MaulidhiahBelum ada peringkat
- OPTIMIZED TITLESDokumen10 halamanOPTIMIZED TITLESannazirohBelum ada peringkat
- LKPD 6Dokumen9 halamanLKPD 6nurfauziyyahepBelum ada peringkat
- PMDP Bidikmisi Poltekes SemarangDokumen10 halamanPMDP Bidikmisi Poltekes SemarangRBelum ada peringkat
- Contoh Soal Essay BIODokumen14 halamanContoh Soal Essay BIOVanesa NesaBelum ada peringkat
- Gerak Tari KreasiDokumen5 halamanGerak Tari KreasidhinormBelum ada peringkat
- LKPD Enzim KatabolismeDokumen6 halamanLKPD Enzim KatabolismeSilvi Oktaviani SaridewiBelum ada peringkat
- TUGAS HALAMAN 25Dokumen1 halamanTUGAS HALAMAN 25Ilham Guntur MaulanaBelum ada peringkat
- Gametogenesis SsilaDokumen2 halamanGametogenesis SsilaAsilah RasyidBelum ada peringkat
- Bab 7. Hereditas Pada Manusia - Xii IpaDokumen7 halamanBab 7. Hereditas Pada Manusia - Xii IpaAndre JendikaBelum ada peringkat
- PKN Vanessa Xii Mm2Dokumen17 halamanPKN Vanessa Xii Mm2Vanessa AndreaBelum ada peringkat
- Review Film InterstellarDokumen6 halamanReview Film InterstellarInayatun Mu'zizaBelum ada peringkat
- Soal Usp Raudhatul Jannah Dengan KunciDokumen12 halamanSoal Usp Raudhatul Jannah Dengan KunciYulia NingsihBelum ada peringkat
- Soal US Bahasa Indonesia SMA - 1Dokumen10 halamanSoal US Bahasa Indonesia SMA - 1Anandita RizkiaBelum ada peringkat
- Dalam Peredaran Darah ManusiaDokumen60 halamanDalam Peredaran Darah ManusiaSiti Uswaton HasanahBelum ada peringkat
- ALKOHOL-ETER KIMIA Kelas XIIDokumen13 halamanALKOHOL-ETER KIMIA Kelas XIIAulia KhalishaBelum ada peringkat
- IsomerDokumen28 halamanIsomerAlbar100% (1)
- Gol AlkanolDokumen12 halamanGol AlkanolRegina NernereBelum ada peringkat
- Kuis Simak Ui-4 - 210610 - 102943Dokumen3 halamanKuis Simak Ui-4 - 210610 - 102943Brian GilchristBelum ada peringkat
- (Answered) Soal Usbn Pai Sma-Smk K-13 Paket 1Dokumen15 halaman(Answered) Soal Usbn Pai Sma-Smk K-13 Paket 1Queen ABelum ada peringkat
- Alkoksi Alkana (Eter)Dokumen18 halamanAlkoksi Alkana (Eter)Ayu RizsaBelum ada peringkat
- LATIHAN SOAL UASBN 2021 - JawabanDokumen11 halamanLATIHAN SOAL UASBN 2021 - JawabanMardi WayanBelum ada peringkat
- Cara Memasak Makanan Khas DaerahDokumen15 halamanCara Memasak Makanan Khas Daerahnabila0% (1)
- Uji Makanan Dalam Zat MakananDokumen8 halamanUji Makanan Dalam Zat Makananmifty wahidBelum ada peringkat
- Bank Soal Try Out SBMPTN BiologiDokumen4 halamanBank Soal Try Out SBMPTN Biologienongg_Belum ada peringkat
- TALAKDokumen6 halamanTALAKhsfly3424Belum ada peringkat
- LKPD Evolusi 3 BIO - YITNU IBNU SANTOSO - 12 MIPA 2Dokumen3 halamanLKPD Evolusi 3 BIO - YITNU IBNU SANTOSO - 12 MIPA 2BillyDarmawanBelum ada peringkat
- BAB I (Repaired) Hidrok@rbonDokumen47 halamanBAB I (Repaired) Hidrok@rbonMuzakirBelum ada peringkat
- Tugas Mutasi 1Dokumen5 halamanTugas Mutasi 1ditaayu syahfitriBelum ada peringkat
- Konstiusi Republik Indonesia Serikat: Verenigde Staten Van IndonesiëDokumen20 halamanKonstiusi Republik Indonesia Serikat: Verenigde Staten Van IndonesiëCaroline TannesaBelum ada peringkat
- PkwuDokumen4 halamanPkwuAdhitama AlbevanBelum ada peringkat
- Program G To G Korea SelatanDokumen12 halamanProgram G To G Korea SelatanGeuman ChajgoBelum ada peringkat
- Contoh Soal SOalDokumen28 halamanContoh Soal SOalMia Herlina NasutionBelum ada peringkat
- AlkoholDokumen12 halamanAlkoholhidayats65Belum ada peringkat
- Uswatun Khasanah - 2ega - Resume Alkohol Dan EterDokumen13 halamanUswatun Khasanah - 2ega - Resume Alkohol Dan EterUswatun KhasanahBelum ada peringkat
- Kimia 12 1 Sifat Koligatif Larutan PDFDokumen15 halamanKimia 12 1 Sifat Koligatif Larutan PDFmuhamad tharmiziBelum ada peringkat
- Tata Tertib Dan PenegakannyaDokumen2 halamanTata Tertib Dan PenegakannyaAsyari Nurul FitriBelum ada peringkat
- Berikut ini jawaban untuk soal-soal pilihan ganda di atas:1. C2. E 3. D4. B5. B6. D7. B 8. CDokumen7 halamanBerikut ini jawaban untuk soal-soal pilihan ganda di atas:1. C2. E 3. D4. B5. B6. D7. B 8. CWildana67% (3)
- Kimia 11 3 Laju Reaksi-1Dokumen13 halamanKimia 11 3 Laju Reaksi-1Asyari Nurul FitriBelum ada peringkat
- KIMIA REDOKSDokumen18 halamanKIMIA REDOKSAndin Tasyalia BudayaBelum ada peringkat
- PolimerDokumen9 halamanPolimerErwinda WindaBelum ada peringkat
- Kimia 11 4 Kesetimbangan KimiaDokumen13 halamanKimia 11 4 Kesetimbangan Kimiakansha nursalsabilaBelum ada peringkat
- RPP X - 3Dokumen19 halamanRPP X - 3SudjanaBelum ada peringkat
- KIMIA MODULDokumen20 halamanKIMIA MODULAgestya HernawatiBelum ada peringkat
- RPP 2Dokumen19 halamanRPP 2Desi AsnalBelum ada peringkat
- KOROSI BESIDokumen6 halamanKOROSI BESIAsyari Nurul FitriBelum ada peringkat
- GLBBDokumen24 halamanGLBBAkhy Syamsudin Al-fatihBelum ada peringkat
- New Format KKM Excel Kelas 10 Asli 2018Dokumen37 halamanNew Format KKM Excel Kelas 10 Asli 2018Christeon IyonBelum ada peringkat
- RPP 1Dokumen13 halamanRPP 1Oom Saepul RohmanBelum ada peringkat
- KD 3.7 AlkaliDokumen14 halamanKD 3.7 AlkaliAsyari Nurul FitriBelum ada peringkat
- Halogen KimiaDokumen24 halamanHalogen KimiaAsyari Nurul FitriBelum ada peringkat
- HUKUM FARADAYDokumen7 halamanHUKUM FARADAYAsyari Nurul FitriBelum ada peringkat
- Sma Negeri Padang RPP KimiaDokumen9 halamanSma Negeri Padang RPP Kimiacindra lamusu0% (1)
- KD 3.1 Dan 3.2 SIFAT KOLIGATIFDokumen22 halamanKD 3.1 Dan 3.2 SIFAT KOLIGATIFGiytaa CupicupiiBelum ada peringkat