Analisis Materi
Diunggah oleh
Agung PrawotoJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Analisis Materi
Diunggah oleh
Agung PrawotoHak Cipta:
Format Tersedia
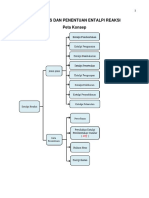
ANALISIS MATERI
1. Fakta
1. Salah satu contoh reaksi eksoterm adalah pembakaran.
2. Salah satu contoh reaksi endoterm adalah pelarutan urea dalam air.
2. Konsep
1. Persamaan termokimia adalah persamaan reaksi atau persamaan kimia yang
mengikutsertakan nilai perubahan entalpi.
2. Entalpi Pembentukan Standar adalah kalor yang diperlukan atau dibebaskan untuk proses
pembentukan 1 mol senyawa dari unsur-unsurnya yang stabil dalam keadaan standar (298
K,1atm)
3. Entalpi Penguraian Standar adalah kalor yang diperlukan atau dibebaskan untuk proses
penguraian 1 mol senyawa menjadi unsur-unsurnya yang stabil dalam keadaan standar (298
K,1atm)
4. Entalpi Pembakaran Standar adalah kalor yang dibebaskan untuk pembakaran 1 mol zat unsur
atau senyawa pada keadaan standar (298 K ,1 atm).
5. Entalpi Pelarutan Standar adalah kalor yang dibebaskan atau diperlukan untuk melarutkan 1
mol zat pada keadaan standar (298 K, 1 atm, dan konsentrasi 1 M).
6. Perubahan entalpi netralisasai adalah perubahan entalpi yang terjadi pada saat reaksi antara
asam dengan basa baik tiap mol asam atau tiap mol basa.
7. Reaksi penetralan merupakan reaksi yang terjadi antara Larutan Asam Kuat dan Larutan Basa
Kuat menghasilkan Garam dan Air. pH penetralan = 7 (Netral).
8. Pembakaran didefenisikan sebagai reaksi kimia yang di dalamnya suatu zat bereaksi dengan
Oksigen (O2) yang menghasilkan kalor dan zat hasil reaksi tertentu.
9. Reaksi Penguraian: reaksi yang terjadi untuk menguraikan senyawa menjadi unsur-
unsurnya.
Anda mungkin juga menyukai
- Laporan Praktikum TermokimiaDokumen24 halamanLaporan Praktikum Termokimiakhofidhotur rofiah88% (8)
- 1.g Refleksi Pembelajaran - Identifikasi MasalahDokumen1 halaman1.g Refleksi Pembelajaran - Identifikasi MasalahAgung Prawoto100% (2)
- LK 1.3 Penentuan Penyebab MasalahDokumen4 halamanLK 1.3 Penentuan Penyebab MasalahAgung PrawotoBelum ada peringkat
- Perubahan EntalpiDokumen5 halamanPerubahan EntalpiMuhammad ShidiqBelum ada peringkat
- Perubahan EntalpiDokumen2 halamanPerubahan Entalpiwidya oktaBelum ada peringkat
- PERSAMAAN TERMOKIMIA DAN DH StandarDokumen5 halamanPERSAMAAN TERMOKIMIA DAN DH StandarMunandar MunandarBelum ada peringkat
- Makalah Kimia FisikaDokumen10 halamanMakalah Kimia FisikaShendy PratamaBelum ada peringkat
- Tambahan TinjauanDokumen17 halamanTambahan TinjauanasriBelum ada peringkat
- Makalah Perubahan EntalpiDokumen8 halamanMakalah Perubahan EntalpiTiara NopiraBelum ada peringkat
- Reaksi Eksoterm Dan Reaksi EndotermDokumen3 halamanReaksi Eksoterm Dan Reaksi EndotermRidho Rokim100% (1)
- Term Okimi ADokumen11 halamanTerm Okimi Aadella reditaBelum ada peringkat
- Menentukan Delta H ReaksiDokumen10 halamanMenentukan Delta H ReaksiZahabi AlkaniBelum ada peringkat
- Jenis-Jenis Entalpi ReaksiDokumen7 halamanJenis-Jenis Entalpi ReaksiNURHANIPAHBelum ada peringkat
- Termokimia - Wikipedia Bahasa Indonesia, Ensiklopedia BebasDokumen7 halamanTermokimia - Wikipedia Bahasa Indonesia, Ensiklopedia BebasNabila Nur AlifaBelum ada peringkat
- Persamaan Termokimia Dan Jenis Perubahan Entalpi StandarDokumen3 halamanPersamaan Termokimia Dan Jenis Perubahan Entalpi StandarNurrahim Bambang SholihinBelum ada peringkat
- KTutorial Menjawab Soal Tentang JenisDokumen7 halamanKTutorial Menjawab Soal Tentang JenisReza AuliaBelum ada peringkat
- Tugas Resume Kelompok 3Dokumen3 halamanTugas Resume Kelompok 3Patria WibowoBelum ada peringkat
- Reaksi Termokimia Dan Perbahan EntalpiDokumen2 halamanReaksi Termokimia Dan Perbahan EntalpiAriny ZaqiyahBelum ada peringkat
- Kimia Bab 2 Rangkuman Termokimia & Energitika 11 SmaDokumen8 halamanKimia Bab 2 Rangkuman Termokimia & Energitika 11 SmarischanganjukBelum ada peringkat
- TERMOKIMIA (1) Reaksi Endoterm Dan Reaksi Eksoterm, Entalpi Dan Perubahan Entalpi, Perubahan Entalpi Standar, Dan Persamaan TermokimiaDokumen18 halamanTERMOKIMIA (1) Reaksi Endoterm Dan Reaksi Eksoterm, Entalpi Dan Perubahan Entalpi, Perubahan Entalpi Standar, Dan Persamaan Termokimialia agustinaBelum ada peringkat
- Once Upon A Time in KoreaDokumen1 halamanOnce Upon A Time in KoreaMelisa PandjaitanBelum ada peringkat
- Kimia TermodinamikaDokumen7 halamanKimia TermodinamikaAdhetya NingrumBelum ada peringkat
- Persamaan TermokimiaDokumen4 halamanPersamaan TermokimiaZainal HasibuanBelum ada peringkat
- Entalpi StandarDokumen10 halamanEntalpi StandarNovitasari VitaBelum ada peringkat
- Laporan Termokimia PDFDokumen9 halamanLaporan Termokimia PDFzoelfadillh0% (1)
- Perubahan EntalpiDokumen14 halamanPerubahan EntalpiFanya AlyaBelum ada peringkat
- Modul 1Dokumen17 halamanModul 1Dilla NisaBelum ada peringkat
- 3-ANALISIS VOLUMETRI TAMBANG Bag 1 (Compatibility Mode)Dokumen24 halaman3-ANALISIS VOLUMETRI TAMBANG Bag 1 (Compatibility Mode)Yoga Anugrah Pratama PutraBelum ada peringkat
- Termokimia - Wikipedia Bahasa Indonesia, Ensiklopedia BebasDokumen6 halamanTermokimia - Wikipedia Bahasa Indonesia, Ensiklopedia BebasFaiz nur FauzanBelum ada peringkat
- Entalpi Dan PerubahannyaDokumen16 halamanEntalpi Dan PerubahannyaSintya doh KyungsooBelum ada peringkat
- Konsep TermokimiaDokumen2 halamanKonsep TermokimiaMartinus Ciko Rolly100% (1)
- TermokimiaDokumen18 halamanTermokimiaCut HaqBelum ada peringkat
- Rangkuman Materi TermokinmiaDokumen4 halamanRangkuman Materi Termokinmiashella168Belum ada peringkat
- Jenis Entalpi PDFDokumen11 halamanJenis Entalpi PDFMuhammad CharishBelum ada peringkat
- Bab Iii - Termokimia (Pertemuan 2)Dokumen11 halamanBab Iii - Termokimia (Pertemuan 2)Jonathan Oswald Rayford MayautBelum ada peringkat
- Laporan Praktikum Kimia DasarDokumen15 halamanLaporan Praktikum Kimia DasarJose ChristianBelum ada peringkat
- Kalor ReaksiDokumen13 halamanKalor ReaksiBellaDwiAulinaBelum ada peringkat
- Kimia Dasar 1 EnergitikaDokumen10 halamanKimia Dasar 1 EnergitikaRully RimansyahBelum ada peringkat
- Laporan PENGAMATAN KIMIA 1Dokumen23 halamanLaporan PENGAMATAN KIMIA 1Khoirunnisa RahmawatiBelum ada peringkat
- Modul 3 TermokimiaDokumen12 halamanModul 3 Termokimiarizky kadhafiBelum ada peringkat
- Termokimia NewDokumen60 halamanTermokimia NewVhyiitrii Shanqk Peñjhaqa HaatiiBelum ada peringkat
- Termokimia (Pendahuluan) JDokumen6 halamanTermokimia (Pendahuluan) JWindy Wulandari0% (1)
- Termokimia Kelompok 1Dokumen20 halamanTermokimia Kelompok 1macro computerBelum ada peringkat
- 6 TermokimiaDokumen17 halaman6 TermokimiaAldilla ZuhraBelum ada peringkat
- Termokimia 1Dokumen54 halamanTermokimia 1Hafidz Naufal SyamaidzarBelum ada peringkat
- Termokimia (Artikel)Dokumen11 halamanTermokimia (Artikel)Sri MulyatiBelum ada peringkat
- TERMOKIMIADokumen2 halamanTERMOKIMIAUmi RohmayantiBelum ada peringkat
- Lapter P1 Kalor ReaksiDokumen26 halamanLapter P1 Kalor ReaksiDiah Ayu SafitriBelum ada peringkat
- SadasdDokumen21 halamanSadasdAldi JonataBelum ada peringkat
- TERMOKIMIADokumen34 halamanTERMOKIMIAAnggraeni eniBelum ada peringkat
- TermokimiaDokumen7 halamanTermokimiaerdyBelum ada peringkat
- LKPD Perubahan EntalpiDokumen2 halamanLKPD Perubahan EntalpiWa Ode JuniatiBelum ada peringkat
- TermokimiaDokumen20 halamanTermokimiaIndah NovitaBelum ada peringkat
- Term Okimi ADokumen19 halamanTerm Okimi ADeri SaputraBelum ada peringkat
- PERCOBAAN I (Termokimia)Dokumen33 halamanPERCOBAAN I (Termokimia)Sunflower100% (1)
- Isi LKPDDokumen14 halamanIsi LKPDAgung PrawotoBelum ada peringkat
- Analisis PengetahuanDokumen2 halamanAnalisis PengetahuanAgung PrawotoBelum ada peringkat
- Analisis KonsepDokumen4 halamanAnalisis KonsepAgung PrawotoBelum ada peringkat
- RPP TermokimiaDokumen8 halamanRPP TermokimiaAgung PrawotoBelum ada peringkat
- Modul ThermokimiaDokumen141 halamanModul ThermokimiaAgung PrawotoBelum ada peringkat