Larutan Penyangga
Diunggah oleh
Muflikhah Noor AsmiarsariJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Larutan Penyangga
Diunggah oleh
Muflikhah Noor AsmiarsariHak Cipta:
Format Tersedia
- 1 - KIMIA SMA
LARUTAN
PENYANGGA
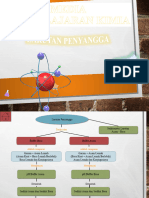
Larutan penyangga: suatu larutan yang mampu mempertahankan ph pada kisarannya apabila terjadi
upayaa untuk menaikkan atau menurunkan ph Ada dua larutan penyangga:
Larutan penyangga asam; terdiri dari asam lemah (HA) dan basa konjugasinya (A-),
dilambangkan dengan HA/A-. HA(aq) H+(aq) + A-(aq) Exp : CH3COOH/CH3COOCH3COOH(aq) H+(aq) + CH3COO-(aq)
Larutan penyangga basa; terdiri dari basa lemah (B) dan asam konjugasinya (BH+),
dilambangkan dengan B/BH+ B(aq) + H2O(l) BH+(aq) + OH-(aq) Exp : NH3/NH4+ NH3(aq) + H2O(l) NH4H+(aq) + OH-(aq) Prinsip kerja larutan penyangga dapat dilihat pada contoh berikut ini:
Bukan larutan penyangga
+ 0.01 M HCl Air murni
Air murni + 0.01 M HCl
Pada larutan bukan penyangga ketika ditambahkan , sejumlah mol asam terjadi perubahan ph secara drastis dari 7 menjadi 2
pH = 7 Larutan penyangga asam HA /A
-
pH = 2
CH3 COOH/ CH3COO -
+ 0.01 M HCl
Larutan penyangga + 0.01 M HCl pH = 4.66
Pada larutan penyangga ketika ditambahkan sejumlah , mol asam, pH larutan tidak berubah secara signifikan (hanya sekitar 0.08 poin, tergantung banyaknya mol asam yang ditambahkan
pH = 4.74
pH larutan penyangga asam dapat dipertahankan pada kisarannya, bila terjadi penambahan sedikit asam kuat, sedikit basa kuat, dan pengenceran. pH larutan penyangga basa dapat dipertahankan pada kisarannya, bila terjadi penambahan basa kuat, Cara membuat larutan penyangga adalah sebagai berikut: asam kuat, dan pengenceran.
Penyangga asam CH3COOH/CH3COO-
Asam lemah CH3COOH hanya terurai sebagian kecil sehingga CH3COO- yang terbentuk sedikit sekali. Untuk membuat larutan penyangga ini, konsentrasi CH3COO- harus dinaikkan.
Terionisasi sebagian
CH3COOH (aq)
Asam lemah
H+(aq) + CH 3COO - (aq)
Basa konjugasi
Konsentrasi basa konjugasi CH3COO- dapat dinaikkan dengan cara:
http://jejaringkimia.blogspot.com RINO SAFRIZAL
- 2 - KIMIA SMA
Menambahkan garam seperti CH3COONa ke dalam asam lemah CH3COOH
Tambahan basa konjugasi Terionisasi sebagian
CH 3COONa
(aq)
Na +(aq) + CH 3COO - (aq)
Garam natrium asetat
Menambahkan basa kuat seperti NaOH ke dalam asam lemah berlebih
Tam bahan basa konjugasi Terionisasi sebagian
+
CH 3COOH
(aq )
+ NaOH
(aq)
Na
(aq)
+ CH 3COO -(aq ) + H2O(l)
Basa kuat
Penyangga basa NH3/NH4+
Basa lemah NH3 juga terurai sedikit menjadi NH4+. Untuk membentuk larutan penyangga ini, maka konsentrasi ion NH4+ harus dinaikkan.
Terionisasi sebagian
NH3(aq) + H2O(l )
Basa lemah
NH4+(aq) + OH -(aq)
Asam konjugasi
Konsentrasi asam konjugasi NH4+ dapat dinaikkan dengan cara: Menambahkan garam seperti NH4Cl ke dalam larutan basa lemah
Tambahan asam konjugasi
NH3Cl (aq)
Amonium klorida
NH4+(aq) + Cl -(aq)
Menambahkan asam kuat seperti HCl ke dalam basa lemah berlebih
Tambahan asam konjugasi
NH3(aq) + HCl(aq)
Asam klorida
NH4+ (aq) + Cl -(aq)
Menentukan pH larutan penyangga pH penyangga asam HA/A- bergantung pada tetapan ionisasi Ka dan perbandingan konsentrasi
asam lemah HA dan basa konjugasi ApH = pKa - log n HA nA
-
----------------------------------------------------------------------------- 1 Di mana: pKa n HA nA
-
= - log Ka = jumlah mol asam lemah HA = jumlah mol basa konjugasi ApH penyangga basa B/BH+ bergantung pada tetapan ionisasi Kb dan perbandingan konsentrasi
basa lemah B dan asam konjugasi BH+
pH = pKb - log nB n BH+
-----------------------------------------------------------------------------2 Di mana:
http://jejaringkimia.blogspot.com RINO SAFRIZAL
- 3 - KIMIA SMA
pKb nB
= - log Kb = jumlah mol basa lemah B n BH+ = jumlah mol asam konjugasi BH+
http://jejaringkimia.blogspot.com
RINO SAFRIZAL
Anda mungkin juga menyukai
- Larutan PenyanggaDokumen16 halamanLarutan PenyanggaPedi Apriansyah100% (1)
- Sistem BufferDokumen11 halamanSistem BufferObet Buni PonaBelum ada peringkat
- Materi KD 3.12.1 Larutan PenyanggaDokumen4 halamanMateri KD 3.12.1 Larutan PenyanggaAbeBelum ada peringkat
- Kesetimbangan Asam-BasaDokumen30 halamanKesetimbangan Asam-BasaLelianna BarusBelum ada peringkat
- Media Larutan Penyangga MateriDokumen8 halamanMedia Larutan Penyangga MateriWardian AntoniBelum ada peringkat
- Larutan PenyanggaDokumen7 halamanLarutan PenyanggaSyafiqaBelum ada peringkat
- Makalah Larutan PenyanggaDokumen20 halamanMakalah Larutan PenyanggaGhea Rigo Navida Insides67% (3)
- LARUTAN PENYANGGA Buffer Solution PDFDokumen7 halamanLARUTAN PENYANGGA Buffer Solution PDFChaca ChadijahBelum ada peringkat
- 6-7. Larutan Penyangga & Hidrolisis XI IPA Genap 23-24 (Share)Dokumen16 halaman6-7. Larutan Penyangga & Hidrolisis XI IPA Genap 23-24 (Share)Neko HatsuneBelum ada peringkat
- Larutan DaparDokumen19 halamanLarutan DaparIden DzuhurBelum ada peringkat
- Bahan AjarDokumen5 halamanBahan AjarMichael Obaja FebrianoBelum ada peringkat
- Kimia Dasar - Kesetimbangan Asam BasaDokumen40 halamanKimia Dasar - Kesetimbangan Asam BasaIti IIBelum ada peringkat
- BAB 3. Larutan PeyanggaDokumen11 halamanBAB 3. Larutan PeyanggaOcta RenitaBelum ada peringkat
- Larutan PenyanggaDokumen34 halamanLarutan Penyanggawd_amaliaBelum ada peringkat
- Larutan Penyangga (Buffer) Kimdas 2Dokumen40 halamanLarutan Penyangga (Buffer) Kimdas 2Danang PK-1BBelum ada peringkat
- Larutan Penyangga AsamDokumen10 halamanLarutan Penyangga Asamayupujilarasati26Belum ada peringkat
- Cara Kerja Larutan Penyangg1Dokumen8 halamanCara Kerja Larutan Penyangg1Prima ElfBelum ada peringkat
- MODUL Larutan Penyangga MamahDokumen7 halamanMODUL Larutan Penyangga Mamahfadhila anjaniBelum ada peringkat
- Buffer Dan TitrasiDokumen21 halamanBuffer Dan Titrasikim shin liuBelum ada peringkat
- Larutan PenyanggaDokumen21 halamanLarutan PenyanggaAgus Darmadi Sala100% (7)
- Larutan Penyangga FixedDokumen37 halamanLarutan Penyangga FixedAhmad Fajar NoviantoBelum ada peringkat
- Larutan PenyanggaDokumen27 halamanLarutan PenyanggaDaniatul FitriBelum ada peringkat
- Larutan BufferDokumen12 halamanLarutan BufferTara DamayantiBelum ada peringkat
- Hidrolisis GaramDokumen11 halamanHidrolisis GaramRetri AtikaBelum ada peringkat
- Kesetimbangan Asam-BasaDokumen39 halamanKesetimbangan Asam-BasaRizki AuliaBelum ada peringkat
- Larutan PenyanggaDokumen26 halamanLarutan Penyanggahana amabrwatiBelum ada peringkat
- Manajemen Asam BasaDokumen8 halamanManajemen Asam BasaNadiah Ulfah FajrindBelum ada peringkat
- Larutan PenyanggaDokumen24 halamanLarutan PenyanggaocktiBelum ada peringkat
- Larutan Penyangga FIXDokumen37 halamanLarutan Penyangga FIXz7gv47vbmxBelum ada peringkat
- Bahan Ajar BufferDokumen5 halamanBahan Ajar BufferRafiqo hafidBelum ada peringkat
- Anggi Fatika - Handout Larutan PenyanggaDokumen16 halamanAnggi Fatika - Handout Larutan PenyanggaanggifaaaBelum ada peringkat
- Asam Dan BasaDokumen116 halamanAsam Dan BasaSafril JuntakBelum ada peringkat
- Modul Hidrolisis Dan BufferDokumen3 halamanModul Hidrolisis Dan BufferDionovtaBelum ada peringkat
- Bab 4 Larutan PenyanggaDokumen5 halamanBab 4 Larutan PenyanggaMirza Irwansyah AmmaryBelum ada peringkat
- Larutan PenyanggaDokumen10 halamanLarutan PenyanggaAnis safitriBelum ada peringkat
- Hidrolisis, Buffer, TitrasiDokumen17 halamanHidrolisis, Buffer, TitrasiJihanvelayatiBelum ada peringkat
- Laporan Praktikum Kimia DasarDokumen9 halamanLaporan Praktikum Kimia DasarNisa GaluhBelum ada peringkat
- TeksDokumen5 halamanTeksNiken Arma HidayahBelum ada peringkat
- Draft Lks Larutan PenyanggaDokumen10 halamanDraft Lks Larutan PenyanggalusiBelum ada peringkat
- Quantum Edu Center - Ringkasan Materi Kimia Kelas XI Semester 2Dokumen25 halamanQuantum Edu Center - Ringkasan Materi Kimia Kelas XI Semester 2Agus Styawan75% (8)
- BufferDokumen44 halamanBufferYanBelum ada peringkat
- Kimia RasyidDokumen5 halamanKimia RasyidRasyid SyahridhoBelum ada peringkat
- Asam Dan BasaDokumen26 halamanAsam Dan BasaAnanda DwiBelum ada peringkat
- Larutan PenyanggaDokumen3 halamanLarutan PenyanggaMnurimran MadunBelum ada peringkat
- LB 3Dokumen6 halamanLB 327. SYAHRIN AZRIL IZULKHAQUEBelum ada peringkat
- Reaksi Penetralan AsamDokumen10 halamanReaksi Penetralan AsamAneed KasparovBelum ada peringkat
- Larutan PenyanggaDokumen19 halamanLarutan PenyanggaShillea Olimpia Melyta100% (1)
- Asam - BasaDokumen38 halamanAsam - BasaRoselina TurnipBelum ada peringkat
- Larutan PenyanggaDokumen38 halamanLarutan PenyanggaariniBelum ada peringkat
- Larutan PenyanggaDokumen13 halamanLarutan PenyanggaStanley SahetapyBelum ada peringkat
- Kimia Kurva Titrasi Asam BasaDokumen7 halamanKimia Kurva Titrasi Asam BasaReyhan MahadikaBelum ada peringkat
- Kegiatan Pembelajaran 3Dokumen7 halamanKegiatan Pembelajaran 3Herry Purwanto PanjaitanBelum ada peringkat
- Larutan BufferDokumen3 halamanLarutan BufferNursifa RatnasariBelum ada peringkat
- Bahan Ajar Larutan PenyanggaDokumen8 halamanBahan Ajar Larutan PenyanggaAiisatul MunawarohBelum ada peringkat