Jurnal Thalasemia
Diunggah oleh
Nurinda TamalaJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Jurnal Thalasemia
Diunggah oleh
Nurinda TamalaHak Cipta:
Format Tersedia
Tinjauan Pustaka
Gangguan pertumbuhan
sebagai komplikasi talasemia • mayor
Nur Robbiyah, Hakimi, Melda Deliana, Siska Mayasari.
Departemen Ilmu Kesehatan Anak Fakultas Kedokteran Universitas Sumatera Utara/
Rumah Sakit Umum Pusat H. Adam Malik, Medan
Abstrak
Talasemia Is-mayor merupakan penyakit kelainan darah yang diturunkan secara genetik. Gangguan pertumbuhan
merupakan komplikasi yang sering dijumpai pada pasien talasemia Is-mayor. Patogenesis gangguan pertumbuhan pada
pasien talasemia Is-mayor disebabkan oleh multi faktor diantaranya anemia kronis dan hipoksia, gangguan fungsi hati,
defisiensi zink dan asam folat, iron overload dan toksisitas anti kelasi besi. Manajemen yang tepat bagi setiap pasien
talasemia Is-mayor, seperti pengenalan dini gangguan pertumbuhan, pemberian terapi kelasi yang tepat adalah sangat
penting untuk memperbaiki kualitas hidup.
Kata kunci : talasemia ß-mayor; gangguan pertumbuhan
Abstract
Beta-thalassemias major are a group of hereditary blood disorders disease. Growth disorders are afrequent complication of
patient with Beta-thalassemias major. The pathogenesis of disorders is multifactorial and is mainly due to chronic anemia and
hypoxia, chronic liver disease, zinc and folic acid deficiency, iron overload and intensive use of chelating agents. Proper
management of each patient with beta-thalassemias major include early recognition of growth disorders and appropriate of
iron chelation therapy is very important to improve the quality of life.
Keywords : beta-thalassemias major; growth disorders
PENDAHULUAN gangguan pertumbuhan pada pasien talasemia Is-mayor
Talasemia Is-mayor merupakan penyakit kelainan darah bervariasi.
yang diturunkan secara genetik, dengan karakteristik kurangnya Studi di Malaysia didapati 54.4%,5 studi di Iran didapati
atau tidak ada sintesa rantai Is hemoglobin, yang 62%,6 sedangkan studi di India didapati 54% anak talasemia
mengakibatkan penurunan kadar hemoglobin dalam sel darah Is-mayor mengalami gangguan pertumbuhan.7,8
merah, penurunan produksi sel darah merah dan anemia.1,2 Tingginya angka kejadian gangguan pertumbuhan pada
Penanganan paling utama pada pasien talasemia Is-mayor talasemia Is-mayor, selain disebabkan oleh anemia kronis
adalah pemberian transfusi darah secara rutin. Pasien talasemia yang tidak mendapat transfusi yang adekuat, beberapa faktor
Is-mayor yang tidak mendapatkan terapi transfusi atau tidak yang berperan terhadap terjadinya kerusakan organ endokrin
mendapat transfusi yang adekuat kerap mengalami keterlam- adalah iron overload, toksisitas Desferoxamine (DFO) yaitu
batan pertumbuhan dan pubertas.2 iron chelathing agent yang berfungsi untuk mengurangi
Efek transfusi darah secara rutin dapat memperpanjang kelebihan besi, faktor emosional, defisiensi zink dan asam
kelangsungan hidup penderita talasemia Is-mayor, namun folat serta gangguan fungsi hati.1,3,9
dapat menimbulkan keadaan iron overload. Komplikasi yang Beberapa pemeriksaan untuk menilai gangguan
dapat terjadi akibat iron overload adalah hemosiderosis yang pertumbuhan yang terjadi pada pasien talasemia Is-mayor yaitu
pada akhirnya akan menyebabkan gangguan pada berbagai pengukuran tinggi badan, kecepatan pertumbuhan, penilaian
organ seperti hati, jantung, dan organ endokrin.2,3 potensi tinggi genetik (PTG), status pubertas, usia tulang, fungsi
Beberapa kelainan endokrin yang ditimbulkan antara lain tiroid dan Growth hormone (GH).9
gangguan pertumbuhan dan perkembangan, keterlambatan Untuk mengurangi kejadian gangguan pertumbuhan pada
pubertas yang dapat disertai dengan kerusakan pada aksis pasien talasemia Is-mayor harus dilakukan manajemen pembe-
hipotalamus-hipofisis dan diabetes mellitus (DM).4 rian transfusi yang benar, pemberian terapi iron chelating agent
Dari beberapa penelitian dilaporkan angka kejadian yang tepat, monitoring pertumbuhan pada semua anak talasemia
E-mail : nurrobbiyah75@yahoo.co.id
44 | Majalah Kedokteran Nusantara • Volume 47 • No. 1 • April 2014
Nur Robbiyah, dkk Gangguan pertumbuhan sebagai komplikasi talasemia • mayor
I-mayor dan pemberian terapi GH bila memang dijumpai tahun, faktor emosional, defisiensi zink dan asam folat serta
defisiensi GH.1,9 anemia kronis dan hipoksia merupakan faktor penyebab terja-
dinya gangguan pertumbuhan pada pasien talasemia I-mayor.16
DEFINISI Penyakit kronis mempengaruhi kesehatan psikologis dan
Pertumbuhan didefinisikan sebagai proses meningkatnya kepercayaan diri pasien talasemia I-mayor. Gangguan cemas,
ukuran sel oleh penambahan jaringan, dapat diamati pada depresi, gangguan emosi dan gangguan somatik adalah masa-
seluruh organisme, bagian tubuh, sistem organ dan pada sel.10 lah psikologis yang banyak ditemukan pada pasien talasemia I-
Pertumbuhan merupakan proses interaksi beberapa faktor mayor.13
seperti faktor genetik, lingkungan terutama nutrisi, serta Gangguan psikologis dapat mempengaruhi gangguan
pengaruh faktor endokrin. Pertumbuhan pada anak terjadi pertumbuhan dengan mempengaruhi hipofisis anterior
terutama pada lempeng epifisis yang merupakan tempat mengakibatkan terjadinya defisiensi GH.10
terjadinya deposisi tulang sehingga terjadi penambahan tinggi Defisiensi zink merupakan faktor yang berperan dalam
badan.11 gangguan pertumbuhan pada pasien talasemia I-mayor. Zink
Pertumbuhan terbagi menjadi beberapa tahapan yaitu sebagai elemen penting pada banyak aktifitas metabolisme,
pertumbuhan prenatal, pertumbuhan pasca natal yang seperti sintesis DNA pada sel-sel pertumbuhan dan sintesis
terbagi menjadi fase bayi, kanak-kanak dan fase pubertas. protein.
Pertumbuhan pasca natal pada fase bayi ditandai oleh Zink diabsorbsi pada usus kecil, dan lebih dari 80% zink
pertumbuhan yang pesat, kemudian diikuti penurunan kece- berikatan dengan albumin dalam sirkulasi darah. Defisiensi
patan tumbuh secara progresif.11,12 zink dapat menyebabkan keterlambatan perkembangan,
Masa pubertas mempunyai dua peranan pada pertumbuhan kebotakan, diare dan kehilangan berat badan.
yaitu akselerasi kecepatan pertumbuhan dan maturasi skeletal Zink diekresi melalui urin dan meningkat akibat hemolisis
yang meningkat akibat penutupan lempeng tulang epifisis. yang terjadi pada pasien talasemia, pemberian agen kelasi
Beberapa faktor hormonal berperan dalam mempengaruhi besi juga dapat meningkatkan ekskresi zink melalui urin.9,12,18
pertumbuhan pebertas yaitu GH, Insuline Like Growth Hormone Anemia kronis dan hipoksia terjadi akibat penderita tala-
Factor- I (IGF-I), hormon steroid seks, dan hormon tiroid.10,11 semia I mayor tidak mendapat transfusi yang adekuat, hal ini
Gangguan pertumbuhan adalah gangguan pada kecepatan juga menyebabkan gangguan pertumbuhan, anak tumbuh
pertumbuhan tinggi berdasarkan umur dan derajat pubertas, lebih kecil dari saudara kandungnya yang normal.1
apakah anak tersebut pendek atau tinggi dari pengukuran Hipoksia yang berat akan merangsang produksi
tinggi dan dari potensi tinggi orang tua.12 eritropoetin dengan ekspansi yang terus menerus tetapi tidak
Pola pertumbuhan pada pasien talasemia yang mendapat efektif pada sumsum tulang yang menyebabkan
transfusi relatif normal sampai usia 9 sampai 10 tahun, mulai hipersplenisme. Splenomegali meningkatkan konsumsi darah,
terganggu dimana kecepatan pertumbuhan mulai melambat meningkatkan kelebihan besi, memperburuk anemia yang
yang menyebabkan terjadinya perawakan pendek.13-15 memberikan pengaruh negatif terhadap pertumbuhan.17
Dikatakan perawakan pendek bila : 10-15 Akan tetapi anemia kronis dan hipoksia saat ini tidak lagi
1. Tinggi badan dibawah persentil 3 atau -2 SD untuk usia memberikan kontribusi yang lama terhadap terjadinya
dan jenis kelamin gangguan pertumbuhan apabila pasien talasemia mayor
2. Tinggi badan signifikan dibawah PTG yaitu -2 SD dibawah mendapat transfusi secara teratur.9
PTG Jika transfusi diberikan secara teratur dan kadar Hb
3. Kecepatan pertumbuhan yang lambat dipertahankan lebih dari 9 g/dL maka anak akan mengalami
Rata-rata kecepatan pertumbuhan pada fase yang berbeda: pertumbuhan dan perkembangan yang normal sampai usia
a) Fase prenatal : 1.2 sampai 1.5 cm perminggu 10-12 tahun.2,8,17
b) Fase bayi : 23 sampai 28 cm pertahun Pemberian transfusi yang regular pada pasien talasemia
c) Kanak-kanak : 5 sampai 6.5 cm pertahun I-mayor menyebabkan terjadi iron overload. Hal ini dapat
d) Pubertas: 8.3 cm/pertahun (perempuan) memicu terjadinya kerusakan jaringan akibat penumpukan
9,5 cm pertahun (laki-laki) radikal bebas pada organ.
4. Pertumbuhan menurun memotong garis persentil pada Transfusi darah yang diberikan secara teratur akan
kurva pertumbuhan terutama setelah usia 18 bulan. mengakibatkan pemenuhan kapasitas pengikatan besi
transferin di tubuh, akibatnya besi bebas ini akan terakumulasi
Patofisiologi gangguan pertumbuhan pada pasien tala- dalam jaringan dan darah. Tanpa intervensi terapi, besi bebas
semia R-mayor yang dikenal dengan non transferin binding protein (NTBI) akan
Gangguan pertumbuhan pada pasien talasemia I-mayor bersirkulasi sistemik ke jaringan sebagai radikal bebas dan
disebabkan oleh multi faktor yaitu disebabkan oleh anemia merusak lemak, protein dan DNA sehingga menimbulkan
kronis dan hipoksia, gangguan fungsi hati, defisiensi zink kerusakan organ seperti hati jantung dan organ endokrin.1,3,16,19
dan asam folat, iron overload, toksisitas DFO, faktor Setiap unit sel darah merah menghantarkan 200 sampai
emosional, dan gangguan endokrin.9,16,17 250 mg besi melalui transfusi, tanpa pemberian agen kelasi
Pada tahap awal kehidupan, yaitu usia satu sampai lima besi 10 sampai 20 unit atau lebih taransfusi sel darah merah
The Journal of Medical School, University of Sumatera Utara | 45
Nur Robbiyah, dkk
akan meningkatkan risiko kerusakan organ.20 hemosiderosis pada organ tersebut. Gonadotropin yang
Kelebihan besi pada organ endokrin pada beberapa studi dihasilkan oleh hipofisis anterior sangat sensitif terhadap
memperlihatkan kelainan endokrin, yang paling banyak adalah kerusakan oksidatif yang disebabkan oleh kelebihan zat besi.
hipogonadotropik hipogonadisme, defisiensi GH, diabetes me- Pada MRI hipofisis anterior dijumpai gambaran penurunan
llitus, hipotiroid, hipoparatiroid dan insufisiensi adrenal.4,21-25 intensitas sinyal spin–echo dari hipofisis, hal ini dikaitkan
Pengaruh hormonal sebagai penyebab gangguan pertum- dengan meningkatnya deposisi besi di hipofisis anterior dan
buhan pada pasien talasemia Is-mayor sangatlah kompleks, dapat menjadi alat investigasi yang berguna dalam penilaian
selain disebabkan oleh hipogonadisme, hipotiroidisme, jaras hemosiderosis hipofisis.9,25
GH-IGF-I secara nyata berperan terhadap gangguan pertum- Untuk meneliti pengaruh pubertas terlambat terhadap
buhan.9 pertumbuhan linier remaja talasemia digunakan skala Tanner
Pada pemeriksaan dengan Magnetic Resonance Imaging dalam memantau perkembangan seksualnya, pengukuran
(MRI) didapati deposisi besi pada kelenjar hipofisis anterior.9,24 hormon gonadotropin seperti: Luteinizing Hormone (LH),
Deposisi besi menyebabkan kerusakan hipofisis anterior Folicle-Stimulating Hormone (FSH) dan Hormon Testosteron.
yang mengakibatkan terganggunya jaras GH-IGF-I.9,25 Didapati hasil bahwa keterlambatan pubertas berpengaruh
Kerusakan pada hipofisis anterior menyebabkan pelepasan terhadap gangguan pertumbuhan pada pasien talasemia.24
GH terganggu, yang mengakibatkan produksi IGF-I dan Penumpukan besi pada sel gonad pada hipofisis anterior
IGFBP3 oleh hati terganggu karena stimulasi GH terhadap hati menyebabkan berkurangnya sekresi hipofisis anterior yang
berkurang, sehingga terjadi penurunan GH dan IGF-I. memicu terjadinya hipogonadotropik hipogonadisme dan
Defisiensi GH dan IGF-I mempengaruhi kecepatan pubertas terlambat.13 (gambar 2).
pertumbuhan tulang pada lempeng pertumbuhan tulang.10
(gambar 1)
46 Gambar 1. Jaras GH-IGF-I26
Beberapa studi melakukan uji provokasi untuk menilai
respons GH pada pasien talasemia Is-mayor yang mengalami
perawakan pendek. Satu studi melaporkan sekresi GH yang
normal pada beberapa anak namun beberapa anak dijumpai
responsnya menurun setelah dilakukan uji provokasi.27
Studi lain yang juga melakukan uji provokasai didapati
respons GH terhadap Growth Hormone Releasing Hormon
(GHRH) dilaporkan menurun,28 satu studi yang lain didapati
responsnya normal.29 Sedangkan serum IGF-I dan IGFBP
didapati rendah pada sebagian besar sampel setelah uji uji
provokasi.29,30
Hipogonadisme merupakan komplikasi endokrin paling
sering pada pasien talasemia Is-mayor dan merupakan penye-
bab penting gangguan pertumbuhan pada saat remaja.
Hipogonadotropik-hipogonadisme terjadi akibat kerusakan
hipotalamus dan hipofisis anterior yang disebabkan oleh Gambar 3. Jaras Hipotalamus-hipofisis-gonad31
46 | Majalah Kedokteran Nusantara • Volume 47 • No. 1 • April 2014
Gangguan pertumbuhan sebagai komplikasi talasemia • mayor
Beberapa studi melaporkan prevalensi hipotiroidisme pada dan saudara kandung anak tersebut. Perkiraan tinggi
talasemia I-mayor, pada penelitian ini dijumpai hubungan yang dewasa seorang anak berhubungan dengan target tinggi
signifikan antara perawakan pendek dengan hipotiroid.32,33 kedua orang tua.10 Potensial tinggi genetik (PTG)
Hormon tiroid berperan penting dalam maturasi tulang, dihitung dengan menggunakan rumus berikut:10
mempengaruhi sekresi GH, mempengaruhi kondrosit secara
langsung dengan meningkatkan sekresi IGF-I, serta - PTG laki-laki : Tinggi ayah + ( tinggi ibu + 13 cm) ± 8,5 cm
memacu maturasi kondrosit.11 2
Kadar serum ferritin yang tinggi selama dekade pertama
kehidupan akibat pemberian transfusi mengakibatkan - PTG Perempuan : Tinggi ibu + (tinggi ayah-13 cm) ± 8,5 cm
terjadinya perawakan pendek, keadaan ini merupakan indikasi 2
untuk pemberian terapi iron chelating agent yang berguna
untuk mencegah atau membatasi komplikasi ini.3,9 Bila didapati pola pertumbuhan anak mengalami deviasi
Obat pertama yang tersedia adalah Desferoxamine (DFO).2 dari orang tua atau saudara kandungnya maka di dapati
Akan tetapi beberapa studi menunjukkan tingginya kejadian kondisi patologis yang mendasarinya, tetapi bila didapati
perawakan pendek pada anak dan remaja talasemia yang kelainan patologis yang nyata dari orang tua maka
mendapat pengobatan dengan DFO secara intensif.1,3,9 Hal ini pengukuran ini tidak dapat digunakan.10
disebabkan oleh intoksikasi DFO yang dapat menghambat 3. Menilai kecepatan pertumbuhan
proliferasi sel, menghambat sintesis DNA, mengganggu Pertumbuhan merupakan suatu proses yang dinamik,
deposisi mineral seperti kuprum dan zink.1,9 sehingga diperlukan pengukuran yang berkala untuk
Mekanisme yang kompleks tersebut menyebabkan platis- mengukur kecepatan pertumbuhan dalam satu satuan
pondilosis dimana dijumpai vertebra menjadi rata, pemendekan waktu.11 Minimal harus ada dua titik pengukuran supaya
tulang panjang,9 dan pemendekan spinal yang menyebabkan dapat menilai kecepatan pertumbuhan. Dengan demikian
penurunan tinggi badan baik dalam keadaan duduk maupun dapat dilihat pola pertumbuhan anak, apakah sejajar
berdiri.9,17 dengan persentil atau melenceng. Anak dengan gangguan
Pemberian terapi iron chelating agent yang terlalu cepat pertumbuhan akan mengalami pertumbuhan di bawah
yaitu pada usia antara 2 sampai 5 tahun dapat juga meng- persentil 25 pada kurva kecepatan pertumbuhan10
ganggu pertumbuhan, hal ini disebabkan karena sebelum 4. Pemeriksaan status pubertas.
tubuh mengalami kelebihan besi akibat pemberian transfusi, Sebagaimana telah dikatakan di atas bahwa keterlambatan
DFO menjadi kelasi terhadap mineral lain selain besi.34 pubertas berpengaruh terhadap gangguan pertumbuhan
pada pasien talasemia.9,25
Prosedur untuk menilai gangguan pertumbuhan Penumpukan besi pada sel gonad pada hipofisis anterior
Gangguan pertumbuhan merupakan komplikasi yang sering menyebabkan berkurangnya sekresi hipofisis anterior yang
dijumpai pada pasien talasemia I-mayor. Pola pertumbuhan memicu terjadinya hipogonadotropik hipogonadisme dan
pada anak tersebut relatif normal sampai usia 10 tahun. Anak pubertas terlambat. Oleh sebab itu perlu dilakukan penilaian
talasemia I-mayor harus secara rutin dimonitor pertumbuhan status pebertas.13
dan perkembangannya sampai mencapai tinggi dewasa dan Status pubertas dapat dinilai dengan menggunakan skala
perkembangan seksual yang lengkap.35 Tanner. Pemeriksaan ini harus dilakukan setiap 6 bulan
Beberapa pemeriksaan yang dilakukan untuk menilai sejak usia 10 tahun sampai mencapai perkembangan
gangguan pertumbuhan yang terjadi pada pasien talasemia seksual yang lengkap. Untuk menilai volume testis dengan
I-mayor:9 menggunakan Orchidometer (Prader)35
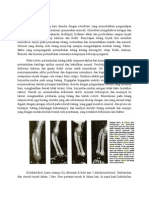
1. Pengukuran tinggi badan berdiri atau duduk. 5. Menilai maturasi tulang.
Pengukuran ini dilakukan setiap 6 bulan, pengukuran Maturasi tulang dapat diamati secara langsung dengan
tinggi badan ini selanjutnya diproyeksikan pada kurva melihat pertumbuhan lempeng epifisis dengan menggu-
pertumbuhan sesuai usia dan jenis kelamin.9 Kurva nakan X-ray.
pertumbuhan digunakan untuk memantau pertumbuhan Pada anak normal, didapati pusat perkembangan epifisis
anak sesuai dengan populasi acuannya. Untuk negara- sesuai usia, yang memungkinkan untuk dihasilkannya
negara yang tidak memiliki kurva pertumbuhan, WHO standart maturasi tulang pada masing jenis kelamin
menganjurkan penggunaan kurva The Centres Disease selama masa anak dan remaja.12
Control and Prevention ( CDC) sebagai acuan, akan Usia tulang ( bone age ) merupakan pengukuran kuantitatif
tetapi kurva ini menggunakan populasi Amerika Serikat, maturasi fisik tulang, caranya adalah dengan memban-
sehingga tidak sesuai untuk setiap negara dan perlu dingkan Wrist X-ray pasien dengan Wrist X-ray normal
penyesuaianpenyesuaian tertentu. 11 untuk laki-laki dan perempuan seperti yang terlihat pada
2. Pengukuran Potensial Tinggi Genetik (PTG) atlas Greulich and Pyle. Kegunaan dari penilaian usia
Oleh karena faktor genetik mempunyai pengaruh penting tulang ini adalah untuk memonitor potensi pertumbuhan
terhadap pertumbuhan dan potensi tinggi seorang anak, dari waktu ke waktu, dapat juga digunakan untuk menentu-
maka sangat penting menilai perawakan dari orang tua kan perkiraan tinggi dewasa.12
The Journal of Medical School, University of Sumatera Utara | 47
Nur Robbiyah, dkk
6. Pemeriksaan darah rutin, jumlah ferritin, fungsi hati dan 4. Evaluasi endokrin.
zink, elektrolit dan urin rutin. Evaluasi endokrin harus dilakukan bila dijumpai penurunan
7. Pemeriksaan fungsi tiroid (T3,T4,TSH), GH dan IGF-I. kurva pertumbuhan, penurunan kecepatan pertumbuhan (<
persenti 25) dan keterlambatan maturitas tulang.35,37
Manajemen penatalaksanaan gangguan pertumbuhan Evaluasi ini meliputi:37
pada pasien talasemia R-mayor - Penilaian status diet oleh ahli gizi
Manajemen penatalaksanaan gangguan pertumbuhan - Pemeriksaan laboratorium : Serum Ca, PO4, albumin,
pada pasien talasemia Is-mayor, harus mencakup semua asam urat, kultur
aspek yang menjadi penyebab gangguan pertumbuhan urin, T4, TSH dan IGF-I
tersebut, seperti transfusi yang tidak optimal, gangguan 5. Diagnosa pasti penyebab gangguan pertumbuhan
endokrin, defisiensi zink, dan toksisitas DFO. Hal ini dilakukan untuk memastikan apakah gangguan
Manajemen yang tepat bagi setiap pasien talasemia Is- pertumbuhan disebabkan oleh defisiensi GH, gangguan
mayor, seperti pengenalan dini gangguan pertumbuhan, hormon lainnya, defisiensi nutrisi, atau disebabkan oleh
pemberian terapi kelasi yang tepat adalah sangat penting toksisitas DFO. Bila dijumpai defisiensi GH harus segera
untuk memperbaiki kualitas hidup.9 dilakukan uji stimulasi GH untuk memastikan adanya
1. Pemberian transfusi secepatnya bila diagnosis telah defisiensi GH.15 Uji stimulasi GH yang dilakukan dapat
ditegakkan. berupa uji toleransi insulin, uji arginin, uji levadova, uji
Transfusi teratur seumur hidup harus dilakukan untuk klonidin, ataupun dengan latihan fisik38
menekan eritropoesis, mencegah hipoksia kronis dan 6. Pemberian terapi GH bila dijumpai defisiensi GH.
mencegah hipersplenisme. Lamanya jarak antara setiap Pemberian terapi GH telah menunjukkan peningkatan
transfusi adalah 2 sampai 6 minggu tergantung berat pertumbuhan untuk jangka pendek dan juga peningkatan
badan, umur, pekerjaan dan jadwal sekolah. Pemantauan tinggi akhir saat dewasa pada anak-anak dengan berbagai
rutin Hb sebelum transfusi, dimana akan optimal bila kadar macam masalah pertumbuhan.11,39 Tetapi penggunaan
Hb sebelum transfusi 9 g/dL sampai 10.5 g/dL.3,13 terapi GH ini hanya direkomendasikan bila memang
2. Pemberian suplementasi seperti zink dan asam folat Pada dijumpai defisiensi GH.15,37 Hal ini disebabkan efek samping
satu studi yang membandingkan antara dua kelompok, yang dapat muncul akibat pemakaian terapi GH tersebut.40
dimana kelompok pertama adalah pasien talasemia Is- Kriteria diagnosis defisiensi GH:11
mayor yang mendapat suplementasi zink dengan dosis 60 - TB dibawah persentil 3 atau -2SD
mg sekali sehari selama 18 bulan, sedangkan kelompok - Kecepatan pertumbuhan di bawah P25
kedua adalah kelompok pasien talasemia Is-mayor yang - Usia tulang terlambat > 2 tahun
tidak mendapat zink. Pada penelitian tersebut dihasilkan - Kadar GH<7 ng/ml pada 2 jenis uji provokasi -
pemberian suplementasi zink hanya bermanfaat pada IGF-I rendah
pasien talasemia Is-mayor yang mengalami defisiensi zink, - Tidak ada kelainan dismorfik tulang atau sindroma
sedangkan profilaksis zink tidak mempunyai efek terhadap tertentu.
pertumbuhan linier.18 Recombinant human GH (rhGH) merupakan GH sintetik
3. Pencegahan terhadap Iron overload yang mulai ada sejak tahun 1980an, yang bekerja sebagai
Terapi iron chelating agent dapat diberikan jika pasien pengganti GH di hipofisis anterior pasien dengan defisiensi
sudah menerima 100ml/kg PRC, serum feritin lebih dari GH. Dosis yang direkomendasikan untuk defisiensi GH
1000 µg/L, jika anak sudah tiga sampai lima tahun adalah 23-39 µg/kgbb/hari atau 0.7-1.0 mg/m2/hari dengan
menggunakan DFO dan tidak dijumpai tanda-tanda gagal dosis maksimal 2.7 mg/hari. Respons yang dinilai untuk
tumbuh dan ekskresi besi dinilai baik, dan konsentrasi besi memantau terapi GH :41
di hati (diukur 1 tahun setelah transfusi) melebihi 7 mg/g 1. Penilaian secara regular terhadap pertumbuhan anak
berat kering hati yang diukur dengan menggunakan biopsi setiap 3 bulan selama satu tahun.
hati maupun MRI.1 Terapi iron chelating agent dimulai 2. Bila respons pengobatan memuaskan, interval penilaian
dengan pemberian DFO dengan dosis 20-40 mg/kgbb/hari dapat diperpanjang menjadi 4-6 bulan
selama 8 sampai 12 jam, 5 sampai 7 hari perminggu, dosis 3. Pemeriksaan fungsi tiroid dilakukan pertahun atau bila
maksimal tidak boleh melebihi 50 mg/kgbb/hari.13-15,35 Suatu ada indikasi
penelitian membandingkan antara iron chelating agent oral 4. Penilaian status hipofisis untuk menilai kemungkinan
yaitu deferiprone dan subkutan yaitu DFO. Pada studi defisiensi hormon lain yang tersembunyi akibat
tersebut diambil kesimpulan bahwa iron chelating agent pemakaian terapi GH
oral sedikit lebih efektif dibandingkan dengan pemberian 5. Terapi hormon seks untuk menginduksi pubertas pada
iron chelating agent subkutan sebagai terapi iron chelating waktu yang tepat, bila ada indikasi
agent pada hepar, dan sangat potensial dalam 6. Penilaian terhadap perkembangan, respons dan
mengeluarkan besi dari kelenjar endokrin dan jantung, berbagai perubahan selama pengobatan.
karena kerja deferiprone dapat melakukan penetrasi Terapi GH harus segera dihentikan bila respons pengobatan
hingga intraselular.36 tidak adekuat yaitu bila peningkatan kecepatan pertumbuhan
48 | Majalah Kedokteran Nusantara • Volume 47 • No. 1 • April 2014
Gangguan pertumbuhan sebagai komplikasi talasemia • mayor
< 2 cm/tahun.41 Guideline for the clinical management of thalassemia. 2nd
Ed. Cyprus: Thalassemia International Federation; 2011.
RINGKASAN p. 64-70.
Gangguan pertumbuhan merupakan komplikasi yang cukup 15. Ibrahim HM, Ayob Y, Mahayiddin AA, Sathar J, Musa Z,
banyak terjadi pada anak yang menderita talasemia ß-mayor. Bakri R, et al. Management of transfusion dependent
Anemia kronis, transfusi darah yang tidak adekuat, penumpukan thalassaemia. Malaysia: Ministry of Health Malaysia;
besi pada organ-organ endokrin dan efek samping dari penggu- 2009. p.1-84.
naan terapi kelasi besi merupakan beberapa penyebab terja- 16. Skordis N. Endocrine investigation and follow up in
dinya gangguan pertumbuhan pada pasien talasemia ß-mayor. thalassemia: times for specific guidlines. Thalassemia
Tatalaksana yang tepat dapat mencegah dan mengatasi reports. 2011;1:1-16.
gangguan pertumbuhan pada pasien talasemia ß- mayor. 17. Sanctis V, Urso, Scialpi, Mangiagli. Endocrine complications
in ß-thalassemia major. In: Maggio A, Hoffbrand AV, editors.
DAFTAR PUSTAKA Clinical aspects and therapy of haemoglobinopathies. Italy:
1. Weatherall DJ, Clegg JB. The ß- thalassaemias. In: Proprieta letteraria riservata; 2004. p. 293-310.
Weatherall DJ, Clegg JB, editors. The thalassaemia 18. Faranoush M, Rahiminejad MS, Karamizadeh Z,
syndrome. 4th Ed. London: Blackwell Science; 2001. p. Ghorbani R, Owji SM. Zinc supplementation effect linear
287-356. growth in transfusion dependent ß thalassemia. IJBC.
2. Galanello R, Origa R. Beta-thalasssemia. Orphanet J of 2008;1:29- 32.
Rare Disease. 2010;5:11-5. 19. Prabhu R, Prabhu V, Prabhu RS. Iron Overload in beta
3. Olivieri NF, Brittenham GM. Iron-chelating therapy and thalassemia –a revew. J Biosci Tech. 2009;1;20-31.
the treatment of thalassemia. Blood J. 1997;89:739-61. 20. Barton JC, Edwards CQ, Phatak PD, Britton RS, Bacon
4. Najafipour F, Aliashgarjadeh A, Niafar M, Mobaseri M, BR. Handbook of iron overload. New York: Cambridge
Agamohamadzadeh N, Sorkhabi RS. Evaluation of glucose university Press; 2010. p. 233-41.
metabolism, thyroid function, growth and development 21. Mehvar A, Azarkeivan A, Faranoush M, Mehvar N,
pattern and calcium status in patients with thalassemia Saberinedjhad J, Ghorbani R. Endocrinophaties with
major. Medwel J. 2008;3:867-73. transfution dependent betha thalassemia. Pediatr Hem
5. Hamidah A, Rahmah R, Azmi T, Aziz J, Jamal R. Short Onk. 2008;25:187-94.
stature and truncal shortening in transfusion dependent 22. Shamshirzas AA, Bekheirnia MR, Kamgar M,
thalassemia patients: result from a thalassemia center in Pourzahedgilani N, Bouzari N, Habibzadeh M, et al.
Malaysia. Shouteast Asian J. 2001;32:625-30. Metabolic and endocrinologic complications in beta-
6. Moayeri H, Oloomi Z. Prevalence of growth and puberty thalassemia major: a multicenter study in Taheran. BMC
failure with respect to growth hormone and gonadotropin Endocrine Disorders. 2003;3:1-6.
secretion in beta-thalassemia major. Arc Iranian. 2006; 23. Khan FUR, Khan MH, Ayub T, Shah SH. Frekuency of
9:329-34. complications in beta thalassemia major in D.I. Khan.
7. Bhala AK, Marwaha RK, Kaur H. Longitudinal growth Biomedica. 2007;23:31-3.
attainments of transfusion dependent ß-thalassemia 24. Soliman AT, Khalafallah H, Ashour R. Growth and factors
children. Mankin quarterly. 2008;48:484-93. affecting it in thalassemia major. Hemoglobin. 2009;33:116-
8. Saxena A. Growth retardation in thalassemia major 26.
patients. Int J Hum Genet. 2003;4:237-46. 25. Low LCK. Growth of children with ß-thalassemia major.
9. Kyriakou A, Skordis N. Thalassemia and aberration of Indian J Ped. 2005;72:159-63.
growth and puberty. Medit J Hemat Infec Dis. 2009;4:1-8. 26. Paulev PE, Calleja GZ. Other hormones and disorders.
10. Grimberg A, Leon DD. Disorders of growth. In: Mosang In: Paulev PE, Calleja GZ, editors. New human fisiology.
T, editor. Pediatric endocrinology. Philadelphia: Elsevier 2nd Ed. Copenhagen: Elsevier; 2010. p. 251-3.
Mosby; 2005. p. 127-67. 27. Karamifar H, Amirhakimi GH. Linier growth deficiency in
11. Batubara J, Susanto R, Cahyono HA. Pertumbuhan dan ß-thalassemia patiens: is it growth hormone dependent?
gangguan pertumbuhan. In: Batubara J, Trijaya B, Pulungan IJMS. 2002;27:47-50.
AB, editors. Buku ajar endokrinologi anak. Jakarta: Ikatan 28. Fica S, Albu A, Vladareanu F, Barbu C, Bunghez R, Nitu
Dokter Anak Indonesia; 2010. p. 19-41. L, et al. Endocrine disorders in ß- thalassemia major:
12. Patel L, Clayton PE. Normal and disordered growth. In: cross sectional data. Act Endocr. 2005;1:201-12.
Brook CGD, Clyton PE, Brown RS, Savage MO, editors. 29. Roth C, Perkum A, Bartz M, Jarry H, Eber S, Lakomek
Clinical pediatric endocrinology. 5th Ed. Massachusette: M. Short stature and failure of pubertal development in
Blackwell; 2005. p. 90-111. thalassemia major: evidence for hypothalamic neurose-
13. Dubey AP, Parakh A, Dublish S. Current trends of the cretory disfuncion of growth hormone secretion and
management of beta thalassemia. Ind J Pediatr. defective pituitary gonadotropin secretion. Eur J pediatr.
2008;7:739- 43. 1997;156:777-83.
14. Cappellini MD, Congenite CA, Cohlen A, Piga A, Porter J. 30. Vogiatzi MA, Macklin EA, Tractenberg FL, Fung EB, Cheung
The Journal of Medical School, University of Sumatera Utara | 49
Nur Robbiyah, dkk Gangguan pertumbuhan sebagai komplikasi talasemia • mayor
AM, Vichinscy E. Differences in the prevalence of 36. Wang CH, Wu KH, Tsai FJ, Peng CT, Tsai CH.
growth, endocrine and vitamin D abnormalities among Comparison of oral and subcutaneous iron chelation
the various thalassemia syndromes in North America. therapies in the prevention of major endocrinopathies in ß
British J of haematology. 2009;146:546-56. thalassemia major patients. Hemoglobin. 2006;2:257-62.
31. Reiter EO, D’Ercole AJ. Disorders of anterior pituitary 37. Elghany WA. Guidelines for monitoring and management of
gland, hypothalamus and growth. In: Rudolf AM, Hotcler endocrine function in children and adolescents with B
MK, Lister G, Siegel NJ, editors. Rudolf’s pediatric. 23rd thalassemia major. University Hospital of Leicester. 2010;1-4.
Ed. California: McGraw-Hill; 2003. p. 2002. 38. Hindmarsh PC, Swift PGF. An assessment of growth
32. Rindang C, Batubara JL, Amalia P, Satari H. Some aspects hormone provocation tests. Arch dis. 1995;72:362-68.
of thyroid dysfunction in thalassemia major patients with 39. Lee PA, Germak J, Gut R, Khutoryansky N, Ross J.
severe iron overload. Paediatr indones. 2011;51:67-72. Identification of factors associated with good response to
33. Eshragi P, Tamaddoni A, Zarifi K, Mohammadhasani A, growth hormone therapy in children with short stature:
Aminzadeh M. Thyroid function in major thalassemia result from the ANSWER program. Int J pediatric
patients: is it related to height and chelation therapy? endocrinol. 2011;6:1-7.
Casp J Inern Med. 2011;2:189-93. 40. Darendaliler F. Safety of growth hormone treatment. J
34. Angelucci E, Barosi G, Camaschella C, Cappelini DM, Clin Res Ped endo. 2009;1:36-43.
Cazzola, Galanello R. Italian society of hematology practice 41. Kirk J, Butler G. Treatment of children with recombinant
guidelines for the management of iron overload in thalas- human growth hormone (r-hGH) shared care guidelines.
semia major and related disorders. Haematologica. 2008; London: British society for paediatric endocrinology and
93.741-52. diabetes (BSPED); 2006. p. 1-6.**
35. Sayani F, Warner M, Wu J, Rieger DW, Humphreys K,
Odame I. Guidelines for the clinical care of patient with
thalassemia in Canada. Toronto: Thalassemia
foundation of Canada; 2009. p. 15-38.
50 | Majalah Kedokteran Nusantara • Volume 47 • No. 1 • April 2014
Anda mungkin juga menyukai
- Albert Bandura dan faktor efikasi diri: Sebuah perjalanan ke dalam psikologi potensi manusia melalui pemahaman dan pengembangan efikasi diri dan harga diriDari EverandAlbert Bandura dan faktor efikasi diri: Sebuah perjalanan ke dalam psikologi potensi manusia melalui pemahaman dan pengembangan efikasi diri dan harga diriBelum ada peringkat
- Journal ReadingDokumen15 halamanJournal ReadingRestu Marlia RizkyBelum ada peringkat
- AdhdDokumen12 halamanAdhdNiken Ayu PrastikaBelum ada peringkat
- CKD CaseDokumen38 halamanCKD CaseResista FreshimonaBelum ada peringkat
- Jurnal EndokarditisDokumen5 halamanJurnal EndokarditisirulBelum ada peringkat
- Displasia Bronkopulmoner FixDokumen27 halamanDisplasia Bronkopulmoner FixikBelum ada peringkat
- Tutorial DeliriumDokumen20 halamanTutorial DeliriumDurian ArmsBelum ada peringkat
- Tatalaksana Stroke sk1 NeuroDokumen5 halamanTatalaksana Stroke sk1 NeuroAbiyya Farah Putri, MDBelum ada peringkat
- Disusun Dalam Rangka Memenuhi Tugas Stase Keperawatan Medikal Bedah IIDokumen30 halamanDisusun Dalam Rangka Memenuhi Tugas Stase Keperawatan Medikal Bedah IIDikbel JujusBelum ada peringkat
- Autism Spectrum Disorder: ReferatDokumen22 halamanAutism Spectrum Disorder: ReferatHansenPanjaitanBelum ada peringkat
- PERSIAPAN BMP EDIT-dikonversiDokumen2 halamanPERSIAPAN BMP EDIT-dikonversifransiska agosaniBelum ada peringkat
- CRS Toxoplasmosis Pada HIVDokumen31 halamanCRS Toxoplasmosis Pada HIVAzuan SalimBelum ada peringkat
- Patofisiologi RiketsiaDokumen2 halamanPatofisiologi RiketsiakadeverlyanitaBelum ada peringkat
- KMK No. HK .01 .07-MENKES-1-2018 TTG Pedoman Nasional Pelayanan Kedokteran Tata Laksana ThalasemiaDokumen22 halamanKMK No. HK .01 .07-MENKES-1-2018 TTG Pedoman Nasional Pelayanan Kedokteran Tata Laksana ThalasemiaDewi PrasetiaBelum ada peringkat
- Endokarditis InfektifDokumen27 halamanEndokarditis InfektiffarisBelum ada peringkat
- Intoksikasi Minyak TanahDokumen7 halamanIntoksikasi Minyak TanahanggyalbernandeBelum ada peringkat
- Kegawatdaruratan ARDSDokumen35 halamanKegawatdaruratan ARDSKevin Jaya SBelum ada peringkat
- Referat Emboli ParuDokumen11 halamanReferat Emboli ParuIlham Yuri LubisBelum ada peringkat
- ASKEP ARDS BELUM FIXxxDokumen33 halamanASKEP ARDS BELUM FIXxxMayang AfriolaBelum ada peringkat
- Referat ADHFDokumen30 halamanReferat ADHFjoeunisaBelum ada peringkat
- Serangan SianotikDokumen2 halamanSerangan SianotikSyahfiq IsmailBelum ada peringkat
- Kelenjar Adrenal.Dokumen15 halamanKelenjar Adrenal.Seliya Pliantara100% (1)
- Kasus Speech DelayDokumen9 halamanKasus Speech DelayAjies Abdul ajiesBelum ada peringkat
- Referat Perubahan Mikrobiota Pada NAFLD NAFLDokumen11 halamanReferat Perubahan Mikrobiota Pada NAFLD NAFLKiki Kiekya Agustin HidayatiBelum ada peringkat
- Mind Mapping SleDokumen3 halamanMind Mapping SleMemelBelum ada peringkat
- Pre Planning MMD 2Dokumen19 halamanPre Planning MMD 2AninBelum ada peringkat
- PGD10 Gangguan Cairan QDokumen15 halamanPGD10 Gangguan Cairan QJulia MärðhìyåBelum ada peringkat
- Interpretasi Indeks Trombosit Pada Darah LengkapDokumen5 halamanInterpretasi Indeks Trombosit Pada Darah Lengkaprandy sefriansyahBelum ada peringkat
- Laporan Pendahuluan ThalasemiaDokumen22 halamanLaporan Pendahuluan ThalasemiaAdy pratama18Belum ada peringkat
- Refrat Infeksi Intrakranial GraceDokumen53 halamanRefrat Infeksi Intrakranial GraceprisciliaBelum ada peringkat
- Makalah Diabetes Mellitus 1Dokumen9 halamanMakalah Diabetes Mellitus 1Elise Adelina Sianipar100% (1)
- Tugas WasirDokumen20 halamanTugas Wasirmariatantiri nainggolanBelum ada peringkat
- PF Paru PatologisDokumen11 halamanPF Paru PatologiskemalBelum ada peringkat
- EpispadiaDokumen4 halamanEpispadiaSarah AndrianiBelum ada peringkat
- HiperparatiroidismeDokumen26 halamanHiperparatiroidismeAnisah MuallifahBelum ada peringkat
- Airway Remodeling Pada AsmaDokumen5 halamanAirway Remodeling Pada AsmaLinda SugiartoBelum ada peringkat
- Skenario 2 Kejang MeningitisDokumen29 halamanSkenario 2 Kejang MeningitisDeliwanBelum ada peringkat
- Penatalaksanaan StrokeDokumen5 halamanPenatalaksanaan StroketrisnaBelum ada peringkat
- Referat Gizi BurukDokumen37 halamanReferat Gizi BurukRizki Putri AndiniBelum ada peringkat
- LP Speech Delay SupiDokumen21 halamanLP Speech Delay SupiAgustinBelum ada peringkat
- Slide LapsusDokumen33 halamanSlide LapsusMuhammad Iqbal Al-islamyBelum ada peringkat
- Stroke IskemikDokumen68 halamanStroke IskemikFathnur Sani100% (1)
- Terapi CairanDokumen66 halamanTerapi CairanSBelum ada peringkat
- Tranfusi TukarDokumen6 halamanTranfusi TukarDhnrawBelum ada peringkat
- DeformitasDokumen4 halamanDeformitasPuti Kulindam Suto100% (1)
- Perdarahan Akibat Defisiansi Vit KDokumen3 halamanPerdarahan Akibat Defisiansi Vit KBerlian CitaBelum ada peringkat
- Rangkuman Materi Metodologi PenelitianDokumen6 halamanRangkuman Materi Metodologi Penelitianbrigitap martoyoBelum ada peringkat
- 3 - SIADH - Fix BGT 1Dokumen30 halaman3 - SIADH - Fix BGT 1IMaa Wati AlbiizzahBelum ada peringkat
- Makalah EndokarditisDokumen10 halamanMakalah EndokarditisMade MelaniawatiBelum ada peringkat
- Tiroiditis HashimotoDokumen3 halamanTiroiditis HashimotoCandrika IzzatikaBelum ada peringkat
- Laporan Pendahuluan MeningitisDokumen17 halamanLaporan Pendahuluan MeningitisPutri UtomoBelum ada peringkat
- Skema AnemiaDokumen1 halamanSkema AnemiaaditBelum ada peringkat
- Konsep Asuhan Keperawatan Anak Dengan Hiperaktif (ADHD)Dokumen24 halamanKonsep Asuhan Keperawatan Anak Dengan Hiperaktif (ADHD)VivoraroBelum ada peringkat
- Makalah Child AbuseDokumen17 halamanMakalah Child AbuseDian SalehaBelum ada peringkat
- LP DipsneaDokumen7 halamanLP DipsneaMariam BilangBelum ada peringkat
- BAB 3 FixDokumen16 halamanBAB 3 FixIbanez Gokil BroBelum ada peringkat
- Asma Pada AnakDokumen32 halamanAsma Pada AnakVaniaBelum ada peringkat
- Psikoterapi Untuk Penyalahgunaan NapzaDokumen22 halamanPsikoterapi Untuk Penyalahgunaan NapzaYuni DwitriBelum ada peringkat
- Juvenile Idiopathic ArthritisDokumen48 halamanJuvenile Idiopathic ArthritiszakiaBelum ada peringkat
- Asuhan Keperawatan Pasien Dengan ThalasemiaDokumen21 halamanAsuhan Keperawatan Pasien Dengan ThalasemiajustitiaintanBelum ada peringkat
- Laporan Injeksi Lidokain HCLDokumen43 halamanLaporan Injeksi Lidokain HCLNurinda Tamala100% (2)
- Biodiversitas Vegetasi Dan Fungsi EkosistemDokumen5 halamanBiodiversitas Vegetasi Dan Fungsi EkosistemNurinda TamalaBelum ada peringkat
- Glikosida NosiDokumen75 halamanGlikosida NosiNurinda TamalaBelum ada peringkat
- Pemeriksaan UrineDokumen13 halamanPemeriksaan UrineNurinda TamalaBelum ada peringkat