UU&Etika Kfarmasian
Diunggah oleh
rinda kasihHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
UU&Etika Kfarmasian
Diunggah oleh
rinda kasihHak Cipta:
Format Tersedia
Pada Bab II pasal 4 membahas tentang Kriteria obat yang memiliki izin edar yaitu,pertama, adanya
khasiat yang meyakinkan dan keamanan yang memadai melalui percobaan hewan dan uji klinis serta
bukti lain sesuai dengan status perkembangan ilmu pengetahuan yang bersakutan; kedua, adanya
mutu yang memenuhi syarat yang dinilai melalui proses produksi sesuai Cara Pembuatan Obat Yang
Baik (CPOB), serta spesifikasi dan metoda pengujian bahan yang digunakan dan produk jadi dengan
bukti sahih. Ketiga, penadaan informasi lengkap dan obyektif yang menjamin penggunaan obat yang
tepat, rasional dan aman. Keempat, sesuai kebutuhan nyata masyarakt. Kelima, dibanding obat
standar dan obat yang memiliki izin edar untuk indikasi yang diklaim, kriteria psikotropika harus
memilki keunggulan kemanfaatan dan keamanan. Keenam, harus dilakukan uji klinik di Indonesia
khusus kontrasepsi utnuk program nsional dan obat program lainnya yang nantinya akan ditentukan
kemudian.
Pasal 5 membahas tentang Obat untuk uji klinik harus dibuktikan jika obat aman untuk penggunaan
pada manusia. Dan ketentun lebih lanjut tentang pelaksanaan uji klinik ditetapkan oleh Kepala
Badan.
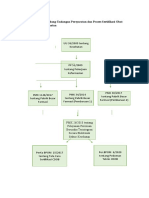
Pada Bab IV membahas tentang Tata Cara Memperoleh Izin Edar. Bagian pertama membahas
mengenai Registrasi yaitu, registrasi diajukan kepada Kepala Badan, juga kriteria dan tata laksana
registrasi ditetapkan Kepala Badan. Dokumen registrasi juga merupakan dokumen rahasia, yang
hanya digunakan untuk keperluan evaluasi oleh yang berwenang.
Bagian kedua membahas tentang Biaya yaitu, registrasi dikenakan biaya dan ditetapkan sesuai
peraturan perundang-undangan.
Bagian ketiga membahas tentang evaluasi dokumen registrasi yang memenuhi ketentuan kriteria
seperti pada pasal 14. Dan untuk melakukan evaluasi dibentuk :
a. Komite Nasional Penilai Obat
b. Panitia Penilai Khasiat-Keamanan
c. Panitia Penilai Mutu, Teknologi, Penandaan dan Kerasionalan Obat
serta pembentukan, tugas dan fungsi Komite Nasional Penilai Obat dan Panitia ditetapkan juga oleh
Kepala Badan.
Bagian keempat membahas tentang Pemberian Izin Edar yaitu, pertama, Kepala badan memberi
persetujuan dan penolokan izin edar berdasar rekomendasi yang diberikan oleh para evaluator.
Kedua, kepala badan melapor izin edar kepada Menteri satu tahun sekali. Dan permohonan
registrasi obat ditolak, biaya tidak dapat ditarik Kembali.
Bagian kelima membahas tentang Peninjauan Kembali, jika registrasi ditolak, pendaftar dapat
mengajukan keberatan melalui tata cara peninjauan kembali yang ditetapkan oleh Kepala Badan.
Bagian keenam, izin edar berlaku 5 tahun dan dapat diperpanjang selama memenuhi ketentuan yang
berlaku.
Bab VI membahas tentang evaluasi kembali.
Anda mungkin juga menyukai
- Panduan Kredensial Tenaga Kesehatan LainDokumen28 halamanPanduan Kredensial Tenaga Kesehatan Lainyoana puspitorini67% (3)
- Penilaian Dan Poin Penting Penilaian Akreditasi Bagian Rekam MedisDokumen30 halamanPenilaian Dan Poin Penting Penilaian Akreditasi Bagian Rekam Medisrekam medis selarasBelum ada peringkat
- Alur Registrasi ObatDokumen7 halamanAlur Registrasi ObatPutri Dewi RiayahBelum ada peringkat
- Panduan Kred Nakes LainDokumen18 halamanPanduan Kred Nakes LainWanda RyBelum ada peringkat
- Registrasi ObatDokumen20 halamanRegistrasi ObatDias Rijaluddin HalimBelum ada peringkat
- Resume Registrasi ProdukDokumen24 halamanResume Registrasi Produkirinkhairina0% (1)
- Portofolio 1Dokumen41 halamanPortofolio 1Ratih Nur RamadhanBelum ada peringkat
- Panduan Kredensial 2022Dokumen10 halamanPanduan Kredensial 2022sintia hartikaBelum ada peringkat
- SPO KredensialDokumen4 halamanSPO Kredensiallucilla_serricata100% (2)
- Registrasi ObatDokumen8 halamanRegistrasi Obatasep_imam_setiadinBelum ada peringkat
- Panduan Penetapan Kewenangan KlinisDokumen7 halamanPanduan Penetapan Kewenangan KlinisGudang farmasi Rs TandunBelum ada peringkat
- Panduan Kredensial Dan RekredensialDokumen6 halamanPanduan Kredensial Dan RekredensialDeviBelum ada peringkat
- Regitrasi ObatDokumen2 halamanRegitrasi Obatrinda kasihBelum ada peringkat
- Aryanto (2008020133)Dokumen6 halamanAryanto (2008020133)AryantoBelum ada peringkat
- Revisi Sertifikasi BPOMDokumen15 halamanRevisi Sertifikasi BPOMDenny Guna PanjaluBelum ada peringkat
- Laporan Lo Tutor e Blok IndustriDokumen8 halamanLaporan Lo Tutor e Blok Industrialfira andiniBelum ada peringkat
- Tugas FarmakonogsiDokumen7 halamanTugas FarmakonogsiNanda SafitriBelum ada peringkat
- Tugas Kelompok - 3-1-1Dokumen12 halamanTugas Kelompok - 3-1-1Nur Fadilla JafarBelum ada peringkat
- Makalah Kel 4 RegsedfarDokumen11 halamanMakalah Kel 4 RegsedfarAlif tiyyah.rBelum ada peringkat
- Resume Blok Industri FarmasiDokumen3 halamanResume Blok Industri FarmasiindyBelum ada peringkat
- Materi Prediksi PreetestDokumen16 halamanMateri Prediksi PreetestDede JefriBelum ada peringkat
- Tugas Kelompok B2Dokumen21 halamanTugas Kelompok B2healtBelum ada peringkat
- Alur Penerimaan Bahan BakuDokumen12 halamanAlur Penerimaan Bahan BakuCindy AnggraeniBelum ada peringkat
- Penugasan Materi Perijinan Dan Sertifikasi Institusi-Kelompok 2Dokumen5 halamanPenugasan Materi Perijinan Dan Sertifikasi Institusi-Kelompok 2RohangkiBelum ada peringkat
- Panduan Kredensial Dan Kewenangan Klinis (Clinical Privilege) Tenaga MedisDokumen24 halamanPanduan Kredensial Dan Kewenangan Klinis (Clinical Privilege) Tenaga MedisDeden AndroidxBelum ada peringkat
- Tugas Proses Registrasi Obat BaruDokumen15 halamanTugas Proses Registrasi Obat BaruPrilint LaiaBelum ada peringkat
- Registrasi ObatDokumen15 halamanRegistrasi ObatNADZIFAH RIZQIANI PUTRI 2015Belum ada peringkat
- Tugas Manreg - 10060321017 - Tarisa Perolin - ADokumen10 halamanTugas Manreg - 10060321017 - Tarisa Perolin - Atarisa perolinBelum ada peringkat
- Uts Hukum Obat Dan Makanan Michelle Angelika S 2010622046Dokumen6 halamanUts Hukum Obat Dan Makanan Michelle Angelika S 2010622046Michelle AngelikaBelum ada peringkat
- Peraturan Menteri Kesehatan R.I. Tentang Wajib Daftar Obat Jadi MenimbangDokumen4 halamanPeraturan Menteri Kesehatan R.I. Tentang Wajib Daftar Obat Jadi MenimbangWELI SASMITABelum ada peringkat
- Hirarki PerundangDokumen8 halamanHirarki Perundangtiara raniBelum ada peringkat
- Panduan Kredensial Dan RekredensialDokumen3 halamanPanduan Kredensial Dan Rekredensialrachel mariamBelum ada peringkat
- Tugas Mata Kuliah Patient Safety Materi Tentang Keamanan Produksi ObatDokumen10 halamanTugas Mata Kuliah Patient Safety Materi Tentang Keamanan Produksi ObatSiska Purnama AsihBelum ada peringkat
- Regarding Clinical Trial Procedure, 28-Feb-2001Dokumen46 halamanRegarding Clinical Trial Procedure, 28-Feb-2001Dedi PurnomoBelum ada peringkat
- Cara Distribusi Obat Yang Baik.Dokumen8 halamanCara Distribusi Obat Yang Baik.AmmaBelum ada peringkat
- FilesDokumen22 halamanFilesSrimaharani SrimaharaniBelum ada peringkat
- Etika ProfesiDokumen13 halamanEtika ProfesiFelysa AmeliaBelum ada peringkat
- Registrasi Sediaan Farmasi Dan Alat Kesehatan IVANI ROSALINA 201751169Dokumen5 halamanRegistrasi Sediaan Farmasi Dan Alat Kesehatan IVANI ROSALINA 201751169Tamara RosaBelum ada peringkat
- Tata Laksana Registrasi ObatDokumen18 halamanTata Laksana Registrasi ObatAnzari Muhammad0% (1)
- KEP KBPOM - NO.02002 - SK - KBPOM TAHUN 2001 - Tentang TATA LAKSANA UJI - 2001 PDFDokumen19 halamanKEP KBPOM - NO.02002 - SK - KBPOM TAHUN 2001 - Tentang TATA LAKSANA UJI - 2001 PDFAgustinus M SilabanBelum ada peringkat
- Kesepakatan Lpa Dan FasyankesDokumen5 halamanKesepakatan Lpa Dan Fasyankesannisa rachmawatiBelum ada peringkat
- 1 PKS LARSI Dengan RS SURVEI MASTER77Dokumen4 halaman1 PKS LARSI Dengan RS SURVEI MASTER77Rafael HamzahBelum ada peringkat
- Resume Peraturan Terkait Obat TradisionalDokumen20 halamanResume Peraturan Terkait Obat TradisionalUsamugiBelum ada peringkat
- Apoteker, Farmasi Kredensial.Dokumen19 halamanApoteker, Farmasi Kredensial.Azwar MudaBelum ada peringkat
- Spo Kredensialtambahan MedisDokumen3 halamanSpo Kredensialtambahan MedishermawanBelum ada peringkat
- Desain Dan Pengembangan Obat BaruDokumen6 halamanDesain Dan Pengembangan Obat BaruADE SEPTA ANGRENI A. MD. FARMBelum ada peringkat
- LPH Lembaga Pemeriksa Halal Pasal 14Dokumen3 halamanLPH Lembaga Pemeriksa Halal Pasal 14ShafiraFauziBelum ada peringkat
- Dody Firmanda 2010 - Komite Medik Rumah Sakit Awal Bros PekanbaruDokumen57 halamanDody Firmanda 2010 - Komite Medik Rumah Sakit Awal Bros PekanbaruDody Firmanda100% (1)
- Permenkes No 917 TH 1993 PDFDokumen4 halamanPermenkes No 917 TH 1993 PDFnur ifdah setia rahayuBelum ada peringkat
- All RegistrasiDokumen12 halamanAll Registrasifadli_nugraha6109Belum ada peringkat
- Project UU AFNIUTSDokumen4 halamanProject UU AFNIUTSwulan purnamaBelum ada peringkat
- MOU-PKS SHK Final Tambahan Uang Muka Kerja 2015Dokumen10 halamanMOU-PKS SHK Final Tambahan Uang Muka Kerja 2015annisafnBelum ada peringkat
- Bab Ii Citra MedikaDokumen13 halamanBab Ii Citra MedikaHARTINI NUHABelum ada peringkat
- Manajemen Laboratorium Akreditasi LabDokumen20 halamanManajemen Laboratorium Akreditasi LabDinaragritaBelum ada peringkat
- Alfira Andini Deviyanti Unknown - SUMMARY SAINS 39Dokumen3 halamanAlfira Andini Deviyanti Unknown - SUMMARY SAINS 39alfira andiniBelum ada peringkat
- Panduan Kredensial MedisDokumen26 halamanPanduan Kredensial MedisAndi KarismaBelum ada peringkat
- 65 - KPS SPO Kredensial Staf MedisDokumen3 halaman65 - KPS SPO Kredensial Staf MedisArif MustawanBelum ada peringkat
- UAS Uji Klinik Obat Alam NUR ASNI H. ASAPADokumen3 halamanUAS Uji Klinik Obat Alam NUR ASNI H. ASAPANur asniBelum ada peringkat
- Panduan Kredensial PPA EditDokumen14 halamanPanduan Kredensial PPA Editishafa rudinsyahBelum ada peringkat
- Kondensasi Dan Pencairan Gas.Dokumen2 halamanKondensasi Dan Pencairan Gas.rinda kasihBelum ada peringkat
- Kesimpulan Sifat KoligatifDokumen2 halamanKesimpulan Sifat Koligatifrinda kasihBelum ada peringkat
- Ketetapan Dalam Memahami Persamaan Gas Ideal, Keadaan Gas Nyata Dan Keadaan Lain Pada Gas NyataDokumen6 halamanKetetapan Dalam Memahami Persamaan Gas Ideal, Keadaan Gas Nyata Dan Keadaan Lain Pada Gas Nyatarinda kasihBelum ada peringkat
- Dampak Negatif Penggunaan Energi Terhadap LingkunganDokumen2 halamanDampak Negatif Penggunaan Energi Terhadap Lingkunganrinda kasihBelum ada peringkat
- Kasus PelecehanDokumen2 halamanKasus Pelecehanrinda kasihBelum ada peringkat
- Bab Xiii Kartu Gesek Bebas BungaDokumen2 halamanBab Xiii Kartu Gesek Bebas Bungarinda kasihBelum ada peringkat
- Tersangka Kasus Brigadir JDokumen3 halamanTersangka Kasus Brigadir Jrinda kasihBelum ada peringkat
- Titrasi Asam BasaDokumen17 halamanTitrasi Asam Basarinda kasihBelum ada peringkat
- Review Artikel - Arsianita Ester WawoDokumen3 halamanReview Artikel - Arsianita Ester Waworinda kasihBelum ada peringkat
- Sara FilsafatDokumen5 halamanSara Filsafatrinda kasihBelum ada peringkat
- Ancenstror AvesDokumen5 halamanAncenstror Avesrinda kasihBelum ada peringkat
- BIODAS MATERI Morffologi TumbuhanDokumen15 halamanBIODAS MATERI Morffologi Tumbuhanrinda kasihBelum ada peringkat
- Indonesia Bersiap Untuk Menuju EndemiDokumen2 halamanIndonesia Bersiap Untuk Menuju Endemirinda kasihBelum ada peringkat
- Struktur Atom Dan Konfigurasi ElektronDokumen32 halamanStruktur Atom Dan Konfigurasi Elektronrinda kasihBelum ada peringkat