Laporan Praktikum Menentukan Trayek PH Larutan Asam Basa Dengan Indikator Alam
Diunggah oleh
tel_net100%(1)100% menganggap dokumen ini bermanfaat (1 suara)
10K tayangan7 halamanJudul Asli
Laporan Praktikum Menentukan Trayek Ph Larutan Asam Basa Dengan Indikator Alam
Hak Cipta
© © All Rights Reserved
Format Tersedia
DOCX, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
100%(1)100% menganggap dokumen ini bermanfaat (1 suara)
10K tayangan7 halamanLaporan Praktikum Menentukan Trayek PH Larutan Asam Basa Dengan Indikator Alam
Diunggah oleh
tel_netHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 7
LAPORAN PRAKTIKUM MENENTUKAN TRAYEK pH LARUTAN ASAM
BASA DENGAN INDIKATOR ALAM
A. Tujuan :
Untuk memahami bagaimana suatu bahan alami dapat digunakan sebagai indikator asam-
basa pada suatu senyawa dan dapat menentukan kisaran trayek pH maupun pOH dari senyawa
tersebut.
B. Landasan Teori :
Suatu sifat senyawa yang sangat penting adanya adalah sifat asam dan basa. Kita mengenal
berbagai macam asam seperti asam cuka, dan asam jawa. Kita juga mengenal berbagai jenis basa
seperti sabun yang biasa kita gunakan dalam kehidupan sehari-hari.
Teori asam basa juga mengalami beberapa pengembangan. Asam dinyatakan merupakan
suatu senyawa yang memiliki pH lebih kecil dari 7. < 7 merupakan pH netral dari reaksi H
+
+OH
-
H
2
O. Sedangkan basa adalah senyawa yang memiliki pH lebih besar dari 7. Batas
maksimum pH suatu senyawa adalah 14. Dari hal tersebut kita dapat menuliskan bahwa pH +
pOH = 14. Menurut Arrhenius, asam merupakan zat yang menghasilkan ion hidrogen dalam
larutan. Sedangkan basa sukar larut dalam air karena basa memiliki ion hidroksida. Suatu asam
dikatakan hipotetis apabila asam tersebut tidak stabil sehingga segera terurai menjadi zat lain.
Teori Arrhenius masih memiliki kelemahan, bahwa tidak semua reaksi asam harus
berlangsung dalam larutan. Kemudian Bronsted-Lowry mendefinisikan asam dan basa dengan
mengatakan bahwa asam merupakan donor proton sedangkan basa merupakan akseptor proton.
Menurut Bronsted-Lowry, asam dan basa ini akan menghasilkan suatu pasangan konjugasi, yaitu
suatu pasangan ketika asam melepaskan ion H
+
nya kepada basa atau akseptor.
Untuk melengkapi teori-teori diatas, Lewis juga mengemukakan bahwa asam dan basa
merupakan perpindahan electron dari suatu senyawa ke senyawa lainnya. Asam berperilaku
sebagai akseptor pasangan elektron sedangkan basa sebagai donor pasangan elektron.
Indikator adalah suatu zat, yang warnanya berbeda-beda sesuai konsentrasi ion-Hidrogen.
Indikator umumnya merupakan suatu asam atau basa organik lemah , yang dipakai dalam larutan
yang sangat encer.
Asam atau basa indikator yang tidak tedisosiasi mempunyai warna yang berbeda dengan
hasil disosiasinya, sehingga memudahkan praktikan dalam menentukan apakah larutan tersebut
bersifat asam atau basa.
Berikut adalah beberapa jenis indikator yang sering digunakan:
Indikator
Warna
Asli
Trayek
pH
Warna
Asam Basa
Metil Jingga
Coklat
Jingga
3,1-4,1
Merah
Marun
Kuning
Kehijauan
Metil
Merah
Coklat
Merah
4,2-6,2 Merah
Kuning
Kecoklatan
Bromtimol
Biru
Merah 6,0-7,6 Jingga Biru
Kertas
Lakmus
Merah 6,2-7,2 Merah Biru
Fenolftalein Bening 8,0-10,0 Bening Merah Muda
Selain Indikator di atas larutan asam dan basa dapat ditentukan dengan menggunakan
bahan-bahan alami yang berwarna seperti, daun suji, kunyit , bunga mawar, bunga kembang
sepatu, kol merah, bit, bawang merah, dll. Misalkan bit pada kondisi netral berwana merah akan
berubah menjadi warna ungu dalam larutan asam dan kuning dalam larutan basa.
Walau demikian, warna yang diberikan tentunya memiliki jangkauan yang terbatas. Batas-
batas pH ketika indikator mengalami perubahan warna disebut trayek perubahan warna indikator
tersebut.
C. Alat dan bahan :
1. Air cuka 13. Fenolftalein
2. Minuman Bersoda (Sprite) 14. Daun Suji
3. Larutan Abu Gosok 15. Bunga Mawar
4. Larutan Sabun Mandi 16. Kunyit
5. Pipet Tetes 17. Bawang Merah
6. Tabung Reaksi 18. Bunga Kembang Sepatu
7. Metil Jingga 19. Bawang Merah
8. Metil Merah 20. Mangkuk Porselen
9. Bromtimol Biru 21. Kol Merah
10. Kertas Lakmus 22. Air
11. Tumbukan
12. Cawan
D. Langkah kerja :
Langkah kerja menggunakan indikator metil jingga (MJ), metil merah (MM), bromtimol biru
(BB), kertas lakmus, dan fenolftalein, sebagai berikut:
1. Sediakan beberapa sempel antara lain : cuka dapur, minuman bersoda, larutan abu gosok,
dan larutan sabun mandi.
2. Dari masing-masing larutan ujilah dengan menggunakan lima macam indikator metil jingga
(MJ), metil merah (MM), bromtimol biru (BTB), kertas lakmus, dan fenolftalein (PP) dengan
cara: ambil 1 mL masing-masing larutan sempel masukan ke dalam tabung reaksi dan tambahkan
masing-masing larutan dengan 3 tetes indikator-indikator tersebut!
Langkah kerja dengan menggunakan indikator alami, sebagai berikut:
1. Pertama-tama, bahan-bahan yang sudah dibawa seperti kol merah, bunga kembang sepatu,
daun suji, bunga mawar, kunyit, bawang merah, dan bit diletakkan dalam cawan, kemudian
dicampur dengan sedikit air.
2. Lalu letakkan pada cawan yang terpisah untuk masing-masing bahan.
3. Kemudian gunakan tumbukan sehingga terdapat serat-serat dari masing-masing bahan alami
tersebut.
4. Teteskan serat dari bahan-bahan tersebut pada mangkuk porselen yang tersedia. Untuk
masing-masing bahan, teteskan pada 2 slot yang ada di lumpang porselen.
5. Teteskan Air Cuka ke salah satu dari 2 slot yang tersedia dari masing-masing bahan.
Kemudian teteskan Air Sabun pada slot yang tersisa / slot lainnya.
6. Amati dan catat perubahan warna dari masing-masing serat bahan alami yang ditetesi
masing-masing Air Cuka maupun Air Sabun.
E. Data Pengamatan
Hasil Pengamatan Indikator Bahan Metil Jingga (MJ), Metil Merah (MM),
Bromtimol Biru (BTB), Lakmus, dan Fenolftalein (PP).
Larutan
Sampel
MJ MM BTB Lakmus PP pH
Cuka Merah Ungu Jingga Merah
Tak
Berwarna
< 8
Minuman
Bersoda
(Sprite)
Merah Ungu Jingga Merah
Tak
Berwarna
< 8
Larutan
Abu
Jingga Kuning Biru Biru Ungu > 10
Air Sabun Jingga Kuning Biru Biru Ungu > 10
Hasil Pengamatan Indikator Bahan dari Alam
No. Bahan
Alami
Warna Asli Warna
Air Cuka Air Sabun
1 Kol Merah Ungu Merah Muda Kuning
2 Bunga
Kembang
Sepatu
Merah
Muda
Rose Pink Hijau Muda
3 Daun Suji Hijau Tua Hijau Tua Hijau Tua
4 Bunga
Mawar
Merah Merah Marun
Coklat
Kekuningan
5 Kunyit Kuning Kuning Kecoklatan
6 Bawang
Merah
Bening Bening Hijau Muda
F. Kesimpulan :
Dari hasil percobaan diatas, kita dapat menyimpulkan beberapa kesimpulan. Suatu senyawa
dipastikan memiliki asam basa yang berbeda-beda dalam range pH= 1-14 dimana pH=7 adalah
pH netral. Oleh karena itu, maka dibuatlah suatu percobaan guna mengetahui berapa pH atau
keasaman suatu senyawa. Dengan menggunakan senyawa-senyawa seperti pada tabel diatas
yaitu Metil jingga, metil merah, bromtimol biru, kertas Lakmus maupun fenolftalein maka kita
dapat mengetahui berapa pH suatu senyawa.
Tetapi dilain pihak, kita juga dapat menggunakan bahan-bahan alami sebagai pengukur/
indikator pH. Dari percobaan diatas, kita dapat menyimpulkan bahwa tidak semua bahan alami
dapat digunakan sebagai indikator trayek pH. Hal ini dapat dilihat bahwa Daun Suji tidak
mengalami perubahan warna yang mencolok sehingga sulit bila digunakan sebagai indikator.
Untuk melihat trayek pH dari masing-masing bahan alami, kita dapat melihatnya dengan
membandingkan slot asam pada bahan alami dengan slot asam pada senyawa-senyawa indikator
metil jingga dll. Dari tabel tersebut, warna yang paling mirip dapat dikatakan sebagai range pH
bahan alami tersebut.
Dari percobaan diatas, kita dapat menyimpulkan bahwa kol merah merupakan salah satu
indikator bahan alami yang paling baik karena ketika diberikan asam, warnanya akan menjadi
merah seperti Asam pada metil jingga(MJ), dan ketika basa warnanya menjadi kuning kehijauan.
Bunga kembang sepatu dan bunga mawar juga cukup baik bila digunakan sebagai indikator
karena masih adanya perubahan warna yang terlihat.
Maka kita dapat menyatakan bahwa semua senyawa memiliki pH yang berbeda-beda,
namun dalam pengukurannya, yang dapat digunakan sebagai indikator trayek pH dapat
digolongkan menjadi indikator bahan alami yang baik seperti kol merah karena adanya
perubahan warna yang mencolok untuk pH yang berbeda-beda, maupun indikator sebagian
seperti kunyit karena perubahan warna yang hanya sensitif pada senyawa basa, atau yang tidak
dapat digunakan sebagai indikator sama sekali, yaitu daun suji.
Dengan adanya indikator bahan alami ini, kita dapat memperkirakan berapa besarnya pH
suatu senyawa, akankah suatu senyawa memiliki sifat asam atau basa dengan penggunaan
indikator bahan alami ini secara efektif.
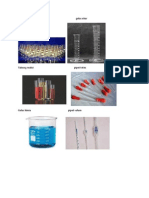
LAMPIRAN
Minuman Bersoda (Sprite)
Larutan Abu
Air Cuka
Air Sabun
aKet : Larutan setelah ditambahkan:
No. 1 = Bromtimol Biru
No. 2 = Kertas Lakmus
No. 3 = Metil Jingga
No. 4 = Metil Merah
No. 5 = Fenolftalein
Anda mungkin juga menyukai
- Laporan Praktikum Kenaikan Titik Didih KimiaDokumen5 halamanLaporan Praktikum Kenaikan Titik Didih KimiaGiri Harta YogeswaraBelum ada peringkat
- LAPORAN PRAKTIKUM KIMIA Trayek PHDokumen9 halamanLAPORAN PRAKTIKUM KIMIA Trayek PHIkyawan 1999100% (1)
- Reaksi Bolak BalikDokumen6 halamanReaksi Bolak BalikbagusBelum ada peringkat
- Percobaan IVDokumen12 halamanPercobaan IVAfrizan NurpermadiBelum ada peringkat
- Praktikum Konsep MolDokumen15 halamanPraktikum Konsep MolMeiliani meliBelum ada peringkat
- Soal Titrasi Asam BasaDokumen30 halamanSoal Titrasi Asam Basarehamita0% (1)
- Praktikum KimiaDokumen4 halamanPraktikum KimiaWinda FransiskaBelum ada peringkat
- Laporan Praktikum KimiaDokumen10 halamanLaporan Praktikum KimiaginaBelum ada peringkat
- Laporan Kimia (Larutan Penyangga)Dokumen10 halamanLaporan Kimia (Larutan Penyangga)Novi HardiyantiBelum ada peringkat
- Laporan Praktikum Laju Reaksi Part 3Dokumen20 halamanLaporan Praktikum Laju Reaksi Part 3ImaBelum ada peringkat
- Laporan KImia Trayek PHDokumen7 halamanLaporan KImia Trayek PHAzmie RBelum ada peringkat
- LaporanDokumen21 halamanLaporanArifatul Aini100% (1)
- Pengaruh Luas Permukaan Terhadaplaju ReaksiDokumen3 halamanPengaruh Luas Permukaan Terhadaplaju ReaksiMang'Funday Nack SubegedeBelum ada peringkat
- Keseimbangan Kimia Dalam TubuhDokumen6 halamanKeseimbangan Kimia Dalam TubuhastariBelum ada peringkat
- INDIKATOR ASAM BASA DARI EKSTRAK DAUN PANDAN (Hasil+analisa)Dokumen4 halamanINDIKATOR ASAM BASA DARI EKSTRAK DAUN PANDAN (Hasil+analisa)intanichy100% (1)
- Aidil Nur Rezki Xid Laporan Praktikum Hidrolisis GaramDokumen9 halamanAidil Nur Rezki Xid Laporan Praktikum Hidrolisis Garamabdul azizBelum ada peringkat
- Laporan Praktikum KimiaDokumen6 halamanLaporan Praktikum KimiaaufaBelum ada peringkat
- Laprak Kimia Indikator Asam BasaDokumen10 halamanLaprak Kimia Indikator Asam BasaDidi RiyadiBelum ada peringkat
- Laporan Kimia 1Dokumen8 halamanLaporan Kimia 1Nur Rohman0% (1)
- Mengamati Reaksi Bolak-BalikDokumen3 halamanMengamati Reaksi Bolak-BalikKharis MaulanaBelum ada peringkat
- Laporan Praktikum Kimia DasarDokumen21 halamanLaporan Praktikum Kimia DasarCAsalsabila F MBelum ada peringkat
- Pengaruh Suhu Dan Katalis Terhadap Laju ReaksiDokumen2 halamanPengaruh Suhu Dan Katalis Terhadap Laju ReaksiFayzaHafizahBelum ada peringkat
- Laporan Hasil Praktikum REAKSI-REAKSI KIMIADokumen20 halamanLaporan Hasil Praktikum REAKSI-REAKSI KIMIAReni Anggraeni IIBelum ada peringkat
- Laporan Praktikum Larutan Asam Dan BasaDokumen4 halamanLaporan Praktikum Larutan Asam Dan BasaCika Syafitri100% (2)
- Laporan Praktikum Kesetimbangan KimiaDokumen7 halamanLaporan Praktikum Kesetimbangan KimiaJung Hyun SunBelum ada peringkat
- PercobaanDokumen4 halamanPercobaansonialidya50% (2)
- Kelarutan Dan Hasil Kali KelarutanDokumen23 halamanKelarutan Dan Hasil Kali KelarutanDwiayuAdinda100% (2)
- Karya Ilmiah Larutan Asam Dan BasaDokumen11 halamanKarya Ilmiah Larutan Asam Dan BasaMawaddah Utm100% (1)
- Laporan Lengkap 4Dokumen15 halamanLaporan Lengkap 4Ribca Martha LaoliBelum ada peringkat
- Laporan Praktikum Pengaruh Konsentrasi Terhadap Pergeseran Kesetimbangan KimiaDokumen4 halamanLaporan Praktikum Pengaruh Konsentrasi Terhadap Pergeseran Kesetimbangan KimiaI Putu Adi Payana PutraBelum ada peringkat
- Laporan Praktikum Kimia Dasar Ii Sel Volta'Dokumen15 halamanLaporan Praktikum Kimia Dasar Ii Sel Volta'tika apriliawatiBelum ada peringkat
- Praktikum Indikator Sifat Asam Dan BasaDokumen11 halamanPraktikum Indikator Sifat Asam Dan BasaTriadi NasherBelum ada peringkat
- Titik Beku Larutan Elektrolit Dan Non ElektrolitDokumen7 halamanTitik Beku Larutan Elektrolit Dan Non ElektrolitpangukirBelum ada peringkat
- LAPORAN KIMIA - Pergeseran KesetimbanganDokumen7 halamanLAPORAN KIMIA - Pergeseran KesetimbanganLatifah S Ningrum100% (1)
- Laporan Praktikum KimiaDokumen8 halamanLaporan Praktikum Kimiaandriyanysah0% (1)
- Indikator Buatan & AlamiDokumen4 halamanIndikator Buatan & AlamiNuur Poku100% (4)
- Laporan Praktikum HidrolisisDokumen20 halamanLaporan Praktikum Hidrolisisnovichaimaninsa100% (2)
- Laporan Praktikum KimiaDokumen12 halamanLaporan Praktikum Kimiatengku.asyidahBelum ada peringkat
- LAPORAN HASIL PRAKTIKUM Pergeseran Kesetimbangan KimiaDokumen10 halamanLAPORAN HASIL PRAKTIKUM Pergeseran Kesetimbangan KimiaAprilio BudimanBelum ada peringkat
- Pembahasan Tugas 2Dokumen3 halamanPembahasan Tugas 2Elisna Jayanti100% (1)
- Laporan Kimia Urea RafiDokumen4 halamanLaporan Kimia Urea RafiBikin LogoBelum ada peringkat
- Laporan Hasil Percobaan Reaksi KimiaDokumen6 halamanLaporan Hasil Percobaan Reaksi KimiaDina Fira100% (1)
- IsiDokumen15 halamanIsiRibca Martha LaoliBelum ada peringkat
- Penurunan Tekanan Uap JenuhDokumen11 halamanPenurunan Tekanan Uap Jenuhaghi ghaniyaBelum ada peringkat
- Derajat KeasamanDokumen13 halamanDerajat KeasamanLaila YuniarBelum ada peringkat
- Laporan Praktikum Dea AnielaDokumen8 halamanLaporan Praktikum Dea Anielayuyun verawatiBelum ada peringkat
- Praktikum SMADokumen6 halamanPraktikum SMALaila RismawatiBelum ada peringkat
- Kimia Untuk Smama Kelas Xi k13n Edisi Revisi PDFDokumen2 halamanKimia Untuk Smama Kelas Xi k13n Edisi Revisi PDFReni Aeryanti50% (2)
- Laporan Praktikum KimiaDokumen33 halamanLaporan Praktikum KimiaAlex PutraBelum ada peringkat
- Praktikum Ke V Kelompok 3 Grup 3Dokumen34 halamanPraktikum Ke V Kelompok 3 Grup 3NURUL IHKSANI -Belum ada peringkat
- Laporan Percobaan Kimia Perubahan EntalpiDokumen8 halamanLaporan Percobaan Kimia Perubahan EntalpiRaka Angga Prawira100% (1)
- Soal Jawab Kimia OrganikDokumen12 halamanSoal Jawab Kimia OrganikElsi Eci0% (1)
- Pengaruh Zat Terlarut Pada Titik Beku LarutanDokumen4 halamanPengaruh Zat Terlarut Pada Titik Beku LarutanEl-kapitan Adetia100% (1)
- Rangkuman Materi NetralisasiDokumen2 halamanRangkuman Materi NetralisasiRirin Nur FitrahBelum ada peringkat
- Laporan Praktikum KimiaDokumen11 halamanLaporan Praktikum KimiaYurikaBelum ada peringkat
- Hasil Praktikum Reaksi Redoks Dan Sel VoltaDokumen12 halamanHasil Praktikum Reaksi Redoks Dan Sel VoltaarslanBelum ada peringkat
- TTS Hidrolisis Septyana 29Dokumen3 halamanTTS Hidrolisis Septyana 29Septyana Nida FaizahBelum ada peringkat
- LAPORAN-blm FiksDokumen5 halamanLAPORAN-blm Fiksnggumba susanaBelum ada peringkat
- Laporan Praktikum KimiaDokumen10 halamanLaporan Praktikum KimiaFebrian Aditya PutraBelum ada peringkat
- Percobaan 8Dokumen18 halamanPercobaan 8resky apriyani simamoraBelum ada peringkat
- Surat Pernyataan Izin Orang TuaDokumen1 halamanSurat Pernyataan Izin Orang Tuatel_netBelum ada peringkat
- Tugas KelompokDokumen4 halamanTugas Kelompoktel_netBelum ada peringkat
- Neraca Teknis Dan Neraca AnalitikDokumen7 halamanNeraca Teknis Dan Neraca Analitiktel_netBelum ada peringkat
- Fitri MardikaDokumen1 halamanFitri Mardikatel_netBelum ada peringkat
- Sari InstrumentasiDokumen5 halamanSari Instrumentasitel_netBelum ada peringkat
- Makalah Cara Kerja Dan Penanganan Di Lab KimiaDokumen25 halamanMakalah Cara Kerja Dan Penanganan Di Lab Kimiatel_netBelum ada peringkat
- Proposal PenelitianDokumen10 halamanProposal Penelitiantel_netBelum ada peringkat
- KromatografiDokumen22 halamanKromatografitel_netBelum ada peringkat
- Kata Pengantar Dan Daftar IsiDokumen2 halamanKata Pengantar Dan Daftar Isitel_netBelum ada peringkat
- Kelainan Dan Penyakit Genetic Adalah Penyimpangan Dari Sifat Umum Atau Sifat RataDokumen3 halamanKelainan Dan Penyakit Genetic Adalah Penyimpangan Dari Sifat Umum Atau Sifat Ratatel_netBelum ada peringkat
- Kop Surat Panitia Pembangunan Mushalla NamirohDokumen1 halamanKop Surat Panitia Pembangunan Mushalla Namirohtel_netBelum ada peringkat
- Kop Surat Panitia Pembangunan Mushalla NamirohDokumen1 halamanKop Surat Panitia Pembangunan Mushalla Namirohtel_netBelum ada peringkat
- Kelainan Dan Penyakit Genetic Adalah Penyimpangan Dari Sifat Umum Atau Sifat RataDokumen3 halamanKelainan Dan Penyakit Genetic Adalah Penyimpangan Dari Sifat Umum Atau Sifat Ratatel_netBelum ada peringkat
- Kelompok+7 +Olahraga+Dan+Kesehatan+Dalam+Perspektif+IslamDokumen23 halamanKelompok+7 +Olahraga+Dan+Kesehatan+Dalam+Perspektif+IslamJery CrostianBelum ada peringkat
- Proposal TBDokumen20 halamanProposal TBtel_netBelum ada peringkat
- Gernish Dari Bawang BombaiDokumen2 halamanGernish Dari Bawang Bombaitel_netBelum ada peringkat
- Bab 1Dokumen12 halamanBab 1tel_netBelum ada peringkat
- Kata PengantarDokumen2 halamanKata Pengantartel_netBelum ada peringkat
- Proposal Adel 1Dokumen31 halamanProposal Adel 1tel_netBelum ada peringkat
- Kata Pengantar Proposal AsiDokumen2 halamanKata Pengantar Proposal AsiRio Van Der SarBelum ada peringkat
- Proposal URINEDokumen47 halamanProposal URINEtel_net100% (3)