Q&A
Diunggah oleh
Cik SuHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Q&A
Diunggah oleh
Cik SuHak Cipta:
Format Tersedia
Teknik Menjawab Kimia SPM ( KERTAS 2) oleh Pn Beh Chek Sim, Guru Cemerlang Kimia ( 2016)
1. Soalan bentuk Namakan dan nyatakan bahan kimia atau proses
-Formula dan simbol tidak digalakkan untuk jawapan soalan struktur dan esei atau semasa melabel rajah
-Simbol dan formula hanya digunakan untuk persamaan kimia
-Bahan Kimia ditulis ber sama keadaan fizik ( pepejal,larutan,gas) dan dengan diberi kepekatan jika perlu untuk prosedur
-Nombor pengoksidaan dalam kurungan hendaklah guna angka Roman VII, VI dll
-Sebatian organik ikut nama IUPAC
-Formula ion dibenarkan untuk soalan esei tertentu seperti Kadar Tindak balas ( Teori Pelanggaran)dan Elektrokimia tetapi
Formula ion hendaklah tepat.
Bi
l
1.
2.
3.
4.
5.
6.
7.
8.
9.
Contoh Soalan (SPM)
Jawapan yang kurang tepat
Jawapan yang tepat
Namakan gas yang mengeruhkan air kapur
Selain daripada air bromin, nyatakan nama
satu bahan reagen yang digunakan untuk
membezakan etena dan etana
Namakan ion-ion dalam larutan
CO2
Kalium manganat
Karbon dioksida
Kalium manganat (VII)
berasid
Cu2+, SO42-, H+, OH-
Nyatakan formula ion dalam asid
hidroklorik
Namakan proses untuk tindak balas
berikut 2SO2 + O2 2 SO3
Ion hidrogen, ion klorida, ion
hidroksida
Proses sentuh
Ion kuprum(II) , Ion sulfat,
ion hidrogen, ion hidroksida
H+, Cl-,OH-
Namakan satu gas adi
Bila serbuk zink dimasukkan ke dalam
suatu larutan biru, pepejal perang kuprum
terhasil. Nyatakan nama larutan biru
tersebut.
Nyatakan reagen yang digunakan untuk
proses pengoksidaan etanol ke asid etanoik
Namakan sebatian organik berikut
Ar
Kuprum sulfat
Argon
Kuprum(II) Sulfat
Kalium dikromat
Kalium dikromat (VI) berasid
2 metilbutena
2 metilbut-2-ena
Proses Sentuh
Pasti ada tanda sengkang
10
.
11.
12
.
2.
Namakan proses untuk tindak balas yang
ditunjukkan dalam persamaan berikut:
NaOH + HCl NaCl + H2O
Tuliskan formula empirik untuk
magnesium oksida
Namakan proses industry untuk menghasil
ammonia
Penutralan/
Nutralisation
Peneutralan
MGo
MgO
Proses Habber
Proses Haber
Apakah yang dimaksudkan dengan PERSAMAAN KIMIA, PERSAMAAN ION
dan PERSAMAAN SEPARUH ?
Bi
l
1.
2.
3.
4.
Contoh Soalan
Jawapan yang kurang tepat
Jawapan yang tepat
Tuliskan persamaan kimia
untuk tindak balas di
antara logam zink dan
larutan asid hidroklorik
Zn + HCl Zn Cl2 + H2
Zn + 2HCl => ZnCl2 + H2
ZN + 2HCl ZNCl2 + 2H
Zn + 2HCl
Tuliskan persamaan ion
untuk tindak balas di
antara logam zink dan
larutan asid hidroklorik
Tuliskan persamaan ion
untuk tindak balas di
antara asid hidroklorik dan
larutan natrium hidroksida
Tuliskan persamaan
separuh untuk tindak balas
pengoksidaan magnesium
ZnCl2 + H2
Zink + asid hidroklorik zink klorida +
hydrogen
Zn + 2HCl = ZnCl2 + H2
Zn + 2HCl ZnCl2 + H2
Zn + 2H+ Zn2+ + H2
HCl + NaOH NaCl + H2O
H+ + OH-
2 Mg + O2 2 MgO
Mg 2 e Mg2+
O 2- O2 + 2e
Mg
Mg2+
+ 2e
H2O
Teknik Menjawab Kimia SPM ( KERTAS 2) oleh Pn Beh Chek Sim, Guru Cemerlang Kimia ( 2016)
5.
Tuliskan persamaan untuk
tindak balas pembakaran
methane
6.
Tuliskan persamaan untuk
proses Haber
7.
Tuliskan persamaan untuk
Contohproses
Soalan
Sentuh
CH4 + O2 CO2 + H2O
N2 + 3H2
2SO2 + O2
CH4 + 2 O2
2H2O
CO2
2NH3
2 SO3
Jawapan kurang tepat
Jawapan yang tepat
Apakah yang diperhatikan bila pita magnesium
dimasukkan dalam larutan asid nitrik cair
Gas hidrogen
dibebaskan
Buih dihasilkan
Gelembung gas tanpa
warna
2.
Apakah yang diperhatikan di katod dalam elektrolisis
larutan kuprum(II) sulfat
Kuprum terbentuk
Enapan perang
3.
Gas hidrogen kering dialirkan ke atas serbuk kuprum(II)
oksida, apakah perubahan yang dapat diperhatikan ?
Pepejal perang
Kuprum
Pepejal hitam kuprum(II)
oksida menjadi perang
4.
Jika gas etena dialirkan ke dalam air bromin, nyatakan
perubahan yang berlaku
Warna air bromin
menjadi
putih/jernih/tanpa
warna
Warna perang air bromin
menjadi tanpa warna
5.
Nyatakan perubahan warna kuprum(II) sulfat selepas
tindak balas penyesaran dengan pepejal zink
Larutan menjadi tanpa
warna
Dari biru ke tanpa
warna
6.
Nyatakan perubahan warna kalium manganat (VII) bila
bertindak balas dengan etanol
Menjadi tanpa warna
Dari ungu ke tanpa warna
7.
Nyatakan perubahan warna kalium dikromat(VI) bila
bertindak balas dengan etanol
Nyatakan perubahan warna kepada penunjuk fenoltalein
apabila alkali dititrat dengan asid
Nyatakan perubahan warna kertas litmus bila di masukkan
ke dalam tabung uji berisi klorin
Nyatakan perubahan pada warna larutan ferum(II) sulfat
bila ditambah dengan air bromin
Menjadi hijau
Dari jingga ke hijau
Menjadi tanpa warna
Dari merah jambu ke tanpa
warna
Dari biru ke merah kemudian
dilunturkan
Warna perang bromin
menjadi tanpa warna.
Warna hijau ferum(II) sulfat
menjadi perang
Bi
l
1.
8.
9.
10
.
Menjadi putih
Warna bromin jadi
tanpa warna
Warna perang
ferum(III) sulfat
terbentuk
3. Menyatakan pemerhatian dengan tepat
-Tulis apa yang dilihat dan bukan kesimpulan, - Nyatakan perubahan warna dengan merujuk kepada warna asal dan
warna akhir,-Jangan guna istilah coklat untuk perang, kemerahan, kekuningan dan sebagainya. Berikut adalah warna yang
tepat untuk bahan kimia yang biasa digunakan ( pastikan guru anda menunjukkan bahan sebenar supaya dapat diingat)
(i)kuprum(II) sulfat = biru (ii) kalium manganat(VII) = ungu (iii) kalium dikromat(VI)= jingga
(iv) ferum(II) sulfat = hijau (v) ferum(III) sulfat = perang (vi) air bromin = perang (vii) larutan iodin = perang
(viii) gas bromin= perang (ix) gas iodin =ungu (x) kuprum(II) karbonat = hijau (xi) kuprum(II) oksida = hitam
(xii) gas klorin = kuning kehijauan (xiii) gas nitrogen dioksida = perang (xiv) Nyalaan pembakaran kalium=ungu
4.
Nyatakan ujian kimia pengesahan mengikut konsep :
KPI ( Kaedah, Pemerhatian ,
Inferens)
-Gunakan kata perbuatan di dalam jawapan seperti Tambah, Gaul bersama, Salurkan gas ,Masukkan, Letakkan pada mulut
tabung uji , Titiskan, Tuang, Turas, Panaskan dengan kuat, panaskan dengan perlahan, Kacau, Goncang dll
Bi
Contoh Soalan
Jawapan kurang
Jawapan tepat
l
tepat
1.
Nyatakan ujian untuk gas yang
dibebaskan di anod untuk
elektrolisis asid hidroklorik
cair
Nyatakan ujian untuk gas yang
dibebaskan bila asid ditambah
kepada logam karbonat
Uji dengan kayu
uji berbara
K :Masukkan kayu uji berbara dalam tabung uji berisi oksigen
P: Kayu uji berbara akan menyala
I: Gas oksigen dibebaskan
Air kapur keruh
K :Alirkan gas melalui tabung uji yang mengandungi air kapur
P: Air kapur berkeladak putih/menjadi keruh
I: Gas karbon dioksida dibebaskan
3.
Nyatakan ujian untuk gas yang
dibebaskan bila asid ditambah
dengan magnesium
Guna kayu uji
menyala
Bunyi pop
K:Dekatkan kayu uji menyala pada mulut tabung uji
P:Kayu uji menyala akan mengeluarkan bunyi pop dan padam
I : Gas hidrogen dibebaskan
4.
Nyatakan ujian untuk gas yang
Meluntur kertas
K:Masukkan kertas litmus biru lembap dalam tabung uji
2.
Teknik Menjawab Kimia SPM ( KERTAS 2) oleh Pn Beh Chek Sim, Guru Cemerlang Kimia ( 2016)
dibebaskan di anod untuk
elektrolisis asid hidroklorik
pekat
litmus
P:Kertas litmus biru tukar jadi merah kemudian dilunturkan
I:Gas Klorin dibebaskan
5.
Nyatakan ujian untuk
mengesahkan kehadiran ion
sulfat
Gunakan barium
klorida.Mendaka
n putih terbentuk
6.
Semasa proses pemindahan
elektron pada suatu jarak,
Nyatakan ujian untuk
mengesahkan kehadiran iodin
Uji gas ammonia
Guna larutan
kanji
K: Masukkan 2 cm3 larutan barium klorida 1 moldm-3 dalam
tabung uji
P: Mendakan putih terbentuk
I: Mendakan putih ialah barium sulfat. Ion sulfat hadir.
K:Masukkan 2 cm3 larutan kanji dalam tabung uji yang
mengandungi larutan iodin
P: Pewarnaan biru terhasil
I: Iodin hadir
K: Masukkan kertas litmus merah lembab dalam tabung uji
P: Kertas litmus merah tukar jadi biru
I : Gas beralkali iaitu gas ammonia terhasil
7.
5.
Kertas litmus
tukar biru
Soalan esei untuk menghuraikan suatu eksperimen (Kertas 2)
Tidak payah tulis tujuan, masalah,hipotesis,pembolehubah atau lukis rajah
Kalau soalan sebut terangkan prosedur, tulis prosedur sahaja,Kalau soalan sebut ,dalam jawapan hendak nyatakan
radas, kaedah,pemerhatian,Ikutlah apa yang dikehendaki. Penerangan tambahan tidak akan diberi markah.
Boleh tulis kaedah dalam ayat aktif dan jangan lupa nyatakan kuantiti , isipadu atau kepekatan dengan tepat dan logik.
SPM 2012 ( Soalan 10)
Catalyst and size of reactants can also affect the rate of reaction between acid and zinc.Choose one of these two
factors and describe an experiment to show how this factor affects the rate of reaction.[10 marks]
Mangkin dan saiz bahan tindak balas juga dapat mempengaruhi kadar tindak balas antara asid dengan
zink.Pilih satu daripada dua faktor ini dan huraikan satu eksperimen untuk menunjukkan bagaimana faktor
ini dapat mempengaruhi kadar tindak balas.[10 markah]
Rajah tidak memberi markah tetapi membantu anda menulis prosedur dengan tepat dan juga
senarai semua peralatan dan bahan kimia dengan betul.Jangan tulis sediakan radas seperti ditunjukkan
dalam rajah.
Ketulan zink
1.Isikan air dalam besen. [1]
2 Isikan buret dengan air dan telangkupkannya dalam besen [1]
3 Rekodkan bacaan awal buret [1 ]
4 Sukatkan 20cm3 1 M asid hidrokori dengan silinder penyukat
5. Tuang kan asid hidroklorik cair dalam kelalang kon [1]
6. Masukkan 2 g of ketulan zink[1]
7 Ambil bacaan buret untuk setiap sela masa 30 saat [1]
8 Rekod pemerhatian anda[1]
9. Ulangkan langkah 1-8 untuk menggantikan ketulan zink dengan serbuk zink
Penjadualan data (1 markah)
Masa/Time/s
Isipadu gas hidrogen/Volume of
hydrogen/cm3
30
60
90
120
150
180
Graf sebagai pentaksiran data ( 1 markah)
Label paksi dan
graf (yang mana
eksperimen untuk
ketulan zink dan
yang mana untuk
serbuk zink)
Teknik Menjawab Kimia SPM ( KERTAS 2) oleh Pn Beh Chek Sim, Guru Cemerlang Kimia ( 2016)
Kesimpulan: Kadar tindakbalas menggunakan serbuk zink lebih tinggi
( 1 mark)
Soalan Ramalan:
Pernyataan: Sebatian ionik boleh mengkonduksi elektrik dalam keadaan lebur dan akueus.
Dengan menamakan dua jenis sebatian ionik , huraikan satu eksperimen untuk membukti pernyataan tersebut.
Dalam jawapan anda hendaklah disertakan rajah berlabel, prosedur dan pemerhatian.
7.
N
O
1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
13.
14.
15.
16.
17.
18.
19.
20.
21
22
Pernyataan yang kurang tepat lawan yang tepat
TIDAK TEPAT
Bila logam magnesium direndam dalam larutan
kuprum(II) sulfat, mendakan perang terbentuk
Atom Argon stabil kerana mempunyai susunan
yang stabil/susunan elektron yang lengkap/8
elektron/petala terluar diisi dengan elektron
Atom natrium di Kala 3 sebab mengandungi 3
petala elektron
Kadar tindak balas semakin cepat
Kadar tindak balas menjadi semakin lambat
Magnesium lebih aktif daripada zink
Untuk eksperimen penyesaran, dan sel kimia,
magnesium lebih reaktif dari kuprum
Sebatian ionik boleh mengalir elektrik
Tambah ammonia
Cawan polistirin digunakan untuk
mengelakkan kehilangan haba
Fungsi titian garam/pasu berliang untuk
mengasingkan dua elektrolit sambil
melengkap litar
Kadar tindak balas menjadi semakin lambat
Panaskan kuprum karbonat
Bromin menjadi tanpa warna
Magnesium menderma dua elektron untuk
membentuk ion magnesium
Ion Plumbum(II) menerima 2 elektron
Magnesium boleh menurunkan kuprum(II)
oksida kepada kuprum kerana magnesium lebih
elektropositif daripada kuprum oksida
Daya tarikan antara molekul adalah
tinggi/rendah
Hidrokarbon adalah sebatian yang
mengandungi unsur hidrogen dan unsur
karbon
Elektrolit terdiri daripada ion-ion yang
bergerak
Asid adalah bahan yang larut dalam air
menghasilkan ion hidrogen
Alkali adalah bahan yang larut dalam air
menghasilkan hidroksida
TEPAT
enapan perang terbentuk
...........susunan elektron oktet yang stabil
............mengandungi 3 petala diisi oleh elektron
..Kadar tindak balas semakin tinggi
.. Kadar tindak balas semakin rendah
Magnesium lebih reaktif daripada zink
..........magnesium lebih elektropositif daripada kuprum
mengalir elektrik dalam keadaan leburan dan akueus
..larutan ammonia
..........mengurangkan kehilangan haba
.membenarkan ion mengalir melaluinya sambil
melengkap litar
rendah
Panaskan kuprum(II) karbonat
Warna perang bromin menjadi tanpa warna
Satu Atom magnesium menderma..
Satu ion plumbum(II) .
lebih reaktif
......................lemah
............unsur hidrogen dan unsur karbon sahaja
....................bergerak bebas
........mengion dalam air .........
........mengion dalam air ......
Teknik Menjawab Kimia SPM ( KERTAS 2) oleh Pn Beh Chek Sim, Guru Cemerlang Kimia ( 2016)
23
24
25
26.
27.
28.
29.
30.
Daya tarikan antara atom sebatian kovalen
lemah
Susunan elektron natrium = 2:8:1
Natrium menghilangkan elektron untuk
mencapai kestabilan
Nombor neutron C-12 ialah 12
Besi(II) dioksida kepada besi(III)
Kuantiti zink digunakan ialah 4g
Nombor pengoksidaan kromium ialah 6
Haba peneutralan ialah haba yang dibebaskan
bila asid bertindakbalas dengan alkali
.........antara molekul...........
2.8.1
Satu atom natrium menghilangkan satu elektron untuk
mencapai susunan elektron oktet yang stabil
Nombor nukleon .....
Ion ferum(II) ....... ion ferum (III)
Jisim zink.....
Nombor pengoksidaan kromium ialah +6
Haba peneutralan ialah haba yang dibebaskan bila satu mol ion
hidrogen bertindak balas dengan satu mol ion hidroksida
menghasilkan satu mol air.
Tip melukis dengan tepat
-Rajah hendaklah berfungsi
-Semua peralatan yang penting hendaklah dilabel
-Nama bahan kimia hendaklah dalam ayat penuh bukan simbol
-Penyumbat hendaklah tidak terbenam dan dilorek
-Buret hendaklah di kaki retotkan
-Larutan dilorek dengan garis putus-putus
- Letakkan anak panah untuk menunjukkan arah aliran gas
-Tidak payah lukis kaki retot untuk jangkasuhu
-Tidak payah lukis penunu Bunsen , hanya letakkan anak panah dan perkataan ,panaskan
Melukis rajah
-Tunjukkan aras meniskus untuk air
-Lukiskan kelalang kon untuk penitratan bukan bikar
- Use conical flask for titration and not beaker
-Tidak payah lukis kasa dawai untuk haba pembakaran
-Pastikan tiada kasa dawai untuk haba pembakaran
-Pastikan jangkasuhu tidak sentuh dasar bikar
-Suis hendaklah ditutup atau tidak payah lukis suis
- Aliran elektron ditanda dengan anak panah pada litar atau selari di luar litar tetapi bukan merentasi larutan
-Bila lukis atom , hendaklah sekurang-kurangnya 3 lapisan dengan bulatan yang sama saiz. (Guna pembaris bulat)
-Jangan lupa tulis perkataan tenaga untuk gambarajah aras tenaga
-Jangan lupa label paksi untuk graf bersama unit
SPM 2013 : Lukis formula struktur alkena, eksperimen pendehidratan,rajah aras tenaga
SPM 2012 : Lukis formula struktur isomer, sebatian ionik magnesium oksida , eksperimen penulenan
SPM 2011 : Lukis susunan elektron ion natrium , eksperimen pemindahan elektron pada suatu jarak
SPM 2010: Lukis formula struktur isomer, sebatian kovalen,eksperimen penyaduran sudu
Ramalan: Lukis susunan elektron karbon dioksida, eksperimen menentukan haba pembakaran
etanol, formula struktur ester , sel kimia ,peneutralan
Pengiraan
Semua langkah hendaklah ditunjukkan.
Jom jawab soalan SPM
SPM 2011
. Hydrochloric acid is a strong acid. Table shows two solutions of hydrochloric acid, P and Q,
of different concentrations.
Asid hidroklorik ialah asid kuat. Jadual menunjukkan dua larutan asid hidroklorik,
P dan Q, dengan kepekatan yang berlainan.
Hydrochloric acid solution
Larutan asid hidroklorik
Concentration (mol dm3)
Kepekatan (mol dm3)
0.100
0.001
Teknik Menjawab Kimia SPM ( KERTAS 2) oleh Pn Beh Chek Sim, Guru Cemerlang Kimia ( 2016)
Table
Jadual
(a)State the meaning of an acid.
Nyatakan maksud asid.
Solution that dissolves in water to produce hydrogen
_Bahan
yang mengion dalam air menghasilkan ion
hidrogen________________________
[1 mark]/[1 markah]
(b)Why hydrochloric acid is a strong acid?
Mengapakah asid hidroklorik ialah asid kuat?
Ionises in water
[1 mark]
/[1 markah]
Mengion lengkap dalam air menghasilkan
kepekatan ion hidrogen yang tinggi
(c) Solutions P and Q have different pH values.
Larutan P dan Q mempunyai nilai pH yang berbeza.
(i) Which solution gives a lower pH value?
Larutan yang manakah memberi nilai pH yang lebih rendah?
P[1 mark]/[l markah]
(ii) Give one reason for the answer in (c)(i).
Beri satu sebab bagi jawapan di (c)(i).
It has more H+
[1 mark]/[ 1 markah]
Larutan P mengandungi
kepekatan ion hidrogen yang tinggi
(d)25 cm3 of 0.1 mol dm-3 sodium hydroxide solution is put in a conical flask. Then a few drops of
phenolphthalein are added. This solution is titrated with solution P.
25 cm3 larutan natrium hidroksida 0.1 mol dm3 dimasukkan ke dalam kelalang kon. Kemudian beberapa
titis fenolftalein ditambah. Larutan ini dititratkan dengan larutan P.
(i)
State the type of reaction between sodium hydroxide solution and
(ii)
(iii)
solution P.
Nyatakan jenis tindak balas antara larutan natrium hidroksida
dengan larutan P.
Nutralisation/Penutralan [1 markah]
Peneutralan
What is the colour change of the mixture at the end point?
Apakah perubahan warna campuran itu pada takat akhir
Colourless/Tak berwarna
Merah jambu ke tanpa warna
[1 mark]/[1 markah]
Write the chemical equation for the reaction.
Teknik Menjawab Kimia SPM ( KERTAS 2) oleh Pn Beh Chek Sim, Guru Cemerlang Kimia ( 2016)
Tulis persamaan kimia bagi tindak balas itu.
Hcl + NaOh = NacL + H20
HCl + NaOH
(iv)
[2 marks]/[2 markah]
Calculate the volume of hydrochloric acid used.
Hitung isi padu asid hidroklorik yang digunakan.
25 cm3 ( mesti tunjuk kiraan)
Ma Va = A
Mb Vb B
0.1x Va= 1
0.1 x 25 1
NaCl + H2O
Va= 0.1 x 25 = 25 cm3
0.1
[2 marks]
[2 markah]
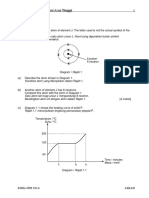
10( Table shows the proton number of elements P, Q, R and S.
b) Jadual menunjukkan nombor proton bagi unsur P, Q, R dan S.
Table/Jadual
Based on Table, choose two elements that form a compound with a high melting point
and a high boiling points. Explain how the compound is formed and draw the electron
arrangement for the compound.[10 marks]
Berdasarkan Jadual, pilih dua unsur yang boleh membentuk sebatian yang mempunyai
takat lebur dan takat didih yang tinggi.
Terangkan bagaimana sebatian itu terbentuk dan lukis susunan elektron untuk sebatian
tersebut.
Note : Ask student to memorize element 1 to 20 in the periodic table , so they can
recognize)
P = carbon Q=Oxygen, R = potassium, S= calcium
This is how to teach the students to write correctly follow the format and the code.
Q and R// Q and S ( 1 mark)
Kod
Jawapan
Susunan
elektron
Derma
Atom R mempunyai susunan elektron 2.8.8.1
(1)
Atom Q mempunyai susunan elektron 2.6(1)
Teknik Menjawab Kimia SPM ( KERTAS 2) oleh Pn Beh Chek Sim, Guru Cemerlang Kimia ( 2016)
Atom R menderma satu elektron valens
kepada atom Q supaya mencapai
Susunan elektron oktet 2.8.8 yang stabil
(1)
Atom Q menerima dua elektron daripada
dua atom R supaya mencapai
Susunan elektron oktet 2.8 yang stabil (2)
Ion
Ion R+ terhasil dan ion Q 2- terhasil
Stabil
Rujuk atas
Daya
tarikan
Ion R+ dan Ion Q2- ditarik dengan daya tarikan
elektrostatik yang kuat
Formula
Sebatian ionik dengan formula R2Q terbentuk.
Rajah ( Ada nukleus dilabel, bilangan petala dan bilangan elektron tepat)
Nucleus , Number of shells and number of electrons correct ( 1 mark)
Label charge, R and Q correctly ( 1 mark)
Teknik Menjawab Kimia SPM ( KERTAS 2) oleh Pn Beh Chek Sim, Guru Cemerlang Kimia ( 2016)
Technique to answer question based on rate of reaction
EXPERIMENT
Concentration of acid/Kepekatan asid
Initial temperature/Suhu awal
Catalysts/Mangkin
Condition of Zinc/Keadaan zink
Reaction time/Masa tindak balas
I
0.1 M
30 C
No
II
0.1 M
30 C
No
III
0.1 M
40 C
No
IV
0.1M
40C
Yes
V
0.2 M
40 C
No
Powder
Serbuk
50
Granulated
Serpihan
65
Powder
Serbuk
40
Powder
Serbuk
30
Powder
Serbuk
25
A student carried out four experiments to investigate the effect of concentration, temperature and
catalyst on
the rate of reaction between hydrochloric acid and zinc metal for each experiment.
The time taken for the zinc metal to dissolve is recorded and the results is tabulated as follows
Seorang murid menjalankan 4 eksperiment untuk mengkaji kesan kepekatan, suhu dan mangkin ke
atas kadar
Tindak balas di antara asid hidroklorik cair dan logam zink.Masa untuk logam zink melarut
direkodkan dan keputusan dijadualkan seperti di atas.
(a)Write the ionic equation for the reaction between zinc and acid.
II
Tulis persamaan ionik untuk tindak balas di antara zink dan asid
+
2+
Zn + 2H Zn
+ H2
( 1 markah seimbang , 1 markah formula betul)
(b)(i)On the same axis, sketch the graph of volume of hydrogen gas against time for Experiment I an
II.
Pada paksi yang sama, lakarkan graf isipadu gas hydrogen melawan masa untuk eksperimen I
dan II
(ii)Compare the rate of reaction between Experiment I and II. Explain by refering to the collision
theory why there is a difference in the rate of the reaction in the experiment
Bandingkan kadar tindak balas di antara eksperimen I dan II. Terangkan perbezaan tersebut
dengan
menggunakan teori pelanggaran.
Time/s
Teknik Menjawab Kimia SPM ( KERTAS 2) oleh Pn Beh Chek Sim, Guru Cemerlang Kimia ( 2016)
SIZE OF ZINC IN EXPERIMENT I IS SMALLLER
THAN EXP ii
Total surface area perunit volume of zinc is bigger in
exp 1 than exp II
Frequency of collision between zinc atom and H +
ion is higher in experiment I compare to experiment
II
Frequency of effective collision between zinc atom
and H+ ion is higher in experiment I compare to
experiment II
Rate of reaction of experiment I is higher than
experiment II
Teknik Menjawab Kimia SPM ( KERTAS 2) oleh Pn Beh Chek Sim, Guru Cemerlang Kimia ( 2016)
(c) Compare the rate of reaction between Experiment I and III. Explain by refering to the collision
theory why there is a difference in the rate of the reaction in the experiment
Bandingkan kadar tindak balas di antara eksperimen I dan III.Terangkan perbezaan dengan
merujuk
kepada teori pelanggaran.
Suhu asid set III adalah lebih tinggi daripada suhu
Saiz zink set I adalah lebih kecil daripada set II (1)
asid set I
Jumlah
luas ion
permukaan
zinkzink
perunit
padu dalam
set I
Tenaga
kinetik
hidrogen dan
atom dalam
set
IIIadalah lebih tinggi daripada set II (1)
Frekuensi
perlanggaran
antara
atom zink dan ion H+
adalah
lebih tinggi
daripada set
I
lebih tinggi
dalam setantara
I berbanding
Frekuensi
perlanggaran
atom zinkdengan
dan ion set
H+II
lebih
tinggi perlanggaran berkesan di antara atom zink
Frekuensi
dalam
set H+
I berbanding
dengan
set set
II I berbanding dengan
dan ion
lebih tinggi
dalam
Frekuensi
perlanggaran berkesan di antara atom zink
set II
dan
ion H+
lebihbalas
tinggiuntuk
dalam eksperimen
set III berbanding
Kadar
tindak
set I lebih tinggi
dengan
daripada set II
set I
Kadar tindak balas untuk eksperimen set III lebih
tinggi
daripada set I
(d) Compare the rate of reaction between Experiment III and IV. Explain by refering to the collision
theory why there is a difference in the rate of the reaction in the experiment
Bandingkan kadar tindak balas di antara eksperimen III dan IV.Terangkan perbezaan dengan
merujuk
kepada teori pelanggaran.
Larutan kuprum(II) sulfat adalah mangkin
Mangkin telah merendahkan tenaga pengaktifan
Tenaga pengaktifan yang rendah membolehkan
lebih banyak atom zink dan ion hidrogen yang
berlanggar mencapai tenaga pengaktifan tersebut.
Frekuensi perlanggaran antara atom zink dan ion
H+
Teknik Menjawab Kimia SPM ( KERTAS 2) oleh Pn Beh Chek Sim, Guru Cemerlang Kimia ( 2016)
lebih tinggi dalam set IV berbanding dengan set
III
Frekuensi perlanggaran berkesan di antara atom
zink
dan ion H+ lebih tinggi dalam set IV berbanding
dengan set III
Kadar tindak balas untuk eksperimen set IV
lebih tinggi daripada set III
(e)
Compare the rate of reaction between Experiment III and Experiment V. Explain by refering to the
collision
theory why there is a difference in the rate of the reaction in the experiments.
Bandingkan kadar tindak balas di antara eksperimen III dan V.Terangkan perbezaan dengan
merujuk
kepada teori pelanggaran.
Kepekatan asid hidroklorik dalam eksperimen V
lebih tinggi dalam set IV
Bilangan ion hidrogen perunit padu dalam set V lebih
tinggi daripada eksperimen set IV
Frekuensi perlanggaran antara atom zink dan ion
H+
lebih tinggi dalam set V berbanding dengan set IV
Frekuensi perlanggaran berkesan di antara atom
zink
dan H+ ion lebih tinggi dalam set V berbanding
dengan
set IV
Teknik Menjawab Kimia SPM ( KERTAS 2) oleh Pn Beh Chek Sim, Guru Cemerlang Kimia ( 2016)
Kadar tindak balas untuk eksperimen set V
lebih tinggi daripada set IV
[10 markah]
Anda mungkin juga menyukai
- Nota NutrisiDokumen24 halamanNota Nutrisianis fazilaBelum ada peringkat
- SPM ChemDokumen181 halamanSPM Chemkslew14Belum ada peringkat
- Chemistry K3 SPM 2010 - Kupasan Mutu Jawapan CalonDokumen12 halamanChemistry K3 SPM 2010 - Kupasan Mutu Jawapan CalonCikgu FaizalBelum ada peringkat
- Kimia Tingkatan 4Dokumen2 halamanKimia Tingkatan 4nna80100% (2)
- Modul Tropikal Kimia: GaramDokumen20 halamanModul Tropikal Kimia: GaramMohd Haidil100% (1)
- Ting 5 Kertas 3 Fizik Upsa 2022Dokumen7 halamanTing 5 Kertas 3 Fizik Upsa 2022NORINA BINTI MOHD NOR KPM-GuruBelum ada peringkat
- Kertas 1 Kimia Tingkatan 4 DwibahasaDokumen21 halamanKertas 1 Kimia Tingkatan 4 DwibahasawanyanaBelum ada peringkat
- Kimia K2 T4Dokumen10 halamanKimia K2 T4intan rohaida100% (1)
- KSSM Kimia t5 AmaliDokumen48 halamanKSSM Kimia t5 AmaliNABIL FAUZIBelum ada peringkat
- Sistem Pengangkutan TumbuhanDokumen13 halamanSistem Pengangkutan Tumbuhankembara08Belum ada peringkat
- Latihan Elektrokimia 1Dokumen13 halamanLatihan Elektrokimia 1persona2918Belum ada peringkat
- Soalan Struktur2Dokumen22 halamanSoalan Struktur2Macai Operasi100% (1)
- Documents - Tips - 15 Kesalahan Lazim Dalam Jawapan Kimia Calon SPM PDFDokumen2 halamanDocuments - Tips - 15 Kesalahan Lazim Dalam Jawapan Kimia Calon SPM PDFhafizah manapBelum ada peringkat
- Laporan Bengkel Kimia SPM 2021Dokumen5 halamanLaporan Bengkel Kimia SPM 2021Nurul HidayahBelum ada peringkat
- Soalan ObjektifDokumen35 halamanSoalan ObjektifSiva Guru100% (1)
- Elektrokimia (Soalan Ulangkaji)Dokumen4 halamanElektrokimia (Soalan Ulangkaji)Liza RaziBelum ada peringkat
- M1 BK4 Modul Aras TinggiDokumen24 halamanM1 BK4 Modul Aras TinggiZarith Hidayah IsmileBelum ada peringkat
- Bab 4 Sebatian KarbonDokumen5 halamanBab 4 Sebatian KarbonMaryati KematBelum ada peringkat
- Soalan 8 Dan 9 Biologi SPM EseiDokumen9 halamanSoalan 8 Dan 9 Biologi SPM EseiSunita JobliBelum ada peringkat
- Jsi Kimia Kertas 1Dokumen2 halamanJsi Kimia Kertas 1sharinhanumBelum ada peringkat
- Ujian Amali Biologi PPC 2021Dokumen7 halamanUjian Amali Biologi PPC 2021Cynthia LingBelum ada peringkat
- Pelan Strategik BiologiDokumen14 halamanPelan Strategik BiologiJoyce Cheng100% (4)
- Fizik k3 AmaliDokumen7 halamanFizik k3 AmaliAnonymous 91401yBelum ada peringkat
- RPT KSSM Kimia Tingkatan 4 Tahun 2021Dokumen30 halamanRPT KSSM Kimia Tingkatan 4 Tahun 2021NUR DIANA BINTI OTHMAN MoeBelum ada peringkat
- Latihan Sel KimiaDokumen2 halamanLatihan Sel KimiafizahBelum ada peringkat
- Folio Kimia Tingkatan 4 Bab 9Dokumen1 halamanFolio Kimia Tingkatan 4 Bab 9Hassan Ukong0% (1)
- Biologi PAT T4 Zon TGH 2017Dokumen35 halamanBiologi PAT T4 Zon TGH 2017Noor Hidayah Ibrahim100% (1)
- Kuiz Makmal SainsDokumen1 halamanKuiz Makmal SainsnanarahmannaimBelum ada peringkat
- Skema Pemarkahan Sains Tingkatan 1Dokumen4 halamanSkema Pemarkahan Sains Tingkatan 1Irdina NabilahBelum ada peringkat
- Soalan Pameran Kimia 2014Dokumen10 halamanSoalan Pameran Kimia 2014ZulBelum ada peringkat
- Ujian JulaiDokumen5 halamanUjian JulaiAsyikin Ahmad KhanBelum ada peringkat
- Nota GaramDokumen1 halamanNota GaramHafinaz BahariBelum ada peringkat
- Ujian Selaras 1 Biologi Tingkatan 4Dokumen12 halamanUjian Selaras 1 Biologi Tingkatan 4Rizal Saeran100% (1)
- SPM 4551 2009 Biology k1Dokumen41 halamanSPM 4551 2009 Biology k1pss smk selandarBelum ada peringkat
- Sains Tingkatan 2Dokumen7 halamanSains Tingkatan 2amadkacakBelum ada peringkat
- 9.1 SATELIT Jawapan LatihanDokumen10 halaman9.1 SATELIT Jawapan LatihanFATIN NABILABelum ada peringkat
- Format Jsu KimiaDokumen16 halamanFormat Jsu KimiaifzaeBelum ada peringkat
- Teknik KFCDokumen11 halamanTeknik KFCrahimBelum ada peringkat
- Latihan Fizik Waktu Cuti 2015Dokumen9 halamanLatihan Fizik Waktu Cuti 2015SULIANI DANNYBelum ada peringkat
- Paper3 F4&skemaDokumen12 halamanPaper3 F4&skemacikgu HK0% (1)
- Soalan CTH 1Dokumen7 halamanSoalan CTH 1HanyHannyBelum ada peringkat
- SOALAN Past Years ElectrochemistryDokumen25 halamanSOALAN Past Years ElectrochemistryNorzilah MazaharBelum ada peringkat
- Borang Post Mortem SPM 2018 - KIMIADokumen2 halamanBorang Post Mortem SPM 2018 - KIMIAAlexBelum ada peringkat
- Baja KalFos Kulit Telur Untuk Elak Bunga Dan Buah Gugur Sebelum MatangDokumen8 halamanBaja KalFos Kulit Telur Untuk Elak Bunga Dan Buah Gugur Sebelum MatangShafidahSaadBelum ada peringkat
- 26 - Kem Kecemerlangan SPMDokumen4 halaman26 - Kem Kecemerlangan SPMGeez EzaniBelum ada peringkat
- Pecutan Akhir SPMDokumen87 halamanPecutan Akhir SPMpiyabaik100% (10)
- Soalan Kbat NuklearDokumen3 halamanSoalan Kbat NuklearBaktiar HasnanBelum ada peringkat
- Latihan Sains Tingkatan 3 Bab 6 Tanah Dan SumbernyaDokumen2 halamanLatihan Sains Tingkatan 3 Bab 6 Tanah Dan SumbernyaMichelleMuroh60% (5)
- Kertas Amali Siri ElektrokimiaDokumen5 halamanKertas Amali Siri ElektrokimiadonutBelum ada peringkat
- Biologi Skema SPM Bio Kertas3 Set 1Dokumen11 halamanBiologi Skema SPM Bio Kertas3 Set 1api-3841296100% (1)
- 1.2e. Pengiraan Nilai Tenaga SPM 2004 - 2011Dokumen14 halaman1.2e. Pengiraan Nilai Tenaga SPM 2004 - 2011shurinaabrahim100% (7)
- Bio K3Dokumen5 halamanBio K3Sharifah Izyan Al-QudryBelum ada peringkat
- Skema Jawapan Pat t2 Sains PDFDokumen7 halamanSkema Jawapan Pat t2 Sains PDFQzairudin Mat Jusoh100% (1)
- Matematik Pelan Tindakan Dan Pelan OperasiDokumen13 halamanMatematik Pelan Tindakan Dan Pelan OperasiAnonymous VKuGYRpUv100% (1)
- -Dokumen12 halaman-Zahra Faras SukmaBelum ada peringkat
- Latihan Soal USBN Vol. 3Dokumen11 halamanLatihan Soal USBN Vol. 3KHOMNYOYt PlayzBelum ada peringkat
- Reaksi-Reaksi Kimia 2Dokumen5 halamanReaksi-Reaksi Kimia 2fera audinaBelum ada peringkat
- Tugas Akhir Kimia TH 2019-2020Dokumen6 halamanTugas Akhir Kimia TH 2019-2020FatmawatiBelum ada peringkat
- Percobaan 4 Reaksi-Reaksi KimiaDokumen10 halamanPercobaan 4 Reaksi-Reaksi KimiaRivanda RikiansyahBelum ada peringkat
- Try Out Un Kimia Paket 1 TH 2013 PDFDokumen12 halamanTry Out Un Kimia Paket 1 TH 2013 PDFhari.suryanto8417Belum ada peringkat
- Visi Dan Misi Jabatan Pelajaran SarawakDokumen5 halamanVisi Dan Misi Jabatan Pelajaran SarawakCik SuBelum ada peringkat
- Laporan Kewangan DLPDokumen1 halamanLaporan Kewangan DLPCik SuBelum ada peringkat
- Aktiviti KRNDokumen63 halamanAktiviti KRNmawar beseri100% (1)
- Program Pintar Cerdas Zon Malaysia TimurDokumen12 halamanProgram Pintar Cerdas Zon Malaysia TimurCik SuBelum ada peringkat
- Kemahiran MembacaDokumen3 halamanKemahiran MembacaCik SuBelum ada peringkat