Regresi Linier - Soal Pra Praktikum Minggu Ke-1 Senin Siang
Diunggah oleh
andono kusuma jatiJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Regresi Linier - Soal Pra Praktikum Minggu Ke-1 Senin Siang
Diunggah oleh
andono kusuma jatiHak Cipta:
Format Tersedia
LABORATORIUM KOMPUTASI PROSES
DEPARTEMEN TEKNIK KIMIA FAKULTAS TEKNIK
UNIVERSITAS DIPONEGORO
SOAL PRA PRAKTIKUM REGRESI LINIER
1. Senyawa A mengalami reaksi di dalam reaktor batch yang memiliki volume konstan.
Reaksi yang terjadi adalah reaksi irreversible orde satu dengan stoikiometri reaksi A → R.
Reaksi yang terjadi dianalisa sehingga didapatkan hubungan waktu (t) terhadap
konsentrasi senyawa A (CA). Diketahui bahwa konsentrasi awal senyawa A masuk reaktor
(CA0) adalah 10 mol/L.
𝐶𝐴 𝐶𝐴
t [menit] CA [mol/L] −𝑙𝑛 −𝑙𝑛 ℎ𝑖𝑡𝑢𝑛𝑔
𝐶𝐴0 𝐶𝐴0
0 10
20 8.3
40 6.7
60 5.5
100 4.3
120 3.5
180 2.5
300 1
Didapatkan juga persamaan berikut ini karena reaksi yang terjadi adalah reaksi irreversible
orde satu:
𝐶𝐴 𝑡
𝑑𝐶𝐴 𝑑𝐶𝐴
− = 𝑘𝐶𝐴 → [− ∫ = 𝑘 ∫ 𝑑𝑡] … … … … … … … … … … … (1)
𝑑𝑡 𝐶𝐴
𝐶𝐴0 0
Dari data-data yang didapatkan tersebut, kerjakanlah:
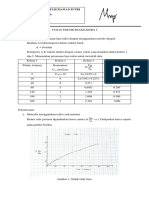
a. Lengkapilah tabel di atas dan buat/munculkan di console, serta buat grafik
𝑪
perbandingan waktu (sumbu x) vs −𝒍𝒏 (𝑪 𝑨 ) (sumbu y)
𝑨𝟎
b. Cari nilai k reaksi (bonus apabila diberi satuannya)
c. Perkirakan konsentrasi senyawa A setelah 360 menit
LABORATORIUM KOMPUTASI PROSES
DEPARTEMEN TEKNIK KIMIA FAKULTAS TEKNIK
UNIVERSITAS DIPONEGORO
PETUNJUK
1. Nilai (b) atau (intercept) dianggap 0, sehingga persamaan regresi linier yang terbentuk
[y=ax]
2.
3.
Anda mungkin juga menyukai
- Problem 9.7 and 7.9 (Chemical Reaction Engineering Third Edition Octave Levenspiel)Dokumen12 halamanProblem 9.7 and 7.9 (Chemical Reaction Engineering Third Edition Octave Levenspiel)Cindy SaskiaBelum ada peringkat
- Laporan Resmi 1 CSTRDokumen31 halamanLaporan Resmi 1 CSTRAnonymous xAnOZRdBelum ada peringkat
- Berikut Beberapa Contoh Reaksi AdisiDokumen8 halamanBerikut Beberapa Contoh Reaksi AdisiakbarBelum ada peringkat
- Kimia Fisika BlablablaDokumen13 halamanKimia Fisika BlablablaFariszBelum ada peringkat
- 8-Perancangan Reaktor BatchDokumen5 halaman8-Perancangan Reaktor BatchTio ScreamoBelum ada peringkat
- Ujian SUSULAN TRK Lanjut 2022Dokumen2 halamanUjian SUSULAN TRK Lanjut 2022Herald MatiusBelum ada peringkat
- Persamaan Arrhenius Dan Energi AktivasiDokumen10 halamanPersamaan Arrhenius Dan Energi Aktivasikurnia lenggogeniBelum ada peringkat
- Bank Soal Uas Semester 5 Tekkim PDFDokumen33 halamanBank Soal Uas Semester 5 Tekkim PDFMUHAMAD YULIANTOBelum ada peringkat
- Modul Simulasi Proses Periode 1Dokumen42 halamanModul Simulasi Proses Periode 1Lutfia KhasanahBelum ada peringkat
- KinetikaDokumen11 halamanKinetikaYunita SariBelum ada peringkat
- Latihan Sa - DyDokumen3 halamanLatihan Sa - DyAde YogaBelum ada peringkat
- p5 Bab3Dokumen9 halamanp5 Bab3PuLung SambadhaBelum ada peringkat
- 2 - B - Tri Wahyu Puji LestariDokumen5 halaman2 - B - Tri Wahyu Puji LestariTriwahyu /28Belum ada peringkat
- Latihan Soal KinetikaDokumen5 halamanLatihan Soal Kinetikahaura rafifah ilvi habibahBelum ada peringkat
- TuuuDokumen44 halamanTuuuHasbi AsshidiqiBelum ada peringkat
- BAB V Reaktor Batch IdealDokumen12 halamanBAB V Reaktor Batch IdealNurul A T FadhlyBelum ada peringkat
- Laporan Reaktor Tubular DesliaDokumen21 halamanLaporan Reaktor Tubular DesliaIra Triasi NainggolanBelum ada peringkat
- Megawati Setiawan Putri - Tugas 2 TRK IDokumen5 halamanMegawati Setiawan Putri - Tugas 2 TRK IMegawati Setiawan PutriBelum ada peringkat
- Cover MAKALAH KimfisDokumen35 halamanCover MAKALAH KimfisFauzan HantoroBelum ada peringkat
- Reaktor CSTRDokumen12 halamanReaktor CSTRHilmi Abubakar ShidiqBelum ada peringkat
- DIKTAT Komputasi TerapanDokumen40 halamanDIKTAT Komputasi TerapanAhmad IrgiBelum ada peringkat
- Tugas 2 TRK LanjutDokumen23 halamanTugas 2 TRK LanjutLailyBelum ada peringkat
- Uap MTK 2-Kode BDokumen6 halamanUap MTK 2-Kode Bpriska olshopBelum ada peringkat
- Soal TRKDokumen9 halamanSoal TRKDinda MeilaniBelum ada peringkat
- Soal 1Dokumen2 halamanSoal 1djokoBelum ada peringkat
- Reaktor Ideal Aliran KontinyuDokumen19 halamanReaktor Ideal Aliran KontinyuAhmad AsfahaniBelum ada peringkat
- Tugas-Kinetika-2017Dokumen10 halamanTugas-Kinetika-2017Andrean ZukempotBelum ada peringkat
- Reaktor Ideal Aliran Kontinyu PDFDokumen16 halamanReaktor Ideal Aliran Kontinyu PDFAdrian WijayaBelum ada peringkat
- Diktat 1 UOP 2021Dokumen29 halamanDiktat 1 UOP 2021hannnndraysssBelum ada peringkat
- Kinetika 1 Web2 Updated 2007Dokumen20 halamanKinetika 1 Web2 Updated 2007Cintia PebriBelum ada peringkat
- Matlab - Tugas2D - Soal1dan3 - Laporan - Nurika Andana Putri - 3335190078Dokumen28 halamanMatlab - Tugas2D - Soal1dan3 - Laporan - Nurika Andana Putri - 3335190078Nurika AndanaBelum ada peringkat
- Kinetika Reaksi Saponifikasi Etil AsetatDokumen15 halamanKinetika Reaksi Saponifikasi Etil Asetathanis mileniaBelum ada peringkat
- TRK2 A - Tugas1Dokumen1 halamanTRK2 A - Tugas1MohammadRakhaWidiansyahBelum ada peringkat
- Kinetika KimiaDokumen17 halamanKinetika KimiaAgung Prawira Negara0% (1)
- Penentuan Orde Reaksi (Minggu4) A2241Dokumen69 halamanPenentuan Orde Reaksi (Minggu4) A2241gamalielBelum ada peringkat
- SoalDokumen6 halamanSoalEvi LutfianiBelum ada peringkat
- Materi 4-1Dokumen6 halamanMateri 4-1Muhamad Thohir AzhariBelum ada peringkat
- Bab 2Dokumen17 halamanBab 2Firmanto VanjaitanBelum ada peringkat
- Proposal RiakDokumen22 halamanProposal RiakDian Remarthin GirsangBelum ada peringkat
- Tugas Reaktor IsotermalDokumen22 halamanTugas Reaktor IsotermalKezni SavitriBelum ada peringkat
- 6-Batch ReactorDokumen13 halaman6-Batch ReactorLauren RandoBelum ada peringkat
- N. LAMPIRANDokumen46 halamanN. LAMPIRANDonald KitchenBelum ada peringkat
- BAB II Esterifikasi (Metanol)Dokumen6 halamanBAB II Esterifikasi (Metanol)putripus100% (1)
- Tugas TRK 79-83Dokumen7 halamanTugas TRK 79-83Willy Al KusariBelum ada peringkat
- Tugas Kimia Dasar - Teknik Geologi 2017Dokumen5 halamanTugas Kimia Dasar - Teknik Geologi 2017Iqbal Muhammad FajarBelum ada peringkat
- Tugas 1 Analisis Data KinetikDokumen2 halamanTugas 1 Analisis Data Kinetikfarah khilma yusticaBelum ada peringkat
- Tugas Teknik Reaksi Kimia LanjutDokumen10 halamanTugas Teknik Reaksi Kimia Lanjutrinnynovia09Belum ada peringkat
- Bank Soal Semester 5Dokumen61 halamanBank Soal Semester 5Chairani ShafiraBelum ada peringkat
- KINETIKA - KEL.3 - KterkaitanLajuDgnKonsReaktanDokumen19 halamanKINETIKA - KEL.3 - KterkaitanLajuDgnKonsReaktanSalsabila LuthfiyahBelum ada peringkat
- Perhitungan Konversi Reaktor XanthasiDokumen37 halamanPerhitungan Konversi Reaktor Xanthasiiva nur ilmaBelum ada peringkat
- Proposal Kerja Praktek Pusri Nia&wakhyuDokumen11 halamanProposal Kerja Praktek Pusri Nia&wakhyuandono kusuma jatiBelum ada peringkat
- Andono Kusuma Jati LPJ Sapra Oxygen-16 2021 BismillahDokumen7 halamanAndono Kusuma Jati LPJ Sapra Oxygen-16 2021 Bismillahandono kusuma jatiBelum ada peringkat
- Surat TugasDokumen1 halamanSurat Tugasandono kusuma jatiBelum ada peringkat
- Revisi Kelompok 7Dokumen4 halamanRevisi Kelompok 7andono kusuma jatiBelum ada peringkat
- Anderson Van Daud S - 21030118130151 - UTS Pinch Kelas BDokumen6 halamanAnderson Van Daud S - 21030118130151 - UTS Pinch Kelas Bandono kusuma jatiBelum ada peringkat
- Revisi Kelompok 6Dokumen5 halamanRevisi Kelompok 6andono kusuma jatiBelum ada peringkat
- Revisi Kelompok 5Dokumen4 halamanRevisi Kelompok 5andono kusuma jatiBelum ada peringkat
- Revisi Kelompok 1Dokumen5 halamanRevisi Kelompok 1andono kusuma jatiBelum ada peringkat
- Revisi Kelompok 3Dokumen4 halamanRevisi Kelompok 3andono kusuma jatiBelum ada peringkat
- Laporan Praktik Kerja Departemen Operasi Pusri - Ib PT Pupuk Sriwidjaja Palembang - Sumatera SelatanDokumen108 halamanLaporan Praktik Kerja Departemen Operasi Pusri - Ib PT Pupuk Sriwidjaja Palembang - Sumatera Selatanandono kusuma jatiBelum ada peringkat
- Revisi Kelompok 4Dokumen5 halamanRevisi Kelompok 4andono kusuma jatiBelum ada peringkat
- 4.2 HDP DonoDokumen5 halaman4.2 HDP Donoandono kusuma jatiBelum ada peringkat
- Tugas Individu DryingDokumen5 halamanTugas Individu Dryingandono kusuma jatiBelum ada peringkat
- TUGAS MAKALAH IsopropanolDokumen11 halamanTUGAS MAKALAH Isopropanolandono kusuma jatiBelum ada peringkat
- 2 Basic Programming - SBSDokumen13 halaman2 Basic Programming - SBSandono kusuma jatiBelum ada peringkat
- 1-Materi Teori KOMPRESOR Dan Sistem Udara Tekan Selasa 20-10-2020 - 13.b5Dokumen18 halaman1-Materi Teori KOMPRESOR Dan Sistem Udara Tekan Selasa 20-10-2020 - 13.b5andono kusuma jatiBelum ada peringkat
- Tugas Kespros Nigeria Bagian DonoDokumen9 halamanTugas Kespros Nigeria Bagian Donoandono kusuma jatiBelum ada peringkat
- Rencana Kerja Magang - Chiesa Salsabila - Universitas Diponegoro - Chiesa SalsabilaDokumen1 halamanRencana Kerja Magang - Chiesa Salsabila - Universitas Diponegoro - Chiesa Salsabilaandono kusuma jatiBelum ada peringkat
- Tali-Temali Untuk PemulaDokumen24 halamanTali-Temali Untuk Pemulaandono kusuma jatiBelum ada peringkat
- Pengumuman Insentif PKM AI Dan GT Tahun 2021Dokumen55 halamanPengumuman Insentif PKM AI Dan GT Tahun 2021andono kusuma jatiBelum ada peringkat
- Tugas Kelompok P3k Andono Kusuma JatiDokumen14 halamanTugas Kelompok P3k Andono Kusuma Jatiandono kusuma jatiBelum ada peringkat
- Pembagian Kelompok KimfisDokumen2 halamanPembagian Kelompok Kimfisandono kusuma jatiBelum ada peringkat
- Andono Kusuma Jati - 21030118110001 - UTS PinchDokumen8 halamanAndono Kusuma Jati - 21030118110001 - UTS Pinchandono kusuma jatiBelum ada peringkat
- Selvi Khairunisah Ashar - BAB IDokumen18 halamanSelvi Khairunisah Ashar - BAB Iandono kusuma jatiBelum ada peringkat
- Tugas 1 Utilitas - Andono Kusuma Jati - 21030118110001Dokumen10 halamanTugas 1 Utilitas - Andono Kusuma Jati - 21030118110001andono kusuma jatiBelum ada peringkat
- Laboratorium Komputasi Proses Jurusan Teknik Kimia Fakultas Teknik Universitas Diponegoro 2019Dokumen2 halamanLaboratorium Komputasi Proses Jurusan Teknik Kimia Fakultas Teknik Universitas Diponegoro 2019andono kusuma jatiBelum ada peringkat
- Laboratorium Komputasi Proses Departemen Teknik Kimia Fakultas Teknik Universitas DiponegoroDokumen1 halamanLaboratorium Komputasi Proses Departemen Teknik Kimia Fakultas Teknik Universitas Diponegoroandono kusuma jatiBelum ada peringkat