6 Termokimia
Diunggah oleh
Ahmad NurjamanJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
6 Termokimia
Diunggah oleh
Ahmad NurjamanHak Cipta:
Format Tersedia
Laboratorium Kimia Terapan UP MKU
Politeknik Negeri Bandung
MODUL 6
TERMOKIMIA
I.
TUJUAN
Setelah melakukan praktikum ini diharapkan mahasiswa dapat:
1.
Mempelajari setiap reaksi kimia disertai dengan perubahan energi,
2.
Menghitung perubahan kalor beberapa reaksi dengan percobaan yang sederhana.
II.
DASAR TEORI
Termokimia atau energetika kimia adalah ilmu yang mempelajari perubahan kalor dalam reaksi
kimia. Hukum yang mendasari ini adalah Hukum Termodinamika 1,
U = q w
dimana:
U = perubahan energi dalam
q = kalor
w = kerja
Dalam percobaan ini perubahan kalor yang diamati dilakukan pada tekanan konstan dan sistem
yang diamati menyangkut cair-padat sehingga perubahan volume dapat diabaikan. Akibatnya
kerja yang bersangkutan dengan sistem dapat pula diabaikan (PV 0). Oleh karena itu
perubahan entalpi (H) sama dengan perubahan energi dalam (U).
Jumlah kalor yang terlibat dalam reaksi dapat ditentukan dengan menggunakan kalorimeter.
Besaran fisika yang diamati adalah temperatur. Kalorimeter dibuat sedemikian rupa sehingga
menyerupai termos ideal dimana tidak terjadi perpindahan kalor dari dan ke sistem. Tapi, perlu
diperhatikan bahwa tetap terjadi perpindahan kalor dari kalorimeter ke isinya (campuran reaksi
yang akan ditentukan kalor reaksinya) atau sebaliknya.
Oleh karena itu kalorimeter harus ditera, yakni dengan menentukan kalor yang diserap oleh
kalorimeter. Jumlah kalor yang diserap oleh kalorimeter untuk menaikkan temperatur sebesar 1
derajat disebut tetapan kalorimeter.
26
Laboratorium Kimia Terapan UP MKU
Politeknik Negeri Bandung
III.
ALAT DAN BAHAN
Bahan:
Zn bubuk
CuSO4 0.5 M
HCl 2 M
NaOH 2 M
Etanol
Alat:
Kalorimeter
Termometer
Buret
Stopwatch
Gelas Kimia
Hotplate/pemanas
KESELAMATAN KERJA
IV.
5.1
Gunakan jas lab lengan panjang pada saat praktikum.
Hindari kontak larutan NaOH, HCl, Etanol dan CuSO4 dengan kulit.
Simpanlah campuran reaksi kedalam tempat yang disediakan.
CARA KERJA DAN CARA PERHITUNGAN
Menentukan tetapan kalorimeter
1.
Masukkan 20 ml air kedalam kalorimeter dengan menggunakan buret serta
catat temperatur (T1).
2.
Panaskan 20 ml air hingga temperaturnya 10 derajat diatas temperatur pada
no.1. Catat temperatur (T2).
3.
Campurkan air panas kedalam kalorimeter, aduk dan amati temperaturnya
setiap menit selama 10 menit.
4.
Buatlah kurva temperatur vs waktu untuk menentukan temperatur
pencampuran/akhir (Ta).
Perhitungan:
t
= T2 - Ta
T
= Ta T1
Kalor yang diserap air dingin = massa air dingin x kalor jenis x T = Q1
Kalor yang diberikan air panas = massa air panas x kalor jenis x t = Q2
Kalor yang diterima kalorimeter = Q2 Q1 = Q3
Tetapan kalorimeter = Q3/ T
Massa jenis air = 1 gr.cm-3 dianggap konstan
Kalor jenis air = 4.2 j g-1K-1
5.2 Penentuan kalor reaksi Zn(s) CuSO4(aq)
1.
Masukkan 40 ml CuSO4 0.5 M kedalam kalorimeter, catat temperaturnya
setiap menit selama 2 menit (T awal).
2.
Timbang dengan teliti bubuk Zn sebanyak 1.5 gram.
3.
Masukkan bubuk Zn kedalam kalorimeter dan catat perubahan temperatur
setiap 1 menit selama 10 menit.
4.
Buat grafik terhadap waktu dan tentukan kenaikan temperatur (T akhir).
27
Laboratorium Kimia Terapan UP MKU
Politeknik Negeri Bandung
Perhitungan:
T = T akhir T awal
Kalor yang diserap kalorimeter = k x T
Kalor yang diserap larutan = massa larutan x kalor jenis larutan x T
Kalor reaksi = Kalor yang dierap kalorimeter + Kalor yang diserap larutan
H reaksi = kalor reaksi/mol pereaksi
Massa jenis larutan ZnSO4 = 1.14 gr.cm-3
Kalor jenis/kapasitas kalor larutan ZnSO4 = 3.52 j g-1K-1
5.3
Penentuan kalor pelarutan Etanol-Air
1. Masukkan 18 ml air kedalam kalorimeter dengan buret. Catat temperatur setiap
menit selama 2 menit.
2. Ukur temperatur etanol setiap menit selama 2 menit dalam buret kedua, masukkan
etanol ini kedalam kalorimeter sebanyak 29 ml tepat. Kocok campuran dan catat
temperatur setiap menit selama 4 menit.
3. Ulangi percobaan dengan perbandingan volume air-etanol sesuai dengan tabel dibawah
ini.
tabel perbandingan volume air dan etanol
No.
1
2
3
4
5
6
Volume (mL)
Air
Etanol
18
29
27
19.3
36
14.5
36
11.6
26
5.8
45
4.8
Perhitungan:
Massa jenis etanol = 0.793 gr/cm3 maka volume molar =........?
Massa jenis air = 1 gr.cm-3
Volume molar air = ......
Kalor jenis etanol = 1.92 j g-1K-1
Kalor yang diserap air = m(air) x c(air) x Ta
Kalor yang diserap etanol = m (etanol) x c(etanol) x Tm
Kalor yang diserap kalorimeter = k x T
Mol Etanol = m(etanol)/46
Mol Air = m(air)/18
T = Ta
Hitunglah H pencampuran etanol-air untuk berbagai perbandingan volume diatas
Q = kalor pelarutan
= kalor yang diserap air + kalor yang diserap etanol + kalor yang diserap kalorimeter
28
Laboratorium Kimia Terapan UP MKU
Politeknik Negeri Bandung
H Pelarutan = Vol .Ethanol
Q
Vol .MolarEthanol
Q
mole tan ol
Isikanlah hasil perhitungan anda kedalam tabel yang terlampir dibawah
ini.
5.4
Buatlah kurva H Pelarutan terhadap mol etanol/mol air.
Dari kurva tentukan H Pelarutan Etanol encer tak terhingga
Penentuan kalor penetralan NaOH-HCl
1.
Masukkan 20 ml HCl 2 M kedalam kalorimeter. Catat temperatur larutan.
2.
Ukur 20 ml NaOH 2 M, catat temperatur dan usahakan agar temperatur sama
dengan temperatur HCl.
3.
Campurkan NaOH tersebut dengan HCl, catat temperatur setiap menit
selama 5 menit.
4.
Buatlah kurva T vs waktu untuk menentukan perubahan temperatur (T).
Perhitungan:
Tentukan H penetralan
Kerapatan larutan = 1.03 gr.cm-3
Kalor jenis larutan = 3.96 j g-1 K-1
Massa larutan =....
Kalor yang diserap larutan = massa larutan x kalor jenis air x T
Kalor yang diserap kalorimeter = k x T
Kalor reaksi = Kalor yang diserap larutan + kalor yang diserap kalorimeter
H penetralan =
kalor reaksi
mol hasil reaksi
29
Laboratorium Kimia Terapan UP MKU
Politeknik Negeri Bandung
VI.
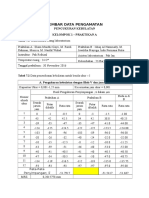
DATA PENGAMATAN
Penentuan tetapan kalorimeter
T1 = ......
T2 = ......
Data pengamatan temperatur air
Waktu/Menit
Temperatur (oC)
1
2
3
4
5
6
7
8
9
10
Penentuan kalor reaksi CuSO4-Zn(s)
Data pengamatan temperatur CuSO4
Waktu/Menit
Temperatur (oC)
0.5
1
1.5
2
Data pengamatan temperatur campuran reaksi
Waktu/Menit
Temperatur (oC)
1
2
3
4
5
6
7
8
9
10
30
Laboratorium Kimia Terapan UP MKU
Politeknik Negeri Bandung
Penentuan kalor pelarutan etanol-air
No.
4.4
Volume (mL)
Air
Etanol
Massa (gram)
Air
Etanol
Mol
Air
Etanol
Tm
Ta
Ta
H/mo
Penentuan kalor penetralan NaOH-HCl
Temperatur NaOH = Temperatur HCl = ...........
Data pengamatan temperatur campuran reaksi
Waktu/Menit
Temperatur (oC)
0.5
1
1.5
2
2.5
3
3.5
4
4.5
5
31
Mol
etanol/
Mol
etanol
Anda mungkin juga menyukai
- Fahrul Rahmadani - P-1.4 - 2Dokumen13 halamanFahrul Rahmadani - P-1.4 - 2M Rifqi AGBelum ada peringkat
- 6 TermokimiaDokumen6 halaman6 Termokimia10-Fathan Rivaldy-maleoBelum ada peringkat
- Laporan Praktikum Kimia Fisik Panas RreaDokumen22 halamanLaporan Praktikum Kimia Fisik Panas RreaSeptian Eka TruenoBelum ada peringkat
- Laporan - M6 - Novia Ramadhina - K6 - 1A TENDokumen17 halamanLaporan - M6 - Novia Ramadhina - K6 - 1A TENIneu NurhalimahBelum ada peringkat
- Jurnal KalorimeterDokumen4 halamanJurnal Kalorimeterrio budimanBelum ada peringkat
- Laporan Praktikum Ki1101 Kimia Dasar IaDokumen12 halamanLaporan Praktikum Ki1101 Kimia Dasar IaIndah Nurina Fitri Hapsari100% (1)
- Praktek Perc.3Dokumen10 halamanPraktek Perc.3have funBelum ada peringkat
- KALORIMETERDokumen12 halamanKALORIMETERrizkira08 rahmaatinBelum ada peringkat
- Diktat Praktikum TermokimiaDokumen6 halamanDiktat Praktikum TermokimiaIntan CahyaningrumBelum ada peringkat
- KalorimeterDokumen7 halamanKalorimeterUpi AlmasariBelum ada peringkat
- Termokimia B Rev PERCOBAAN II Sem 1 1920Dokumen5 halamanTermokimia B Rev PERCOBAAN II Sem 1 1920Salsa PutriBelum ada peringkat
- Termokimia Rev Percobaan III Sem 1 1920Dokumen5 halamanTermokimia Rev Percobaan III Sem 1 1920AufanNurilHaqBelum ada peringkat
- Laporan Praktikum Kimia Dasar P03 Termokimia Ade Siti Hapsah 1907111095Dokumen10 halamanLaporan Praktikum Kimia Dasar P03 Termokimia Ade Siti Hapsah 1907111095Ade Siti HapsahBelum ada peringkat
- Laporan Termokimia JadiDokumen25 halamanLaporan Termokimia JadiAzka MartaBelum ada peringkat
- Kalor PelarutanDokumen5 halamanKalor PelarutanEkaReverIIBelum ada peringkat
- Lap. Prk. Penentuan Panas PelarutanDokumen17 halamanLap. Prk. Penentuan Panas PelarutanAde Ayu Wulan Suci100% (2)
- Laporan Tetap Panas NetralisasiDokumen9 halamanLaporan Tetap Panas NetralisasiSiti RahmayantiBelum ada peringkat
- KF Objek 5 Kel 5Dokumen21 halamanKF Objek 5 Kel 5Riefkyansyah PutraBelum ada peringkat
- Penentuan Entalpi Reaksi Dan Energi DalamDokumen5 halamanPenentuan Entalpi Reaksi Dan Energi DalamBad boyBelum ada peringkat
- Penentuan Entalpi Reaksi Dan Energi DalamDokumen5 halamanPenentuan Entalpi Reaksi Dan Energi DalamBad boyBelum ada peringkat
- Penentuan KalorDokumen14 halamanPenentuan KalorVictorBelum ada peringkat
- LaporankimiaDokumen25 halamanLaporankimiaAhmad Faiz Nasshor100% (1)
- R1D121063 Sartika TermokimiaDokumen23 halamanR1D121063 Sartika TermokimiaAbdul RachimBelum ada peringkat
- Laporan Praktikum KIDokumen13 halamanLaporan Praktikum KI030 irfan nur an nafiBelum ada peringkat
- Materi PKF S1Dokumen21 halamanMateri PKF S1ahmadhelmiase7621Belum ada peringkat
- T02 - Laporan Praktek KalorimeterDokumen11 halamanT02 - Laporan Praktek KalorimeterainiiiBelum ada peringkat
- Laporan Tetap Panas NetralisasiDokumen14 halamanLaporan Tetap Panas NetralisasiRizky Herliana Niswita100% (1)
- Panas PelarutanDokumen24 halamanPanas PelarutanPutuFridaOktaningtiasWidiarthiBelum ada peringkat
- Laporan Hasil Praktikum TermokimiaDokumen16 halamanLaporan Hasil Praktikum TermokimiaDwi AnggorowatiBelum ada peringkat
- Lembar Kerja Siswa KalorimetriDokumen3 halamanLembar Kerja Siswa KalorimetrikhairinaBelum ada peringkat
- Laporan Praktikum Termokimia Kelompok 6Dokumen7 halamanLaporan Praktikum Termokimia Kelompok 603Anak Agung Ayu Sandya PratiwiBelum ada peringkat
- ADokumen7 halamanAMuhamad ArdiansyahBelum ada peringkat
- Modul 4 Praktikum Kimia Dasar 2022Dokumen6 halamanModul 4 Praktikum Kimia Dasar 2022Syihan AufarBelum ada peringkat
- TERMOKIMIADokumen14 halamanTERMOKIMIADyan SeptyaningsihBelum ada peringkat
- Acara I Tetapan Kalorimeter Dan Kalor PenetralanDokumen10 halamanAcara I Tetapan Kalorimeter Dan Kalor PenetralanRizki Amalia PBelum ada peringkat
- Hukum HessDokumen12 halamanHukum HessMurni_arifahBelum ada peringkat
- Nadira Aby Xavier - P-1.3 - 2Dokumen15 halamanNadira Aby Xavier - P-1.3 - 2Nadira Aby XavierBelum ada peringkat
- Menentukan Perubahan Entalpi Dengan KalorimeterDokumen9 halamanMenentukan Perubahan Entalpi Dengan KalorimeterApriliaRizky86% (7)
- Laporan Praktikum KalorimeterDokumen6 halamanLaporan Praktikum KalorimeterYumaaBelum ada peringkat
- Laporan Kimia Kalor ReaksiDokumen12 halamanLaporan Kimia Kalor Reaksimariapardede66Belum ada peringkat
- Modul Praktikum Kimia FisikDokumen49 halamanModul Praktikum Kimia FisikMuhammad FajrinBelum ada peringkat
- Laporan Praktikum Perubahan EntalpiDokumen8 halamanLaporan Praktikum Perubahan Entalpitrias_doraemonBelum ada peringkat
- Panas NetralisasiDokumen16 halamanPanas NetralisasiDwiayuAdindaBelum ada peringkat
- Praktikum Menghitung Kalor ReaksiDokumen4 halamanPraktikum Menghitung Kalor ReaksiJawad Shahab100% (1)
- Kelompok 5 Kimia EntalpiDokumen16 halamanKelompok 5 Kimia EntalpiJhonPariamanSaragihBelum ada peringkat
- Percobaan 5Dokumen4 halamanPercobaan 5021 064 Nur AlindaBelum ada peringkat
- Laporan Praktikum Kimia Kalori Meter SederhanaDokumen5 halamanLaporan Praktikum Kimia Kalori Meter SederhanaBurhanus Shidqy100% (1)
- Laporan Panas ReaksiDokumen14 halamanLaporan Panas ReaksiWynne RaphaelaBelum ada peringkat
- Laporan Praktikum 6 KimiaDokumen17 halamanLaporan Praktikum 6 KimiaKevin KomedienBelum ada peringkat
- LKS Kalorimeter KlasikDokumen5 halamanLKS Kalorimeter KlasikRizaBelum ada peringkat
- PENENTUAN PERUBAHAN ENTALPI DAN ENERGI DALAM - Docx GILANG 3 BARUDokumen5 halamanPENENTUAN PERUBAHAN ENTALPI DAN ENERGI DALAM - Docx GILANG 3 BARUBad boyBelum ada peringkat
- Praktikum TermokimiaDokumen8 halamanPraktikum TermokimiaJason DTBelum ada peringkat
- Percobaan 2 Termokimia FixDokumen17 halamanPercobaan 2 Termokimia FixSisilia JannatiBelum ada peringkat
- LAPORAN KIMIA - Termokimia Uji ReaksiDokumen7 halamanLAPORAN KIMIA - Termokimia Uji ReaksiishfakpsBelum ada peringkat
- LKS PraktikumDokumen8 halamanLKS PraktikumKostantina AninamBelum ada peringkat
- Rangkaian Alarm V12 Motor Vega ZRDokumen1 halamanRangkaian Alarm V12 Motor Vega ZRAhmad NurjamanBelum ada peringkat
- KINDIMDokumen5 halamanKINDIMAhmad NurjamanBelum ada peringkat
- Materi Mesin PressDokumen23 halamanMateri Mesin PressSurya SaputraBelum ada peringkat
- Makalah Kebakaran HutanDokumen63 halamanMakalah Kebakaran HutanAhmad NurjamanBelum ada peringkat
- KINDIMDokumen5 halamanKINDIMAhmad NurjamanBelum ada peringkat
- K3 Bahaya Pengelasan Dan Pengendaliannya PDFDokumen76 halamanK3 Bahaya Pengelasan Dan Pengendaliannya PDFAhmad NurjamanBelum ada peringkat
- Unsur KetahananDokumen16 halamanUnsur KetahananAhmad NurjamanBelum ada peringkat
- BAB II Tinjauan PustakaDokumen19 halamanBAB II Tinjauan PustakaBarri KarizkiBelum ada peringkat
- Laporan Praktikum Uji TarikDokumen20 halamanLaporan Praktikum Uji TarikAhmad NurjamanBelum ada peringkat
- Kelompok 1.1Dokumen9 halamanKelompok 1.1Ahmad NurjamanBelum ada peringkat
- Laporan Uji Keras FixDokumen12 halamanLaporan Uji Keras FixAhmad NurjamanBelum ada peringkat
- DapusDokumen1 halamanDapusAhmad NurjamanBelum ada peringkat
- 017 - Surat Penawaran Kerjasama (PT BAT)Dokumen3 halaman017 - Surat Penawaran Kerjasama (PT BAT)Ahmad NurjamanBelum ada peringkat
- Laporan KebulatanDokumen25 halamanLaporan KebulatanAhmad NurjamanBelum ada peringkat
- Uji TarikDokumen32 halamanUji TarikAhmad NurjamanBelum ada peringkat
- NoktahDokumen1 halamanNoktahAhmad NurjamanBelum ada peringkat
- Gambar ProyeksiDokumen4 halamanGambar ProyeksiAhmad NurjamanBelum ada peringkat
- Hayam Kongkorongok SubuhDokumen1 halamanHayam Kongkorongok SubuhDenis RamdaniBelum ada peringkat
- LT Soal MTK Un SMPDokumen0 halamanLT Soal MTK Un SMPwsriyunitaBelum ada peringkat
- 9.quality Control PDFDokumen55 halaman9.quality Control PDFAhmad NurjamanBelum ada peringkat
- 8 Pelapisan - LogamDokumen3 halaman8 Pelapisan - LogamAhmad NurjamanBelum ada peringkat
- LT Soal MTK Un SMPDokumen0 halamanLT Soal MTK Un SMPwsriyunitaBelum ada peringkat