Pembuatan Amonia
Diunggah oleh
Siti AliyasihJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Pembuatan Amonia
Diunggah oleh
Siti AliyasihHak Cipta:
Format Tersedia
1
xa.yimg.com/kq/groups/3004572/1821750935/name/BAB+I,II.doc
09.46
BAB I
PENDAHULUAN
1.1 Latar Belakang Pendirian Pabrik
Seiring dengan perkembangan teknologi, kebutuhan akan bahan-bahan kimia
semakin besar sehingga pembangunan industri kimia perlu lebih diprioritaskan. Industri
kimia merupakan salah satu industri vital dan strategis, untuk itu hampir setiap negara
di dunia, tak terkecuali Indonesia banyak memberikan perhatian pada pengembangan
industri kimia, mengingat industri ini banyak mempunyai keterkaitan dengan
pengembangan industri lainnya.
Salah satu bahan kimia yang banyak digunakan adalah amonia. Bahan kimia ini
dapat diproduksi dari gas sintesis sebagai bahan intermediet dalam industri kimia.
Secara langsung amonia digunakan sebagai bahan baku pembuatan pupuk (urea,
ammonium nitrate, ammonium sulphate) dan bahan baku pada proses pembuatan nitric
acid dan lain sebagainya.
Proyeksi kebutuhan ammonia dalam negeri semakin meningkat seiring dengan
peningkatan industri-industri yang menggunakannya. Oleh karena itu, maka pendirian
pabrik ammonia akan membawa dampak positif, hal ini disebabkan karena untuk
memenuhi kebutuhan dalam negeri disamping itu juga dapat mensuplai kebutuhan pasar
ekspor di berbagai negara.
1.2 Prospek dan Pemasaran
Prospek dari Produksi amonia sangat bagus, hal ini bisa dilihat dari
penggunaannya yang banyak diberbagai kebutuhan dan ditambah lagi besarnya peluang
eksport ke berbagai negara. Hal ini bisa diamati pada tabel 1.1.
Tabel 1.1. Data Proyeksi Kebutuhan Amonia di Pasar Dalam Negeri
Tahun
2009
2010
2011
2012
2013
Jumlah (Ton)
3.980.746
4.219.591
4.979.118
5.506.904
5.892.387
Sumber : Diolah oleh indochemical
Dari Tabel 1.1 terlihat bahwa kebutuhan amonia di dalam negeri cenderung
mengalami peningkatan rata-rata 10.40 % per tahun. Hal ini disebabkan oleh sudah
berdirinya beberapa pabrik pupuk di Indonesia serta untuk meningkatkan permintaan
pasar luar negeri.
Dengan luasnya cakupan penggunaan amonia di Indonesia, baik secara industri
maupun secara langsung menunjukkan bahwa permintaan akan amonia cukup besar
dengan kata lain prospek pemasarannya sangat menjanjikan.
Nilai Gross Profit Margin (GPM) yang didapat untuk pembuatan amonia adalah
sebesar Rp.10.100/Kg NH3 (Data Perhitungan di Lampiran A). Nilai GPM
ini
diperkirakan cukup menarik perhatian investor untuk mendirikan pabrik amonia, karena
nilai tambah produk lima kali lipat dari harga bahan baku.
1.3 Pemilihan Lokasi
Bontang memiliki letak geografis yang strategis yaitu 120 km dari Kota
Samarinda dan bagian utara berbatasan dengan selat makasar . Disamping juga telah
memiliki fasilitas jalan yang memadai, dengan demikian transportasi darat dari sumber
bahan baku, dan pasar tidak lagi menjadi masalah. Untuk sarana transportasi juga telah
memiliki pelabuhan PT.Badak NGL, PT.PKT dan PT. Indominco Mandiri serta
pelabuhan Tanjung Laut yang sedang dibangun sehingga pengiriman barang antar pulau
maupun untuk ekspor lebih lancar. Peta lokasi pendirian pabrik dapat dilihat pada
lampiran C.
1.4 Kapasitas Produksi
Kapasitas produksi dari pabrik akan mempengaruhi perhitungan teknis maupun
ekonomis dalam perancangan pabrik. Pada dasarnya, semakin besar kapasitas produksi,
maka kemungkinan keuntungan juga semakin besar. Pabrik amonia ini direncanakan
memiliki kapasitas produksi sebesar 50.000 ton/tahun. Kapasitas itu dipilih berdasarkan
perkiraan kebutuhan amonia di Indonesia tahun 2013 sekitar 5.892.387 ton/tahun.
Dengan asumsi tidak adanya penambahan pabrik amonia baru sehingga kapasitas
produksi amonia konstan. Maka kekurangan produksi amonia sekitar 290.000 ton/tahun.
Pabrik ini direncanakan memenuhi 17% kekurangan kebutuhan amonia (Data
Perhitungan di Lampiran B.
BAB II
DESKRIPSI PROSES
2.1 Teknologi Proses
Proses pembuatan amonia dari gas alam dan gas sintesis dapat dilakukan dengan
4 proses antara lain :
a. Proses Haber-Bosh
Proses pembuatan amonia dari nitrogen dan hidrogen pertama kali ditemukan oleh Fritz
Haber tahun 1908, seorang ahli kimia dari Jerman. Untuk skala industri pembuatan
ammonia ditemukan oleh Carl Bosch, seorang ahli kimia juga dari Jerman. Persamaan
reaksi sintesis amonia sebagai berikut:
N2 (g) + 3H2 (g) 2NH3 (g) H= 46.1 KJ/mol
Berdasarkan prinsip kesetimbangan maka konstanta kesetimbangan reaksi tidak
hanya tergantung pada temperatur dan tekanan tetapi juga dipengaruhi oleh
perbandingan komposisi nitrogen dan hidrogen. Kondisi yang menguntungkan untuk
pembentukan amonia adalah reaksi ke kanan pada suhu rendah dan tekanan tinggi.
Namun reaksi tersebut berlangsung sangat lambat pada suhu rendah, bahkan pada suhu
500 oC sekalipun. Di pihak lain karena reaksi ke kanan eksoterm maka penambahan
suhu akan mengurangi rendemen. Proses Haber-Bosh pertama dilangsungkan pada suhu
500 oC dan tekanan 150 350 atm menggunakan katalis serbuk besi yang dicampur
dengan Al2O3, MgO, CaO dan K2O.
b. Proses Kellog
Proses ini merupakan proses sintesa amonia menggunkan bahan baku dari gas
alam dengan reaksi utama antara gas hidrogen dan nitrogen menjadi amonia yang
berlangsung pada seksi ammonia converter. Kondisi optimal yang digunakan pada
proses ini adalah menjaga reaksi pada tekanan 140 150 kg/cm2 dan temperatur 360
500 oC. Ammonia converter yang digunakan terdiri dari dua jenis, yaitu Kellog
horizontal ammonia converter dan Kellog vertical quench converter.
Gas sintesis murni yang didapat dari proses ini terdiri dari campuran H 2 (74.2%),
N2 (24.7%), CH4 (0.8%) dan Ar (0.3%). Semua komposisi gas tersebut kemudian
dipisahkan dengan treatment tertentu sehingga gas sintesis yang dihasilkan hanya
mengandung komponen H2 dan N2. Selanjutnya, proses inti terbentuknya amonia terjadi
di dalam ammonia converter yang mereaksikan gas nitrogen dan hidrogen
menghasilkan amonia.
c. Proces Lurgi
Pada proses Lurgi reaksinya berlangsung dalam reactor fixed bed dengan
menggunakan oksigen dan steam pada kisaran tekanan 2000 3000 kPa (20 30 atm).
Oksigen dan steam dimasukkan kedalam gasifier melalui celah ke dalam rotary grate.
Temperatur gasifikasi sekitar 560 620 oC dan tergantung dari karakteristik umpan.
Kandungan metan dan karbondioksida masing-masing 10% dan 28% dalam gasifier.
Crude gas dari Lurgi gasifier yang diproses dalam beberapa langkah yaitu pengolahan
limbah panas, shift conversion, penghilangan tar, phenol dan produk lain. Nitrogen cair
melalui proses scrubbing akan menghasilkan gas sintesis yang murni dilanjutkan proses
kompresi dan terakhir proses pembuatan amonia.
d. Proses Koppers Totzek
Proses ini berawal dari gasification steam generation washing pada fase cair
dengan tekanan yang rendah dan suhu yang tinggi. Campuran homogen dari batubara,
oksigen dan steam memiliki suhu 1925oC. Steam dan karbon bereaksi endotermik
sehingga terjadi penurunan suhu hingga 1480oC. Gas sintesis yang dihasilkan memiliki
sulfur, CO dan CO2 yang bersifat racun bagi katalis, sehingga perlu dilakukan proses
penghilangan sulfur, CO dan CO2. Gas sintesis yang telah murni kemudian diumpankan
dalam ammonia converter dengan katalis Fe2O3 yang sangat reaktif pada suhu 300 oC
500oC. Konversi amonia overall yang dihasilkan proses ini adalah 88,8%. (Kirk Othmer,
1998)
Untuk dapat mengetahui proses yang akan dipilih dalam memproduksi amonia
maka dapat dilihat kondisi operasi pada masing-masing proses seperti pada tabel 2.1.
Berdasarkan tabel 2.1 maka Proses yang dipilih adalah Kellogg Process (USA) karena
konversi sangat tinggi pada tekanan dan suhu rendah dapat menghasilkan amonia yang
lebih banyak, hal lain juga didukung oleh aktivitas katalis Ruthenium 20 kali lebih
besar dibandingkan katalis besi (Fe , Al2O3, Fe2O3).
Tabel 2.1 Perbandingan Data kondisi Proses Pembuatan Amonia
Proses
Haber Bosch
Kellogg
Lurgi
Koppers
Suhu
Tekanan
Konversi
Energi(GJ/t NH3)
500 C
150-350 atm
20-25%
80 90
365 C
14-15 atm
99,82%
27,1
560-620 C
20- 30 atm
61%
50 56
Totzek
1925 oC
123 atm
88,8%
44
2.2 Spesifikasi Bahan Baku dan Produk
Bahan baku yang digunakan untuk pembuatan amonia adalah gas sintesis yang
dapat diperoleh dari berbagai bahan baku seperti batu bara, petroleum coke, naphtha,
gas alam, dan fuel oil. Gas sintesis yang berasal dari gas alam dipilih sebagai bahan
baku karena mudah didapatkan, komponen pengotor yang dimilikinya lebih sedikit
dibanding sumber bahan baku lain. Hal ini akan memudahkan proses produksi sintesis
amonia. Komponen gas sintesis selengkapnya dapat dilihat pada Lampiran D.
Produk dihasilkan berupa amonia dengan spesifikasi kemurnian minimal 99,5%
dan H2O 0,5% (PT. Pupuk Sriwijaya, 2009). Produk amonia yang siap dipasarkan dalam
bentuk cair disimpan dalam tangki penyimpanan amonia.
2.3 Uraian Singkat Proses
Pemilihan alur sintesis amonia didasarkan pada komponen umpan terutama
komponen pengotor yang ada, konversi produk yang dihasilkan dengan bantuan katalis,
dan karakteristik katalis yang digunakan. Komponen umpan berpengaruh pada jumlah
unit pemurnian umpan yang diperlukan, berkaitan dengan karakteristik katalis yang
digunakan. Komponen pengotor ini tidak diharapkan dalam sintesis amonia karena
menjadi racun katalis yang akan menurunkan aktivitas katalis. Sedangkan konversi
reaksi menentukan perlu tidaknya aliran recycle untuk meningkatkan laju pembentukan
produk.
Umpan gas sintesis dikompresi sebelum memasuki proses selanjutnya. Kenaikan
tekanan tersebut bertujuan untuk menyesuaikan umpan dengan kondisi operasi sintesis
amonia. Pengotor yang terdapat dalam gas sintesis adalah CO, CO2, dan H2O. Sebelum
memasuki ammonia converter, pengotor CO2 dihilangkan pada CO2 purifier pada suhu
47oC 80oC dengan tekanan 3 - 4 atm. Kemudian H2O dan CO dikeringkan dengan
dryer. Blok diagram sintesis amonia, dapat dilihat pada Gambar 2.1.
NH3
Air
Syn gas
Air
Nitrogen
Separator
Mixer
Feed
Reformer
Purification
Treating
Compressor
NH3
Converter
CH4, H2
N2 CO, CO2
Steam Drum
Refrigerator
Uap Air
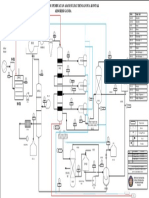
Gambar 2.1 Diagram Alir Pembuatan Amonia dari gas sintesis
Umpan gas sintesis yang telah murni dari pengotor dialirkan ke dalam synthesis gas
compressor. Kadar nitrogen yang rendah dari umpan akan ditambahkan melalui
nitrogen mixing, nitrogen didapat dari pemisahan udara. Dalam converter akan terjadi
reaksi sintesis amonia pada suhu 250oC 300oC dengan tekanan 3-5 MPa. Konversi
yang diharapkan dengan penggunaan katalis yang dipilih adalah 20% per pass pada titik
kesetimbangan. Keluaran converter amonia yang berupa campuran amonia dengan gas
sintesis yang belum terkonversi diumpankan ke dalam kondensor. Di dalam converter
amonia terjadi reaksi pembentukan amonia dengan reaksi:
3H2 + N2
katalis
2NH3
Dalam condensor, produk amonia akan dicairkan sehingga terpisah dari gas sintesis
yang belum terkonversi. Gas sintesis yang belum terkonversi diumpankan dalam gas
separator untuk memisahkan komponen gas yang ada. CH 4 dan Ar di alirkan ke fuel
gas. Sedangkan nitrogen dan hydrogen direcycle menuju synthesis gas compressor
untuk diumpankan kembali ke ammonia converter. Laju alir produk NH3 yang
dihasilkan adalah 6 ton/jam. (Data Perhitungan di Lampiran E).
2.4
Pemakaian Katalis
Katalis yang digunakan dalam reaksi pembuatan amonia ini adalah katalis
(Ruthenium, ZnO,CoMo, Nikel) dan absorbent (MDEA, Benfield).Katalis yang
digunakan berbasis Ruthenium (Ru) dengan support Magnesium Oksida (MgO) yang
diteliti oleh Muhler, dkk (2004). Katalis berbasis Ruthenium (Ru) dipilih karena mampu
mengkonversi hingga produk 20 % per pass pada suhu 250-300oC dan tekanan 3-5 MPa
(Larrichev, 2007). Sedangkan dengan katalis Fe, kondisi operasi pada suhu 380-520 oC
dan tekanan 120-220 bar (Forni dan Pernicone, 2006). Sehingga energi terpakai jauh
lebih hemat.
MgO dipilih sebagai support katalis karena lebih stabil dibandingkan support
karbon konvensional yang mudah terhidrogenasi (Muhler, 2004). Aktivitas Katalis Ru
5-20 kali lebih besar dari katalis besi (Appl, 1999, hal 62 dan Muhler, 2004). Katalis
dibuat dengan mengkontakkan Ru melalui impregnasi support dengan Ru3(CO)12 dalam
tetrahydtofurane, atau melalui chemical vapour deposition (CVD) Ru3(CO)12. Promotor
yang baik (alkali logam, alkali logam bumi, lantanida, dan kombinasinya) kemudian
ditambahkan. Katalis diaktivasi dengan perlakuan hidrogen. Recovery katalis dilakukan
dengan mencuci spent katalis untuk mendapatkan kembali promoter. Katalis sisa cucian
dipanaskan 70oC dalam pelarut asam nitrit 1 M berlebih. Support MgO berubah menjadi
larutan magnesium nitrat, dipisahkan dari sisa logam Ru dengan sentrifugasi atau
penyaringan.
2.5
Kinetika Reaksi
Konstanta kecepatan reaksi pembuatan amonia dapat dinyatakan dalam
Ea
k A. exp
RT
persamaan :
11727
k 3,64.10 8 exp
Pers. 2.1
Pers. 2.2
dalam hubungan ini :
k
: konstanta kecepatan reaksi
: pre exponential factor (1/jam)
Ea
: energi aktivasi (kkal/kmol)
: tetapan gas (kkal/kmol.K)
: suhu operasi (K)
Dari persamaan tersebut dapat diketahui bahwa semakin tinggi suhu, maka
kecepatan reaksi pembentukan amonia akan semakin besar. Akan tetapi, reaksi
pembentukan amonia merupakan reaksi yang bersifat sangat eksotermis sehingga akan
melepaskan panas yang sangat besar. Panas reaksi akan dilepaskan oleh permukaan
katalis dan menyebabkan suhu naik dengan cepat, sehingga efektifitas dan umur katalis
akan terus berkurang. Untuk itu, maka diperlukan adanya kontrol temperatur yang baik
melalui pendinginan. (Kirk Otmer, 1978).
Anda mungkin juga menyukai
- Uraian Proses AmmoniaDokumen16 halamanUraian Proses AmmoniaIlman Tafdhila100% (2)
- Pembuatan Amonia Dengan Proses Haldor TopsoeDokumen11 halamanPembuatan Amonia Dengan Proses Haldor TopsoeUtami Threeana LusiBelum ada peringkat
- KP Teknik Kimia Candal Dept. 3 A Evaluasi Triple Effect Evaporator UNDIPDokumen128 halamanKP Teknik Kimia Candal Dept. 3 A Evaluasi Triple Effect Evaporator UNDIPMuhammad Ridwan TanjungBelum ada peringkat
- Pupuk Urea - PPTDokumen25 halamanPupuk Urea - PPTArika prasejatiBelum ada peringkat
- Deskripsi Proses Pembuatan Pupuk Iskandar MudaDokumen41 halamanDeskripsi Proses Pembuatan Pupuk Iskandar Mudamela1214100% (1)
- Laporan Tugas Khusus KPDokumen39 halamanLaporan Tugas Khusus KPeniBelum ada peringkat
- Persentasi Proses AmoniakDokumen38 halamanPersentasi Proses Amoniakzakaria 22Belum ada peringkat
- Kp-PusriDokumen19 halamanKp-Pusriputra pratamaBelum ada peringkat
- OPTIMASI STRIPPERDokumen11 halamanOPTIMASI STRIPPERElisabeth Sonisora Wau0% (1)
- Perancangan Pabrik KimiaDokumen63 halamanPerancangan Pabrik KimiaDwi RamadhaniBelum ada peringkat
- Tugas Khusus RagagucciDokumen40 halamanTugas Khusus RagaguccilibbissujessyBelum ada peringkat
- DPHEDokumen33 halamanDPHESintya ningsihBelum ada peringkat
- Lampiran A Neraca Massa FIXDokumen11 halamanLampiran A Neraca Massa FIXAnonymous VJFlyRY0Belum ada peringkat
- Tugas KhususDokumen7 halamanTugas KhususthupackBelum ada peringkat
- Operasi Furnace Pada ADUDokumen28 halamanOperasi Furnace Pada ADUGerald RahanraBelum ada peringkat
- Pertanyaan Analisa Teknik Kimia Kelompok 3 (Desulfurizer)Dokumen5 halamanPertanyaan Analisa Teknik Kimia Kelompok 3 (Desulfurizer)Astri HandayaniBelum ada peringkat
- PEMULIHAN ANTIBIOTIK DENGAN ULTRAFILTRASIDokumen9 halamanPEMULIHAN ANTIBIOTIK DENGAN ULTRAFILTRASIFarah bahiraBelum ada peringkat
- (123doc - VN) Pra Rancangan Pabrik Pembuatan Fenol Dari Tandan Kosong Kelapa Sawit Dengan Proses Pirolisis Dengan Kapasitas 10 000 Ton TahunDokumen445 halaman(123doc - VN) Pra Rancangan Pabrik Pembuatan Fenol Dari Tandan Kosong Kelapa Sawit Dengan Proses Pirolisis Dengan Kapasitas 10 000 Ton TahundhikaBelum ada peringkat
- Shut Down Kompresor - Kel 2BDokumen14 halamanShut Down Kompresor - Kel 2BalvinaBelum ada peringkat
- Pembuatan Amonia Dengan Proses Haldor TopsoeDokumen11 halamanPembuatan Amonia Dengan Proses Haldor TopsoeJihaanmqrbnBelum ada peringkat
- Kelompok 5 3a S1 Industri Sintesa AmoniaDokumen29 halamanKelompok 5 3a S1 Industri Sintesa AmoniaLintang NorfitriaBelum ada peringkat
- 0e105f8ec5146f9737d0ea5f79ad4868(1)Dokumen258 halaman0e105f8ec5146f9737d0ea5f79ad4868(1)Bryant CoolBelum ada peringkat
- Sistem KendaliDokumen14 halamanSistem Kendalibagas fajar rosyidiBelum ada peringkat
- JajakskddasDokumen63 halamanJajakskddasAndyNugrohoBelum ada peringkat
- Reaktor Fixed Bed Multitube-2Dokumen27 halamanReaktor Fixed Bed Multitube-2Tissa Novida Aulia ZahraBelum ada peringkat
- Fluida Panas untuk Transfer PanasDokumen2 halamanFluida Panas untuk Transfer PanasBrian ObiedyanBelum ada peringkat
- Plate Dan Packed TowerDokumen40 halamanPlate Dan Packed TowerMaria MargarethaBelum ada peringkat
- Makalah Phonska Kelompok 3Dokumen20 halamanMakalah Phonska Kelompok 3Astria Nur AfifahBelum ada peringkat
- FORMALDEHIDADokumen10 halamanFORMALDEHIDAalmengarun0% (1)
- HE Water To Water Kelompok 5Dokumen27 halamanHE Water To Water Kelompok 5NDA17Belum ada peringkat
- BAB IV TK Condenser CarbamateDokumen25 halamanBAB IV TK Condenser Carbamatezulfanimelda9Belum ada peringkat
- Arthur P.tonggiro - L2C008017 - Tugas Khusus Furnace 011 F101 Bab I - Bab VDokumen55 halamanArthur P.tonggiro - L2C008017 - Tugas Khusus Furnace 011 F101 Bab I - Bab VJenifer Oktriana TonggiroBelum ada peringkat
- Saturated Vs Superheated Steam Jenuh UapDokumen3 halamanSaturated Vs Superheated Steam Jenuh UapDhiyaul Ihsanti0% (1)
- Laporan Total HardnessDokumen14 halamanLaporan Total HardnessvinaBelum ada peringkat
- Neraca Massa Pra Rancangan Pabrik Asam Sulfat Dari SulfurDokumen13 halamanNeraca Massa Pra Rancangan Pabrik Asam Sulfat Dari SulfurLuqman Sahlan RomadhonaBelum ada peringkat
- Laporan Praktikum Adsorpsi Air DryingDokumen15 halamanLaporan Praktikum Adsorpsi Air DryingMuh Aslam NurBelum ada peringkat
- Barometric CondenserDokumen7 halamanBarometric CondenserArifRochmanHartonoBelum ada peringkat
- Proses Pembakaran BelerangDokumen4 halamanProses Pembakaran BelerangLaras Rahma HidayatiBelum ada peringkat
- Makalah AminasiDokumen15 halamanMakalah AminasiDesi SupiyantiBelum ada peringkat
- Pra Rencana Pabrik Pulp Dari Batang Kapas Dengan Proses Kraft (Sulfat) KapasitasDokumen448 halamanPra Rencana Pabrik Pulp Dari Batang Kapas Dengan Proses Kraft (Sulfat) KapasitasCristiano Hamdiansyah SempadianBelum ada peringkat
- Resume Proses Pembuatan Asam NitratDokumen4 halamanResume Proses Pembuatan Asam NitratAbdul ApandiBelum ada peringkat
- Aerasi Dan DeaerasiDokumen21 halamanAerasi Dan DeaerasirookeyguyBelum ada peringkat
- EVAPORASI UREADokumen8 halamanEVAPORASI UREARizky Bagas PermanaBelum ada peringkat
- TUGAS 1 LATIHAN SOAL BRIAN VARIABEL PROSESDokumen2 halamanTUGAS 1 LATIHAN SOAL BRIAN VARIABEL PROSES0358Brian Dwi RiswantoTKBelum ada peringkat
- REBOILERDokumen39 halamanREBOILERAyik SevenfoldBelum ada peringkat
- Modul Komputasi Proses IndustriDokumen101 halamanModul Komputasi Proses Industrisusi100% (1)
- Asam Sulfat 15.10.19.16Dokumen1 halamanAsam Sulfat 15.10.19.16MegaBelum ada peringkat
- DAFTAR PERTANYAAN PendadaranDokumen4 halamanDAFTAR PERTANYAAN PendadaranRofi'ul HakimBelum ada peringkat
- JagungDokumen6 halamanJagungardhi_ashengBelum ada peringkat
- KELLOGG PROSESDokumen28 halamanKELLOGG PROSESEzra Ariella WibowoBelum ada peringkat
- Bab I, IiDokumen8 halamanBab I, IibtjajadiBelum ada peringkat
- Proposal Prarancangan PabrikDokumen16 halamanProposal Prarancangan PabrikRisali AddiniBelum ada peringkat
- Pra Rancangan Pabrik Ammonia Dengan Proses KellogDokumen17 halamanPra Rancangan Pabrik Ammonia Dengan Proses KellogRisali Addini100% (1)
- Pembuatan Ammonia dari TKKSDokumen8 halamanPembuatan Ammonia dari TKKSRonatio AritonangBelum ada peringkat
- Uraian Proses AmmoniaDokumen17 halamanUraian Proses AmmoniaPHabiant DaniesHaBelum ada peringkat
- Tugas Pik-1 4 Ardian Fauzi Nh3Dokumen7 halamanTugas Pik-1 4 Ardian Fauzi Nh3Ardian FauziBelum ada peringkat
- OPTIMIZED TITLE FOR AMMONIA AND UREA PLANT DESIGN DOCUMENTDokumen46 halamanOPTIMIZED TITLE FOR AMMONIA AND UREA PLANT DESIGN DOCUMENTNina AdrianaBelum ada peringkat
- Pengolahan Limbah Air RegenerasiDokumen100 halamanPengolahan Limbah Air RegenerasiSophia AuliasariBelum ada peringkat
- LimbahCairDokumen14 halamanLimbahCairSiti AliyasihBelum ada peringkat
- PLA SusuDokumen12 halamanPLA SusuFadli Maulana FikriBelum ada peringkat
- 1.06 SedimentasiDokumen6 halaman1.06 SedimentasiEster Yusmarina NababanBelum ada peringkat
- PP No 46 2013Dokumen9 halamanPP No 46 2013Nanik NurjayantiBelum ada peringkat
- Filsafat PancasilaDokumen38 halamanFilsafat PancasilaSiti AliyasihBelum ada peringkat
- Pengelolaan Limbah dan AirDokumen4 halamanPengelolaan Limbah dan AirSiti AliyasihBelum ada peringkat
- Makalah PLA Klapa SawitDokumen22 halamanMakalah PLA Klapa SawitFadli Maulana FikriBelum ada peringkat
- Sifat Fisik Dan Kimia Amoniak KellogDokumen2 halamanSifat Fisik Dan Kimia Amoniak KellogSiti AliyasihBelum ada peringkat
- LOGAM MULIADokumen2 halamanLOGAM MULIANita ApriliyaniBelum ada peringkat
- Modul Ion ExchangeDokumen14 halamanModul Ion ExchangezakauteamBelum ada peringkat
- Tugas K3 IndividuDokumen22 halamanTugas K3 IndividuSiti AliyasihBelum ada peringkat
- Keselamatan Dan Kesehatan Kerja k3 PadaDokumen24 halamanKeselamatan Dan Kesehatan Kerja k3 PadaSiti AliyasihBelum ada peringkat
- Democratic CitizenshipDokumen23 halamanDemocratic CitizenshipSiti AliyasihBelum ada peringkat
- Blangko Percobaan FluidisasiDokumen4 halamanBlangko Percobaan FluidisasiSiti AliyasihBelum ada peringkat
- OPTIMASI FLUIDISASIDokumen16 halamanOPTIMASI FLUIDISASIViant NurulitaBelum ada peringkat
- Sistem Pembersihan Pipa Fluidisasi UntukDokumen7 halamanSistem Pembersihan Pipa Fluidisasi UntukSiti AliyasihBelum ada peringkat
- K3 Dalam KimiaDokumen60 halamanK3 Dalam Kimiamfhakim845268Belum ada peringkat
- Silabus - K3 2014Dokumen1 halamanSilabus - K3 2014Siti AliyasihBelum ada peringkat
- Pertemuan 1 Pengenalan Dasar Sistem KontrolDokumen11 halamanPertemuan 1 Pengenalan Dasar Sistem KontrolZachary Pradana GoodbyenightmareBelum ada peringkat
- MESIN FRAISDokumen13 halamanMESIN FRAISAldy OtonxBelum ada peringkat
- Dasar - Dasar Mikrobiologi - Andriano Suryawan Utama, 3335131867Dokumen42 halamanDasar - Dasar Mikrobiologi - Andriano Suryawan Utama, 3335131867Siti AliyasihBelum ada peringkat
- Metode Runge KuttaDokumen4 halamanMetode Runge KuttaNurul 'Nunu' Fazriyah100% (4)
- Slide Pengantar Pengolahan Air Bersih ITBDokumen72 halamanSlide Pengantar Pengolahan Air Bersih ITBSiti AliyasihBelum ada peringkat
- Deret Taylor Dan Analisis GalatDokumen37 halamanDeret Taylor Dan Analisis GalatMashdar ChanBelum ada peringkat
- Pengolahan Limbah SawitDokumen15 halamanPengolahan Limbah SawitSiti AliyasihBelum ada peringkat
- Modul Teknik Pemesinan FraisDokumen101 halamanModul Teknik Pemesinan FraisSarjito100% (1)
- Makalah Paper TRKDokumen25 halamanMakalah Paper TRKSiti AliyasihBelum ada peringkat
- Teknik Reaksi KimiaDokumen19 halamanTeknik Reaksi KimiaSiti AliyasihBelum ada peringkat