4.3 HDR
Diunggah oleh
andono kusuma jatiHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
4.3 HDR
Diunggah oleh
andono kusuma jatiHak Cipta:
Format Tersedia
4.
3 Pengaruh Konsentrasi Na2SO3 terhadap Nilai Konstanta Transfer Massa Gas-Cair
600
580
560
Kla rata-rata (L/s)
540
KLa
520
500
480
0.024 0.025 0.026 0.027 0.028 0.029 0.03 0.031 0.032
Konsentrasi Na2SO3 (N)
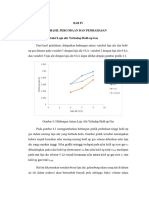
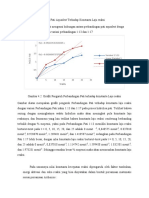
Gambar 4.3 Hubungan konsentrasi Na2SO3 dengan KLa
Pada gambar di atas dapat dilihat bahwa terjadi peningkatan KLa rata-rata di setiap
penambahan konsentrasi Na2SO3. Pada konsentrasi 0,025 N didapatkan KLa rata-rata sebesar
519.41. Pada konsentrasi 0,027 N didapatkan KLa rata-rata sebesar 570.243. Pada variabel
konsentrasi 0,031 N didapatkan KLa rata-rata sebesar 591.058Dari grafik diatas dapat
disimpulkan bahwa semakin tinggi nilai konsentrasi Na2SO3 maka semakinbesar KLa rata-
ratanya. Menurut Prisma (2012), semakin tinggi konsentrasi suatu larutan maka semakin tinggi
pula nilai viskositas suatu larutan tersebut (Arini dkk., 2019). Hubungan antara konsentrasi dan
viskositas ditunjukan oleh
persamaan berikut:
μ = ke0.26c
dimana, μ = viskositas (Pa.s)
c = konsentrasi (gr/dL)
(Greenfield, 1976 dalam Arini dkk., 2019)
Semakin bertambahnya nilai viskositas maka akan menurunkan luas permukaan
perpindahan massa gas-gas yang menyebabkan penurunan koefisien transfer massa. Penurunan
nilai koefisien perpindahan massa ini dikarenakan dengan semakin tingginya nilai viskositas
suatu larutan, maka mengindikasikan larutan tersebut semakin jenuh. Dengan semakin jenuhnya
suatu larutan, maka larutan tersebut akan sulit untuk ditembus oleh udara, karena daya yang
diperlukan untuk menembus cairan semakin besar sebagai akibat semakin kuat gaya gesek antara
lapisan gas dan cairannya. Sehinnga daya yang ada pada gas juga harus digunakan untuk
melawan gaya gesekantara lapisan gas dan cairannya. Hal ini mengakibatkan kecepatan
perpindahan massa menurun sehingga laju perpindahan oksigen akan semakin kecil. Hal ini
mengakibatkan koefisien perpindahan massa semakin berkurang juga (Haryani dan Widayat,
2011).
Pada percobaan, perhitungan KLa menggunakan metode sulfit yaitu dengan cara
mereaksikan natrium sulfit dengan oksigen yang ada dalam udara yang dinyatakan sebagai
berikut:
Na2SO3 + 1⁄2 O2→ Na2SO4 + Na2SO3(sisa)
Natrium sulfit bereaksi dengan oksigen dalam udara membentuk natrium sulfat. Karena
tidak semua natrium sulfit bereaksi dengan oksigen maka terdapat natrium sulfit sisa. Kemudian
natrium sulfit sisa dianalisa dengan titrasi iodometri yang dinyatakan sebagai berikut:
Na2SO3(sisa) + KI + KIO3→ Na2SO4 + 2KIO2 + I2
Natrium sulfit yang sisa direaksikan dengan KI yang berlebih membentuk natrium sulfat
dan iodida. Untuk mengetahui konsentrasi natrium sulfit sisa, maka konsentrasi iodida yang
terbentuk harus dianalisa terlebih dahulu. Iodida yang terbentuk dapat dianalisa dengan
mereaksikan iodida dengan natrium tiosulfat yang titik akhir titrasinya ditandai dengan
perubahan warna
kuning menjadi kuning hampir hilang. Reaksi antara natrium tiosulfat dengan iodida dinyatakan
sebagai berikut:
I2 + Na2S2O3 → Na2S4O6 + 2NaI
Hasil yang diperoleh pada percobaan menyimpang dari teori yang ada. Menurut teori,
semakin tinggi konsentrasi cairan maka nilai KLa semakin kecil, namun hasil menunjukan nilai
KLa yang semakin besar. Hal ini disebabkan digunakannya metode sulfit didasarkan pada
oksidasi sulfitmenjadi sulfat oleh oksigen. Persamaan reaksi oksidasinya sebagai berikut.
NA2SO3 + 1⁄2 O2 Na2SO4
(Bahrin dkk., 2015)
Dari persamaan reaksi diatas tersebut dapat dijelaskan reaksi yang berlangsung dalam
reaktor yaitu oksigen yang dialirkan akan bereaksi dengan sulfit yang terlarut dalam air sehingga
berubah menjadi sulfit. Dari hal tersebut oksigen yang mulanya pada fase gas bereaksi dengan
sulfit pada fase cair, sehingga menjadi sulfat pada fase cair. Oleh karena itu, oksigen mengalami
perpindahan fase gas-cair berbanding lurus pada konsentrasi sulfit yang terlarut karena nantinya
oksigen dalam fase gas menjadi fase cair dengan cara bereaksi dengan sulfit yang terlarut,
sehingga koefisien perpindahan massa volumetrik (KLa) terpengaruh didalamnya. Dikarenakan
nilai viskositas yang semakin tinggi, maka dari itu nilai Na2SO3 yang terlarut semakin tinggi ,
sedangkan variabel konsentrasi terendah nilai KLa terendah.
Kesimpulan dari percobaan ini adalah hasil yang didapatkan tidak sesuai dengan teori.
Seharusnya, semakin tinggi konsentrasinya menyebabkan meningkatnya viskositas sehingga
koefisien transfer massa semakin turun. Namun, tinggi juga hal ini dikarenakan penentuan KLa.
Hasil tidak sesuai teori karena peningkatan viskositasdan densitas sehingga larutan akan semakin
jenuh menyebabkan tumbukanantara partikel Na2SO3 dengan oksigen berjalan lebih lambat dan
laju perpindahan oksigen akan semakin kecil. Hal ini didukung oleh penelitian lain yang pernah
dilakukan yaitu tentang efek keadaan cairan terhadap perpindahan massa pada reaktor
bergelembung menunjukkan bahwa semakin tinggi viskositas suatu cairan maka akan
menurunkan luas permukaan perpindahan massa gas – cair yang menyebabkan penurunan
koefisien transfer massa (Mouza et al., 2005 dalam Widayat dkk., 2011). Semakin besar densitas,
maka perpindahan massa menjadi lebih kecil (Widayat dkk., 2011).
DAFTAR PUSTAKA
Haryani, Kristinah dan Widayat 2011. Pengaruh Viskositas dan laju alir terhadap
hidrodinamika dan perpindahan massa dalam proses produksi asam sitrat dengan
bioreactor.Universitas diponegoro.Semarang.
Bahrin, D., Susanto, H., & Subagjo. (2015). Penyusunan Kriteria PemilihanProses Flue
Gas Desulfurization. Prosiding Seminar Nasional Teknik Kimia “Kejuangan” Pengembangan
Teknologi Kimia untuk Pengolahan Sumber Daya Alam Indonesia, 4, 1–9. Christi, M. Y., 1989,
Air-lift Bioreactor,
Anda mungkin juga menyukai
- 4.1 Pengaruh Konsentrasi Naoh Terhadap Jumlah Mol Co2 Yang Terserap Pada Berbagai Waktu ReaksiDokumen13 halaman4.1 Pengaruh Konsentrasi Naoh Terhadap Jumlah Mol Co2 Yang Terserap Pada Berbagai Waktu ReaksiFudhail AbdurrahmanBelum ada peringkat
- Memahami Laju Konstanta PerpindahanDokumen19 halamanMemahami Laju Konstanta PerpindahanFebrian Glendi PraditaBelum ada peringkat
- P2 Bab 4Dokumen8 halamanP2 Bab 4Fahmi ZakariaBelum ada peringkat
- AerasiDokumen21 halamanAerasiRayhan Lutfi100% (1)
- Adoc - Pub - Bab II Tinjauan Pustaka Kesetimbangan Dalam LarutaDokumen21 halamanAdoc - Pub - Bab II Tinjauan Pustaka Kesetimbangan Dalam LarutaMuhammad Annajmi AlhadidBelum ada peringkat
- Laporan Kimia Fisik II (Repaired)Dokumen83 halamanLaporan Kimia Fisik II (Repaired)Lara AshtiraBelum ada peringkat
- 1982-Article Text-3530-1-10-20191230Dokumen6 halaman1982-Article Text-3530-1-10-20191230Desra wellyBelum ada peringkat
- Salt DiffusionDokumen24 halamanSalt Diffusionragilia maulidiaBelum ada peringkat
- AnorganikDokumen8 halamanAnorganikindahBelum ada peringkat
- Kelompok 5 - Kelarutan Dan Hasil Kali KelarutanDokumen7 halamanKelompok 5 - Kelarutan Dan Hasil Kali KelarutanMisBelum ada peringkat
- Hasil Dan Pembahasan. Jurnal TranslatedocxDokumen2 halamanHasil Dan Pembahasan. Jurnal Translatedocxtaritsu icuBelum ada peringkat
- Jurnal Absorbsi CO2 Dengan NaohDokumen6 halamanJurnal Absorbsi CO2 Dengan NaohAbdullah Ardhi FirmansyahBelum ada peringkat
- Jurnal Skripsi ULIVADokumen8 halamanJurnal Skripsi ULIVAUliva RahmawatiBelum ada peringkat
- Bab III Praktikum IIDokumen6 halamanBab III Praktikum IIJulhamEfendiBelum ada peringkat
- Penentuan Kadar Sulfat Menggunakan TurbiDokumen4 halamanPenentuan Kadar Sulfat Menggunakan TurbikartikaBelum ada peringkat
- Rudy SeniatiDokumen8 halamanRudy Seniatiaish zainalBelum ada peringkat
- Difusi IntegralDokumen15 halamanDifusi IntegralAvivPujaanBelum ada peringkat
- Bab Iv Hasil Percobaan Dan Pembahasan 4.1 Pengaruh Variabel Laju Alir Terhadap Hold-Up GasDokumen4 halamanBab Iv Hasil Percobaan Dan Pembahasan 4.1 Pengaruh Variabel Laju Alir Terhadap Hold-Up Gasahmad fauzanBelum ada peringkat
- BAB 4 Arus DensitasDokumen4 halamanBAB 4 Arus DensitasArij Al AsfariBelum ada peringkat
- Tugas BernadetaDokumen5 halamanTugas BernadetaDetha HunganBelum ada peringkat
- Review GeankoplisDokumen15 halamanReview GeankoplishafizBelum ada peringkat
- 147 321 1 SMDokumen10 halaman147 321 1 SMTihajarBelum ada peringkat
- Bab 2Dokumen4 halamanBab 2Niar'zz Cie AydiarzBelum ada peringkat
- MATERI KULIAH KIMDAS (Kelarutan) 2020 Pertemuan-9Dokumen41 halamanMATERI KULIAH KIMDAS (Kelarutan) 2020 Pertemuan-9Desy Natalia PurbaBelum ada peringkat
- ViskovitasDokumen13 halamanViskovitassiti meimunahBelum ada peringkat
- Penetapan Naac Dengan HCL Dengan Metode KonduktometriDokumen8 halamanPenetapan Naac Dengan HCL Dengan Metode KonduktometriRizky Cahya PutraBelum ada peringkat
- Jurnal Absorbsi - 1 Senin PDFDokumen5 halamanJurnal Absorbsi - 1 Senin PDFAnonymous a8990NEBelum ada peringkat
- Laporan Praktikum Kimia AnorganikDokumen11 halamanLaporan Praktikum Kimia AnorganikLiaRudyBelum ada peringkat
- Devis Saputra - 23030122120029 - P5Dokumen37 halamanDevis Saputra - 23030122120029 - P5Devis Saputra1Belum ada peringkat
- Rudy SeniatiDokumen8 halamanRudy SeniatiDesra wellyBelum ada peringkat
- Transfer GasDokumen18 halamanTransfer GasDITA PUTRI PURWANINGSIH Teknik LingkunganBelum ada peringkat
- Kelompok 7 - Kelas F - RevisiDokumen23 halamanKelompok 7 - Kelas F - RevisiArbainBelum ada peringkat
- Viskositas Terhadap Suhu Arya Wulandari 2311081030 PDFDokumen24 halamanViskositas Terhadap Suhu Arya Wulandari 2311081030 PDFFandhy Ino IciBelum ada peringkat
- Percobaan 6Dokumen7 halamanPercobaan 6eunhyoonBelum ada peringkat
- KimfisDokumen8 halamanKimfisnayaraelfarizaBelum ada peringkat
- Kecepatan ReaksiDokumen37 halamanKecepatan ReaksiRahmaBelum ada peringkat
- TK007Dokumen6 halamanTK007fmd16Belum ada peringkat
- Pengaruh Konsentrasi NaOH Terhadap Nilai K2Dokumen1 halamanPengaruh Konsentrasi NaOH Terhadap Nilai K2Intan Clarissa SophianaBelum ada peringkat
- PDTK 2 - Percobaan 4 - Kelompok VDokumen22 halamanPDTK 2 - Percobaan 4 - Kelompok VZaidan NaufalBelum ada peringkat
- Approach To Design Pharmaceutical Cocrystal-DikonversiDokumen6 halamanApproach To Design Pharmaceutical Cocrystal-Dikonversisutan kayoBelum ada peringkat
- Analisis Hasil PerhitunganDokumen4 halamanAnalisis Hasil PerhitunganKameliya Hani MillatiBelum ada peringkat
- Kinetika Reaksi Hidrogen Peroksida Dan Asam IodidaDokumen5 halamanKinetika Reaksi Hidrogen Peroksida Dan Asam IodidaRezaNoegrahaBelum ada peringkat
- Laju Reaksi Dan Kecepatan ReaksiDokumen10 halamanLaju Reaksi Dan Kecepatan ReaksiFirdaus Er DsBelum ada peringkat
- Materi KelarutanDokumen16 halamanMateri KelarutanHarisBelum ada peringkat
- Kelarutan Dan Koefisien Aktivitas Elektrilit KuatDokumen16 halamanKelarutan Dan Koefisien Aktivitas Elektrilit KuatVinna Durrotul AzizahBelum ada peringkat
- Xiv KonduktometrikDokumen57 halamanXiv KonduktometrikMOCHILBelum ada peringkat
- Laporan Praktikum GravimetriDokumen10 halamanLaporan Praktikum Gravimetrim.razkyfardanBelum ada peringkat
- Hardness Removal Kelompok 5Dokumen10 halamanHardness Removal Kelompok 5Anas AzmiBelum ada peringkat
- Laporan PFK 6 - Hardness Removal - NewDokumen10 halamanLaporan PFK 6 - Hardness Removal - NewRinBelum ada peringkat
- 1 PBDokumen10 halaman1 PBMiracle Faith Melody LBelum ada peringkat
- Jurnal TreDokumen9 halamanJurnal TreTrio MadridBelum ada peringkat
- Kelarutan Dan Hasil Kali Kelaruta1Dokumen8 halamanKelarutan Dan Hasil Kali Kelaruta1yusdinBelum ada peringkat
- Absorbsi PDFDokumen43 halamanAbsorbsi PDFAnnisa Dien Rachmawati0% (1)
- Worksheet TITRASI Iodometri 2021 - Fannisa Hafidhia Suryana - 2007769 - Kimia-C 2020Dokumen12 halamanWorksheet TITRASI Iodometri 2021 - Fannisa Hafidhia Suryana - 2007769 - Kimia-C 2020Fannisa SuryanaBelum ada peringkat
- ABSTRAK SedimentasiDokumen1 halamanABSTRAK SedimentasiNurRiskawatiBelum ada peringkat
- Laporan Telur Sarah Revisi 2Dokumen19 halamanLaporan Telur Sarah Revisi 2SarahBelum ada peringkat
- Revisi Kelompok 3Dokumen4 halamanRevisi Kelompok 3andono kusuma jatiBelum ada peringkat
- Surat TugasDokumen1 halamanSurat Tugasandono kusuma jatiBelum ada peringkat
- Proposal Kerja Praktek Pusri Nia&wakhyuDokumen11 halamanProposal Kerja Praktek Pusri Nia&wakhyuandono kusuma jatiBelum ada peringkat
- Revisi Kelompok 5Dokumen4 halamanRevisi Kelompok 5andono kusuma jatiBelum ada peringkat
- Anderson Van Daud S - 21030118130151 - UTS Pinch Kelas BDokumen6 halamanAnderson Van Daud S - 21030118130151 - UTS Pinch Kelas Bandono kusuma jatiBelum ada peringkat
- Andono Kusuma Jati LPJ Sapra Oxygen-16 2021 BismillahDokumen7 halamanAndono Kusuma Jati LPJ Sapra Oxygen-16 2021 Bismillahandono kusuma jatiBelum ada peringkat
- Laporan Praktik Kerja Departemen Operasi Pusri - Ib PT Pupuk Sriwidjaja Palembang - Sumatera SelatanDokumen108 halamanLaporan Praktik Kerja Departemen Operasi Pusri - Ib PT Pupuk Sriwidjaja Palembang - Sumatera Selatanandono kusuma jatiBelum ada peringkat
- Revisi Kelompok 4Dokumen5 halamanRevisi Kelompok 4andono kusuma jatiBelum ada peringkat
- 2 Basic Programming - SBSDokumen13 halaman2 Basic Programming - SBSandono kusuma jatiBelum ada peringkat
- 4.2 HDP DonoDokumen5 halaman4.2 HDP Donoandono kusuma jatiBelum ada peringkat
- Revisi Kelompok 7Dokumen4 halamanRevisi Kelompok 7andono kusuma jatiBelum ada peringkat
- Revisi Kelompok 6Dokumen5 halamanRevisi Kelompok 6andono kusuma jatiBelum ada peringkat
- 1-Materi Teori KOMPRESOR Dan Sistem Udara Tekan Selasa 20-10-2020 - 13.b5Dokumen18 halaman1-Materi Teori KOMPRESOR Dan Sistem Udara Tekan Selasa 20-10-2020 - 13.b5andono kusuma jatiBelum ada peringkat
- Tugas Kespros Nigeria Bagian DonoDokumen9 halamanTugas Kespros Nigeria Bagian Donoandono kusuma jatiBelum ada peringkat
- Tali-Temali Untuk PemulaDokumen24 halamanTali-Temali Untuk Pemulaandono kusuma jatiBelum ada peringkat
- Revisi Kelompok 1Dokumen5 halamanRevisi Kelompok 1andono kusuma jatiBelum ada peringkat
- Rencana Kerja Magang - Chiesa Salsabila - Universitas Diponegoro - Chiesa SalsabilaDokumen1 halamanRencana Kerja Magang - Chiesa Salsabila - Universitas Diponegoro - Chiesa Salsabilaandono kusuma jatiBelum ada peringkat
- TUGAS MAKALAH IsopropanolDokumen11 halamanTUGAS MAKALAH Isopropanolandono kusuma jatiBelum ada peringkat
- Tugas Kelompok P3k Andono Kusuma JatiDokumen14 halamanTugas Kelompok P3k Andono Kusuma Jatiandono kusuma jatiBelum ada peringkat
- Pembagian Kelompok KimfisDokumen2 halamanPembagian Kelompok Kimfisandono kusuma jatiBelum ada peringkat
- Andono Kusuma Jati - 21030118110001 - UTS PinchDokumen8 halamanAndono Kusuma Jati - 21030118110001 - UTS Pinchandono kusuma jatiBelum ada peringkat
- Pengumuman Insentif PKM AI Dan GT Tahun 2021Dokumen55 halamanPengumuman Insentif PKM AI Dan GT Tahun 2021andono kusuma jatiBelum ada peringkat
- Tugas Individu DryingDokumen5 halamanTugas Individu Dryingandono kusuma jatiBelum ada peringkat
- Laboratorium Komputasi Proses Jurusan Teknik Kimia Fakultas Teknik Universitas Diponegoro 2019Dokumen2 halamanLaboratorium Komputasi Proses Jurusan Teknik Kimia Fakultas Teknik Universitas Diponegoro 2019andono kusuma jatiBelum ada peringkat
- Tugas 1 Utilitas - Andono Kusuma Jati - 21030118110001Dokumen10 halamanTugas 1 Utilitas - Andono Kusuma Jati - 21030118110001andono kusuma jatiBelum ada peringkat
- Laboratorium Komputasi Proses Departemen Teknik Kimia Fakultas Teknik Universitas DiponegoroDokumen1 halamanLaboratorium Komputasi Proses Departemen Teknik Kimia Fakultas Teknik Universitas Diponegoroandono kusuma jatiBelum ada peringkat
- Selvi Khairunisah Ashar - BAB IDokumen18 halamanSelvi Khairunisah Ashar - BAB Iandono kusuma jatiBelum ada peringkat