KD 7 Unsur Transisi
Diunggah oleh
Lutfi Shidqi MardianJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
KD 7 Unsur Transisi
Diunggah oleh
Lutfi Shidqi MardianHak Cipta:
Format Tersedia
Bab 3 Kimia Unsur
6. Unsur Periode Keempat ( Unsur Transisi ) & Ion Kompleks
a. Pengertian
Unsur Transisi merupakan unsur-unsur yang elektron terakhirnya mengisi sub kulit d. Oleh karena itu
unsur transisi disebut juga unsur blok d. Dalam sistem periodik unsur transisi terletak antara
golongan IIA – IIIA dan dimulai dari periode ke-4 dan terakhir pada periode 7. Pada unsur transisi
terdapat pula unsur transisi dalam yaitu deret lantanida ( blok 4f ) dan deret aktinida ( blok 5f ). Unsur
transisi dalam terletak pada golongan IIIB
b. Konfigurasi Elektron & Letaknya dalam Sistem Periodik
Unsur Konfigurasi Golongan Periode Unsur Konfigurasi Golongan Periode
Elektron Elektron
21 Sc ( Ar ) 4s2 3d1 IIIB 4 26Fe ( Ar ) 4s2 3d6 VIIIB 4
22Ti ( Ar ) 4s2 3d2 IVB 4 27Co ( Ar ) 4s2 3d7 VIIIB 4
23V ( Ar ) 4s2 3d3 VB 4 28Ni ( Ar ) 4s2 3d8 VIIIB 4
24Cr ( Ar ) 4s1 3d5 VIB 4 29Cu ( Ar ) 4s13d10 IB 4
25Mn ( Ar ) 4s2 3d5 VIIB 4 30Zn ( Ar ) 4s23d10 IIB 4
c. Sifat-sifat
Unsur Sc Ti V Cr Mn Fe Co Ni Cu Zn
Energi Ionisasi 631 658 650 652,8 717,4 711 758 736,7 745,4 906,4
Warna Logam Perak Perak Perak- Perak Abu-abu Abu-abu Abu-abu Perak Merah Biru-
putih putih baja putih
Titik Cair, oC 1541 1660 1890 1857 1244 1535 1459 1552 1083,4 320,9
Titik Didih, oC 2831 3287 3380 2672 1962 2750 2870 2732 2567 765
Afinitas Elektn 18,1 7,6 50,7 64,3 <0 15,7 63,8 111,5 118,5 <0
Keeletronegtfn 1,36 1,54 1,63 1,66 1,55 1,90 1,88 1,91 1,90 1,69
Eo Red ( Volt ) -2,08 -0,86 -1,2 -0,74 -0,183 -0,0036 -0,28 -0,23 +0,34 +0,76
Sc3+/Sc Ti4+/Ti V2+/V Cr3+/Cr Mn3+/Mn Fe3+/Fe Co2+/Co Ni2+/Ni Cu2+/Cu Zn2+/Zn
1. Bersifat Logam
Semua unsur transisi bersifat logam, hal ini disebabkan pada sub kulit terluar hanya terisi oleh
satu atau dua elektron maka berakibat energi ionisasinya kecil sehingga mudah untuk
melepaskan elektron. Dibandingkan dengan unsur golongan utama ( golongan A ) unsur transisi
lebih keras dan titik cair atau titik didihnya lebih tinggi. Ini akibat dari elektron yang lebih banyak
pada kulit yang belum lengkap ( sub kulit d ), sehingga membentuk ikatan logam yang lebih kuat.
2. Ionnya Berwarna
Unsur Ion Warna Unsur Ion Warna
Sc Sc3+ Tak berwarna Mn Mn2+ Merah-muda
Ti Ti2+ Ungu Mn3+ Merah-coklat
Ti3+ Ungu-hijau MnO42- Hijau
Ti4+ Tak berwarna MnO4- Ungu
V V2+ Ungu Fe Fe2+ Hijau
V3+ Hijau Fe3+ Jingga
VO2+ Biru Co Co2+ Merah-muda
VO43+ Merah Co3+ Biru
Cr Cr2+ Biru Ni Ni2+ Hijau
Cr3+ Hijau Cu Cu+ Tak-berwarna
CrO42- Kuning Cu2+ Biru
Cr2O72- Jingga Zn Zn2+ Tak-berwarna
3. Bersifat Katalis
Unsur transisi lebih banyak dipakai sebagai katalis pada reaksi-reaksi kimia sebab dapat
mempercepat reaksi dengan cara menimbulkan aspek permukaan ( bidang sentuk reaksi ) yang
lebih luas.
Contoh :
- V2O5 katalis pada industri pembuatan asam sulfat ( Proses Kontak )
- Serbuk besi pada industri pembuatan amoniak ( Proses Haber Bosch )
- Logam platina dan nikel pada reaksi-reaksi organik
- Ion Zn2+ pada reaksi hidrolisis protein menjadi asam amino
- Ion Cu2+ pada reaksi pembentukan haemoglobin
4. Terpengaruh Medan Magnet
Bahan Ajar Kimia Kelas XII SMA Negeri 1 Cibarusah
Bab 3 Kimia Unsur
Unsur atau ion logam transisi kebanyakan terpengaruh oleh medan magnet ( paramagnetik )
karena ada beberapa elektron pada orbital-orbitalnya belum berpasangan, makin banyak jumlah
elektron yang tidak berpasangan makin terpengaruh oleh medan magnet ( feromagnetik ).
Sebaliknya jika semua elektron pada orbital-orbitalnya sudah penuh maka tidak terpengaruh
medan magnet ( diamagnetik ).
5. Bilangan Oksidasi
Bil. Oks
Unsur +1 +2 +3 +4 +5 +6 +7
Sc +3
Ti +3 +4
V +1 +2 +3 +4 +5
Cr +2 +3 +4 +5 +6
Mn +2 +3 +4 +5 +6 +7
Fe +2 +3 +4 +5 +6
Co +2 +3 +4 +5
Ni +2 +3 +4
Cu +1 +2 +3
Zn +2
Catatan : - bilangan oksidasi yang ditulis tebal stabil
- bilangan oksidasi yang ditulis tidak tebal tidak stabil
6. Membentuk Ion Kompleks
Rumus umum ion kompleks : [ M(P)x(Q)y]z M = atom pusat ( kation logam transisi )
P, Q = ligan ( anion / molekul )
x,y = jumlah ligan
x+y = bilangan koordinasi
z = muatan ion kompleks ( + / - )
Contoh :
1. Tentukan atom pusat, ligan, muatan ion kompleks dan bilangan koordinasi dari ion
kompleks [ Fe(H2O)2(SO4)4]5-
Jawab :
- atom pusat Fe3+ - muatan ion kompleks = -5
- ligan H2O dan SO4 - bilangan koordinasi = 6
2. Tuliskan rumus ion kompleks jika tersusun atas atom pusat Cr 3+, ligan NH3 dan C2O42-
dengan bilangan koordinasi 6 serta muatan ion kompleks -3 !
Jawab :
Misal bilangan oksidasi atom pusat = +3, jumlah NH3= x dan jumlah ligan C2O42- = y
Maka : 3 + x ( 0 ) + y ( -2 ) = -3 y = 3
x+y=6x=3
Jadi rumus ion kompleksnya : [Cr(NH3)3(C2O4)3]3-
3. Tuliskan reaksi ionisasi ion kompleks : [Fe(S2O3)3(SCN)2Cl]7-
Jawab : [Fe(S2O3)3(SCN)2Cl]7- Fe3+ + 3 S2O32- + 2SCN- + Cl-
Bahan Ajar Kimia Kelas XII SMA Negeri 1 Cibarusah
Bab 3 Kimia Unsur
Tatanama Ion Kompleks
1. Tentukan jumlah ligan
Jika jumlahnya 1 = mono, 2 = di, 3 = tri, 4 = tetra, 5 = penta, 6 = heksa, 7 = hepta, 8 =
okta, 9 = nona, 10 = deka
2. Tulis nama ligan
1. H2O = aquo 6. F- = floro 11. C2O42- = oksalato
2-
2. NH3 = amino 7. S2O3 = tiosulfato 12. OH- = hidrokso
3. NO2- = nitrito 8. SO42- = sulfato 13. I- = Iodo
4. Cl- = kloro 9. SCN- = tiosiano
5. Br- = bromo 10. CN- = siano
3. Jika ion kompleks bermuatan negatif nama atom pusat diakhiri kata “at”.
4. Tulis bilangan oksidasi atom pusat dengan angka romawi dalam tanda “( )”
Contoh :
1. Tuliskan nama ion kompleks : a. [Cr(NH3)3(C2O4)3]3- b. [Fe(S2O3)3(SCN)2Cl]7-
2. Tuliskan rumus ion kompleks dari :
a. ion tetra amino tembaga ( II )
b. ion trioksalato disiano monoIodo nikelat ( III )
Jawab :
1. a. ion triamino trioksalato kromat (III) b. ion tritiosulfato ditiosiano monobromo ferat (III)
2. a. [Cu[NH3]4]2+ b. [Ni(C2O4)3(CN)2Br]6-
Nama
Kelas
No Absen
Aktifitas 21
UJI KOMPETENSI UNSUR-UNSUR PERIODE KEEMPAT ( UNSUR TRANSISI )
1. Tentukan golongan dan periode dari :
a. 24Cr c. 39Y e. 59Pr
b. 29Cu d. 78Pt f. 92U
Jawab :
……………………………………………………………………………………………………………………
2. Tentukan mana yang lebih terpengaruh medan magnet antara
a. 25Mn dan 26Fe
b. 24Cr3+ dan 25Mn2+
Jawab :
……………………………………………………………………………………………………………………
3. Apa yang anda ketahui tentang unsur transisi dalam !
Jawab :
……………………………………………………………………………………………………………………
4. Mengapa unsur transisi mempunyai bilangan oksidasi lebih dari satu jenis !
Jawab :
……………………………………………………………………………………………………………………
5. Mengapa semua unsur transisi bersifat logam !
Jawab :
……………………………………………………………………………………………………………………
6. Mengapa titik cair & titik didih logam seng terendah diantara logam transisi lain dalam periode keempat !
Jawab :
……………………………………………………………………………………………………………………
7. Tuliskan reaksi pembentukan ion kompleks pada :
a. Fe3+ + 6 NH3
b. Cr3+ + 4 H2O + 2 OH-
Jawab :
……………………………………………………………………………………………………………………
Bahan Ajar Kimia Kelas XII SMA Negeri 1 Cibarusah
Bab 3 Kimia Unsur
8. Tuliskan rumus ion kompleks ( dan namanya ) yang terjadi dari :
a. atom pusat Co3+, 4 ligan S2O32- dan 2 ligan Cl-
b. atom pusat Mn4+, 2 ligan C2O42- , 2 ligan SCN-, 1 ligan OH- dan 1 ligan NO3-
Jawab :
……………………………………………………………………………………………………………………
9. Tuliskan rumus ion atau senyawa kompleks dari :
a. Dikloro dihidrokso nikelat (II)
b. Tetraaquo tembaga (II) sulfat
c. Diamino seng (II) tetraoksalato ditiosulfato manganat (III)
Jawab :
……………………………………………………………………………………………………………………
10. Tuliskan rumus ion kompleks dan namanya dari :
a. atom pusat Fe3+, ligan oksalato dan hidrokso, bilangan koordinasi 6, muatan ion kompleks = -5
b. atom pusat Mn3+, 3 ligan sulfato, 2 ligan siano dan 1 ligan tiosiano
Jawab :
……………………………………………………………………………………………………………………
Diperiksa tgl. Paraf Guru
HIBRIDISASI DAN BENTUK GEOMETRI ION KOMPLEKS
Bentuk geometri ion kompleks ditentukan oleh hibridisasi yang terjadi pada setiap ion kompleks.
Hibridisasi juga dipengaruhi oleh kekuatan medan ligan, dimana setiap ligam mempunyai kekuatan yang
berbeda. Berikut ini disajikan daftar hibridisasi dan bentuk geometrinya :
No Bilangan Koordinasi Hibridisasi Bentuk Geometri
1. 2 sp Linier
2. 4 sp3 Tetrahedral
4 dsp2 Segiempat Planar
3. 6 d2sp3 Oktahedral
6 sp3d2 Oktahedral
Hibridisasi d2sp3 dinamakan juga orbital dalam ( inner orbital ), sedangkan sp 3d2 disebut orbital luar ( outer
orbital ).
Urutan kekuatan medan ligan :
CO > CN- > NO2- > NH3 > SCN- >> H2O > C2O42- > OH- > F- > Cl- > Br- > I-
kuat lemah
Contoh Soal :
Tentukan hibridisasi dan bentuk geometri ion kompleks berikut ini :
1. [Cu(NH3)4]2+ , Nomor atom Cu = 29
2. [Cu(OH)4]2-
3. [Co(CN)6]3- , Nomor atom Co = 27
4. [CoCl4]3-
Jawab :
1. 29Cu : ( Ar ) 4s1 3d10 4p0
Bilangan oksidasi Cu pada ion kompleks [Cu(NH3)4]2+ adalah = +2, maka
Cu2+ : ( Ar ) 3d9 4s0 4p0 yang dibuat diagram orbital
Cu2+ : ( Ar ) ll ll ll ll l
[Cu(NH3)4]2+ : Ar ) ll ll ll ll xx xx xx xx xx xx = PEB NH3
2. [CuF4]2+ : ( Ar ) ll ll ll ll l xx xx xx xx xx = PEB F-
3. [Co(CN)6]2+ : ( Ar ) ll ll ll xxxx xx xx xx xx xx = PEB CN-
Bahan Ajar Kimia Kelas XII SMA Negeri 1 Cibarusah
Bab 3 Kimia Unsur
4. [CuCl6]2+ : ( Ar ) ll l l l l xx xx xx xx xx xx xx = PEB Cl-
No Bilangan Koordinasi Hibridisasi Bentuk Geometri
1. [Cu(NH3)4]2+ sp3 Tetrahedral
2. [CuF4]2+ dsp2 Segiempat Planar
3. [Co(CN)6]3- d2sp3 Oktahedral
4. [CuCl6]3- sp3d2 Oktahedral
F
H3N NH3
H3N Ag NH3 Cu
Linier Cu
H3N NH3 F F
Segi empat planar
F
Tetrahedral Oktahedral
1. Unsur Radioaktif
a. Pengertian
Pada sistem periodik unsur ada beberapa unsur yang mempunyai inti tidak stabil seperti Po, At,
Rn, Fr, Ra, U dan lain-lain maka unsur-unsur tersebut cenderung memancarkan sinar radioaktif
seperti sinar alfa, beta dan gamma yang tujuannya untuk mencapai kestabilan intinya. Unsur-
unsur tersebut di atas kita sebut Unsur Radioaktif.
b. Kestabilan Inti
Unsur radioaktif mempunyai inti tidak stabil yang disebabkan oleh perbandingan proton dan
neutron dalam inti tidak seimbang. Inti yang tidak stabil ada tiga kelompok yaitu : >1 , <1 dan
inti berat ( p>83 ) , maka untuk mencapai kestabilan unsur tersebut memancar sinar
radioaktif. Ketiga kelompok unsur radioaktif teresbut dapat di buat “ Pita kestabilan Inti “ di bawah
ini.
Neutron =1 Pada pita kestabilan dibagi tiga daerah yaitu daerah di atas
pita kestabilan ( >1 ), di bawah pita kestabilan ( <1 )
dan di seberang pita kestabilan ( p>83 ).
>1 Contoh:
p>83 Apakah nuklida Mg, Ca dan U bersifat radioaktif ?
<1 Jawab : Mg ( p=12, n=13 maka >1 jadi radioaktif )
Ca ( p=20, n=19 maka <1 jadi radioaktif )
20 83 proton U ( p>83 maka radioaktif )
Cara mencapai kestabilan inti :
1. Unsur di atas pita kestabilan ( > 1 )
-
- memancarkan sinar beta ( e= ) : n p+ e Contoh : C N+ e
- memancarkan neutron ( n ), contoh : K K+ n
2. Unsur di bawah pita kestabilan ( < 1 )
- memancarkan positron ( e+ = +
) : p n + e+ Contoh : C B+ e+
- memancarkan protron ( p ), Contoh : N C+ p
- memancarkan sinar X ( menangkap elektron dari kulit K ) : Ar + e Cl + X
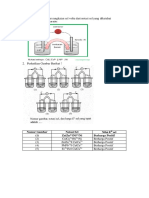
Mekanisme terbentuknya Sinar X ( Rontgen )
Nuklida dengan perbandingan < 1, untuk mengubah proton menjadi neutron menangkap elektron dari kulit K
( paling dekat dengan inti ) sehingga inti stabil. Elektron yang pindah ke inti diisi oleh elektron dari kulit yang lebih
luarnya ( kulit L ) dan seterusnya berarti elektron berenergi tinggi menjadi elektron berenergi rendah, sehingga ada
kelebihan energi dipancarkan sebagai sinar yang disebut sinar X ( sinar Rontgen )
Bahan Ajar Kimia Kelas XII SMA Negeri 1 Cibarusah
Bab 3 Kimia Unsur
3. Unsur di seberang pita kestabilan ( p>83 )
- memancarkan sinar alfa = He , Contoh : U Th +
c. Laju Peluruhan dan Waktu Paruh
- Laju Peluruhan
=- N N = jumlah inti radioaktif t waktu, No = jumlah inti radioaktif t = 0
= tetapan peluruhan
= jumlah inti yang mengalami peluruhan tiap satuan waktu
=- N =- N ln N = - t + C ln No = - ( 0 ) + C C = ln No
ln N = - t + No ln N – ln No = - t ln = - t ln = t
2,303 log = t atau N = No . e - t
e = 2,718
- Waktu Paruh ( T atau t ½ ) = waktu yang diperlukan zat radioaktif menjadi setengahnya dari
semula.
Pada saat t = t ½ , maka N = ½ No sehingga =½=e- t
Maka :
t½= ( = tetapan peluruhan )
Jika t = t ½ maka N = ( ½ )n . No ( n = t / t½ )
Contoh :
1. Gas Rn mempunyai waktu paruh 3,82 hari. Hitunglah :
a. Tetapan peluruhan
b. % atom Rn yang meluruh selama 30 hari
Jawab :
a. 3,82 = = 0,181 hari-1
b. 2,303 log = 0,181 x 30 = 229,086 N = 0,00437 No = 0,437%
% atom Rn yang meluruh selama 30 hari = 100% - 0,437% = 99,563%
2. Nuklida Cu-64 memancarkan sinar beta mempunyai waktu paruh 12,8 hari
a. Tuliskan reaksi peluruhannya
b. Nuklida apa yang dihasilkan pada peluruhan tersebut !
c. Hitung waktu yang dibutuhkan agar keaktifannya tinggal 20% !
Jawab :
a. Cu Zn +
b. Zn-64
c. 12,8 = = 0,0541 hari-1 2,303 log = 0,0541x t t = 29,954 jam
d. Reaksi Inti ( Nuclear Reaction )
- Reaksi Penembakan
Contoh : N+ n C+ e ( n = partikel penembak ringan )
Cf + N Unp + 4 n ( N = partikel penembak berat )
- Reaksi Fisi ( Reaksi Pembelahan )
Contoh : Pu + n Kr + Ce + 2 n
Penggunaan Reaksi Fisi :
1. Reaksi Fisi Tidak Terkendali : Contoh Bom Nuklir
2. Reaksi Fisi Terkendali : Contoh Reaktor Nuklir
- Reaksi Fusi ( Reaksi Penggabungan )
Bahan Ajar Kimia Kelas XII SMA Negeri 1 Cibarusah
Bab 3 Kimia Unsur
Contoh : H + H + H + H He + 2 e ( reaksi ini terjadi di matahari )
( Untuk renungan 1 kh Hidrogen menghasilkan energi yang setara dengan pembakaran 20.000 ton
batubara “ sayang manusia belum memanfaatkannya“ )
e. Deret Keradioaktifan
Contoh : U Bi + 7 +5
f. Kegunaan Zat Radioaktif
1. Sumber Radiasi
a. Bidang Kedokteran ( terapi kanker Co-60, radiologi dengan sinar X )
b. Bidang Industri ( memeriksa sambungan logam dengan sinar X)
c. Bidang Pertanian ( efesiensi pemakaian pupuk P-32, pemualiaan bibit )
d. Pengawetan Makanan
e. Pemberantasan Hama ( Radiasi terhadap hewan jantan mandul )
2. Perunut / Penelusur
a. Bidang Kedokteran ( Na-24 pemeriksaan aliran darah, I –131 kelenjar gondok )
b. Bidang Industri ( Kebocoran pipa bawah tanah, aliran lumpur sungai Na-24 )
c. Bidang Kimia ( Mekanisme Reaksi O-18 )
d. Bidang Biologi ( Fotosintesis C-14 )
Nama
Kelas
No Absen
Aktifitas 22
UJI KOMPETENSI UNSUR RADIOAKTIF
1. Manakan unsur berikut yang bersifat radioaktif :
a. C c. K
b. Mg d. Th
Jawab :
……………………………………………………………………………………………………………………
2. Bagaimana caranya unsur tersebut dibawah ini untuk menjadi stabil :
a. C c. K
b. Mg d. Th
Jawab :
……………………………………………………………………………………………………………………
3. Lengkapilah reaksi peluruhan berikut dan tuliskan notasinya dalam bentuk x ( a, b ) y:
a. 94Be + 21H + 10n
63 1
b. 29Cu + 1H + 10n
127
c. 53I + 53I + 10n
128
35 1
d. 17Cl + 0n + 21H
Jawab :
……………………………………………………………………………………………………………………
4. Zat radioaktif mula-mula sebesar 64 gram setelah meluruh tinggal 2 gram. Jika waktu paruhnya 5 jam,
hitunglah lama peluruhannya !
Jawab :
……………………………………………………………………………………………………………………
5. Suatu zat radioaktif setelah meluruh selama 10 hari tinggal 12,5%. Hitunglah waktu paruh zat radioaktif
tersebut !
Jawab :
……………………………………………………………………………………………………………………
6. Waktu paruh Sr-90 yang meluruh menjadi Y-90 sebesar 28,1 tahun.
a. Tuliskan reaksi peluruhannya
b. Partikel apa yang dipancarkan
c. Jika awal peluruhan massa Sr sebesar 90 gram, tentukan massa akhir peluruhannya !
Jawab :
Bahan Ajar Kimia Kelas XII SMA Negeri 1 Cibarusah
Bab 3 Kimia Unsur
……………………………………………………………………………………………………………………
……………………………………………………………………………………………………………………
……………………………………………………………………………………………………………………
7. Untuk menyelidiki umur papirus Mesir maka sepotong papirus dibakar sempurna. Gas CO2 yang
terbentuk dideteksi dengan alat Geiger Muller, yang menunjukkan data 14,7 cpm per gram C-14.
Diketahui bagi organisme hidup, alat Geiger Muller menunjukkan 15,3 cpm per C-14. Jika waktu paruh
Carbon-14 adalah 5730 tahun. Hitunglah umur papirus tersebut !
Jawab :
……………………………………………………………………………………………………………………
……………………………………………………………………………………………………………………
……………………………………………………………………………………………………………………
Diperiksa tgl. Paraf Guru
A. Manfaat Unsur dan Senyawa
B. Kadar Unsur dalam produk Kimia
Bahan Ajar Kimia Kelas XII SMA Negeri 1 Cibarusah
Anda mungkin juga menyukai
- Sifat Fisika Dan Kimia Unsur Periode 4Dokumen4 halamanSifat Fisika Dan Kimia Unsur Periode 4Zulfa50% (2)
- Unsur Golongan Transisi Peridode EmpatDokumen10 halamanUnsur Golongan Transisi Peridode EmpatAndrea Dhieta UtamaBelum ada peringkat
- Unsur Transisi Periode Ke EmpatDokumen14 halamanUnsur Transisi Periode Ke EmpatAdriel ChristopherBelum ada peringkat
- 3.3. BAB 2 SISTEM PERIODIK - Ion KompleksDokumen33 halaman3.3. BAB 2 SISTEM PERIODIK - Ion Kompleks29.Sherly Nofia ningsihBelum ada peringkat
- Unsur TransisiDokumen9 halamanUnsur TransisiReguler 2 PsikBelum ada peringkat
- TRANSISIDokumen28 halamanTRANSISI16. Rafi AltariqBelum ada peringkat
- Kimia 2Dokumen19 halamanKimia 2Husna DhiaBelum ada peringkat
- Bab 6 Unsur-Unsur Transisi Periode KeempatDokumen40 halamanBab 6 Unsur-Unsur Transisi Periode KeempatHanavia100% (2)
- Bahan Ajar Unsur TransisiDokumen9 halamanBahan Ajar Unsur TransisiIneke AyuningsihBelum ada peringkat
- Nama Mineral KimiaDokumen18 halamanNama Mineral KimiaWabacBelum ada peringkat
- Bahan Ajar DraftDokumen10 halamanBahan Ajar Draftilham100% (1)
- Unsur - Unsur Transisi Periode KeempatDokumen13 halamanUnsur - Unsur Transisi Periode KeempatSasqia Fesanti0% (1)
- Bab 6 Unsur-Unsur Transisi Periode Keempat FixDokumen38 halamanBab 6 Unsur-Unsur Transisi Periode Keempat FixYouandiBelum ada peringkat
- Golongan 8BDokumen31 halamanGolongan 8BJon FaizalBelum ada peringkat
- Unsur Transisi (Ke 4) BahanDokumen9 halamanUnsur Transisi (Ke 4) Bahananisa rahmiBelum ada peringkat
- Transisi Periode 4 (Autosaved)Dokumen69 halamanTransisi Periode 4 (Autosaved)kanjiroBelum ada peringkat
- Kimia Periode 4Dokumen23 halamanKimia Periode 4nabila safitriBelum ada peringkat
- Nama Mineral KimiaDokumen6 halamanNama Mineral KimiaWabacBelum ada peringkat
- Makalah Kimia Periode 4Dokumen20 halamanMakalah Kimia Periode 4khosy salmahuda2701Belum ada peringkat
- Golongan Unsur Transisi Periode KeempatDokumen7 halamanGolongan Unsur Transisi Periode KeempatristaBelum ada peringkat
- UNSURTRANSISIDokumen6 halamanUNSURTRANSISIanggie oktavianiBelum ada peringkat
- Kimia UnsurDokumen49 halamanKimia UnsurRasyid Syekher ManiaBelum ada peringkat
- Kimia Unsur Golongan VA Dan VIADokumen10 halamanKimia Unsur Golongan VA Dan VIAaisyah sabinaBelum ada peringkat
- Kimia Unsur Golongan VA Dan VIADokumen10 halamanKimia Unsur Golongan VA Dan VIAFebiola Pastika SariBelum ada peringkat
- Tantangan Unsur Transisi Periode 4-1Dokumen6 halamanTantangan Unsur Transisi Periode 4-1wildanaleBelum ada peringkat
- Kimia Unsur Transisi Periode 4Dokumen8 halamanKimia Unsur Transisi Periode 4afdhalBelum ada peringkat
- Kelompok 7 Sifat Unsur Transisi Periode KeempatDokumen14 halamanKelompok 7 Sifat Unsur Transisi Periode KeempatSuci RoyaniBelum ada peringkat
- Pengertian Logam TransisiDokumen4 halamanPengertian Logam TransisiRandy PrasetyoBelum ada peringkat
- Unsur Periode 4Dokumen18 halamanUnsur Periode 4Mokhammad Brian YusufBelum ada peringkat
- Golongan Transisi Oleh Marsela MadaiDokumen38 halamanGolongan Transisi Oleh Marsela MadaiFernandus TakimaiBelum ada peringkat
- Transisi Deret PertamaDokumen46 halamanTransisi Deret PertamaSekar AyuBelum ada peringkat
- Unsur TransisiDokumen9 halamanUnsur TransisiHawari MilatullahBelum ada peringkat
- Kimia Unsur - Unsur Transisi Periode 4Dokumen3 halamanKimia Unsur - Unsur Transisi Periode 4Muh Zamhari RizkiBelum ada peringkat
- Bab 3 - Kimia UnsurDokumen49 halamanBab 3 - Kimia UnsurAdwitya Candra WulanBelum ada peringkat
- Unsur Transisi KimiaDokumen15 halamanUnsur Transisi KimiaElviraBelum ada peringkat
- No. 3 Sampai 4 A, LKM 10 KIMSURDokumen5 halamanNo. 3 Sampai 4 A, LKM 10 KIMSURAyu Ningtias SaputriBelum ada peringkat
- Unsur TransisiDokumen10 halamanUnsur TransisiAlifia NurfatikhaBelum ada peringkat
- Raihan Azaki Golongan IVADokumen5 halamanRaihan Azaki Golongan IVATata Anugrah KelanaBelum ada peringkat
- Sifat Periode 4Dokumen3 halamanSifat Periode 4Anisa ZaqiBelum ada peringkat
- Kimia UnsurDokumen27 halamanKimia UnsurZaky RamadhanBelum ada peringkat
- Unsur Transisi Periode Ke Empat PPT AmazingDokumen52 halamanUnsur Transisi Periode Ke Empat PPT AmazingFajarBelum ada peringkat
- Konfigurasi ElektronDokumen7 halamanKonfigurasi ElektronRizmuhafBelum ada peringkat
- Unsur Transisi Periode Ke 4Dokumen36 halamanUnsur Transisi Periode Ke 4sintadevi puspitsariBelum ada peringkat
- Tugas Mid Ringkasan Periode 4 Unsur TransisiDokumen17 halamanTugas Mid Ringkasan Periode 4 Unsur TransisiSukrisno SyukriBelum ada peringkat
- UNSUR TRANSISI 08 Converted CompressedDokumen40 halamanUNSUR TRANSISI 08 Converted CompressedLailatul BadriyahBelum ada peringkat
- Pendahuluan Sifat Unsur TransisiDokumen19 halamanPendahuluan Sifat Unsur TransisiSekar AyuBelum ada peringkat
- Kelompok 6Dokumen3 halamanKelompok 6Khafid Ibnu Al-QoyyimBelum ada peringkat
- Unsur Kimia Periode KeempatDokumen7 halamanUnsur Kimia Periode KeempatRistika Nur IsnainiBelum ada peringkat
- Materi Kimia Xii Seri 18 KD 3.8 & 4.8Dokumen16 halamanMateri Kimia Xii Seri 18 KD 3.8 & 4.8WayiBelum ada peringkat
- MAKALAH KIMIA Periode 4Dokumen25 halamanMAKALAH KIMIA Periode 4darmi.smkmuh1plgBelum ada peringkat
- Unsur Transisi Periode 4Dokumen35 halamanUnsur Transisi Periode 4bucin skijeuBelum ada peringkat
- Periode 4-4Dokumen36 halamanPeriode 4-4Adeline nimsBelum ada peringkat
- Unsur Transisi Periode 4Dokumen32 halamanUnsur Transisi Periode 4mayangBelum ada peringkat
- MakalahDokumen15 halamanMakalahYuhanidha SitiBelum ada peringkat
- Periode 4Dokumen36 halamanPeriode 4Herdianta SebayangBelum ada peringkat
- Kisi KisiDokumen28 halamanKisi KisizahraBelum ada peringkat
- Unsur Transisi Periode 4Dokumen1 halamanUnsur Transisi Periode 4sscbandung100% (9)