I.
Judul Percobaan DARAH
: PENENTUAN KADAR GLUKOSA
II.
Hari/tanggal Percobaan
: Selasa, 8 November 2011
III.
Selesai Percobaan
: Selasa, 8 November 2011
IV.
Tujuan Percobaan
: Menentukan kadar glukosa darah
V.
Tinjauan Pustaka Glukosa, suatu gula monosakarida, adalah salah satu karbohidrat terpenting yang digunakan sebagai sumber tenaga bagi hewan dan tumbuhan.glukosa dengan rumus molekul C6H12O6 dengan berat molekul 180,18 merupakan heksosa monosakarida yang mengandung enam atom karbon. Glukosa merupakan aldehide karena mengandung gugus-CHO. Lima karbon dan satu oksigennya membentuk cincin yang disebut "cincin piranosa", bentuk paling stabil untuk aldosa berkabon enam. Dalam cincin ini, tiap karbon terikat pada gugus samping hidroksil dan hidrogen kecuali atom kelimanya, yang terikat pada atom karbon keenam di luar cincin, membentuk suatu gugus CH2OH. Struktur cincin ini berada dalam kesetimbangan dengan bentuk yang lebih reaktif, yang proporsinya 0.0026% pada pH 7. Glukosa merupakan salah satu hasil utama fotosintesis dan awal bagi respirasi. Bentuk alami (D-glukosa) disebut juga dekstrosa, terutama pada industri pangan. Glukosa merupakan hasil fotosintesis pada tumbuhan dan beberapa prokariota. Glukosa juga terbentuk dalam hati dan otot rangka dari pemecahan simpanan glikogen (polimer glukosa) serta disintesis dalam hati dan ginjal dari zat antara melalui proses yang disebut glukoneogenesis.
�Struktur glukosa
Gula Darah Dalam ilmu kedokteran, gula darah adalah istilah yang mengacu kepada tingkat glukosa di dalam darah. Konsentrasi gula darah, atau tingkat glukosa serum, diatur dengan ketat di dalam tubuh. Glukosa yang dialirkan melalui darah adalah sumber utama energi untuk sel-sel tubuh. Banyak pengaruh langsung yang disebabkan dari masalah gula darah. Bila level gula darah menurun atau terlalu rendah berkembanglah kondisi fatal yang disebut hipoglisemia yang mempunyai kadar gula darah dibawah 70-90 mg/100 ml. Gejala-gejalanya adalah perasaan lelah, mudah tersinggung dan kehilangan kesadaran. Bila levelnya tinggi disebut hiperglikemia yang mempunyai kadar gula darah diatas 70-90mg/100ml. Darah manusia normal mengandung glukosa dalam konsentrasi tetap aitu sekitar 70-90mg/100ml. Tingkat ini meningkat setelah makan dan biasanya berada pada level terendah pada pagi hari, sebelum orang makan. Diabetes mellitus adalah penyakit yang paling menonjol yang disebabkan oleh gagalnya pengaturan gula darah. Meskipun disebut "gula darah", selain glukosa, kita juga menemukan jenis-jenis gula lainnya, seperti fruktosa dan galaktosa. Namun demikian, hanya tingkatan glukosa yang diatur melalui insulin dan leptin.
Tingkat gula darah diatur melalui umpan balik negatif untuk
mempertahankan keseimbangan di dalam tubuh. Level glukosa di dalam darah dimonitor oleh pankreas. Bila konsentrasi glukosa menurun, karena dikonsumsi untuk
�memenuhi kebutuhan energi tubuh, pankreas melepaskan glukagon, hormon yang menargetkan sel-sel di lever (hati). Kemudian sel-sel ini mengubah glikogen menjadi glukosa (proses ini disebut glikogenolisis). Glukosa dilepaskan ke dalam aliran darah, hingga meningkatkan level gula darah. Apabila level gula darah meningkat, entah karena perubahan glikogen, atau karena pencernaan makanan, hormon yang lain dilepaskan dari butir-butir sel yang terdapat di dalam pankreas. Hormon ini, yang disebut insulin, menyebabkan hati mengubah lebih banyak glukosa menjadi glikogen. Proses ini disebut gliogenosis, yang mengurangi level gula darah. Diabetes mellitus tipe 1 disebabkan oleh tidak cukup atau tidak dihasilkannya insulin, sementara tipe 2 disebabkan oleh respon yang tidak memadai terhadap insulin yang dilepaskan ("resistensi insulin"). Kedua jenis diabetes ini mengakibatkan terlalu banyaknya glukosa yang terdapat di dalam darah. Untuk menentukan kadar glukosa dalam darah dapat dilakukan dengan menentukan nilai absorbansi dari darah yang bebas dari protein. Darah yang bebas protein direaksikan dengan Cu alkalis, dimana glukosa darah akan mereduksi ion Cu2+ dalam suasana basa, yang hasil reduksinya akan bereaksi dengan arsenomolibdat menghasilkan warna biru. Larutan ini diukur absorbansinya pada panjang gelombang maksimum yaitu 660 nm. Dengan menggunakan Hukum Lambert-Beer
konsentrasi glukosa dalam darah dap;at ditentukan . hukum Lambert-Beer menyatakan :
A= k x C x L
Keterangan : A = absorbansi (serapan cahaya) k = koefisien ekstingsi molar larutan l = tebal kuvet C = konsentrasi sampel Berdasarkan hukum Lambert-Beer, serapan cahaya berbanding lurus dengan konsentrasinya.
�VI. RANCANGAN PERCOBAAN Alat dan Bahan Alat : Spektronik 20 Penangas air Sentrifus Pipet larutan Cu alkalis gelas ukur Tabung reaksi Gelas kimia
Bahan: Larutan (BaOH)2 0,3 N Larutan standar 1,0 mg/ L Larutan ZnSO4.7H2O 5% Pereaksi arsenomolibdat
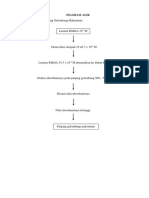
�Alur 1. Deprotenasi Filtrat Darah
Darah Diambil 0,1 ml yang oxalated Dimasukkan dalam tabung centrifuse yang berisi 1,9 ml aquades Diaduk dengan baik + 1,5 ml Ba(OH)2 Diaduk hingga rata + 1,5 ml ZnSO4 . 7 H2O 5% Dicampur dengan baik Didiamkan Disentrifus slama 30 menit didekantasi
Filtrat darah Diuji dengan biuret
Residu
Filtrat darah bebas protein
�2. Penentuan Kadar Glukosa Darah
1 ml filtrat bebas protein
- Dimasukkan dalam tabung reaksi
Ditambah 1 ml pereaksi Cu alkalis
Dimasukkan dalam air dingin
Ditambahkan 1 ml pereaksi arsenomolibdat
- Di aduk sampai rata - Dibaca absorbansinya dengan alat spektronik 20 Pada 660 nm
Absorbansi
3. Penentuan Kurva Standar 1. Pembuatan larutan standar 0,04 mg/ml dari 0,05 mg/ml
Glukosa 0,05 mg/ml
- Diambil 20 ml - Dimasukkan dalam labu ukur 25 ml - Diencerkan dengan aquades hingga tanda batas
Glukosa 0,04 mg/ml
�Pembuatan larutan standar glukosa 0,03 mg/ml dari 0,04 mg/ml glukosa
Glukosa 0,04 mg/ml
- Diambil 18,75 ml - Dimasukkan dalam labu ukur 25 ml - Diencerkan dengan aquades hingga tanda batas
Glukosa 0,03 mg/ml
Pembuatan larutan standar glukosa 0,02 mg/ml dari 0,03 mg/ml glukosa
Glukosa 0,03 mg/ml
- Diambil 16,67 ml - Dimasukkan dalam labu ukur 25 ml - Diencerkan dengan aquades hingga tanda batas
Glukosa 0,02 mg/ml
�Pembuatan larutan standar glukosa 0,01 mg/ml dari 0,02 mg/ml glukosa
Glukosa 0,02 mg/ml
- Diambil 12,5 ml - Dimasukkan dalam labu ukur 25 ml - Diencerkan dengan aquades hingga tanda batas
Glukosa 0,01 mg/ml
2. Pengujian Larutan standar
glukosa
0,01 mg/ml; 0,02 mg/ ml; 0,03 mg/ml; 0,04mg/ml; 0,05mg/ml
Imasukkan 1 ml dan dimasukkan tbung reaksi Ditambah 1 ml Cu alkalis Dimasukkan dalam air mendidih 20 menit Dimasukka dalam air dingin Ditambah 1 ml arsenomolibdat Diaduk hingga rata Dibaca absorbansi pada 660 nm
absorbansi
�4. Pembuatan Larutan Blanko
1 ml aquades
Dimasukkan dalam tabung reaksi Ditambah pereaksi Cu alkalis Dimasukkan dalam air mendidih selama 20 menit Dimasukkan dalam air dingin Ditambh 1 ml arsenomolibdat Diaduk hingga merata Diamati perubahanna Dihitung absorbansinya pada 660 nm
Absorbansi
VIII. ANALISA DATA DAN PEMBAHASAN Penentuan Kurva Standar Pada percobaan ini bertujuan untuk membuat larutan standar yang akan dicari nilai absorbansinya sehingga dapat dibuat sebuah kurva kalibrasi (A vs C) untuk mendapatkan persamaan kurva. Langkah pertama adalah melakukan pengenceran larutan glukosa 0,05 mg/ml menjadi 0,04 mg/ml, 0,04 mg/ml menjadi 0,03 mg/ml, 0,03 mg/ml menjadi 0,02 mg/ml dan 0,02 mg/ml menjadi 0,01 mg/ml. (langkah penganceran telah diperlihatkan pada alur dengan perhitungan pengenceran yang dalampirkan). Selanjutnya diambil 1ml masing-masing larutan standar hasil pengenceran kemudian dimasukkan ke dalam tabung reaksi. Selanjunya ditambah 1 ml pereaksi Cu alkalis sehingga menjadi berwarna biru jernih. Kelima tabung reaksi tersebut dipanaskan selama 20 menit untuk mempercepat reaksi ion Cu+ yang direduksi oleh gula menjadi ion kupro (Cu2+) dan mengendap sebagai Cu2O yang berwarna merah bata yang jumlahnya meningkat seiring dengan peningkatan konsentrasi larutan glukosa standar. Setelah itu didinginkan supaya reaksi berjalan
�stabil karena jika terlalu panas kemungkinan akan ada komponen senyawa yang rusak atau habis karena menguap dan masing-masing larutan ditambahkan 1ml arsenomolibdat (hijau jernih), pereaksi arsenomolibdat ini berfungsi untuk melarutkan lagi kuprooksida dan warna larutan akan berubah menjadi biru kehijauan disebabkan oleh adanya oksidasi Mo serta diaduk hingga merata, dan diperoleh tabung 1 berwarna biru kehijauan jernih, tabung 2 berwarna biru kehijauan jernih (+), tabung 3 berwarna biru kehijauan jernih (++), tabung 4 berwarna biru kehijauan jernih (+++) dan tabung 5 juga berwarna biru kehijauan jernih (++++). Kemudian kelima larutan tersebut dibaca absorbansinya pada 660 nm yang merupakan panjang gelombang maksimum sehingga diperoleh absorbansi maksimum. Sebelum dihitung absorbansinya larutan standar diencerkan 5 kali dengan cara mengambil 1 ml masing-masing sampel dan ditambah 4 ml aquades, kemudian baru dihitung nilai absorbasinya dan diperoleh nilai absorbasi larutan standar: Konsentrasi dalam (mg/ml) 0,01 0,02 0,03 0,04 0,05 Absorbanasi 0,201 0,310 0,443 0,707 0,596
Dari larutan standar tersebut dapat dibuat kurva kalibrasi (A vs C) dan diperoleh persamaan reaksi sebagai berikut :
Tabel 2. konsentrasi dalam 5 kali pengenceran dan nilai absorbansi larutan standar dikurangi blanko
Konsentrasi 0,002 0,004 0,006 0,008 0,01
Absorbasi 0,104 0,213 0,346 0,41 0,499
�Kuva kalibrasi (a vs C)
Kuva Kalibrasi Larutan Standar (A vs C)
0.6 0.5 Absorbansi 0.4 0.3 0.2 0.1 0 0 0.002 0.004 0.006 konsentrasi 0.008 0.01 0.012 y = 49.35x + 0.0183 R = 0.9863
Dan diperoleh persamaan kurva Y = 49,35x + 0,018 Dimana Y adalah nilai absorbansi sampel dikurangi absorbansi blanko. X adalah nilai konsentrasi sampel.
Deprotenasi Filtrate Darah Pada percobaan ini bertujuan untuk menghilangkan kandungan protein dalam darah. Langkah pertama yang dilakukan adalah mengambil 0,1 ml darah murni (oxalated) lalu dimasukkan ke dalam tabung sentrifus yang berisi 1,9 ml aquades. Penambahan aquades ini menunjukkan sampel darah telah diencerkan 20 kali dan berfungsi melarutkan albumin darah. Kemudian diaduk dengan baik agar tercampur sempurna. Selanjutnya ditambah 1,5 ml Ba(OH)2 0,3 N yang berwarna putih keruh sehingga warna larutan berubah menjadi coklat seperti teh. Penambahan Ba(OH)2 ini bertujuan untuk mengendapkan kembali albumin darah yang telah larut dalam aquades. Kemudian ditambah 1,5 ml ZnSO4.7H2O 5% sehingga warna larutan berubah menjadi hijau lumut yang keruh. Penambahan ZnSO4.7H2O 5% ini berfungsi sebagai katalis dalam proses pengendapan
�albumin oleh Ba(OH)2. Selanjutnya sampel tersebut disentrifus selama 30 menit untuk memisahkan albumin yang terkandung dalam darah. Setelah disentrifuse, terbentuk dua lapisan pada larutan, lapisan atas berupa larutan tidak berwarna jernih, sedangkan lapisan bawah berupa endapan hijau lumut. Campuran ini dipisahakan dengan cara dekantasi agar endapan tidak ikut diuji, selanjutnya diambil sedikit filtrate dan diuji dengan biuret, setelah ditambahkan beberapa tetes biuret, larutan tetap jernih. Hal ini membuktikan bahwa filtrate darah tersebut sudah tidak mengandung protein karena tidak berwarna ungu saat diuji dengan biuret.
Penentuan Kadar Glukosa Darah Dalam percobaan ini bertujuan untuk mencari nilai absorbansi sampel darah yang sudah tidak mengandung protein, supaya dapat dicari kadarnya. Langkah pertama adalah mengambil 1 ml filtrate darah bebas protein dan dimasukkan dalam tabung reaksi. Selanjutnya ditambahkan 1ml peraksi Cu alkalis yang berwarna biru jernih (+),sehingga terbentuk larutan berwarna biru jernih (+).Penambahan Cu alkalis ini berfungsi untuk menguji kadungan glukosa dalam filtrate darah tersebut, jika berwarna biru, maka filtrate darah tersebut mengandung glukosa. Selanjutnya, filtrate darah dipanaskan selama 20 menit untuk mempercepat reaksi ion Cu+ yang direduksi oleh gula menjadi ion kupro (Cu2+) dan mengendap sebagai Cu2O yang berwarna merah bata. Setelah dipanaskan, kemudian didinginkan dan filtrate darah ditambahkan 1ml arsenomolibdat (hijau jernih), pereaksi arsenomolibdat ini berfungsi untuk melarutkan lagi kuprooksida dan warna larutan akan berubah menjadi biru kehijauan disebabkan oleh adanya oksidasi Mo. Penambahan Ba(OH)2 sebelumnya juga membantu terjadinya reduksi ion Cu2+ karena Ba(OH)2 membantu menciptakan suasana basa karena ion Cu2+ direduksi dalam suasana basa. Intensitas warna larutan adalah ukuran banyaknya gula yang ada di dalam filtrat. Kemudian, filtrate darah ini dibaca absorbansinya pada panjang gelombang 660nm yang merupakan panjang gelombang maksimum sehingga diperoleh absorbansi maksimum. Dan diperoleh absorbansinya sebesar 0,909. Untuk
�mendapatkan nilai Absorbansi murni, nilai absorbansi sampel darah harus dikurangi absorbansi blanko karena blanko mempunyai nilai tersendiri yang terkandung dalam sampel. Sehingga diperoleh absorbansi sampel murni sebesar 0,812 Karena nilai aborbansi darah tidak memasuki rentang nilai absorbasi standar (0,201-0,596) sehingga perhitungan kadar gula dalam darah tidak dapat dihitung. Supaya dapat dihtung kita harus menaikkan nilai absorbansi pada larutan standart. Akan tetapi untuk taraf pembelajaran kita dapat mencari kadar glukosa dalam darah tersebut, dan diperoleh kadar gula darah sebesar 1,6 x 10-2 mg/ml atau 1,6 mg/100 ml (perhitungan terlampir). Dan setelah dikalikan dengan banyaknya pengenceran (20 kali pengenceran) menjadi 32 mg/100 ml Kadar gula darah tersebut sangatlah rendah dan bisa dikatakan hipoglisemia yang mempunyai kadar gula darah dibawah 70-90 mg/100 ml.
Larutan Blanko Pada percobaan ini bertujuan membuat larutan blanko dari 1ml aquades. Pembuatan larutan blanko ini berfungsi untuk menentukan nilai kandungn glukosa murni, karena nilai larutan blanko mempunyai nilai tersendiri yang terkandung dalam glukosa. Sehingga untuk memperoleh nilai glukosa murni harus dikurangi dengan nilai larutan blanko. Perlakuan dalam pembuatan larutan blanko sama halnya dengan pembuatan larutan standar ataupun pembuatan larutan sampel, tetapi yang membedakan adalah zat yang diberi perlakukan adalah 1 ml aquades. Setelah larutan blanko siap larutan diencerkan 5 kali dan kemudian dihitung nilai absorbansinya pada 660 nm yang merupakan panjang gelombang maksimum sehingga diperoleh absorbansi maksimum. Dan diperoleh nilai absorbansi larutan blanko 0,097.
IX. DISKUSI
�Pada percobaan ini kami tidak dapat menghitung nilai kadar gula dalam darah karena nilai absorbansi sampel tidak sesuai atau tidak berada pada rentang absorbansi larutan standar. Hal ini dapat terjadi karena kami kurang memperhitungkan dalam pengenceran. Sehingga nilai absorbansi yang diperoleh tidak tepat. Seharusnya terlebih dahulu kita menghitung nilai absorbansi sampel sehingga pengenceran larutan standar dapat ditentukan dengan tepat agar absorbansi sampel dapat memasuki rentang absorbansi larutan standar.
XI. KESIMPULAN Deprotenasi Filtrate Darah Pada percobaan ini bertujuan untuk menghilangkan kandungan protein dalam darah. Penentuan Kurva Standar Pada percobaan ini bertujuan untuk membuat larutan standar yang akan dicari nilai absorbansinya sehingga dapat dibuat sebuah kurva kalibrasi (A vs C) untuk mendapatkan persamaan kurva. Dan diperoleh persamaan kurva Y = 49,35x + 0,018
Larutan Blanko Pada percobaan ini bertujuan membuat larutan blanko dari 1ml aquades. Pembuatan larutan blanko ini berfungsi untuk
menentukan nilai kandungan glukosa murni, karena nilai larutan blanko mempunyai nilai tersendiri yang terkandung dalam glukosa. Sehingga untuk memperoleh nilai glukosa murni harus dikurangi dengan nilai larutan blanko. Penentuan Kadar Glukosa Darah Diperoleh absorbansi larutan sampel darah sebesar 0,909 dan menjadi 0,812 setelah dikurangi blanko..
Karena nilai aborbansi darah tidak memasuki rentang nilai absorbasi standar (0,201-0,596) sehingga perhitungan kadar gula dalam darah tidak dapat dihitung. Supaya dapat dihtung kita harus menaikkan nilai absorbansi pada larutan standart. Akan tetapi untuk taraf pembelajaran kita dapat mencari kadar glukosa dalam darah tersebut, dan diperoleh kadar gula darah sebesar 1,6 x 10-2 mg/ml atau 16 x 10-4 mg/100 ml (perhitungan terlampir). Kadar gula darah tersebut sangatlah rendah dan bisa dikatakan hipoglisemia yang mempunyai kadar gula darah dibawah 70-90 mg/100 ml.
XII.JAWABAN PERTANYAAN 1. Perhitungan kadar glukosa darah Y = 49,35x + 0,018, dimana y = Absorbansi sampel murni 0,812 = 49,35 x + 0,018 0,812 0,018 = 49,35 x 0,794 = 49,34 x X = 1,6 x 10 -2 mg/ ml X = 1,6 mg/100 ml Dikalikan faktor pengenceran (20 kali pengenceran) = 32 mg/100 ml 2. Fungsi pemanasan adalah untuk mempercepat reaksi ion Cu+ yang direduksi oleh gula menjadi ion kupro (Cu2+) dan mengendap sebagai Cu2O. 3. Peranan hormon insulin dalam proses pengaturan kadar glukosa darah yaitu apabila kadar glukosa dalam darah telah habis atau berkurang dari jumlah tertentu, hormon insulin akan merangsang hati untuk mengubah glikogen menjadi glukosa supaya dapat digunakan sebagai tenaga untuk kontraksi o
�DAFTAR PUSTAKA Yunita, Leni. 2011. Perangkat Pembelajaran Biokimia Petunjuk Praktikum Biokimia I. Surabaya: Unesa Press Anonim. 2011. Laporan Praktikum Menentukan Kadar. (Online).
(http://pengawuran.blogspot.com/2011/04/laporan-praktikummenentukan-kadar.html; diakses tanggal 5 November 2011 pukul 18:00 WIB) Darmaqua. 2008. Penentuan Kadar Glukosa dalam Darah. (Online).
(http://darmaqua.blogspot.com/2008/04/penentuan-kadar-glukosa-dalamdarah.html; diakses tanggal 5 November 2011 pukul 18:30 WIB) Sonyasa.2010. Penentuan Kadar Glukosa Dalam Darah,Html,Online. Diakses tanggal 05 November 2011
Surabaya, 1 November 2011 Mengetahui, Dosen/ Asisten Pembimbing Praktikan,
Dian Mustikasari 083194207
Endah Rohmawati 093194216
Sugeng Hariadin 093194219
�LAMPIRAN 1. Perhitungan Pengenceran Larutan Standar 1). M1 x V2 0,05 x V1 V1 2). M1 x V2 0,04 x V1 V1 3). M1 x V1 0,03 x V1 V1 4). M1 x V1 0,02 x V1 V1 = M2 x V2 = 0,04 x 25 ml = 20 ml = M2 x V2 = 0,03 x 25 ml = 18,75 ml = M2 xV2 = 0,02 x 25 ml = 16,67 ml = M2 x V2 = 0,01 x 25 ml = 12,5 ml
2. Perhitungan kadar glukosa darah Y = 49,35x + 0,018, dimana y = Absorbansi sampel murni 0,812 = 49,35 x + 0,018 0,812 0,018 = 49,35 x 0,794 = 49,34 x X = 1,6 x 10 -2 mg/ ml X = 1,6 mg/100 ml x 20 = 32 mg/100 ml
�Foto Praktikum
a). Darah + Ba(OH)2 ZnSO4.7H2O 5%
b). Darah + Ba(OH)2 +
c). Larutan standar protein
d) sampel darah bebas
�e). sampel darah (uji) blanko
e). larutan