04 Handout Teori Kinetika Reaksi
04 Handout Teori Kinetika Reaksi
Diunggah oleh
Krisna PamungkasHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
04 Handout Teori Kinetika Reaksi
04 Handout Teori Kinetika Reaksi
Diunggah oleh
Krisna PamungkasHak Cipta:
Format Tersedia
dy/teori kinetika reaksi kimia/2007/halaman 1 dari 5 halaman
Ada 2 (dua) pendekatan teoretik untuk menjelaskan kecepatan reaksi, yaitu:
(1) Teori tumbukan (collision theory)
(2) Teori keadaan transisi (transition-state theory) atau teori kompleks aktif atau teraktifkan
(activated-complex theory)
TEORI TUMBUKAN (KOLISI)
Dasar: Reaksi hanya dapat berlangsung jika molekul-molekul reaktan saling bertumbukan.
Namun demikian, tidak setiap tumbukan akan menghasilkan reaksi. Hanya tumbukan yang
berhasil atau efektif saja yang akan menghasilkan reaksi.
Tumbukan yang berhasil (efektif):
Jika tersedia jumlah energi yang cukup dan orientasi (atau posisi) yang tepat untuk
memutuskan atau memecahkan ikatan dan membentuk ikatan kimia yang baru.
Tinjaulah sebuah reaksi homogen: A + B produk reaksi ... (1)
Kecepatan reaksi (1) yang dilambangkan dengan r, atau yang juga merupakan jumlah tumbukan
efektif per satuan waktu, dapat dinyatakan sbb.:
r = P . z . f ... (2)
dengan: P faktor ruang (faktor probabilitas, faktor sterik). Faktor ini menunjukkan fraksi
tumbukan dengn orientasi yang tepat. Untuk penyederhanaan, sering kali diambil
harga: P = 1
z jumlah tumbukan per satuan volume per satuan waktu
f fraksi tumbukan yang efektif, dengan tingkat energi yang cukup.
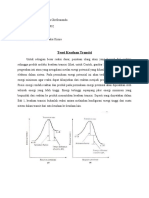
Perhatikan gambar di bawah ini! Dalam sebuah sistem reaksi homogen terdapat molekul-molekul
reaktan A dan B (yang dianggap berbentuk bola dengan diameter masing-masing sebesar d
A
dan d
B
)
yang terdistribusi secara acak. Sebuah molekul A bergerak dengan kecepatan tertentu dan
menumbuk sebuah molekul B yang diam.
Berdasarkan tinjauan reaksi bimolekuler (z = z
AB
) dan teori tumbukan:
B A
B A
B A
2
AB AB
C C
M M
M M
T R 8 d z
2
1
+
= ... (3)
T R
E
e f
= ... (4)
Maka:
B A
T R
E
B A
B A
2
AB
C C e
M M
M M
T R 8 d r
2
1
+
= ... (5)
Keterangan: d
AB
diameter tumbukan [d
AB
= (d
A
+ d
B
)] ... (6)
R tetapan gas [R = k
B
. N
av
] ... (7)
TEORI KINETIKA REAKSI KIMIA
Faktor frekuensi
tumbukan (atau faktor
pre-eksponensial)
faktor
eksponensial
Konstanta kecepatan reaksi, k
(temperature-dependent term)
concentration-dependent term
d
AB
B
A
d
A
d
B
A
B
B
B
dy/teori kinetika reaksi kimia/2007/halaman 2 dari 5 halaman
k
B
tetapan Boltzmann ( = 1,38 .10
-23
Joule/Kelvin)
N
av
bilangan Avogadro ( = 6,02 .10
23
)
M
A
, M
B
massa molekul relatif reaktan A, B
T R
E
e
fraksi tumbukan yang melepaskan energi sebesar E atau lebih
Faktor frekuensi tumbukan menyatakan jumlah tumbukan per satuan waktu per
satuan volume.
Beberapa hal yang berkaitan dengan teori tumbukan:
Meskipun teori ini pada awalnya hanya dapat menjelaskan reaksi yang sederhana, namun,
dibandingkan dengan data percobaan untuk sejumlah reaksi gas bimolekuler, teori
tumbukan memberikan hasil yang relatif baik.
Teori tumbukan juga cocok diterapkan untuk beberapa reaksi dalam larutan yang melibatkan
ion-ion sederhana.
Besarnya faktor frekuensi tumbukan yang diprediksi menggunakan teori tumbukan: 10
9
10
11
Penyimpangan yang dihasilkan akan semakin besar seiring dengan meningkatnya
kompleksitas molekul-molekul reaktan yang terlibat.
Kecepatan reaksi bergantung pada konsentrasi reaktan, karena jumlah tumbukan per
detiknya bertambah jika konsentrasi bertambah
Kecepatan reaksi bergantung pada sifat reaktan karena energi aktivasi yang berbeda.
Kecepatan reaksi bergantung pada suhu karena jumlah molekul berenergi cukup untuk
bereaksi merupakan fungsi suhu.
Katalis mempengaruhi kecepatan reaksi (atau mempercepat reaksi) karena memperkecil
energi aktivasi.
Kegagalan-kegagalan teori tumbukan dalam menjelaskan kecepatan reaksi:
Molekul-molekul yang bereaksi mempunyai orientasi tertentu sebelum bereaksi.
Reaksi dapat berlangsung dalam beberapa tahap.
Energi aktivasi tidak saja terlokalisasi dalam ikatan yang akan diputuskan dalam reaksi,
namun juga dalam beberapa ikatan lainnya.
Teori tumbukan tidak dapat digunakan untuk reaksi yang terjadi pada permukaan katalitik.
Contoh:
Gunakan teori tumbukan untuk memprediksi kecepatan reaksi spesifik (k) dari reaksi dekomposisi
hidrogen iodida: 2 HI H
2
+ I
2
pada suhu 321,4
o
C. Asumsikan diameter tumbukan = 3,5 A
o
(= 3,5.10
-8
cm) dan energi aktivasi reaksi = 44000 kal/mol. Evaluasi juga, berapakah harga faktor
frekuensi tumbukan yang dihasilkan!
Penyelesaian:
M
A
= M
B
= M
HI
= 128 Ea = E = 44000 kal/mol
d
AB
= 3,5 . 10
-8
cm T = 321,4
o
C + 273 = 594,4 K
R = 8,314 J/mol.K = 8,314 .10
7
erg/mol.K = 1,987 kal/mol.K
T R
E
B A
B A
2
AB
e
M M
M M
T R 8 d k
2
1
+
=
) 4 , 594 ( ) 987 , 1 (
44000
7 2 8
e
128
2
) 4 , 594 ( ). 10 . 314 , 8 .( 8 ) 10 . 5 , 3 ( k
2
1
=
k = 1,7 . 10
-10
e
-37,4
cm
3
/molekul.detik
Untuk mengubah satuan k menjadi liter/mol.detik, maka angka yang diperoleh di atas harus
dikalikan bilangan Avogadro (= 6,02.10
23
molekul/mol) dan dibagi dengan 1000, sehingga:
ik det . mol / liter 10 . 7 , 5 e . 10 . 02 , 1
1000
10 . 02 , 6
. e . 10 . 7 , 1 k
6 4 , 37 11
23
4 , 37 10
= = =
Dengan demikian, harga kecepatan reaksi spesifik (k) pada kasus ini sebesar 5,7.10
-6
liter/mol.detik dengan faktor frekuensi tumbukan (A) sebesar 1,02.10
11
liter/mol.detik.
dy/teori kinetika reaksi kimia/2007/halaman 3 dari 5 halaman
TEORI KOMPLEKS AKTIF (KEADAAN TRANSISI)
Menurut teori ini, reaksi diawali dengan tumbukan antara molekul-molekul reaktan. Sebelum
membentuk produk reaksi, molekul-molekul yang bereaksi membentuk kompleks teraktifkan yang
berada dalam keadaan kesetimbangan termodinamika dengan molekul reaktan.
Beberapa hal yang berkaitan dengan teori kompleks aktif:
Molekul-molekul memiliki energi vibrasi, rotasi, dan translasi.
Tumbukan antar reaktan menghasilkan kompleks aktif (keadaan transisi), kemudian
terdekomposisi menghasilkan produk.
Kompleks aktif berkesetimbangan dengan reaktan.
Tahap yang mengendalikan kecepatan reaksi (rate limiting step) adalah tahap dekomposisi
kompleks aktif menjadi produk.
Tinjau reaksi homogen : A + B produk reaksi ... (1)
Jika reaksi tersebut mempunyai mekanisme 2 tahap sebagai berikut:
(i) Tahap pembentukan kompleks aktif AB* dari reaktan A dan B:
A + B AB* (K*) ... (8)
(ii) Tahap dekomposisi/penguraian AB* menjadi produk reaksi:
AB* produk reaksi (lambat) ... (9)
Karena AB* berkesetimbangan dengan reaktan, maka konsentrasi AB* ditentukan dari konstanta
kesetimbangan reaksi tahap (i). Kecepatan reaksi overall ditentukan dari kecepatan dekomposisi
AB*, karena merupakan rate limiting step (tahap yang berlangsung paling lambat).
Tahap (ii) lambat, sehingga menentukan atau mengendalikan kecepatan reaksi:
r = C
AB*
... (10)
Tahap (i) cepat dan mencapai kesetimbangan, maka dalam term aktivitas a:
B A
* AB
B A
* AB
B A
* AB
C C
C
a a
a
* K
= = ... (11)
maka:
B A
AB
B A
* AB
C C * K C
= ... (12)
Substitusikan (12) ke (10) menghasilkan:
B A
AB
B A
C C * K r
= ... (13)
Berdasarkan pendekatan termodinamika pada keadaan kesetimbangan: * K ln T R * G = ... (14)
atau:
T R
* G
e * K
= ... (15)
Substitusikan (15) ke (13):
B A
T R
* G
AB
B A
C C e r
= ... (16)
Besarnya :
h
T k
B
= ... (17)
dengan: k
B
konstanta Boltzmann (= 1,38.10
-16
erg/K)
h konstanta Planck (=6,624.10
-27
erg.detik)
Substitusikan (17) ke (16), maka:
B A
T R
* G
AB
B A B
C C e
h
T k
r
= ... (18)
Dari definisi termodinamika (pada kondisi isotermal atau T tetap): S T H G = ... (19)
Substitusikan (19) ke (18), maka:
B A
R
* S
T R
* H
AB
B A B
C C e e
h
T k
r
= ... (20)
atau:
B A
T R
* H
R
* S
AB
B A B
C C e e
h
T k
r
= ... (21)
Faktor frekuensi
tumbukan (atau faktor
pre-eksponensial)
faktor
eksponensial
Konstanta kecepatan reaksi, k
(temperature-dependent term)
concentration-dependent term
dy/teori kinetika reaksi kimia/2007/halaman 4 dari 5 halaman
Contoh:
Dengan teori keadaan transisi dan data termodinamika berikut ini, hitunglah konstanta kecepatan
reaksi fase gas dari reaksi dekomposisi dimetileter (CH
3
OCH
3
) pada suhu 780 K.
H* = 56900 kal/mol; S* = 2,5 kal/mol.K
Gunakan pendekatan keadaan gas ideal.
Penyelesaian:
Harga k yang diprediksi dengan teori kompleks aktif:
T R
* H
R
* S
AB
B A B
e e
h
T k
k
=
Jika gas-gas dianggap sebagai gas ideal, maka:
A
=
B
=
AB*
= 1
sehingga:
) 780 ( ) 987 , 1 (
56900
987 , 1
5 , 2
27
16
e e ) 1 (
ik det . erg 10 . 624 , 6
) K 780 ( ) K / erg 10 . 38 , 1 (
k
=
k = 1,625.10
13
3,535 . e
-36,84
k = 5,744.10
13
. 1,00.10
-16
k = 5,744.10
-3
detik
-1
Jadi, k = 5,744.10
-3
detik
-1
, dengan faktor frekuensi tumbukan sebesar A = .............. detik
-1
PERBANDINGAN DENGAN TEORI ARRHENIUS
Perhatikan harga-harga konstanta kecepatan reaksi (k) dalam persamaan (5) dan (21), dan ingatlah
kembali harga konstanta kecepatan reaksi berdasarkan persamaan Arrhenius (pada materi kuliah
sebelumnya). Ketiga harga k tersebut dapat diringkas dan dibandingkan sebagai berikut:
No. Teori pendekatan
Faktor frekuensi tumbukan
(faktor pre-eksponensial)
Faktor
eksponensial
1. Arrhenius A T
0
[ f(T)]
e
T R
Ea
2. Tumbukan
2
1
B A
B A
2
AB
M M
M M
T R 8 d
+
T
e
T R
E
3.
Kompleks aktif (atau
keadaan transisi)
R
* S
AB
B A B
e
h
T k
T
e
T R
* H
Keterangan: Ea = E = H* = energi aktivasi reaksi
Berdasarkan perbandingan tersebut di atas, terlihat bahwa harga k dapat dinyatakan dalam
persamaan umum:
T R
Ea
m
e T ' A k
= [0 m 1] ... (22)
dengan:
m
T ' A = A = faktor frekuensi tumbukan (faktor pre-eksponensial) ... (23)
Perhatikan bahwa:
Pada persamaan Arrhenius, harga A tidak dipengaruhi oleh suhu (atau, m = 0)
Pada teori tumbukan, harga A sebanding dengan suhu dipangkatkan (atau, m = )
Pada teori kompleks aktif, harga A sebanding dengan suhu pangkat 1 (atau, m = 1)
Pada versi yang lebih kompleks, harga m dapat berada pada rentang: 0 m 3 sampai dengan 4
Sungguhpun demikian, pada umumnya faktor eksponensial (
T R
Ea
e
) jauh lebih sensitif
terhadap adanya perubahan suhu dibandingkan dengan faktor pre-eksponensial (
m
T ' A ).
Dengan demikian, persamaan (22) dapat dianggap identik dengan persamaan Arrhenius:
T R
Ea
e A k
= ... (24)
Kesimpulannya: Teori atau hukum Arrhenius memberikan pendekatan yang cukup baik tentang
kebergantungan harga konstanta kecepatan reaksi terhadap suhu (berdasarkan
teori tumbukan dan teori kompleks aktif).
dy/teori kinetika reaksi kimia/2007/halaman 5 dari 5 halaman
Contoh:
Suatu reaksi mempunyai energi aktivasi sebesar 65 kJ mol
-1
. Kecepatan reaksinya pada suhu 100
o
C
adalah 7,8 x 10
-2
mol L
-1
detik
-1
. Dengan persamaan Arrhenius:
(a) pada suhu berapakah kecepatan reaksinya menjadi sepersepuluh dari kecepatan pada 100
o
C?
(b) hitunglah kecepatan reaksi pada 20
o
C, jika data-data yang lain tetap.
(Coba kerjakanlah sendiri contoh soal ini sebagai latihan! Untuk mengecek hasil perhitungan
Saudara, jawaban soal ini: (a) T = 336 K (atau 63
o
C), dan (b) Kecepatan pada 20
o
C (293 K) = 2,6
x 10
-4
mol L
-1
detik
-1
)
ENERGI AKTIVASI REAKSI
Energi aktivasi reaksi merupakan energi minimum yang harus dimiliki oleh molekul-molekul
reaktan agar menghasilkan reaksi jika saling bertumbukan. Hanya molekul-molekul yang memiliki
energi yang sama dengan atau lebih besar dari energi aktivasi Ea yang dapat menghasilkan reaksi
Dari persamaan (24), dapat dilihat bahwa:
e
T R
Ea
merupakan fraksi molekul yang mempunyai energi sebesar Ea atau lebih besar.
Jika Ea bertambah, maka
e
T R
Ea
berkurang; yang berarti bahwa semakin banyak energi yang
diperlukan dan semakin sukar bagi molekul-molekul untuk mencapai energi ini.
Jika suhu bertambah, maka
e
T R
Ea
bertambah (atau k bertambah besar).
Untuk reaksi yang molekul reaktannya mempunyai banyak ikatan yang perlu
diputuskan, maka energi aktivasinya besar.
Jika hanya sedikit ikatan yang perlu diputuskan, maka energi aktivasinya kecil.
Untuk reaksi tanpa pemutusan ikatan, misalnya: H
+
+ OH
-
H
2
O, energi
aktivasinya sama dengan nol.
Beberapa hal penting yang berkaitan dengan energi aktivasi reaksi:
(1) Energi aktivasi reaksi (seperti yang ditentukan secara eksperimen) merupakan energi untuk
jumlah reaksi secara keseluruhan, bukan masing-masing tahap reaksi. Energi aktivasi
reaksi merupakan selisih antara energi reaktan dan energi tertinggi dari keadaan teraktifkan
(atau keadaan transisi) dalam proses tersebut.
(2) Energi aktivasi untuk setiap tahap selalu berharga positif.
(3) Sesuai dengan distribusi Maxwell-Boltzmann tentang energi molekular, jika suhu
dinaikkan, maka kecepatan reaksi bertambah. Hal ini disebabkan oleh semakin banyaknya
tumbukan yang mempunyai energi lebih besar dari Ea.
Dengan kata lain: Kecepatan reaksi yang tinggi dapat dicapai pada suhu tinggi, harga Ea kecil,
harga A besar, dan/atau konsentrasi reaktan yang besar dalam tahap penentu
kecepatan reaksi.
Anda mungkin juga menyukai
- Bab 13. Chapter 13. Kesetimbangan Reaksi Kimia - Smith-VnanesDokumen79 halamanBab 13. Chapter 13. Kesetimbangan Reaksi Kimia - Smith-VnanesNicky Arwita100% (1)
- Laporan Resmi: Laboratorium Teknik KimiaDokumen34 halamanLaporan Resmi: Laboratorium Teknik KimiaErza NggaraBelum ada peringkat
- Rangkuman Redoks - Tetapan KesetimbanganDokumen1 halamanRangkuman Redoks - Tetapan KesetimbanganTalitha Puspa Kencana100% (1)
- Mekanisme Adsorpsi-DesorpsiDokumen2 halamanMekanisme Adsorpsi-DesorpsiMuhammad Isa100% (1)
- Bab 11 KatalisDokumen7 halamanBab 11 KatalisDwi Septiani PutriBelum ada peringkat
- KSPDokumen17 halamanKSPAristy MirandaBelum ada peringkat
- Kinetika Dan Katalisis: Prodi Teknik Kimia Fti Upn "Veteran" YogyakartaDokumen32 halamanKinetika Dan Katalisis: Prodi Teknik Kimia Fti Upn "Veteran" YogyakartaAreIf Cron BmxStreetBelum ada peringkat
- Panas Pelarutan Laporan TetapDokumen14 halamanPanas Pelarutan Laporan TetapMuhammad Nurrizman AlfariziBelum ada peringkat
- ElektrodeposisiDokumen3 halamanElektrodeposisiMuhammad BalyanBelum ada peringkat
- TK2202 - Teknik Reaksi Kimia IDokumen29 halamanTK2202 - Teknik Reaksi Kimia Ifebri setyawanBelum ada peringkat
- Rangkuman KatalisDokumen6 halamanRangkuman KatalisLora Trismigo PBelum ada peringkat
- ReaktorDokumen12 halamanReaktorHabib Maulana YasmintoBelum ada peringkat
- Bab 13 Kinetika KimiaDokumen54 halamanBab 13 Kinetika KimiaFadilla NovitaBelum ada peringkat
- Sifat Zat MurniDokumen31 halamanSifat Zat MurniCican Ari SandiBelum ada peringkat
- 2 - Dasar-Dasar Kinetika Reaksi Kimia - Gasal 2021-2022 - TimDokumen72 halaman2 - Dasar-Dasar Kinetika Reaksi Kimia - Gasal 2021-2022 - TimEvan Afrista Wiokartina PurbaBelum ada peringkat
- Laporan Praktikum Termodinamika SiskaDokumen54 halamanLaporan Praktikum Termodinamika SiskaSiskaamayaBelum ada peringkat
- Grup B 1631010133 1631010134 Height Equivalent of Theoritical Plate IsiDokumen31 halamanGrup B 1631010133 1631010134 Height Equivalent of Theoritical Plate IsiAnonymous VwgOyPXBelum ada peringkat
- Pseudo First OrderDokumen2 halamanPseudo First OrdermarisaaaBelum ada peringkat
- LTM Reaksi Kimia RumitDokumen4 halamanLTM Reaksi Kimia RumitRenantoPutraWijayaBelum ada peringkat
- Kesetimbangan KimiaDokumen5 halamanKesetimbangan KimiaNina RustianaBelum ada peringkat
- Evaluasi Hasil Analisis Efisiensi Kinerja Sistem EvaporatorDokumen6 halamanEvaluasi Hasil Analisis Efisiensi Kinerja Sistem EvaporatorNukaz PrabuBelum ada peringkat
- Sifat Fisik Dan Kimia Bahan Pembuat Sabun Dan Uji Karakteristik SabunDokumen10 halamanSifat Fisik Dan Kimia Bahan Pembuat Sabun Dan Uji Karakteristik SabunBila JambiBelum ada peringkat
- Konduktivitas Termal Dan Mekanisme Perpindahan EnergiDokumen33 halamanKonduktivitas Termal Dan Mekanisme Perpindahan EnergiAndykaBelum ada peringkat
- Makalah LedakanDokumen21 halamanMakalah LedakanRizki RomadhoniBelum ada peringkat
- Kinetika ReaksiDokumen19 halamanKinetika ReaksisyaidahanjarBelum ada peringkat
- Reaksi ElementerDokumen13 halamanReaksi ElementerĎƵiƙŕię Ʈħę Ęļ PƦoBelum ada peringkat
- Penentuan Orde Reaksi Dan Tetapan Laju ReaksiDokumen27 halamanPenentuan Orde Reaksi Dan Tetapan Laju ReaksioctaviadwiwahyuniBelum ada peringkat
- Pertemuan 3 - Penentuan Laju, Orde Dan Konstanta Laju ReaksiDokumen32 halamanPertemuan 3 - Penentuan Laju, Orde Dan Konstanta Laju ReaksirinjaniBelum ada peringkat
- Panas PelarutanDokumen8 halamanPanas PelarutanMoehammad Dihanzt T-zeroneBelum ada peringkat
- KINETIKA+REAKSI - Bahan AjarDokumen42 halamanKINETIKA+REAKSI - Bahan AjarSurya PradnyaBelum ada peringkat
- Bab 3 Hukum Laju Reaksi & Konsep Orde Reaksi - RevDokumen26 halamanBab 3 Hukum Laju Reaksi & Konsep Orde Reaksi - RevFiBelum ada peringkat
- Ligan Ammonia Dan AirDokumen7 halamanLigan Ammonia Dan AirsafiraadninaBelum ada peringkat
- Katalis HomogenDokumen25 halamanKatalis HomogenNataliakusumaDewi100% (1)
- Jurnal Praktikum Laju Reaksi Secra TitrasiDokumen14 halamanJurnal Praktikum Laju Reaksi Secra TitrasiPurnamadewi ErnaBelum ada peringkat
- Percobaan I Termo IciDokumen5 halamanPercobaan I Termo IciIdam Sulastri TelaumbanuaBelum ada peringkat
- 2-Volume Molar GasDokumen9 halaman2-Volume Molar GasnathalineoBelum ada peringkat
- Fugasitas Nadya ZulfaniDokumen11 halamanFugasitas Nadya Zulfaninadya zulfaniBelum ada peringkat
- Aktivitas Dan Koefisien AktivitasDokumen22 halamanAktivitas Dan Koefisien AktivitasYudis Tira DepariBelum ada peringkat
- Tugas Material 3.1Dokumen5 halamanTugas Material 3.1Anisa Fitri MuyasarohBelum ada peringkat
- Kinetika ReaksiDokumen16 halamanKinetika Reaksianisa riantiBelum ada peringkat
- TuuuDokumen44 halamanTuuuHasbi AsshidiqiBelum ada peringkat
- Laporan Kerja PraktekDokumen17 halamanLaporan Kerja PraktektaufikrachmansusantoBelum ada peringkat
- Percobaan 1 (CSTR)Dokumen19 halamanPercobaan 1 (CSTR)Dicky PortgaceBelum ada peringkat
- TK2202 - Teknik Reaksi Kimia 1 - UTS 2 - CompiledDokumen35 halamanTK2202 - Teknik Reaksi Kimia 1 - UTS 2 - Compiledpanji rahmanBelum ada peringkat
- Bab I Pendahuluan Neraca Massa Dan EnergiDokumen4 halamanBab I Pendahuluan Neraca Massa Dan EnergiROMABelum ada peringkat
- Tugas 6Dokumen10 halamanTugas 6AchdanBelum ada peringkat
- Azeotrop - K ValuesDokumen24 halamanAzeotrop - K ValuesAraBelum ada peringkat
- Diagram Fase HeliumDokumen7 halamanDiagram Fase HeliumMia Kristina DamayantiBelum ada peringkat
- Kelompok 2 KAF-Prinsip Reaksi Kimia 9-14Dokumen6 halamanKelompok 2 KAF-Prinsip Reaksi Kimia 9-14devy ridaBelum ada peringkat
- Difusi Fasa GasDokumen40 halamanDifusi Fasa GasWindy NainggolanBelum ada peringkat
- MTKDokumen279 halamanMTKannisa sabrilaBelum ada peringkat
- Ekstraksi Padat CairDokumen5 halamanEkstraksi Padat CairNunee AyuBelum ada peringkat
- Neraca Massa Dengan Banyak Unit ProsesDokumen20 halamanNeraca Massa Dengan Banyak Unit ProsesalmengarunBelum ada peringkat
- 04 - Handout Teori Kinetika ReaksiDokumen8 halaman04 - Handout Teori Kinetika Reaksiputri chairaniBelum ada peringkat
- Pertemuan - 3 - Dasar2 Kinetika Reaksi - Bagian 2Dokumen30 halamanPertemuan - 3 - Dasar2 Kinetika Reaksi - Bagian 2EmitalutfiahBelum ada peringkat
- PPM TeoriDokumen17 halamanPPM TeorizeriBelum ada peringkat
- KRKdK-Kinetika Reaksi Kimia-Oleh Mustain Zamhari p10 ...Dokumen20 halamanKRKdK-Kinetika Reaksi Kimia-Oleh Mustain Zamhari p10 ...dendi osfaldoBelum ada peringkat
- Bab 2 Kinetika KimiaDokumen69 halamanBab 2 Kinetika KimiaFitrianti Aamiin100% (2)
- Tugas TRK Terjemah - Ega Assyifa G - 3EGBDokumen8 halamanTugas TRK Terjemah - Ega Assyifa G - 3EGBega assyifaBelum ada peringkat
- Stabilitas Kimia Kuliah s1Dokumen66 halamanStabilitas Kimia Kuliah s1bogoshipoBelum ada peringkat