Makalah Kimia
Diunggah oleh
Nurul AfriantiJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Makalah Kimia
Diunggah oleh
Nurul AfriantiHak Cipta:
Format Tersedia
MAKALAH KIMIA
TENTANG FUNGSI LARUTAN PENYANGGA DAN CONTOH DALAM KEHIDUPAN SEHARI-HARI
D I
S U S U N OLEH NAMA:NELVA YANTI KELAS:IX IPA 1
SMA NEGERI 2 BANGKINANG BARAT Tp.2011/2012
KATA PENGANTAR
Alhamdulillah dan puji syukur kehadirat allah swt kami ucapkan terima kasih.tanpa ridho allah mustahil saya bisa membuat makalah ini. Makalah ini adalah tugas yang sangat berat,walaupun demikian saya harus melakukannya demi terwujudnya siswa yang berprestasi. Akhirnya sesuai pepatah Tak ada manusia yang tak bersalah,jadi mohon maaf jika ada penulisan yang salah.
DAFTAR ISI
KATA PENGANTAR .. DAFTAR ISI . 1.Fungsi larutan penyangga.... 2.Larutan penyangga dalam kehidupan sehari hari.
fungsi larutan penyangga dalam kehidupansehari hari
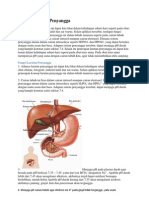
1.Darah Sebagai Larutan Penyangga Ada beberapa faktor yang terlibat dalam pengendalian pH darah, diantaranya penyangga karbonat, penyangga hemoglobin dan penyangga fosfat . aPenyangga Karbonat Penyangga karbonat berasal dari campuran asam karbonat (H2CO3) dengan basakonjugasi bikarbonat (HCO3). H2CO3 (aq)--> HCO3(aq)+ H+(aq) Penyangga karbonat sangat berperan penting dalam mengontrol pH darah.Pelarimaraton dapat mengalami kondisiasidosis, yaitu penurunan pH darah yangdisebabkan oleh metabolisme yang tinggi sehingga meningkatkan produksi ion bikarbonat. Kondisi asidosis ini dapat mengakibatkan penyakit jantung, ginjal,diabetes miletus (penyakit gula) dan diare.Orang yang mendaki gunung tanpaoksigen tambahan dapat menderita alkalosis, yaitu peningkatan pH darah.Kadar oksigen yang sedikit di gunung dapat membuat para pendaki bernafas lebih cepat,sehingga gas karbondioksida yang dilepas terlalu banyak, padahal CO2dapat larutdalam air menghasilkan H2CO3.Hal ini mengakibatkan pH darah akan naik. Kondisi alkalosis dapat mengakibatkanhiperventilasi(bernafas terlalu berlebihan,kadang-kadang karena cemas dan histeris). b.Penyangga Hemoglobin Pada darah, terdapat hemoglobin yang dapat mengikat oksigen untuk selanjutnyadibawa ke seluruh sel tubuh.Reaksi kesetimbangan dari larutan penyangga oksihemoglobin adalah:HHb + O2 (g)mHbO2-+ H+ Asam hemoglobin ion aksi hemoglobinKeberadaan oksigen pada reaksi di atas dapat memengaruhi konsentrasi ion H ,sehingga pH darah juga dipengaruhi olehnya .Pada reaksi di atas O2bersifat basa.Hemoglobin yang telah melepaskan O2 dapat mengikat H+dan membentuk asamhemoglobin.Sehingga ion H+yang dilepaskan pada
peruraian H2CO3merupakanasam yang diproduksi oleh CO2yang terlarut dalam air saat metabolisme.
c.Penyangga Fosfat Pada cairan intra sel, kehadiran penyangga fosfat sangat penting dalam mengatur pHdarah.Penyangga ini berasal dari campuran dihidrogen fosfat (H2PO4-) denganmonohidrogen fosfat (HPO32-). H2PO4 - (aq)+ H+ (aq) "H2PO4(aq) H2PO4(aq)+OH-(aq)--> HPO42-(aq))+ H2O(aq) Penyangga fosfat dapat mempertahankan pH darah 7,4 . Penyangga di luar sel hanyasedikit jumlahnya, tetapi sangat penting untuk larutan penyangga urin. 1.Air Ludah sebagai Larutan Penyangga Gigi dapat larut jika dimasukkan pada larutan asam yang kuat.Email gigi yang rusak dapat menyebabkan kuman masuk ke dalam gigi.Air ludah dapat mempertahankan pH pada mulut sekitar 6,8.Air liur mengandung larutan penyangga fosfat yang dapatmenetralisir asam yang terbentuk dari fermentasi sisa-sisa makanan. 2.Menjaga keseimbangan pH tanaman. Suatu metode penanaman dengan media selain tanah, biasanya ikerjakan dalam kamar kaca dengan menggunakan mendium air yang berisi zat hara, disebutdengan hidroponik .Setiap tanaman memiliki pH tertentu agar dapat tumbuh dengan baik . Oleh karena itu dibutuhkan larutan penyangga agar pH dapat dijaga. 3.Larutan Penyangga pada Obat-Obatan Asam asetilsalisilat merupakan komponen utama dari tablet aspirin, merupakan obat penghilang rasa nyeri.Adanya asam pada aspirin dapat menyebabkan perubahan pH pada perut.Perubahan pH ini mengakibakan pembentukan hormon, untuk merangsang penggumpalan darah, terhambat; sehingga pendarahan tidak dapat dihindarkan.Oleh karena itu, pada aspirin ditambahkan MgO yang dapat mentransfer kelebihan asam Hidrolisis dalam Kehidupan Sehari-hari Aplikasi Konsep hidrolisis dalam kehidupan misalnya adalah:
1. Pelarutan sabun Garam natrium stearat, C17H 35COONa (sabun cuci) akan mengalami hidrolisis jikadilarutkan dalam air , menghasilkan asam stearat dan basanya NaOH. Reaksi: C17H35COONa + H 2O C17H 35COOH + NaOH Oleh karena itu, jika garam tersebut digunakan untuk mencuci, airnya harus bersihdan tidak mengandung garam Ca 2+ atau Mg 2+.garam Ca 2+ dan Mg 2+ banyak terdapat dalam air sadah.Jika air yang digunakan mengandung garam garam Ca 2+,terjadi reaksi 2(C17H 35COOH) + Ca 2+ (C17H 35COO) 2 + H + Sehingga buih yang dihasilkan sangat sedikit.Akibatnya, cucian tidak bersih karenafungsi buih untuk memperluas permukaan kotoran agar mudah larut dalam air . 2. Penjernihan air Penjernihan air minum oleh PAM berdasarkan prinsip hidrolisis, yaitu menggunakansenyawa aluminium fosfat yang mengalamihidrolisis total. Fungsi Hidrolisis dalam Kehidupan Sehari-Hari Agar tanaman tumbuh dengan baik, maka pH tanaman harus dijagam pH tanah didaerah pertanian harus disesuaikan dengan pH tanamannya. Oleh karena itudiperlukan pupuk yang dapat menjaga pH tanah agar tidak terlalu asam atau basa. Biasanya para petani menggunakan pelet padat (NH4)2SO4untuk menurunkan pHtanah.Garam (NH4)2SO4bersifat asam, ion NH4 +akan terhidrolisis dalam tanahmembentuk NH3dan H+yang bersifat asam. Kita juga sering memakai bayclin atau sunklin untuk memutihkan pakaian kita. Produk ini mengandung kira-kira 5 % NaOCl yang sangat reaktif sehingga dapatmenghancurkan pewarna, sehingga pakaian menjadi putih kembali. Garam initerbentuk dari asam lemah HOCl dengan basa kuat NaOH.Ion OCl-terhidrolisismenjadi HOCl dan OH-, sehingga garam NaOCl bersifat basa. Hidrolisis ester-ester kompleks utuk membuat sabun Pembahasan ini berkaitan dengan hidrolisis basa (dengan menggunakan larutannatrium hidroksida) ester-ester besar yang ditemukan dalam lemak dan minyak hewani dan nabati. Jika ester-ester besar yang terdapat dalam lemak dan minyak hewani dan nabatidipanaskan dengan larutan natrium hdiroksida pekat, reaksi yang terjadi persis samadengan reaksi pada ester-ester sederhana. Terbentuk asam karboksilat kali ini, garam natrium dari sebuah asam besar sepertiasam oktadekanoat (asam stearat).Garam-garam ini merupakan komponen sabunyang penting yaitu komponen
yang melakukan pembersihan. Juga terbentuk alkohol kali ini, alkohol yang lebih rumit, propan1,2,3-triol(gliserol).
Anda mungkin juga menyukai
- Manfaat Gerakan Wudhu Untuk Kesehatan Tubuh ManusiaDari EverandManfaat Gerakan Wudhu Untuk Kesehatan Tubuh ManusiaPenilaian: 5 dari 5 bintang5/5 (3)
- Fungsi Larutan Penyangga Dan Hidrolisis Dalam KehidupanDokumen5 halamanFungsi Larutan Penyangga Dan Hidrolisis Dalam Kehidupanfaqih fatoni50% (2)
- Aplikasi Larutan PenyanggaDokumen6 halamanAplikasi Larutan PenyanggaMariati AbdullahBelum ada peringkat
- Fungsi Larutan PenyanggaDokumen4 halamanFungsi Larutan Penyanggarafi_17Belum ada peringkat
- Tugas Portofolio - Galih Taufik Nugraha 11 Ipa 4Dokumen6 halamanTugas Portofolio - Galih Taufik Nugraha 11 Ipa 4aristiawan herdiansyahBelum ada peringkat
- Fungsi Larutan PenyanggaDokumen4 halamanFungsi Larutan PenyanggaNur Desi YaniBelum ada peringkat
- Aplikasi Larutan Buffer PDFDokumen6 halamanAplikasi Larutan Buffer PDFYuliaDelestiBelum ada peringkat
- Fungsi Larutan PenyanggaDokumen11 halamanFungsi Larutan PenyanggaDesi Sari100% (1)
- RPP Larutan PenyanggaDokumen9 halamanRPP Larutan PenyanggaBurhan CfBelum ada peringkat
- Bahan Soal HidrolisisDokumen5 halamanBahan Soal HidrolisisAriny ZaqiyahBelum ada peringkat
- Larutan PenyanggaDokumen5 halamanLarutan PenyanggaDani IbrahimBelum ada peringkat
- Fungsi Larutan Penyangga Dalam Kehidupan SehariDokumen8 halamanFungsi Larutan Penyangga Dalam Kehidupan SehariDusfirah MajidBelum ada peringkat
- Sistem Buffer Tubuh ManusiaDokumen4 halamanSistem Buffer Tubuh ManusiabarbarBelum ada peringkat
- Aplikasi LarutanDokumen10 halamanAplikasi LarutanGinaa SonyaBelum ada peringkat
- Tugas Kimia KelompokDokumen3 halamanTugas Kimia KelompokAfit RiansyahBelum ada peringkat
- Aplikasi Larutan Buffer Dalam Kehidupan SehariDokumen5 halamanAplikasi Larutan Buffer Dalam Kehidupan SehariAnonymous iXl3xk0% (1)
- Sistem Buffer Tubuh ManusiaDokumen6 halamanSistem Buffer Tubuh ManusiaUpEngBelum ada peringkat
- Fungsi Larutan Penyangga UpDokumen4 halamanFungsi Larutan Penyangga Up7yuanBelum ada peringkat
- Aplikasi Larutan Buffer Dalam Kehidupan SehariDokumen11 halamanAplikasi Larutan Buffer Dalam Kehidupan SehariQorri HartantoBelum ada peringkat
- Artikel Kimia Tentang Peranan Larutan PenyanggaDokumen5 halamanArtikel Kimia Tentang Peranan Larutan PenyanggaAndinifth100% (2)
- Larutan PenyanggaDokumen6 halamanLarutan PenyanggaSevriadyBelum ada peringkat
- Fungsi Larutan PenyanggaDokumen3 halamanFungsi Larutan PenyanggaleajulianaBelum ada peringkat
- KimiaDokumen2 halamanKimiaRanti RahmawatiBelum ada peringkat
- Penerapan Larutan Penyangga Dalam KehidupanDokumen8 halamanPenerapan Larutan Penyangga Dalam KehidupanZefanya PapingkayBelum ada peringkat
- RahmadDokumen21 halamanRahmadGALUH SALVIABelum ada peringkat
- Fungsi Larutan PenyanggaDokumen2 halamanFungsi Larutan PenyanggacindyokhotanBelum ada peringkat
- Fungsi Larutan Penyangga Dalam KehidupanDokumen2 halamanFungsi Larutan Penyangga Dalam KehidupanKiki Kirun100% (1)
- Fungsi Larutan Penyangga Dalam Tubuh Makhluk HidupDokumen4 halamanFungsi Larutan Penyangga Dalam Tubuh Makhluk HidupAlvinFloppeeBelum ada peringkat
- Manfaat Larutan BufferDokumen6 halamanManfaat Larutan BufferRyzal AzizBelum ada peringkat
- Sistem Buffer TubuhDokumen14 halamanSistem Buffer TubuhMuhammad WahyuBelum ada peringkat
- Larutan PenyanggaDokumen3 halamanLarutan Penyanggadevilbath15Belum ada peringkat
- Tugas Perbaikan PKMBDokumen23 halamanTugas Perbaikan PKMBgusti ayuBelum ada peringkat
- Sistem BufferDokumen8 halamanSistem Buffer-Erna Kirei-Belum ada peringkat
- Sistem BufferDokumen20 halamanSistem BufferMust AgenkBelum ada peringkat
- Aplikasi Hidrolisis Dalam Kehidupan SehaDokumen2 halamanAplikasi Hidrolisis Dalam Kehidupan Sehalamtiur sihotangBelum ada peringkat
- Materi (Larutan Penyangga)Dokumen6 halamanMateri (Larutan Penyangga)YusafatBelum ada peringkat
- Larutan PenyanggaDokumen16 halamanLarutan PenyanggaCristianto SihombingBelum ada peringkat
- Konsep Asam BasaDokumen34 halamanKonsep Asam BasaMeri SeptianiBelum ada peringkat
- Larutan PenyanggaDokumen8 halamanLarutan PenyanggaBlue ManiaczBelum ada peringkat
- Komponen Larutan PenyanggaDokumen10 halamanKomponen Larutan PenyanggaInes Saraswati RudiantoBelum ada peringkat
- Air Liur (Saliva)Dokumen5 halamanAir Liur (Saliva)Evie Saswari TL TihanBelum ada peringkat
- Hidrolisis GaramDokumen9 halamanHidrolisis GaramAfaf AfiahBelum ada peringkat
- Makalah Gangguan Keseimbangan Asam BasaDokumen22 halamanMakalah Gangguan Keseimbangan Asam BasaNabila Ulfany Ulfa75% (4)
- Laporan Pendahuluan Ketidak Seimbangan Asam BasaDokumen24 halamanLaporan Pendahuluan Ketidak Seimbangan Asam BasaAbdul LatiifBelum ada peringkat
- Laporan Praktikum KimiaDokumen5 halamanLaporan Praktikum KimiadolphinpurpleBelum ada peringkat
- ScienceDokumen2 halamanScienceRafael SiahaanBelum ada peringkat
- Contoh Peristiwa Hidrolisis Dalam Kehidupan SehariDokumen1 halamanContoh Peristiwa Hidrolisis Dalam Kehidupan SehariKhusana NBelum ada peringkat
- Haidar Makalah Larutan PenyanggaDokumen8 halamanHaidar Makalah Larutan Penyanggadewi netBelum ada peringkat
- Modul Larutan PenyanggaDokumen12 halamanModul Larutan PenyanggaRETNO EKA NIANTIBelum ada peringkat
- Sistem Dapar Darah PDFDokumen19 halamanSistem Dapar Darah PDFEka DhianaBelum ada peringkat
- BAB I Asam Basa KepDokumen17 halamanBAB I Asam Basa KepFifi RiskayaniBelum ada peringkat
- Makalah Keseimbangan AsamDokumen15 halamanMakalah Keseimbangan AsamYunita TaelBelum ada peringkat
- Soal PretestDokumen3 halamanSoal PretestAisyah IndahBelum ada peringkat
- Ilmu Dasar Keperawatan Khasbi HusainDokumen25 halamanIlmu Dasar Keperawatan Khasbi HusainHusain BankBelum ada peringkat
- Makalah MegaDokumen18 halamanMakalah MegadendiBelum ada peringkat
- Sistem BufferDokumen13 halamanSistem BufferLida PratamaBelum ada peringkat
- Kesemibangan Asam BasaDokumen38 halamanKesemibangan Asam BasaAhmad Dailah SudrajatBelum ada peringkat