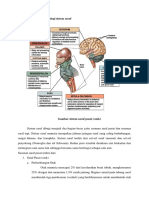
Mekanisme Terjadinya Kejang
Mekanisme Terjadinya Kejang
Diunggah oleh
Andi Pratiwi Indah LestariJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Mekanisme Terjadinya Kejang
Mekanisme Terjadinya Kejang
Diunggah oleh
Andi Pratiwi Indah LestariHak Cipta:
Format Tersedia
Mekanisme Terjadinya Kejang pada Masa Anak
Mahasiswa Fakultas kedokteran Universitas Kristen Krida Wacana
Jl. Arjuna Utara No.6, Jakarta Barat 11510
No. Telp (021) 5694-2061
Fax: (021) 563-1731
___________________________________________________________________________
Abstract
Febrile seizures are seizures associated with fever and age. It says a fever when the body
temperature above 380 C. Usually febrile seizures occurred at age 3 to 5 years and most at the age of
14-18 months. Febrile seizures are common disorders in children. Seizures can also occur due to
infection of the lining of the meninges which can be determined by performing a lumbar puncture.
Key words: febrile seizure, lumbar puncture
Abstrak
Kejang demam adalah bangkitan kejang terkait dengan demam dan umur. Dikatakan demam
apabila suhu tubuh diatas 380 C. Biasanya kejang demam terjadi pada umur 3 sampai 5 tahun dan
terbanyak pada umur 14-18 bulan. Kejang demam merupakan kelainan tersering pada anak. Kejang
juga dapat terjadi akibat adanya infeksi pada lapisan dari meninges yang dapat diketahui
dengan cara melakukan lumbal pungsi.
Kata kunci: kejang demam, lumbal pungsi.
BAB I
PENDAHULUAN
Kejang-kejang merupakan gangguan neurologis yang lazim pada kelompok umur
pediatri dan terjadi dengan frekuensi 4-6 kasus/1.000 anak. Kejang ini merupakan penyebab
yang paling lazim untuk rujukan praktek neurologi anak. Adanya gangguan kejang tidak
merupakan diagnosis tetapi gejala suatu gangguan sistem saraf sentral (SSS) yang mendasari
yang memerlukan pengamatan menyeluruh dan rencana manajemen.
Pada kebanyakan anak, etiologi untuk kejang tidak dapat ditentukan, dan dibuat
diagnosis epilepsi idiopatik. Walaupun hasil akhir pada kebanyakan kejang tidak
terkomplikasi pada anak adalah baik, sejumlah kecil mengalami kejang-kejang menetap yang
1 | Mekanisme Terjadinya Kejang pada Masa Anak
refrakter terhadap obat, dan ini merupakan tantangan diagnostik dan manajemen. Istilah
kejang dan konvulsi dapat secara tidak benar digunakan secara bergantian dengan epilepsi.
Kejang (konvulsi) di definisikan sebagai gangguan fungsi otak tanpa sengaja
parosismal yang dapat nampak sebagai gangguan atau kehilangan kesadaran, aktivitas
motorik abnormal, kelainan perilaku, gangguan sensoris atau disfungsi autonom. Beberapa
kejang ditandai oleh gerakan abnormal tanpa kehilangan atau gangguan kesadaran. Epilepsi
didefinisikan sebagai kejang berulang yang tidak terkait dengan demam atau serangan otak
akut.
BAB II
ISI PEMBAHASAN
KEJANG DEMAM
Kejang demam jarang terjadi pada epilepsi, dan kejang demam ini secara spontan
sembuh tanpa terapi tertentu. Kejang demam ini merupakan gangguan kejang yang paling
lazim pada masa anak, dengan prognosis yang sangat baik secara seragam. Namun, kejang
demam dapat menandakan penyakit akut serius yang mendasari seperti sepsis atau menigitis
bakteria sehingga setiap anak harus diperiksa secara cermat dan secara tepat diamati
mengenai penyebab demam yang menyertai.
Kejang demam adalah tergantung umur dan jarang sebelum umur 9 bulan dan sesudah
umur 5 tahun. puncak umur mulainya adalah sekitar 14-18 bulan dan insiden mendekati 3-4%
anak kecil. Ada riwayat kejang demam keluarga yang kuat pada saudara kandung dan orang
tua, menunjukkan kecenderungan genetik. Penelitian binatang menunjukkan bahwa
vasopresin arginin dapat merupakan mediator penting pada patogenesis kejang akibat
hipertermia.1
Kejang yang terkait dengan kenaikan suhu yang cepat dan biasanya berkembang bila
suhu tubuh mencapai 390C atau lebih. Suhu tubuh kita diatur oleh sebuah pengatur suhu yang
terletak di otak tepatnya dibagian hipotalamus tepatnya dibagian pre optik anterior (pre =
2 | Mekanisme Terjadinya Kejang pada Masa Anak
sebelum, anterior = depan). Hipotalamus sendiri merupakan bagian dari deinsephalon yang
merupakan bagian dari otak depan kita (prosencephalon).
Hipotalamus dapat dikatakan sebagai mesin pengatur suhu (termostat tubuh) karena
disana terdapat reseptor (penangkap, perantara) yang sangat peka terhadap suhu yang lebih
dikenal dengan nama termoreseptor (termo = suhu). Dengan adanya termorespetor ini, suhu
tubuh dapat senatiasa berada dalam batas normal yakni sesuai dengan suhu inti tubuh. Suhu
inti tubuh merupakan pencerminan dari kandungan panas yang ada di dalam tubuh kita.
Kandungan panas didapatkan dari pemasukan panas yang berasal dari proses metabolisme
makanan yang masuk ke dalam tubuh. Pada umumnya suhu inti berada dalam batas 36,5-
37,5°C.
Dalam berbagai aktivitas sehari-hari, tubuh kita juga akan mengelurakan panas
misalnya saat berolahraga. Bilamana terjadi pengeluraan panas yang lebih besar
dibandingkan dengan pemasukannya, atau sebaliknya maka termostat tubuh itu akan segera
bekerja guna menyeimbangkan suhu tubuh inti. Bila pemasukan panas lebih besar daripada
pengeluarannya, maka termostat ini akan memerintahkan tubuh kita untuk melepaskan panas
tubuh yang berlebih ke lingkungan luar tubuh salah satunya dengan mekanisme berkeringat.
Dan bila pengeluaran panas melebihi pemasukan panas, maka termostat ini akan berusaha
menyeimbakan suhu tersebutdengan cara memerintahkan otot-otot rangka kita untuk
berkontraksi (bergerak) guna menghasilkan panas tubuh.
Kontraksi otot-otot rangka ini merupakan mekanisme dari menggigil. Contohnya,
seperti saat kita berada di lingkungan pegunungan yang hawanya dingin, tanpa kita sadari
tangan dan kaki kita bergemetar (menggigil). Hal ini dimaksudkan agar tubuh kita tetap
hangat. Karena dengan menggigil itulah, tubuh kita akan memproduksi panas. Hal diatas
tersebut merupakan proses fisiologis (keadaan normal) yang terjadi dalam tubuh kita
manakala tubuh kita mengalami perubahan suhu. Lain halnya bila tubuh mengalami proses
patologis (sakit). Proses perubahan suhu yang terjadi saat tubuh dalam keadaan sakit lebih
dikarenakan oleh zat toksis (racun) yang masuk kedalam tubuh.
Umumnya, keadaan sakit terjadi karena adanya proses peradangan (inflamasi) di
dalam tubuh. Proses peradangan itu sendiri sebenarnya merupakan mekanisme pertahanan
dasar tubuh terhadap adanya serangan yang mengancam keadaan fisiologis tubuh. Proses
peradangan diawali dengan masuknya racun kedalam tubuh kita. Contoh racun yang paling
mudah adalah mikroorganisme penyebab sakit. Mikroorganisme (MO) yang masuk kedalam
3 | Mekanisme Terjadinya Kejang pada Masa Anak
tubuh umumnya memiliki suatu zat toksin/racun tertentu yang dikenal sebagai pirogen
eksogen.
Dengan masuknya MO tersebut, tubuh akan berusaha melawan dan mencegahnya
yakni dengan memerintahkan tentara pertahanan tubuh antara lain berupa leukosit, makrofag,
dan limfosit untuk memakannya (fagositosit). Dengan adanya proses fagositosit ini, tentara-
tentara tubuh itu akan mengelurkan senjata berupa zat kimia yang dikenal sebagai piroge
endogen (khususnya interleukin 1/ IL-1) yang berfungsi sebagai anti infeksi. Pirogen endogen
yang keluar, selanjutnya akan merangsang sel-sel endotel hipotalamus (sel penyusun
hipotalamus) untuk mengeluarkan suatu substansi yakni asam arakhidonat. Asam arakhidonat
bisa keluar dengan adanya bantuan enzim fosfolipase A2.2
Proses selanjutnya adalah, asam arakhidonat yang dikeluarkan oleh hipotalamus akan
pemacu pengeluaran prostaglandin (PGE2). Pengeluaran prostaglandin pun berkat bantuan
dan campur tangan dari enzim siklooksigenase(COX). Pengeluaran prostaglandin ternyata
akan mempengaruhi kerja dari termostat hipotalamus. Sebagai kompensasinya, hipotalamus
selanjutnya akan meningkatkan titik patokan suhu tubuh (di atas suhu normal).1,2
Adanya peningkatan titik patakan ini dikarenakan mesin tersebut merasa bahwa suhu
tubuh sekarang dibawah batas normal. Akibatnya terjadilah respon dingin/ menggigil.
Adanya proses mengigil ini ditujukan utuk menghasilkan panas tubuh yang lebih banyak.
Adanya perubahan suhu tubuh di atas normal karena memang setting hipotalamus yang
mengalami gangguan oleh mekanisme di atas inilah yang disebut dengan demam atau febris.
Demam yang tinggi pada nantinya akan menimbulkan manifestasi klinik (akibat) berupa
kejang (umumnya dialami oleh bayi atau anak-anak yangdisebut dengan kejang demam)
Kejang khas menyeluruh, tonik-klonik lama beberapa detik sampai 10 menit, diikuti
dengan periode mengantuk singkat pascakejang. Kejang demam yang menetap lebih lama
dari 15 menit menunjukkan penyebab organik seperti proses infeksi atau toksis dan
memerlukan pengamatan menyeluruh. Ketika demam tidak lagi ada pada saat anak sampai
dirumah sakit, tanggung jawab dokter yang paling penting adalah menentukan penyebab
demam dan mengesampingkan meningitis. Jika ada keragu-raguan berkenaan dengan
kemungkinan meningitis, pungsi lumbal dengan pemeriksaan cairan serebrospinalis (CSS)
terindikasi. Infeksi virus saluran pernapasan atas, roseola dan otitis media akut adalah
penyebab kejang demam yang paling sering.
4 | Mekanisme Terjadinya Kejang pada Masa Anak
EEG tidak diperlukan pascakejang demam sederhana karena rekamannya akan
membuktikan bentuk non-epileptik atau normal dan temuan tersebut tidak akan mengubah
manajemen. EEG terindikasi untuk kejang demam apitik atau pada anak yang berisiko untuk
berkembang epilepsi. Kejang demam atipik meliputi kejang yang menetap selama lebih dari
15 menit. Kejang berulang sekama beberapa jam atau hari, dan kejang setempat. Sekitar 50%
anak menderita kejang berulang dan sebagian kecil menderita kejang berulang berkali-kali.
Faktor resiko untuk perkembangan epilepsi sebagai komplikasi kejang demam adalah
riwayat epilepsi keluarga positif. Kejang demam awal sebelum umur 9 bulan, kejang demam
lama atau atipik, tanda perkembangan yang terlambat dan pemeriksaan neurologis abnormal.
Insidens epilepsi adalah sekitar 9% bila beberapa faktor risiko ada dibanding dengan insiden
1% pada anak yang menderita kejang demam dan tidak ada faktor risiko.1,2
Pada terapi pengelolaan rutin bayi normal yang menderita kejang demam sederhana
meliputi pencarian yang teliti terhadap penyebab demam. Cara-cara aktif untuk
mengendalikan demam termasuk penggunaan antipiretik, dan menenangkan orangtua.
Profilaksis antikonvulsan jangka pendek tidak terindikasi. Profilaksis antikonvulsan yang
lama untuk mencegah kejang demam berulang adalah perdebatan dan tidak lagi dianjurkan.
Antiepilepsi seperti fenitonin dan karbamazepin tidak efektif dalam pencegahan kejang
demam berulang dan dapat menurunkan fungsi kognitif pada anak yang diobati dibandingkan
dengan anak yang tidak diobati.
Natrium valproat efektif pada pengelolaan kejang demam, tetapi kemungkinan risiko
obat tidak membenarkan penggunaannya pada penyakit dengan pragnosis yang sangat baik
tanpa pengobatan. Diazeparn oral dianjurkan sebagai metoda yang efektif dan aman untuk
mengurangi risiko kejang demam berulang. Pada mulainya setiap sakit demam, diazeparn 0.3
mg/kg/8 jam peroral diberikan untuk selama sakit (biasanya 2-3 hari). Efek samping biasanya
ringan, tetapi gejala kelesuan, iritabilitas, dan ataksia dapat dikurangi dengan menyesuaikan
dosis.2
Apabila dilihat dari struktur organ target secara makro dapat diketahui penyusun
didalamnya adalah meninges, serebrum, dan medula spinalis. Meninges merupakan selaput
otak. Didalam meninges terdapat duramater yaitu lapisan yang paling kuat dan paling luar,
duramater terdiri dari 2 lapisan yaitu, lamina periosteal (sangat melekat dengan tulang
kepala), lamina meningeal (permukaan dalam yang licin). Kedua lapis duramater tersebut
menyatu kecuali pada saat membentuk sinus duramatris. Di dalam duramater terdapat sinus
5 | Mekanisme Terjadinya Kejang pada Masa Anak
terbesar yaitu sinus sagitalis superior. Duramater melekuk kedalam dan memisahkan cavum
cranii menjadi beberapa bagian. Di dalam profundal duramater terdapat arachnoidmater.
Disini terdapat spatium subdural (ruang potensial antara duramater dan arachnoidmater).3
Sedangkan spatium subarachnoid terisi LCS cairan cerebrospinal (liquor
cerebrospinalis) dan mengandung pembuluh darah yang mendarahi otak. Di ruangan
subarachnoid yang melebar terdapat sisterna karena lapisannya tidak mengikuti lekuk.
Sisterna ada di anterior dan posterior. Serta villi arachnoidales yang memungkinkan LCS
memasukkan sinus duramatris. Didalam meninges pun terdapat piamater yaitu lapisan paling
dalam yang menempel dan merupakan jaringan ikat yang sangat tipis. Piamater melekat erat
pada permukaan otak dan mengikuti gyrus dan sulcus otak.
Serebrum (otak besar) terdiri atas dua belahan yang disebut hemisfer (hemisphere)
ialah sebelah daripada kedua belahan yang membentuk serebrum atau serebelum (otak kecil)
yang terletak disebelah kaudal daripada serebrum. Kaudal berarti di sebelah atau di arah
ujung (ekor) sesuatu. Bila dilihat secara mikro serebrum dibagi menjadi hemisfer serebri kiri
dan kanan. Secara histologis terdiri dari enam lapisan yaitu lapisan molekular, lapisan
granular luar, lapisan sel-sel piramid, lapisan granular dalam, lapisan piramid/ganglioner dan
lapisan sel-sel multiform atau poliform. Semua lapis ini tidak mempunyai batas yang tegas
dan semua berisi neuroglia. Sel-sel di serebrum terdapat sel piramid, sel granuler, sel
horizontal dan sel martinotti.4
Sistem saraf pusat berfungsi untuk menerima dan mengintegrasikan semua rangsang
yang diterima di luar tubuh (eksteroseptif) dan dari dalam tubuh (interoseptif) melalui
reseptor-reseptor tertentu. Histologis SSP dibagi menjadi empat yaitu neuron, neuroglia, serat
saraf dan struktur tambahan. Neuron pada medula spinalis terletak di kolumnar berbentuk
huruf H (di substansi grisea). Pada otak terletak di lapisan permukaan korteks serebri
(substansi grisea). Pada serat saraf umumnya merupakan akson yang panjang dengan atau
tanpa mielin. Sedangkan struktur tambahan terdapat pembuluh darah, cairan serebrospinal,
dan selaput otak.
Apabila dilihat secara mikro otak dan medula spinalis terdiri atas dua lapisan yaitu
substansi grisea/kelabu dan substansi alba/putih. Di dalam substansi grisea/kelabu terdapat
perikarion dan serat saraf tidak bermielin sedangkan di dalam substansi alba/putih terdiri atas
akson yang bermielin. Di medula spinalis potongan melintang terdiri atas substansi alba
(sebelah luar) dan substansi grisea (sebelah dalam) berbentuk huruf H atau kupu-kupu.
6 | Mekanisme Terjadinya Kejang pada Masa Anak
Bagian tengah terhadap kanalis sentralis. Substansi alba berisi akson dan fungsi khusus yaitu
motorik dan sensoris yang disebut funikulus.
Ada tiga funikulus yaitu dorsal, ventral dan lateral. Sedangkan substansi grisea berisi
perikarion, banyak terdapat di sinaps neuron mempunyai sel saraf motorik yang merupakan
sel saraf multipolar. Neuron motorik terdapat di kornu anterior medula spinalis. Sel sarafnya
yaitu dendrit (mengandung substansi Nissl), akson (tidak mengandung S.Nissl/akson hilock)
dan inti beserta anak inti terlihat jelas, besar.5
Dilihat secara makro medula spinalis berawal pada foramen magnum, sebagai
lanjutan dari medula oblongata, dan meneruskan diri sampai setinggi vertebta lumbalis
pertama atau kedua. Medula spinalis terbungkus rapat oleh membran yang disebut pia mater
dan dikelilingi cairan serebrospinalis (LCS) yang merupakan lanjutan langsung LCS yang
mengelilingi otak.
LCS terisi dalam ruang yang tertutup oleh membran ganda – membran fibrosa luar
(dura mater) dan membran transparan halus (araknoid mater) yang melekat erat pada lapisan
dalamnya. ruang diantara membran – membran ini (ruang subdura) biasanya hanya
merupakan ruang potensial dan mempunyai arti praktis yang terbatas. Ruang yang berisi LCS
diantara araknoid mater dan medula spinalis terbungkus oleh pia mater dikenal sebagai ruang
subaraknoid atau ruang intradura. Dura (dan demikian juga ruang subaraknoid) meluas
sebagai pipa yang ujungnya tersembunyi setinggi vertebra sakralis kedua.4,5
Radiks nervus spinalis berjalan ke segmen tubuh di bawah foramen magnum
meninggalkan medula dan melintas melalui ruang subaraknoid. Terdapat 8 nervus servikalis,
7 | Mekanisme Terjadinya Kejang pada Masa Anak
12 nervus torakalis, 5 lumbalis, 5 sakralis, dan 1 koksigealis. Karena medula spinalis berakhir
setinggi L 2 pada orang dewasa, maka semua radiks nervus dibawah lumbah kedua (yaitu
yang membentuk pleksus lumbalis dan sakralis serta mempersarafi tungkai dan perineum)
melintas hampir vertikal ke bawah ruang subaraknoid dalam suatu serabut, yang umumnya
dikenal sebagai “kauda ekuina” (buntut kuda) sebelum meninggalkan foramina
intervertebralis masing-masing. Pada daerah ini nervus terendam dalam LCS dan disinilah
ruang subaraknoid paling mudah dimasuki dengan jarum yang diselipkan diantara vertebra
lumbalis, dan anestesi lokal disuntikkan untuk memberikan blok spinalis (subaraknoid).
Semua nervus torakalis (T1 sampai T2) memberikan serabut vasokonstrikor simpatis.
Ruang epidularis (atau ekstraduralis) terletak di dalam saluran dalam tulang vertebra,
di antara dura dan periosteum yang membatasi bagian dalam lamina vertebra. Periosteum dan
dua bergabung pada foramen magnum sehingga menutupi ruang epidura dibagian superior.
Sebaliknya ruang subaraknoid berlanjut ke kavum kranium. Ruang epiduralis dibatasi di
bagian inferior oleh hiatus sakralis yang tertutup oleh membrana sakrokoksigealis di apeks
tulang sakralis. Ruang epidura berisi nervus spinalis ketika mereka berjalan ke foramina
masing-masing dan juga berisikan jaringan alveolar, arteri dan pleksus vena.
Bagian ruang epidura yang terkandung di dalam bagian tulang sakralis disebut ruang
epidura kauda (atau sakralis). Karena dura mengandung LCS yang berakhir pada S2 pada
orang dewasa maka terdapat ruang diantara dura dengan membrana sakrooksigealis tempat
dimasukkannya penyuntikan anestesi lokal dengan aman sekali melalui membrana
sakrooksigealis.
Ruang paravertebralis dalam regio torakal dibatasi dibagian atas dan bawah oleh
periosteum iga dan dibagian lateral oleh ligamentum kostotransversum. Setiap ruang
paravertebralis torakalis menghantarkan nervus interkostalis masing-masing dari foramen
intervertebralis ke ruang interkostalis. Ruang paravertebralis sendiri-sendiri tidak
berhubungan langsung dengan ruang di atas dan dibawahnya, tetapi secara tidak langsung
melalui ruang epidura melalui foramina intervertebralis.
Pada regio lumbalis hubungan antara ruang menjadi lebih terbuka. Medula spinalis
merupakan bagian susunan saraf pusat yang terletak di dalam kanalis vertebralis dan
menjulur dari foramen magnum ke bagian atas region lumbalis. Trauma pada medula spinalis
dapat bervariasi dari trauma ekstensi fiksasi ringan yang terjadi akibat benturan secara
8 | Mekanisme Terjadinya Kejang pada Masa Anak
mendadak sampai yang menyebabkan transesksi lengkap dari medula spinalis dengan
quadriplegia.
MEKANISME KEJANG
Meskipun mekanisme kejang yang tepat belum diketahui, tampak ada beberapa faktor
fisiologi yang menyebabkan perkembangan kejang. Untuk memulai kejang, harus ada
kelompok neuron yang mampu menimbulkan ledakan discharge yang berarti dan sistem
hambatan GABergik. Perjalanan discharge (rabas) kejang akhirnya tergantung pada eksitasi
sinaps glutamaterik. Bukti baru-baru ini menunjukkan bahwa eksitasi neurotransmitter asam
amino (glutamat, asparatat) dapat memainkan peran dalam menghasilkan eksitasi neuron
dengan bekerja pada reseptor sel tertentu.5
Diketahui bahwa kejang dapat berasal dari daerah kematian neuron dan bahwa daerah
otak ini dapat meningkatkan perkembangan sinaps hipereksitabel baru yang dapat
menimbulkan kejang. Misalnya, lesi pada lobus temporalis (termasuk glioma tumbuh lambat,
hematoma, gliosis dan malformasi arteriovanosus) menyebabkan kejang. Dan bila jaringan
abnormal diambil secara bedah, kejang kemungkinan berhenti. Lebih lanjut, konvulsi dapat
ditimbulkan pada binatang percobaan dengan fenomena membangkitkan.
Pada model ini, stimulasi otak subkonvulsif berulang (misal amigdala) akhirnya
menyebabkan konvulsi menyeluruh. Pembangkitan dapat menyebabkan terjadinya epilepsi
pada manusia pasca cedera otak. Pada manusia telah diduga bahwa aktivitas kejang berulang
dari lobus temporalis abnormal dapat menimbulkan kejang pada lobus temporalis normal
kontralateral dengan pemindahan stimulus melalui korpus kollosum.
Kejang adalah lebih lazim pada bayi dan binatang percobaan imatur. Kejang tertentu
pada populasi pediatri adalah spesifik umur (misal spasme infantil) yang menunjukkan bahwa
otak yang kurang berkembang lebih rentan terhadap kejang spesifik daripada anak yang lebih
tua atau orang dewasa.
Faktor genetik menyebabkan setidaknya 20% dari semua kasus epilepsi familial telah
dikenali, termasuk konvulsi neonatus benigna, epilepsi mioklonik juvenil dan epilepsi
mioklonik progresif. Sangat mungkin bahwa dalam waktu dekat dasar molekuler epilepsi
tambahan seperti epilepsi rolandik benigna dan kejang-kejang linglung akan dikenali. Juga
9 | Mekanisme Terjadinya Kejang pada Masa Anak
diketahui bahwa substansia abu-abu akan memegang peranan integral pada terjadinya kejang
menyeluruh. Aktivitas kejang elektrografi menyebar dalam substansia abu-abu menyebabkan
peningkatan pada ambilan 2-deoksiglukosa, tetapi sedikit atau tidaknya aktivitas metabolik
dalam substansia abu-abu bila binatang imatur mengalami kejang. Telah diduga bahwa
imaturitas fungsional substansia abu-abu dapat memainkan peran pada peningkatan
kerentanan kejang otot imatur.4,5
Lagipula, neuron pars retikulata substansia asam-gama amiobutirat memainkan peran
pada pencegahan kejang. Agaknya bahwa saluran aliran keluar substansia abu-abu mengatur
memodulasi penyebaran kejang tetapi tidak menyebabkan mulainya kejang. Penelitian
tambahan mungkin akan memfokuskan pada penyebab hipereksitabilitas neuron, mekanisme
hambatan tambahan, pencairan mekanisme non sinapsis perambatan kejang dan kelainan
reseptor GABA.
Cara diagnosis kejang dapat dilihat dari pengamatan kejang tergantung pada banyak
faktor, termasuk umut penderita, tipe dan frekuensi kejang dan ada atau tidak adanya temuan
neurologis dan gejala yang bersifat dasar. Pemeriksaan minimum untuk kejang tanpa demam
pertama pada anak yang lainnya sehat meliputi glukosa puasa, kalsium, magnesium, elektrolit
serum dan EEG.
Peragaan discharge paroksismal pada EEG selama kejang klinis adalah diagnostik
epilepsi, tetapi kejang jarang terjadi dalam laboratorium EEG. EEG normal tidak
mengesampingkan diagnosis epilepsi, karena perekaman antar kejang normal pada sekitar
40% penderita. Prosedur aktivasi yang meliputi hiperventilasi, penutupan mata, stimulasi
cahaya, dan bila terindikasi, penghentian tidut dan penempatan elektrode khusus (misal
hantaran zigomatik) sangat meningkatkan hasil positif. Discharge kejang lebih mungkin
direkam pada bayi dan anak daripada remaja atau dewasa.5
Memonitor EEG lama dengan rekaman video aliran pendek dicadangkan pada
penderita yang terkomplikasi dengan kejang lama dan tidak responsif. Monitor EEG ini
memberikan metode yang tidak terhingga nilainya untuk perekaman kejadian yang jarang
diperoleh selama pemeriksaan EEG rutin. Teknik ini sangat membantu dalam kalsifikasi
kejang karena ia dapat secara tetap menentukan lokasi dan frekuensu discharge kejang saat
perubahan perekaman pada tingkat yang sadar dan adanya tanda klinis. Penderita dengan
kejang palsu dapat dengan mudah dibedakan dari kejang epilepsi sejati dan tipe kejang (misal
10 | Mekanisme Terjadinya Kejang pada Masa Anak
kompleks parsial dan menyeluruh) dapat lebih dikenali dengan tepat, yang adalah penting
oada pengamatan anak yang mungkin merupakan calon untuk pembedahan epilepsi.
Peran skenning CT atau MRI pada pengamatan kejang adalah kontroversial. Hasilnya
pada penggunaan rutin tindakan ini pada penderita dengan kejang tanpa demam pertama dan
pemeriksaan neurologis normal adalah dapat diabaikan. Pada pemeriksaan anak dengan
gangguan kejang kronis, hasilnya adalah serupa. Meskipun sekitar 30% anak ini
menunjukkan kelainan struktural (misal atrofi korteks setempat atau ventrikel dilatasi) hanya
sedikit sekali manfaat dari intervensi aktif sebagai akibat dari skenning CT.
Dengan demikian, skenning CT atau MRI harus dicadangkan untuk penderita yang
pemeriksaan neurologis abnormal. Kejang sebagian yang lama tidak mempan dengan terapi
antikonvulsan, defisit neurologis setempat dan bukti adanya kenaikan tekanan intrakranial
merupakan indikasi untuk pemeriksaan pencitraan saraf.
Pemeriksaan CSS terindikasi jika kejang berkemungkinan terkait dengan proses
infeksi, perdarahan subarknoid atau gangguan dermielinasi. Uji metabolik spesifik
digambarkan pada seksi mengenai kejang neonatus dan status epileptikus.
LUMBAL PUNGSI
Kembali pada kasus yang didapat, kejang-kejang yang dialami setelah satu minggu
panas tinggi segera dilakukan lumbal pungsi untuk diketahui apakah terdapat infeksi
didalamnya. Pungsi lumbal dikerjakan guna pemeriksaan sitologi bila terdapat kecurigaan
meningeal karsinomatosis atau meningeal limfomatosis. Sebagai sarana terapi, pungsi lumbal
dapat dikerjakan untuk memasukan methotrexate pada lekemia susunan saraf pusat, atau
amphotericine B untuk meningitis karena jamur mengurangi cairan serebrospinalis sebagai
terapi peningkatan tekanan intrakranial yang bersifat jinak (BIH) atau pada nyeri kepala
akibat perdarahan subaraknoidea.6
11 | Mekanisme Terjadinya Kejang pada Masa Anak
Pungsi lumbal tidak boleh dilakukan pada penderita dengan papiledema (funduskopi)
harus dilakukan setiap akan menentukan adanya sumbatan ruang subaraknoidea medula
spinalis. Pemeriksaan adanya sumbatan ruang subaraknoidea medula spinalis ditentukan
dengan menekan vena jugularis dan dilakukan pengukuran peningkatan dan penurunan
tekanan cairan serebrospinalis. Pemeriksaan dengan manometer tidak dikerjakan secara rutin
dan tidak pernah dilakukan bila terdapat peningkatan tekanan dasar (awal) atau dicurigai
adanya lesi masa.7
Posisi penderita sangat membantu keberhasilan pungsi lumbal. Penderita harus dalam
posisi fetal dengan punggung tegal lurus terhadap tempat tidur. Masukkan jarum ke bawah
kulit (setelah diberikan anestesi lokal) dan tentukan sudut tusukan jarum tersebut. Pastilah
arah jarum sejajar terhadap tempat tidur dan menyudut ke arah umbilikus penderita. Pada
penusukan lebih lanjut, bila jarum tidak masuk ke ruang subaraknoidea atau bila membentur
tulang, arah jarum tidak dapat berubah. Jarum tersebut ditarik kembali hingga sedikit
dibawah kulit dan coba arahkan kembali. Dengan berbagai pengalaman dapat dirasakan saat
jarum masuk ruang subaraknoidea.
Bila pungsi lumbal tidak mungkin dilakukan dalam posisi fetal, penderita didudukkan
dengan memeluk bantal, coba kembali pada posisi duduk (lebih mudah untuk menentukan
garis tengah). Perlu diingat bahwa pengukuran tekanan pada posisi duduk sulit
diinterpretasikan, untuk itu penderita ditidurkan kembali setelah jarum berhasil masuk ruang
subaraknoidea.8
Bila tidak mungkin dilakukan pungsi lumbal karena kelainan tulang atau infeksi lokal
tetapi pemeriksaan cairan serebrospinalis sangat diperlukan, lakukan pungsi sisternal atau
servikal dibawah bimbingan fluoroskopi.
12 | Mekanisme Terjadinya Kejang pada Masa Anak
BAB III
KESIMPULAN
Melalui makalah ini dapat disimpulkan, meskipun mekanisme kejang yang tepat
belum diketahui tetapi mekanisme kejang ini melibatkan sel-sel saraf yang terdapat di
otak. Kejang juga dapat terjadi akibat adanya infeksi pada lapisan dari meninges yang
dapat diketahui dengan cara melakukan lumbal pungsi. Kejang dapat memiliki
multifaktoral penyebab, yang sebenarnya disebabkan oleh adanya muatan listrik yang
terlalu banyak di dalam lapisan korteks serebri yang disebabkan neurotransmitter
inhibitorik berkurang dan neurotransmitter eksitatorik bertambah jumlahnya.
13 | Mekanisme Terjadinya Kejang pada Masa Anak
DAFTAR PUSTAKA
1. Behrman, Kliegman, Arvin. Nelson ilmu kesehatan anak. 15th Ed. Jakarta: EGC,
2000.h. 2059.
2. Corwin EJ. Patofisiologi. 3rd Ed. Jakarta: EGC, 2007.h. 391.
3. Sabiston DC. Buku ajar bedah. Jakarta: EGC, 1994.h. 498-9.
4. Shadily H. Ensiklopedia umum. Yogyakarta: Kanisius, 2012.h. 769.
5. Satyanegara, Hasan RY, Abubakar S, Maulana AJ, Sufarnap E, Benhadi I et al.
Ilmu bedah saraf satyanegara. 4th Ed. Jakarta: PT Gramedia Pustaka Umum,
2010.h. 17-9.
6. Boultan TB, Blog CE. Anestesiologi. 10th Ed. Jakarta: EGC, 1994.h. 123.
7. Weiner HL, Levitt LP. Buku saku neurologi. Jakarta: EGC, 2004.h. 248-51.
8. Rubenstein D, Wayne D, Bradcey J. Kedokteran klinis. 6th Ed Jakarta: Erlangga,
2003.h.101.
14 | Mekanisme Terjadinya Kejang pada Masa Anak
Anda mungkin juga menyukai
- Makalah PatofisiologiDokumen54 halamanMakalah PatofisiologiAdi Subagio100% (3)
- Saraf KranialDokumen12 halamanSaraf KranialTrinoval Yanto Nugroho, S.Kep100% (3)
- PERTUSISDokumen14 halamanPERTUSISJelita SihombingBelum ada peringkat
- Kanker TiroidDokumen22 halamanKanker TiroidJelita SihombingBelum ada peringkat
- Retinitis PigmentosaDokumen31 halamanRetinitis PigmentosaJelita SihombingBelum ada peringkat
- Patofisiologi Gangguan Sistem ImunDokumen27 halamanPatofisiologi Gangguan Sistem ImunIlhamBelum ada peringkat
- Hubungan Etika, Disiplin Dan Hukum Antara Dokter-PasienDokumen18 halamanHubungan Etika, Disiplin Dan Hukum Antara Dokter-PasienJelita Sihombing100% (1)
- DisentriDokumen12 halamanDisentriJelita SihombingBelum ada peringkat
- Anatomi Dan Fisiologi Sistem Pencernaan Manusia-WordDokumen5 halamanAnatomi Dan Fisiologi Sistem Pencernaan Manusia-WordIpiDifiaBelum ada peringkat
- Kontrol Saraf Terhadap Fungsi GastrointestinalDokumen5 halamanKontrol Saraf Terhadap Fungsi GastrointestinalIstiana HidayatiBelum ada peringkat
- Lengkung ReflexDokumen4 halamanLengkung ReflexLuthfi Aulia OktofaniBelum ada peringkat
- Mekanisme BerkeringatDokumen2 halamanMekanisme BerkeringatSetiari Dewi100% (1)
- Ibd (Gerak Refleks)Dokumen21 halamanIbd (Gerak Refleks)Nisfi Laelah GirltsaniieBelum ada peringkat
- PetidinDokumen4 halamanPetidinAyu Putu Prima SeptianiBelum ada peringkat
- Saraf Simpatik Dan ParasimpatikDokumen3 halamanSaraf Simpatik Dan ParasimpatikyulianaBelum ada peringkat
- Makalah Refleks Fisiologis TubuhDokumen12 halamanMakalah Refleks Fisiologis Tubuhanitanaim3100% (1)
- NeurotransmitterDokumen7 halamanNeurotransmitterrmysdsBelum ada peringkat
- Hormon Dalam MetabolismeDokumen16 halamanHormon Dalam MetabolismeSusanti CahyaningtyasBelum ada peringkat
- Makalah-Kimfis (Larutan Non-Elektrolit) NewDokumen20 halamanMakalah-Kimfis (Larutan Non-Elektrolit) NewIrfan Panjaitan67% (3)
- LAPORAN Fisiologi PenglihatanDokumen49 halamanLAPORAN Fisiologi Penglihatanmulkihakam21Belum ada peringkat
- Obat AnalgesikDokumen6 halamanObat AnalgesikYamma Michi Micheoso0% (1)
- Terminologi AnatomiDokumen3 halamanTerminologi AnatomiDevani Bagus AprindaBelum ada peringkat
- Pengertian HomeostasisDokumen6 halamanPengertian HomeostasisRezy Pysesia AlfaniBelum ada peringkat
- LAPORAN PRAKTIKUM Uji Keseimbangan (BP Sugeng)Dokumen5 halamanLAPORAN PRAKTIKUM Uji Keseimbangan (BP Sugeng)YessicaPutriandetaBelum ada peringkat
- Laporan Tes Lateral Flow DiasDokumen18 halamanLaporan Tes Lateral Flow DiasDias Jameela33% (3)
- Gerak Refleks Dan Waktu ReaksiDokumen13 halamanGerak Refleks Dan Waktu Reaksibaiq devi agustina ariskaBelum ada peringkat
- Makalah Sistem SarafDokumen25 halamanMakalah Sistem Sarafnovela memiasihBelum ada peringkat
- DASAR TEORI Sistem InderaDokumen3 halamanDASAR TEORI Sistem InderaOlivia Nabilla MaharaniBelum ada peringkat
- Jenis RefleksDokumen12 halamanJenis RefleksJustisia PadmiyatiBelum ada peringkat
- Makalah Parasimpatis Kel.4 NewDokumen12 halamanMakalah Parasimpatis Kel.4 NewKinanti DaraBelum ada peringkat
- Akhiran Saraf Aferen Dan EferenDokumen9 halamanAkhiran Saraf Aferen Dan EferenSelly SilfanaBelum ada peringkat
- Refleks ArcDokumen10 halamanRefleks ArcLeni YulisBelum ada peringkat
- Transmisi Sinapsis Neurotransmitter Potensial Membran Potensial AksiDokumen5 halamanTransmisi Sinapsis Neurotransmitter Potensial Membran Potensial AksiDyahAyuRisqiNilamsariBelum ada peringkat
- Enzim IntroductionDokumen18 halamanEnzim IntroductionAjie Setiawan SobirinBelum ada peringkat
- Pemeriksaan RefleksDokumen9 halamanPemeriksaan RefleksEsti Kurniati100% (1)
- 2 - Toksisitas Obat-Obat AntidepresanDokumen32 halaman2 - Toksisitas Obat-Obat AntidepresanSanti karaminaBelum ada peringkat
- Anatomi Fisiologi Tulang & SendiDokumen9 halamanAnatomi Fisiologi Tulang & Sendimelvasyahputralase100% (1)
- Komunikasi Antar Sel-2Dokumen12 halamanKomunikasi Antar Sel-2Ratih Sri rezekiBelum ada peringkat
- Anatomi Dan Fisiologi Sistem Saraf JenDokumen7 halamanAnatomi Dan Fisiologi Sistem Saraf JenJane Irene JessicaBelum ada peringkat
- Organ Pada Sistem Imun ManusiaDokumen9 halamanOrgan Pada Sistem Imun Manusiaintan yunandaBelum ada peringkat
- NYERIDokumen8 halamanNYERIBangunFebriantoBelum ada peringkat
- Pemeriksaan FisikDokumen10 halamanPemeriksaan FisikRizka Maulida BeliaBelum ada peringkat
- 1 Sistem Saraf Dan Gerak ReflekDokumen39 halaman1 Sistem Saraf Dan Gerak Reflekmunawwarotul khanifahBelum ada peringkat
- Fibrosis KistikDokumen18 halamanFibrosis KistikRossa SalendriBelum ada peringkat
- Praktikum RefleksDokumen4 halamanPraktikum RefleksAdelia RochmaBelum ada peringkat
- Jenis Dan Fungsi LeukositDokumen3 halamanJenis Dan Fungsi LeukositNers Irnawati MmrBelum ada peringkat
- Tingkatan Organisasi Dalam Tubuh ManusiaDokumen10 halamanTingkatan Organisasi Dalam Tubuh ManusiaGhea Ginanesia50% (2)
- Alur Permukaan JantungDokumen3 halamanAlur Permukaan JantungRika Herlianisa FitriBelum ada peringkat
- Epilepsi PsikomotorDokumen37 halamanEpilepsi PsikomotorMuhammadRifqiFarizanAkbarBelum ada peringkat
- Makalah Persepsi Sensori MataDokumen27 halamanMakalah Persepsi Sensori Matailham thohir100% (1)
- Perbedaan Endoplasma Retikulum HalusDokumen5 halamanPerbedaan Endoplasma Retikulum HalusPutri DEBelum ada peringkat
- REFEARAT Neurologi - Refleks FisiologisDokumen31 halamanREFEARAT Neurologi - Refleks Fisiologisaswalbasuki100% (1)
- Neurofisiologi Motorik Dan IntegratifDokumen46 halamanNeurofisiologi Motorik Dan IntegratifEfedi BagussavezBelum ada peringkat
- Pemeriksaan Laboratorium Terkait RadangDokumen2 halamanPemeriksaan Laboratorium Terkait RadangRahma P T RambeyBelum ada peringkat
- Makalah Epilepsi Kel 3Dokumen17 halamanMakalah Epilepsi Kel 3Adelia PutriBelum ada peringkat
- ADAPTASI SEL. Atrofi Dan Hipertrofi. TIRADokumen3 halamanADAPTASI SEL. Atrofi Dan Hipertrofi. TIRAelsmeeBelum ada peringkat
- Makalah Indera KhususDokumen21 halamanMakalah Indera KhususNurul Fadhilah100% (1)
- Kejang DemamDokumen27 halamanKejang DemamdickyBelum ada peringkat
- Tugas Soca Fix Febris DG DiareDokumen27 halamanTugas Soca Fix Febris DG DiareWawan HermawanBelum ada peringkat
- Laporan Pendahuluan DemamDokumen33 halamanLaporan Pendahuluan DemamMaulana Rian KrisandiBelum ada peringkat
- DEFINISIDokumen7 halamanDEFINISIDewaWisnuBudiSuryawanBelum ada peringkat
- Laporan Pendahuluan DemamDokumen19 halamanLaporan Pendahuluan DemamHeruBlo'on100% (2)
- LP FebrisDokumen13 halamanLP FebrisWulan NurlaelasariBelum ada peringkat
- FebrisDokumen7 halamanFebrisRisdiantiBelum ada peringkat
- LAPORAN PENDAHULUAN Febris Dan VomitusDokumen11 halamanLAPORAN PENDAHULUAN Febris Dan Vomitusayu48433% (3)
- Pengaturan Suhu Tubuh Dan MetabolismeDokumen16 halamanPengaturan Suhu Tubuh Dan MetabolismeJelita SihombingBelum ada peringkat
- Monitoring PerianestesiaDokumen2 halamanMonitoring PerianestesiaJelita SihombingBelum ada peringkat
- Anestesi UmumDokumen11 halamanAnestesi UmumJelita SihombingBelum ada peringkat
- Transient TIC DisorderDokumen39 halamanTransient TIC DisorderJelita Sihombing100% (1)
- Referat Akut AbdomenDokumen39 halamanReferat Akut AbdomenJelita SihombingBelum ada peringkat
- Hubungan Etika, Disiplin Dan Hukum Antara Dokter - PasienDokumen17 halamanHubungan Etika, Disiplin Dan Hukum Antara Dokter - PasienJelita SihombingBelum ada peringkat
- HIFEMADokumen19 halamanHIFEMAJelita SihombingBelum ada peringkat
- DispepsiaDokumen15 halamanDispepsiaJelita SihombingBelum ada peringkat
- Hand Arm VibrationDokumen14 halamanHand Arm VibrationJelita Sihombing0% (1)