Modul Praktikum Farmakognosi 2020
Diunggah oleh
lauren pangestuHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Modul Praktikum Farmakognosi 2020
Diunggah oleh
lauren pangestuHak Cipta:
Format Tersedia
PANDUAN PRAKTIKUM
FARMAKOGNOSI
Disusun Oleh :
Moelyono Moektiwardoyo
Yasmiwar Susilawati
Yoppi Iskandar
Ami Tjitraresmi
Ferry Ferdiansyah Sofian
Ade Zuhrotun
Zelika Mega Ramadhania
Raden Bayu Indradi
Intan Timur Maisyarah
Laboratorium Farmasi Bahan Alam
Fakultas Farmasi
Universitas Padjadjaran
2020
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020
KATA PENGANTAR
Kegiatan praktikum ini merupakan bagian penting yang
menunjang kegiatan perkuliahan demi tercapainya tujuan pendidikan
suatu bidang studi. Menyadari keterbatasan waktu serta pentingnya
peranan kegiatan praktikum untuk mencapai hasil pendidikan yang lebih
terarah dan dengan tingkat kemampuan yang dapat
dipertanggungjawabkan, maka dibuatlah Panduan Praktikum
Farmakognosi ini.
Tujuan dari penyusunan panduan ini adalah untuk membantu para
mahasiswa Fakultas Farmasi Universitas Padjadjaran dalam upaya
mendalami bidang studi Farmakognosi-Farmasi Bahan Alam khususnya
yang berkaitan dengan Identifikasi sampel secara mikroskopik serta
Quality Assurance/kualitas dari mulai simplisia hingga menjadi ekstrak
sebagai bahan baku yang digunakan untuk pembuatan Obat Tradisional.
Sadar akan keterbatasan ilmu dan kemampuan yang kami miliki,
dengan lapang dada kami harapkan adanya kritik dan saran yang
membangun bagi perbaikan panduan ini.
Jatinangor, September 2020
Penyusun
FAKULTAS FARMASI UNIVERSITAS PADJADJARAN i
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020
DAFTAR ISI
Halaman
KATA PENGANTAR ....................................................................... i
DAFTAR ISI ................................................................................... ii
KETENTUAN PRAKTIKUM ............................................................. 1
Modul Identifikasi dan Pewarnaan Pati ............................................ 5
Modul Pewarnaan Metabolit Sekunder ............................................ 12
Modul Identifikasi Sampel Campuran ............................................... 14
Modul Pemeriksaan Kualitas Simplisia ............................................. 16
Modul Ekstraksi ............................................................................. 24
Modul Pemeriksaan Kualitas Ekstrak .............................................. 27
Modul Isolasi dan Penetapan Kualitas Minyak Atsiri ........................ 32
FAKULTAS FARMASI UNIVERSITAS PADJADJARAN ii
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 1
KETENTUAN PRAKTIKUM
Praktikum ini merupakan bagian dari mata kuliah Farmakognosi.
Mata kuliah Farmakognosi terdiri dari 2 SKS kuliah dan 1 SKS praktikum.
Pelaksanaan praktikum terbagi menjadi 2, yaitu pelaksanaan praktikum
secara individual untuk modul pengamatan mikroskopik, dan
pelaksanaan praktikum secara kelompok untuk modul pengujian kualitas
bahan baku terstandar dengan ketentuan sebagai berikut:
A. BAHAN PRAKTIKUM
Kelompok 1: Curcuma domestica (Curcumae domesticae rhizoma)
Kelompok 2: Curcuma xanthorrhiza (Curcumae xanthorrhizae rhizoma)
Kelompok 3: Guazumae ulmifolium (Guazumae folium)
Kelompok 4: Syzygium polyanthum (Polyanthi folium)
B. PEMBAGIAN TUGAS KELOMPOK PRAKTIKUM
Satu shift praktikum dibagi menjadi 4 kelompok dengan
pembagian tugas sebagai berikut :
Kel. Bahan Senyawa Metode Bentuk Aktivitas
Aktif Ekstraksi Sediaan Farmakologi
1 Curcumae Kurkuminoid Maserasi Tablet Anti-iritasi
domesticae usus besar
rhizoma
2 Curcumae Kurkuminoid Maserasi Tablet Anti-
xanthorrhizae hiperglikemik,
rhizoma antiinflamasi
3 Guazumae Kuersetin Maserasi Suspensi Anti-
folium hiperkolesterol
4 Polyanthi Kuersetin Maserasi Suspensi Anti-
folium hiperglikemik
KETENTUAN PRAKTIKUM FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 2
C. JADWAL PELAKSANAAN PRAKTIKUM (Disesuaikan)
Praktikum dilaksanakan dalam waktu 14 pertemuan dengan
penjadwalan sebagai berikut:
Pertemuan Tanggal Kegiatan Uraian
1 7 – 11 Pendahuluan - Tata Tertib & Kontrak Praktikum
September - Responsi Awal : Pengarahan &
2020 Pendahuluan
- Kurve
2 14 – 18 Identifikasi & - Pengamatan makroskopik & mikroskopik
September pewarnaan pati tumbuhan
2020 mikroskopik pati - Pewarnaan pati secara mikroskopik
3 21 – 25 Pewarnaan - Minyak atsiri
September metabolit - Antrakuinon
2020 sekunder - Tanin
- Alkaloid
- Flavonoid
4 28 Identifikasi sampel - Identifikasi makroskopik dan mikroskopik
September – campuran 1 simplisia
2 Oktober - Identifikasi mikroskopik campuran
2020 simplisia
5 5 – 9 Oktober Identifikasi sampel - Identifikasi makroskopik dan mikroskopik
2020 campuran 2 simplisia
- Identifikasi mikroskopik campuran
simplisia
6 12 – 16 Identifikasi sampel - Identifikasi makroskopik dan mikroskopik
Oktober 2020 campuran 3 simplisia
- Identifikasi mikroskopik campuran
simplisia
7 19 – 23 Ujian identifikasi - Ujian identifikasi mikroskopik sampel
Oktober 2020 sampel campuran campuran
8 26 – 30 Pemeriksaan - Sortasi
Oktober 2020 kualitas simplisia & - Organoleptik
ekstraksi - Makroskopik
- Mikroskopik
- Ekstraksi
9 2–6 Pemeriksaan - Susut pengeringan
November parameter non - Kadar Abu
2020 spesifik simplisia & - Kadar Abu Tidak Larut Asam
pemekatan ekstrak - Pemekatan ekstrak
10 9 – 13 Pemeriksaan - KLT Simplisia
November parameter spesifik - Kadar Sari Larut Air
KETENTUAN PRAKTIKUM FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 3
Pertemuan Tanggal Kegiatan Uraian
2020 simplisia & - Kadar Sari Larut Etanol
pemekatan ekstrak - Pemekatan Ekstrak
11 16 – 20 Pemeriksaan - Organoleptik ekstrak
November parameter spesifik - Rendemen ekstrak
2020 ekstrak - Bobot jenis ekstrak
- Pola dinamolisis
12 23 – 27 Pemeriksaan - Kadar air ekstrak
November parameter non - Kadar abu total
2020 spesifik ekstrak & - Kadar abu tidak larut asam
isolasi minyak atsiri - Isolasi minyak atsiri Akhir
13 30 November Evaluasi minyak - Bobot jenis
– 4 Desember atsiri - Pemeriksaan KLT minyak atsiri
2020 - Rotasi optik
- Indeks bias
14 7 – 11 Ujian Akhir Ujian CBT
Desember Praktikum
2020
D. PERLENGKAPAN PRAKTIKUM
Perlengkapan Kelas
1. Plastik Wrap 1 gulung
2. Aluminiun Foil 1 gulung
3. Pipa kapiler 100 buah (1 Angkatan)
Kerlengkapan Kelompok
1. Sendok Tanduk 2 buah
2. Batang Pengaduk 2 buah
3. Pinset 1 buah
4. Electric Dryer 1 buah
5. Penggaris Besi 30 cm 1 buah
6. Tissue Gulung 2 gulung
7. Botol Bening 150 mL 2 botol
8. Botol Vial Bening 10 mL 5 botol
9. Botol Bening 1 L 1 botol
10.Stiker Label (sesuai format) Disesuaikan
11.Jerigen Plastik 10 L 1 buah
12.Logbook 1 buku
13.Koran 1 eksemplar
14.Trash Bag 1 buah
KETENTUAN PRAKTIKUM FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 4
15.Tool Box 1 buah
16.Lap/Kanebo 1 buah
Perlengkapan Pribadi
1. Jas Lab Farmasi UNPAD 1 stel
2. Name Tag (warna biru) 1 buah
3. Pensil 1 buah
4. Masker 1 buah
5. Sarung Tangan Karet 1 buah
6. Pipet Tetes 2 buah
7. Spatel 1 buah
KETENTUAN PRAKTIKUM FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 5
MODUL PRAKTIKUM
IDENTIFIKASI DAN PEWARNAAN PATI
TUJUAN PERCOBAAN
Melakukan identifikasi dan pewarnaan pati dari sampel secara
mikroskopik
TUJUAN INSTRUKSIONAL
Setelah melakukan praktikum ini, mahasiswa diharapkan mampu
mengidentifikasi pati dari sumber yang berbeda secara mikroskopik serta
dapat melakukan pewarnaan untuk mengidentifikasi keberadaan pati
pada sampel.
TEORI
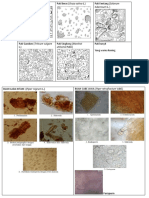
1. Pati Jagung (Amylum Maidis, Corn Starch)
PEMERIAN
Pati jagung, yaitu Amylum maidis, berasal dari biji tumbuhan jagung
(Zea mays L.), yang masak, termasuk suku Graminae, berupa serbuk halus
atau massa bersudut-sudut tidak beraturan, berwarna putih kusam yang
bila digerus bergeresek, tidak berbau, dan tak berasa.
MIKROSKOPIK
Pati jagung terdiri atas butir pati yang berasal dari endosperm
tanduk dan dari endosperm tepung. Butir dari endosperm tanduk
berbidang banyak dan bersudut-sudut (garis tengah kira-kira 2-23 μm),
sedangkan butir dari endosperm tepung berbidang banyak membulat,
dan agak lebih besar (garis tengah 25-32 μm). Sebagian besar berupa butir
poligonal dengan sudut membulat atau berupa butir hampir bulat.
Biasanya hilum di tengah berbentuk titik atau bintang sering dapat
ditemukan pada dua jenis pati tersebut. Cincin (lamela) biasanya tidak ada.
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 6
30 μm
Gambar mikroskopik pati jagung
2. Pati Beras (Amylum Orizae, Rice Starch)
PEMERIAN
Pati beras, yaitu Amylum oryzae, berasal dari biji tumbuhan padi
(Oryza sativa L.), termasuk suku Graminae, berupa serbuk sangat halus,
berwarna putih kusam, tidak berbau, dan tidak berasa.
MIKROSKOPIK
Pati beras, di samping butir yang sangat kecil, berbidang banyak,
dan bersudut-sudut tajam (2-10 μm), di dalam tepung itu terdapat pula
butir majemuk (ukuran sampai 60 μm) yang terbentuk dari butir tunggal
dan masih menampakkan sel endosperm. Bila digerus, butir majemuk
hancur menjadi butir tunggal kecil. Umumnya terdapat dalam butiran
majemuk yang berjumlah 2-100 butiran tunggal. Cincin (lamela) dan
hilumnya tidak dapat diamati. Hilum hanya tampak pada granul yang
besar dan terdapat di tengah.
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 7
10 μm
Gambar mikroskopik pati beras
3. Pati Kentang (Amylum Solani, Potato Starch)
PEMERIAN
Pati kentang, yaitu Amylum solani, berasal dari umbi tumbuhan
kentang (Solanum tuberosum L.), termasuk suku Solanaceae, berupa
serbuk agak kasar, berwarna putih mengkilap yang bergeresek bila
diremuk, tidak berwarna, tidak berbau, dan tidak berasa.
MIKROSKOPIK
Butir pati kentang berbentuk khas, bulat telur memanjang, dengan
garis keliling yang tak teratur. Ukuran berkisar antara 45 dan 75 μm. Hilum
bentuk sepatu kuda terletak di tengah dan terdapat sebagai titik pada
bagian yang sempit, kecil dan tidak jelas. Cincin (lamela) terletak eksentris
dan tampak nyata. Kadang-kadang ditemukan butir pati dengan dua pusat
cincin (butir pati setengah majemuk).
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 8
100 μm
Gambar mikroskopik pati kentang
4. Pati Gandum (Amylum Tritici, Wheat Starch)
PEMERIAN
Pati gandum, yaitu Amylum tritici, berasal dari biji tumbuhan
gandum (Triticum vulgare L.), termasuk suku Graminae, berupa serbuk
sangat halus, berwarna putih kusam, tidak berbau, tidak berasa,
bergeresek bila diremas.
MIKROSKOPIK
Pati gandum terdiri atas butir ”besar” berbentuk lensa bundar atau
jorong, kadang-kadang berbentuk ginjal (garis tengah 20-35 μm, jarang
sampai 50 μm, dengan tebal 9-15 μm) dan butir ”kecil” membulat (2-9 μm).
Hilum terletak di tengah tidak jelas, berupa titik atau celah. Pola cincin
(lamela) sangat halus, yang hanya dapat diamati pada butiran besar.
Ukuran peralihan jarang ditemukan (beda dengan butir pati gandum
hitam).
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 9
50 μm
Gambar mikroskopik pati gandum
5. Pati Singkong (Amylum Manihot, Tapioka Starch)
PEMERIAN
Pati singkong, yaitu Amylum manihot, berasal dari umbi tumbuhan
singkong (Manihot utilisima Pohl.), termasuk suku Euphorbiaceae, berupa
serbuk warna putih, tidak berbau, dan tidak berasa.
MIKROSKOPIK
Pati singkong terdiri dari butir tunggal atau bergerombol. Butir
tunggal berbentuk lonjong atau topi baja dengan ukuran antara 5-25 m.
Hilus terletak di tengah dengan jelas seperti titik atau kadang-kadang
segitiga. Lamela ada tapi kurang jelas.
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 10
25 μm
Gambar mikroskopik pati singkong
ALAT
1. Mikroskop
2. Object glass
3. Cover glass
4. Spatel
BAHAN
Akuades, Iodin, Serbuk Pati Jagung, Pati Beras, Pati Kentang, Pati Gandum,
Pati Singkong, dan Serbuk Kunyit.
TATA KERJA
Pada praktikum ini dilakukan pengamatan bentuk ciri khusus secara
mikroskopik serta pewarnaan dari masing-masing sampel pati.
TUGAS DAN LAPORAN
Hasil pengamatan berupa gambar dikerjakan pada buku gambar. Laporan
praktikum dibuat dengan melengkapi hasil dokumentasi selama praktikum
berlangsung. Tugas praktikum pada modul ini yaitu melakukan pengamatan
sampel dan mencari deskripsi lengkap masing-masing sampel. Laporan dan
tugas tersebut dikirimkan online secara perorangan melalui fasilitas google
classroom.
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 11
TINJAUAN PUSTAKA
Departemen Kesehatan RI. 1995. Materia Medika Indonesia. Jilid VI.
Cetakan Pertama. Direktorat Jenderal Pengawasan Obat dan
Makanan. Jakarta.
Departemen Kesehatan RI. 1989. Materia Medika Indonesia. Jilid V.
Cetakan Pertama. Direktorat Jenderal Pengawasan Obat dan
Makanan. Jakarta.
Departemen Kesehatan RI. 1980. Materia Medika Indonesia. Jilid IV.
Cetakan Pertama. Direktorat Jenderal Pengawasan Obat dan
Makanan. Jakarta.
Departemen Kesehatan RI. 1979. Materia Medika Indonesia. Jilid III.
Cetakan Pertama. Direktorat Jenderal Pengawasan Obat dan
Makanan. Jakarta.
Departemen Kesehatan RI. 1978. Materia Medika Indonesia. Jilid II.
Cetakan Pertama. Direktorat Jenderal Pengawasan Obat dan
Makanan. Jakarta.
Departemen Kesehatan RI. 1977. Materia Medika Indonesia. Jilid I.
Cetakan Pertama. Direktorat Jenderal Pengawasan Obat dan
Makanan. Jakarta.
Jackson, Betty P. and Derek W. Snowdon. 1990. Atlas of Microscopy of
Medical Plants, Culinary Herbs, and Spices. E-book pada
http://www.gigapedia.org/
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 12
MODUL PRAKTIKUM
PEWARNAAN METABOLIT SEKUNDER
TUJUAN PERCOBAAN
Melakukan identifikasi golongan senyawa metabolit sekunder yang
terkandung pada simplisia.
TUJUAN INSTRUKSIONAL
Pewarnaan mikroskopik bahan obat alam dilakukan untuk
mengidentifikasi golongan senyawa metabolit di dalam bahan obat alam,
misalnya tumbuhan. Pewarnaan dilakukan dengan meneteskan pereaksi
warna pada cuplikan dan dibantu dengan penghangatan cuplikan di atas
pembakaran mikro agar pereaksi dapat masuk ke dalam sel sehingga
bereaksi dengan senyawa yang akan diidentifikasi.
ALAT
1. Mikroskop
2. Object glass
3. Cover glass
4. Spatel
5. Bunsen
BAHAN
Merah sudan, KOH 5%, dragendorff, FeCl3, daun sirih, bunga cengkeh, akar
kelembak, kulit kina, buah cabe jawa, kulit buah manggis, buah mengkudu,
daun jati belanda, daun teh, daun salam.
TATA KERJA
Pada praktikum ini dilakukan pengamatan bentuk ciri khusus secara
mikroskopik serta pewarnaan dari masing-masing sampel pati.
TUGAS DAN LAPORAN
Hasil pengamatan berupa gambar dikerjakan pada buku gambar. Laporan
praktikum dibuat dengan melengkapi hasil dokumentasi selama praktikum
berlangsung. Tugas praktikum pada modul ini yaitu melakukan pengamatan
sampel dan mencari deskripsi lengkap masing-masing sampel. Laporan dan
tugas tersebut dikirimkan online secara perorangan melalui fasilitas google
classroom.
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 13
Pewarnaan mikroskopik dilakukan sesuai dengan tabel berikut ini :
Pewarnaan
No Simplisia Pereaksi Hasil
Metabolit
1 Minyak Atsiri Daun Sirih Merah sudan Warna merah
Bunga Cengkeh
2 Kuinon Akar Kelembak Larutan alkali Warna merah
(KOH 5%)
3 Alkaloid Kulit Kina Pereaksi Endapan
Buah Cabe Jawa Dragendorff jingga-coklat
4 Flavonoid* Kulit Buah Manggis Larutan besi (III) Warna hitam-
Buah Mengkudu klorida biru atau hijau
5 Tanin** Daun Jati Belanda Larutan besi (III) Warna hitam-
Daun Teh klorida biru atau hijau
Daun Salam
Keterangan :
*) Pilih salah satu diantara dua simplisia yang mengandung flavonoid
**) Pilih dua diantara tiga simplisia yang mengandung tanin
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 14
MODUL PRAKTIKUM
IDENTIFIKASI SAMPEL CAMPURAN
TUJUAN PERCOBAAN
Melakukan identifikasi fragmen-fragmen simplisia dari sampel
campuran simplisia
TUJUAN INSTRUKSIONAL
Pemeriksaan mikroskopik untuk mengidentifikasi fragmen-fragmen
pengenal pada suatu sampel campuran simplisia. Dengan
mengidentifikasi fragmen-fragmen pengenal, diharapkan praktikan dapat
mengetahui simplisia apa yang terkandung pada suatu campuran tersebut.
ALAT
1. Mikroskop
2. Object glass
3. Cover glass
4. Spatel
5. Bunsen
BAHAN
Akuades, kloralhidrat, sampel campuran simplisia
TATA KERJA
Pada praktikum ini dilakukan pengamatan fragmen-fragmen dari
campuran simplisia. Pengamatan dilakukan secara mikroskopis dengan
membandingkan antara sampel-sampel tunggal, sampel campuran, dan
literatur Farmakope Herbal Indonesia atau Materia Medika Indonesia. Simplisia
yang mungkin merupakan komposisi dari sampel campuran akan disampaikan
saat pelaksanaan praktikum.
TUGAS DAN LAPORAN
Hasil pengamatan berupa gambar dikerjakan pada buku gambar.
Laporan praktikum dibuat dengan melengkapi hasil dokumentasi selama
praktikum berlangsung. Tugas praktikum pada modul ini yaitu melakukan
pengamatan sampel dan mencari deskripsi lengkap masing-masing sampel.
Laporan dan tugas tersebut dikirimkan online secara perorangan melalui
fasilitas google classroom.
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 15
Identifikasi sampel campuran akan dilakukan dengan teknis sebagai
berikut :
No Modul Simplisia tunggal Sampel campuran
1 Identifikasi sampel 4 jenis simplisia 2 campuran simplisia per
campuran 1 sampel (total 3 sampel)
2 Identifikasi sampel 5 jenis simplisia 3 campuran simplisia per
campuran 2 sampel (total 3 sampel)
3 Identifikasi sampel 6 jenis simplisia 3 campuran simplisia per
campuran 3 sampel (total 4 sampel)
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 16
MODUL PRAKTIKUM
PEMERIKSAAN KUALITAS SIMPLISIA
TUJUAN PERCOBAAN
Melakukan pemeriksaan kualitas simplisia meliputi definisi
simplisia, pengujian organoleptik, mikroskopik dan makroskopik untuk
memastikan identitas simplisia yang akan digunakan sebagai bahan baku
pembuatan produk jadi sediaan obat tradisional dan parameter kualitas
simplisia yang terdapat dalam monografi Farmakope Herbal Indonesia.
TUJUAN INSTRUKSIONAL
Setelah melakukan praktikum ini, mahasiswa mampu menganalisis
kebenaran identitas simplisia yang akan digunakan sebagai bahan baku
pembuatan produk jadi sediaan obat tradisional melalui pengujian
organoleptik, mikroskopik dan makroskopik yang kemudian
dibandingkan dengan literatur. Serta, mahasiswa mampu melakukan
pengujian parameter kualitas simplisia dan menganalisa hasil pengujian
dibandingkan dengan literatur.
TEORI
Sudah sejak lama tanaman obat digunakan untuk pencegahan
ataupun pengobatan penyakit-penyakit tertentu di kalangan masyarakat,
dan seiring berjalannya waktu penggunaannya semakin menunjukkan
kemajuan pesat.
Berdasarkan keputusan Kepala BPOM Nomor HK.00.05.4.2411
Tahun 2004 tentang Ketentuan Pokok Pengelompokan dan Penandaan
Obat Bahan Alam Indonesia, obat tradisional dikategorikan menjadi :
Jamu, Obat Herbal Terstandar (OHT) dan Fitofarmaka, yang memiliki
persyaratan masing-masing.
Penentuan identifikasi merupakan suatu langkah yang penting
untuk menjamin kebenaran dari simplisia yang akan digunakan sebagai
bahan baku yang memiliki senyawa aktif dalam pembuatan produk jadi
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 17
obat tradisional. Hal ini berkaitan dengan salah satu persyaratan obat,
yaitu efikasi (khasiat) yang tepat.
Identitas suatu tanaman yang digunakan secara empirik ataupun
pengujian ilmiah, harus diyakini dengan pasti kebenaran jenisnya agar
tujuan pengobatan tercapai.
Pemeriksaan paramater kualitas simplisia sebagai bahan baku
produk jadi harus dilakukan untuk menjamin kualitas bahan dan
keamanan bagi pasien, terutama OHT dan fitofarmaka yang persyaratan
bahan baku esktraknya harus terstandar.
Parameter non-spesifik berfokus pada aspek kimia, mikrobiologi,
dan fisik yang akan mempengaruhi keamanan konsumen dan stabilitas.
Sedangkan, parameter spesifik berfokus pada senyawa atau golongan
senyawa yang bertanggung jawab terhadap aktivitas farmakologi.
Nilai rentang yang ditunjukkan parameter non-spesifik adalah nilai
maksimum yang dihasilkan dan perlu ditetapkan menjadi batas tertinggi
karena nilai ini menunjukkan kemurnian suatu ekstrak. Sedangkan untuk
parameter spesifik yang perlu ditetapkan adalah nilai minimum yang
menjadin batas terendah dan karena nilai ini menunjukkan kualitas suatu
simplisia.
PEMERIKSAAN KUALITAS SIMPLISA
Pemeriksaan simplisia perlu dilakukan untuk memastikan identitas
atau kebenaran simplisia tersebut. Pengujian yang dilakukan adalah
sebagai berikut :
A. Definisi Simplisia
Dilakukannya tinjauan pustaka dari berbagai literatur (dapat dari MMI,
FHI, buku atau jurnal terpercaya). Disebutkannya (sesuai Farmakope
Herbal Indonesia) :
1. Bagian tumbuhan
2. Nama Spesies beserta Author
3. Nama Suku
4. Senyawa Identitas
B. Identitas Simplisia
1. Pemerian (Organoleptik Simplisia)
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 18
Pemeriksaan menggunakan panca indera untuk mendiskripsikan
bentuk, warna, bau serta rasa dari simplisia yang digunakan.
2. Makroskopik Simplisia (Ciri Morfologi)
Pemeriksaan menggunakan panca indera untuk mendiskripsikan
bentuk dan ukuran, warna, bau serta rasa dari simplisia yang
digunakan. Uji makroskopik dilakukan dengan menggunakan kaca
pembesar, alat ukur atau tanpa menggunakan alat. Cara ini
dilakukan untuk mencari khususnya morfologi, ukuran, dan warna
simplisia yang diuji. Kemudian simplisia difoto sesuai dengan
ketentuan FHI:
a. Simplisia difoto dengan ukuran 7x10 cm, orientasi kertas
landscape dengan latar belakang kertas putih yang tidak
memantulkan cahaya (doff) dengan ukuran kertas A4.
b. Pada sepertiga bagian kiri kertas simplisia disebarkan, pada
dua pertiga bagian sisanya simplisia disusun teratur.
c. Diberikan skala pada bagian kanan bawah (skala ditulis dengan
menggunakan computer bukan bagian dari foto simplisia).
d. Simplisia yang difoto harus yang digunakan dalam
penelitian/pengujian.
e. Apabila suatu jenis tumbuhan mempunyai banyak varietas
maka foto simplisia yang disajikan harus sesuai varietas yang
digunakan dalam penelitian/pengujian.
3. Mikroskopik Simplisia
Pengamatan mikroskopis dilakukan dengan melihat fragmen yang
ada pada serbuk simplisia menggunakan mikroskop cahaya,
perbesaran 400x dan kemudian difoto dengan kamera secara
digital. Ukuran foto setiap fragmen adalah 4x6 cm dengan
orientasi landscape. Untuk pengamatan amilum digunakan media
air gliserin. Amilum diamati dengan menunjukkan bentuk amilum,
dan lamelanya. Sedangkan untuk fragmen lainnya, digunakan
media kloralhidrat yang dipanaskan. Pada simplisia daun, fragmen
yang diamati berupa mesofil daun, epidermis dengan stomata,
bentuk berkas pengangkut, kristal kalsium oksalat.
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 19
C. Pola Kromatografi
Pola kromatografi dilakukan untuk memberikan gambaran secara
kualitatif dan melihat pola pemisahan senyawa yang terkandung
dalam tanaman sampel. Sistem dan metode pengujian disesuaikan
dengan sampel masing-masing di Farmakope Herbal Indonesia :
1. Deteksi bercak pada KLT dengan UV 254 nm hanya untuk
senyawa yang dapat dilihat dengan 254 nm, UV 366 nm hanya
untuk senyawa yang berfluoresensi.
2. Flavonoid perlu dideteksi sebelum dan sesudah disemprot dengan
pereaksi AlCl3 atau sitroborat dan dilihat pada UV 366 nm.
3. Untuk golongan senyawa lain, deteksi disesuaikan.
4. Ukuran plat KLT disesuaikan
5. Hasil KLT juga difoto 10x5 cm portrait.
6. Sistem KLT:
a. Fase gerak
b. Fase diam
c. Larutan uji
d. Larutan pembanding
e. Volume penotolan
f. Deteksi
7. Preparasi sistem KLT menurut Suplemen III Farmakope Herbal
Indonesia Edisi I (Kemkes RI, 2013):
a. Larutan uji KLT: 1 g serbuk simplisia ditimbang saksama,
direndam sambil dikocok di atas penangas air dengan 10 mL
pelarut yang sesuai selama 10 menit.
b. Penotolan pada KLT: larutan uji dan larutan pembanding
ditotolkan menurut cara yang tertera pada masing-masing
monografi dengan jarak antara 1,5-2 cm dari tepi bawah
lempeng dan dibiarkan mengering.
c. Penjenuhan bejana: kertas saring dengan tinggi 18 cm dan
lebar sama dengan lebar bejana ditempatkan di dalam
bejana kromatografi. Sejumlah larutan pengembang
dimasukkan ke dalam bejana kromatografi hingga tingginya
0,5-1 cm dari dasar bejana. Bejana ditutup kedap hingga
kertas saring basah seluruhnya. Kertas saring harus selalu
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 20
tercelup ke dalam larutan pengembang pada dasar bejana.
Kecuali dinyatakan lain pada masing-masing monografi,
prosedur KLT dilakukan dalam bejana jenuh.
8. Contoh penyiapan KLT:
D. Paramater Kualitas Simplisia
1. Susut Pengeringan
Tujuan : Memberikan batasan maksimal (rentang) tentang besarnya
senyawa yang hilang pada proses pengeringan.
Prosedur :
Simplisia ditimbang seksama 1-2 gram dan dimasukkan ke dalam
botol timbang dangkal bertutup yang sebelumnya telah dipanaskan
105 oC selama 30 menit dan ditara. Sebelum ditimbang, ekstrak
diratakan dengan menggoyangkan botol hingga mendapat lapisan
setebal 5-10 mm, lalu dimasukkan ke dalam oven 105 oC hingga
bobot tetap dengan keadaan tutup terbuka. Dalam kedaan tertutup,
botol didinginkan dalam desikator hingga suhu ruang sebelum
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 21
ditimbang. Susut pengeringan ekstrak ditetapkan dengan rumus
sebagai berikut :
(𝐂𝐨 + 𝐦) − 𝐂𝐭
𝐒𝐮𝐬𝐮𝐭 𝐩𝐞𝐧𝐠𝐞𝐫𝐢𝐧𝐠𝐚𝐧 = 𝐱𝟏𝟎𝟎%
𝐦
Ket : Co = Bobot botol kosong
Ct = Bobot botol + simplisia
m = Bobot simplisia
2. Kadar Abu Total dan Kadar Abu Tidak Larut Asam
Tujuan : Memberikan gambaran kandungan mineral dan anorganik
internal dan eksternal yang berasal dari proses awal sampai
terbentuknya ekstrak.
Prosedur:
Kadar Abu Total
2 gram simplisia ditimbang dengan seksama ke dalam kurs yang telah
ditara. Suhu dinaikan secara bertahap hingga 600 ± 25oC sampai
bebas karbon. Dinginkan dalam desikator serta timbang berat abu.
Dihitung kadar abu dalam persen terhadap berat sampel awal,
ditetapkan dengan rumus sebagai berikut :
(Ct − Co)
Kadar Abu Total = x100%
m
Ket : Co = Bobot krus kosong
Ct = Bobot krus + simplisia
m = Bobot ekstrak
Kadar Abu Tidak Larut Asam
Abu hasil penetapan kadar abu total dididihkan dengan 25 mL HCl
encer selama 5 menit. Kumplkan bagian yang tidak larut dalam asam.
Lalu saring menggunakan kertas saring bebas abu, cuci dengan air
panas, saring dan timbang kembali. Dihitung kadar abu yang tidak
larut asam dalam persen terhadap berat sampel, ditetapkan dengan
rumus sebagai berikut :
(Ct − Co)
Kadar Abu Tidak Larut Asam = x100%
m
Ket : Co = Bobot krus kosong
Ct = Bobot krus + kertas saring bebas abu
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 22
m = Bobot simplisia
3. Kadar Sari Larut Air dan Kadar Sari Larut Etanol
Tujuan : Memberikan gambaran awal jumlah senyawa kandungan
yang terlarut dalam pelarut tertentu.
Prosedur :
Kadar Sari Larut Air
Simplisia sebanyak 5 gram ditimbang. Kemudian, dimasukkan ke
dalam labu bersumbat, kemudian dilarutkan dalam 100 mL air jenuh
kloroform. Lalu dikocok berkali-kali selama 6 jam pertama, dan
dibiarkan selama 18 jam. Kemudian disaring. Filtrat yang didapat,
diambil 20 mL lalu diuapkan hingga kering dalam cawan penguap
yang telah dipanaskan terlebih dahulu pada 105 oC dan ditara.
Kemudian residu yang didapat, dipanaskan pada 105 oC hingga bobot
tetap. Kadar sari larut air ditetapkan dengan rumus sebagai berikut :
100
(Ct − Co)x
20
Kadar Sari Larut Air = x100%
m
Ket : Co = Bobot cawan kosong
Ct = Bobot cawan + simplisia
m = Bobot simplisia
Kadar Sari Larut Etanol
Simplisia sebanyak 5 gram ditimbang. Kemudian, dimasukkan ke
dalam labu bersumbat, kemudian dilarutkan dalam 100 mL etanol
95%. Lalu dikocok berkali-kali selama 6 jam pertama, dan dibiarkan
selama 18 jam. Kemudian disaring. Filtrat yang didapat, diambil 20
mL lalu diuapkan hingga kering dalam cawan penguap yang telah
dipanaskan terlebih dahulu pada 105 oC dan ditara. Kemudian
residu yang didapat, dipanaskan pada 105 oC hingga bobot tetap.
Kadar sari larut etanol ditetapkan dengan rumus sebagai berikut :
100
(Ct − Co)x
20
Kadar sari larut etanol = x100%
m
Ket : Co = Bobot cawan kosong
Ct = Bobot cawan + simplisia
m = Bobot simplisia
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 23
4. Pemeriksaan Kadar Senyawa Pada Simplisia
Kadar senyawa pada simplisia dilakukan sesuai dengan ketentuan
Farmakope Herbal Indonesia.
PUSTAKA
Depkes RI. 2000. Parameter Standar Umum Ekstrak Tumbuhan Obat.
Dirjen POM. Direktorat Pengawasan Obat Tradisional. 3-5.
BPOM RI. 2004. Keputusan Kepala BPOM Nomor HK.00.05.4.2411 Tahun
2004 tentang Ketentuan Pokok Pengelompokan dan Penandaan
Obat Bahan Alam Indonesia.
Kemkes RI. 2013. Suplemen III Farmakope Herbal Indonesia Edisi I.
Direktorat Jenderal Bina Kefarmasian dan Alat Kesehatan.
Jakarta.
Stahl, E. 1985. Analisis Obat secara Kromatografi dan Mikroskopi.
Penerjemah : Dr. Kosasih Padmawinata dan Dr. Iwang Sudiro.
Penerbit ITB. Bandung.
Modul Praktikum FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 24
MODUL PRAKTIKUM
EKSTRAKSI
TUJUAN PERCOBAAN
Melakukan penyarian metabolit sekunder dari simplisia tanaman
obat dengan metode ekstraksi yang sesuai.
TUJUAN INSTRUKSIONAL
Setelah melakukan praktikum ini, mahasiswa dapat memahami
dan mampu melakukan penyarian metabolit sekunder dari simplisia
tanaman obat.
TEORI
Untuk menjaga kualitas bahan baku yang akan digunakan dalam
pembuatan obat tradisional, pengeringan harus dilakukan terhadap
tanaman obat segar tersebut. Hal ini dilakukan untuk mencegah reaksi
enzimatis yang dapat merusak tanaman obat tersebut. Pengeringan tidak
boleh menggunakan panas tinggi agar tidak terjadi perubahan kimia.
Setelah kering, bahan dapat disimpan lama sebelum dilakukan ekstraksi.
Ekstraksi merupakan proses penarikan kandungan kimia yang
berada dalam campuran (dalam praktikum ini yang dimaksud adalah
simplisia) secara selektif dengan pelarut yang sesuai. Komponen yang
terdapat dalam simplisia akan larut berdasarkan koefisien partisi
(koefisien distribusi) komponen tersebut dalam pelarut yang digunakan /
Like dissolve like.
Ekstraksi dapat dilakukan dengan ekstrasi cara panas dan ekstrasi
cara dingin. Ekstraksi panas (infus, dekok, refluk, digesti dan
menggunakan alat soxhlet) dilakukan jika komponen yang akan
diekstraksi tahan panas (termostabil). Sedangkan ekstraksi cara dingin
(maserasi, perkolasi) digunakan untuk mengekstraksi komponen yang
tidak tahan panas (termolabil). Ekstraksi cara dingin juga digunakan
untuk simplisia yang belum diketahui komponennya, sehingga belum
diketahui kestabilan komponennya.
Berdasarkan kepolarannya, pelarut yang digunakan dalam proses
ekstraksi adalah pelarut non polar, semipolar dan polar. Contoh pelarut
MODUL PRAKTIKUM FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 25
non polar benzena, n-heksana, toluen. Contoh pelarut semi polar etil
asetat, kloroform, aseton. Contoh pelarut polar air, metanol, etanol.
Pelarut yang biasa digunakan untuk ekstraksi bahan baku produk
jadi obat tradisional biasanya menggunakan etanol, akuades (air) atau
campuran etanol-akuades, karena relatif aman, tidak toksik, selektif, dan
relatif tidak mahal serta penggunaan air dimaksudkan untuk mendekati
cara penggunaan secara empiris oleh masyarakat. Pelarut etanol adalah
pelarut universal, yang dapat melarutkan sebagian besar senyawa polar,
sebagian kecil senyawa semi polar dan sebagian kecil senyawa non polar.
Ekstrak yang diperoleh dipekatkan dengan alat penguap vakum
putar (Rotary Vacuum Evaporator) hingga diperoleh ekstrak kental.
Terhadap ekstrak kental dilakukan pengujian parameter standar ekstrak
dan digunakan sebagai bahan awal produk jadi sediaan obat tradisional.
Pemeriksaan paramater standar ekstrak sebagai bahan baku produk jadi
harus dilakukan untuk menjamin kualitas bahan dan keamanan bagi
pasien.
PROSEDUR EKSTRAKSI
Maserasi
Bagian dasar maserator dilapisi dengan kapas sebagai penyaring.
Kemudian dimasukkan sebanyak serbuk simplisia (jumlah disesuaikan) ke
dalam maserator. Tambahkan pelarut etanol 70% secukupnya dan
biarkan selama kira-kira 10 menit agar terjadi proses pembasahan
simplisia, kemudian ditambahkan pelarut etanol sampai seluruh serbuk
simplisia terendam. Didiamkan selama 2x24 jam (kondisional) sambil
sesekali diaduk. Dimana setiap 24 jam, pelarut diganti baru. Ekstrak cair
ditampung. Ukur volume ekstrak cair yang diperoleh kemudian
dipekatkan dengan alat rotavapor pada suhu 30-40o C sehingga
diperoleh ekstrak kental.
MODUL PRAKTIKUM FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 26
Rendemen Ekstrak
Rendemen dapat ditetapkan dengan rumus sebagai berikut :
𝒃𝒆𝒓𝒂𝒕 𝒆𝒌𝒔𝒕𝒓𝒂𝒌 𝒕𝒐𝒕𝒂𝒍
𝑹𝒆𝒏𝒅𝒆𝒎𝒆𝒏 (%) = 𝒙 𝟏𝟎𝟎
𝒃𝒆𝒓𝒂𝒕 𝒔𝒊𝒎𝒑𝒍𝒊𝒔𝒊𝒂
Untuk menetapkan rendemen ekstrak, sejumlah tertentu ekstrak
kental dalam cawan penguap ditimbang kemudian diuapkan di atas
penangas air dengan temperatur 40-50˚C sampai bobot tetap.
Tentukan berat ekstrak setelah penguapan dengan mengurangkan
dengan bobot cawan kosong, kemudian hitung rendemen ekstrak (%
b/b) sesuai dengan rumus di atas.
PUSTAKA
Harborne, J.B. 1973. Phytochemical Methods, A Guide to Modern
Techniques of Plants Analysis. Chapmann and Hall. London, 1-
32.
Depkes RI. 2000. Parameter Standar Umum Ekstrak Tumbuhan Obat.
Dirjen POM. Direktorat Pengawasan Obat Tradisional. 9-12.
Kemkes RI. 2013. Suplemen III Farmakope Herbal Indonesia Edisi I.
Direktorat Jenderal Bina Kefarmasian dan Alat Kesehatan.
Jakarta.
MODUL PRAKTIKUM FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 27
MODUL PRAKTIKUM
PEMERIKSAAN KUALITAS EKSTRAK
TUJUAN PERCOBAAN
Melakukan pemeriksaan parameter standarisasi spesifik dan non-
spesifik ekstrak untuk menjamin kualitas bahan dan keamanan bagi
pasien.
TUJUAN INSTRUKSIONAL
Setelah melakukan praktikum ini, mahasiswa mampu melakukan
pengujian parameter standarisasi ekstrak dan menganalisa hasil
pengujian dibandingkan dengan literatur.
TEORI
Berdasarkan keputusan Kepala BPOM Nomor HK.00.05.4.2411
Tahun 2004 tentang Ketentuan Pokok Pengelompokan dan Penandaan
Obat Bahan Alam Indonesia, obat tradisional dikategorikan menjadi :
Jamu, Obat Herbal Terstandar (OHT) dan Fitofarmaka.
Pemeriksaan paramater standar ekstrak sebagai bahan baku
produk jadi harus dilakukan untuk menjamin kualitas bahan dan
keamanan bagi pasien, terutama OHT dan fitofarmaka yang persyaratan
bahan baku esktraknya harus terstandar.
Parameter non-spesifik berfokus pada aspek kimia, mikrobiologi,
dan fisik yang akan mempengaruhi keamanan konsumen dan stabilitas.
Sedangkan, parameter spesifik berfokus pada senyawa atau golongan
senyawa yang bertanggung jawab terhadap aktivitas farmakologi.
Nilai rentang yang ditunjukkan parameter non-spesifik adalah nilai
maksimum yang dihasilkan dan perlu ditetapkan menjadi batas tertinggi
karena nilai ini menunjukkan kemurnian suatu ekstrak. Sedangkan untuk
parameter spesifik yang perlu ditetapkan adalah nilai minimum yang
menjadin batas terendah dan karena nilai ini menunjukkan kualitas suatu
ekstrak.
MODUL PRAKTIKUM FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 28
PARAMETER STANDARISASI EKSTRAK
1. Parameter Non-Spesifik
a. Bobot Jenis
Tujuan : Memberikan batasan tentang besarnya massa per
satuan volume. Memberikan gambaran kandungan kimia
terlarut.
Prosedur :
Penetapan bobot jenis ekstrak dapat dilakukan sebagai berikut.
Ditimbang piknometer dengan volume tertentu dalam keadaan
kosong. Kemudian piknometer diisi penuh dengan air dan
ditimbang ulang. Kerapatan air dapat ditetapkan. Kemudian
piknometer dikosongkan dan diisi penuh dengan ekstrak, lalu
ditimbang. Melalui berat ekstrak yang mempunyai volume
tertentu, dapat ditetapkan kerapatan ekstrak. Bobot jenis
ekstrak ditetapkan dengan rumus sebagai berikut :
𝒌𝒆𝒓𝒂𝒑𝒂𝒕𝒂𝒏 𝒆𝒌𝒔𝒕𝒓𝒂𝒌
𝑩𝒐𝒃𝒐𝒕 𝒋𝒆𝒏𝒊𝒔 𝒆𝒌𝒔𝒕𝒓𝒂𝒌 =
𝒌𝒆𝒓𝒂𝒑𝒂𝒕𝒂𝒏 𝒂𝒊𝒓
b. Kadar Air
Tujuan : Memberikan batasan minimal atau rentang tentang
besarnya kandungan air di dalam bahan.
Penetapan kadar air ekstrak dapat dilakukan dengan beberapa
cara misalnya dengan titrasi langsung atau tidak langsung
(pereaksi Karl-Fischer), destilasi atau gravimetri. Pada
praktikum ini akan dilakukan penetapan kadar air dengan
destilasi menggunakan destilasi toluene.
Prosedur :
Ke dalam labu bersih dan kering dimasukkan sejumlah ekstrak
kental yang telah ditimbang seksama kemudian tambahkan 200
ml toluene, hubungkan alat. Tuangkan toluene ke dalam labu
penerima melalui alat pendingin. Panaskan labu hati-hati
selama 15 menit. Setelah toluen mendidih, suling dengan
MODUL PRAKTIKUM FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 29
kecepatan lebih kurang 2 tetes tiap detik, hingga sebagian air
tersuling, kemudian naikkan kecepatan penyulingan hingga 4
tetes tiap detik. Setelah semua air tersuling, biarkan tabung
penerima mendingin hingga suhu kamar. Setelah air dan
toluene memisah sempurna, baca volume air. Hitung kadar air
dalam % v/b.
c. Kadar Abu Total dan Kadar Abu Tidak Larut Asam
Tujuan : Memberikan gambaran kandungan mineral dan
anorganik internal dan eksternal yang berasal dari proses awal
sampai terbentuknya ekstrak.
Prosedur:
Kadar Abu Total
2 gram ekstrak ditimbang dengan seksama ke dalam kurs yang
telah ditara. Suhu dinaikan secara bertahap hingga 600 ± 25oC
sampai bebas karbon. Dinginkan dalam desikator serta timbang
berat abu. Dihitung kadar abu dalam persen terhadap berat
sampel awal, ditetapkan dengan rumus sebagai berikut :
(Ct − Co)
Kadar Abu Total = x100%
m
Ket : Co = Bobot krus kosong
Ct = Bobot krus + ekstrak
m = Bobot ekstrak
Kadar Abu Tidak Larut Asam
Abu hasil penetapan kadar abu total dididihkan dengan 25 mL HCl
encer selama 5 menit. Kumplkan bagian yang tidak larut dalam
asam. Lalu saring menggunakan kertas saring bebas abu, cuci
dengan air panas, saring dan timbang kembali. Dihitung kadar abu
yang tidak larut asam dalam persen terhadap berat sampel,
ditetapkan dengan rumus sebagai berikut :
(Ct − Co)
Kadar Abu Tidak Larut Asam = x100%
m
Ket : Co = Bobot krus kosong
Ct = Bobot krus + kertas saring bebas abu
m = Bobot ekstrak
MODUL PRAKTIKUM FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 30
2. Parameter Spesifik
a. Organoleptik Ekstrak
Pemeriksaan menggunakan panca indera untuk mendiskripsikan
bentuk, warna, au dan rasa dari ekstrak yang diperoleh.
b. Pemeriksaan Kadar Senyawa Pada Ekstrak
Pemeriksaan kadar senyawa pada ekstrak dilakukan sesuai
prosedur dari Farmakope Herbal Indonesia untuk masing-masing
tanaman.
PUSTAKA
Depkes RI. 2000. Parameter Standar Umum Ekstrak Tumbuhan Obat.
Dirjen POM. Direktorat Pengawasan Obat Tradisional. 9-12.
BPOM RI. 2004. Keputusan Kepala BPOM Nomor HK.00.05.4.2411 Tahun
2004 tentang Ketentuan Pokok Pengelompokan dan Penandaan
Obat Bahan Alam Indonesia.
Kemkes RI. 2013. Suplemen III Farmakope Herbal Indonesia Edisi I.
Direktorat Jenderal Bina Kefarmasian dan Alat Kesehatan.
Jakarta.
MODUL PRAKTIKUM FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 31
LEMBAR KERJA PRAKTIKUM FARMAKOGNOSI-FARMASI BAHAN ALAM
FAKULTAS FARMASI-UNIVERSITAS PADJADJARAN
PRAKTIKUM : Pengujian Parameter Kualitas Ekstrak
NAMA MAHASISWA : .............................................................
NPM : .............................................................
KELOMPOK : .............................................................
NAMA TANAMAN : .............................................................
NAMA SIMPLISIA : .............................................................
HASIL PERCOBAAN :
A. Rendemen Ekstrak
Volume ekstrak kental : ........................ mL
Berat cawan kosong : ........................ g
Berat cawan + ekstrak : ........................ g
Berat cawan+ekstrak setelah penguapan : ........................ g
Berat simplisia awal : ........................ g
Rendemen ekstrak : ........................ %b/b
B. Parameter Standarisasi Ekstrak
Parameter Hasil Persyaratan Kesimpulan
Pengujian
Spesifik
Identitas Bentuk : Bentuk :
Warna : Warna :
Bau : Bau :
Rasa : Rasa :
Kadar Kandungan Kimia
Non-Spesifik
Bobot Jenis
Kadar Air
Kadar Abu Total
Abu Tidak Larut Asam
Cemaran Mikroba
Angka Lempeng Total (ALT)
Angka Kapang Khamir (AKK)
MODUL PRAKTIKUM FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 32
MODUL PRAKTIKUM
ISOLASI DAN PENETAPAN KUALITAS MINYAK ATSIRI
TUJUAN PERCOBAAN
Melakukan isolasi minyak atsiri dengan cara destilasi air, destilasi
uap dan air, enfleurasi, dan pemerasan, serta melakukan penetapan
kadar minyak atsirinya menggunakan alat destilasi Stahl.
TUJUAN INSTRUKSIONAL
Setelah melakukan praktikum ini mahasiswa mampu melakukan isolasi
minyak atsiri dari suatu simplisia dengan cara destilasi air, destilasi uap
dan air, enfleurasi, dan pengepresan, serta melakukan penetapan kadar
minyak atsirinya menggunakan alat destilasi Stahl.
TEORI
Minyak atsiri merupakan suatu lipophilic mixtures yang mudah
menguap, yang pada umumnya diperoleh dengan cara destilasi uap dari
bagian-bagian suatu tumbuhan. Minyak atsiri mempunyai bau yang khas
dan tersusun oleh suatu susunan senyawa kimia yang kompleks yang
terdiri atas puluhan hingga ratusan komponen. Sifat umum dari minyak
atsiri adalah mudah menguap, berbau aromatik, bila masih segar
umumnya tidak berwarna atau kekuning-kuningan yang berubah
menjadi gelap pada pendiaman, tidak mengeruhkan air, optis aktif,
mempunyai indeks bias tinggi. Minyak atsiri yang diperoleh dengan cara
destilasi bila diteteskan pada kertas saring, tetesan tersebut tidak akan
meninggalkan bekas seperti bintik lemak.
Secara kimia umumnya minyak atsiri terdiri atas komponen-
komponen terpenoid, umumnya monoterpen dan seskuiterpen sebagai
penyusun utama. Selain itu terdapat berbagai komponen lain yang
merupakan komponen minor, yang terdiri atas senyawa-senyawa kimia
alifatik, aromatik, turunan benzena, dan lain-lain. Pada umumnya
komponen minyak atsiri golongan mono dan seskuiterpen merupakan
senyawa kimia turunan isopren C5H8. Monoterpen tersusun atas 2 unit
isopren, sedangkan seskuiterpen tersusun atas 3 unit isopren. Kedua
Modul Praktikum 4 FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 33
golongan tersebut masih terpilah lagi menjadi komponen-komponen lain
berdasarkan gugus fungsionalnya ataupun rangka strukturnya, misalnya
monoterpen dan seskuiterpen asiklik, monosiklik, atau bisiklik,
monoterpen atau seskuiterpen alkohol (misalnya eugenol), monoterpen
atau seskuiterpen aldehid (misalnya sitral), atau monoterpen dan
seskuiterpen keton (misalnya karvon).
Tergantung pada sifat tumbuhan asal atau minyak atsiri yang terkandung
didalamnya, dikenal berbagai cara isolasi minyak atsiri, misalnya :
1. Destilasi uap
Merupakan proses isolasi minyak atsiri dengan bantuan uap air. Air
dan uap air akan menembus dinding sel dan dengan adanya panas,
minyak atsiri akan terbawa oleh uap air. Pada pendinginan, minyak
atsiri akan terkondensasi dan terpisah dari airnya.
2. Pemerasan
Merupakan metode isolasi minyak atsiri yang sangat sederhana.
Bahan langsung diperas atau ditekan dengan suatu alat. Sel-sel yang
mengandung minyak atsiri akan pecah dan minyak atsirinya keluar.
Cara ini digunakan untuk tumbuhan yang mengandung cukup banyak
minyak atsiri. Keburukan cara ini adalah terjadinya pengotoran
minyak atsiri oleh zat warna yang ikut terperas.
3. Penyarian
Minyak atsiri dalam tumbuhan dapat diisolasi dengan cara penyarian
/ ekstraksi menggunakan pelarut yang non polar misalnya heksana,
atau pelarut yang kurang polar seperti misalnya alkohol. Pelarut
penyari kemudian dipisahkan dengan cara destilasi, hingga diperoleh
minyak atsiri yang terbebas dari pelarutnya.
4. Enfleurage
Cara ini merupakan cara klasik untuk isolasi minyak atsiri. Simplisia
yang mengandung minyak atsiri, misalnya bunga mawar ditempatkan
di atas lapisan semacam vaselin di atas papan. Setelah dibiarkan
Modul Praktikum 4 FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 34
beberapa lama, minyak atsiri akan terserap di dalam vaselin,
kemudian dipisahkan dari vaselinnya dengan cara destilasi.
PENETAPAN KADAR MINYAK ATSIRI
Penetapan kadar minyak atsiri yang paling sederhana dan paling
banyak dilakukan karena dianggap mudah, murah, tetapi cukup
terandalkan adalah dengan metode destilasi. Metode ini menggunakan
alat destilasi Stahl.
Cara penetapan kadar menurut metode destilasi Stahl ini ada dua,
yaitu :
Cara pertama :
Campur bahan yang akan diperiksa dalam labu dengan cairan penyuling
(air), pasang alat, isi buret dengan air hingga penuh, panaskan dengan
tangas udara hingga penyulingan berlangsung lambat tetapi teratur.
Setelah penyulingan selesai, biarkan selama tidak kurang dari 15 menit,
catat volume minyak atsiri pada buret. Hitung kadar minyak atsiri
dalam % b/v.
Cara kedua :
Dilakukan seperti cara pertama tetapi sebelum buret diisi penuh dengan
air, lebih dahulu diisi dengan 0,2 mL xilena yang diukur seksama. Volume
minyak atsiri dihitung dengan mengurangkan volume yang dibaca
dengan volume xilena.
Gambar. a. Alat destilasi uap dan air, b. Alat destilasi Stahl
Modul Praktikum 4 FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 35
Cara penetapan kadar minyak atsiri lain yang lebih canggih, lebih akurat,
tetapi memerlukan peralatan yang mahal adalah dengan cara
kromatografi gas. Dengan peralatan mutakhir, dalam sekali penetapan,
selain kadar minyak atsiri, kadar masing-masing komponen penyusun
minyak atsiri tersebut dapat sekaligus langsung diketahui.
PENETAPAN KUALITAS MINYAK ATSIRI
Penetapan kualitas minyak atsiri dilakukan sesuai dengan spesifikasi
masing-masing minyak atsiri yang dikeluarkan oleh Badan Standardisasi
Nasional (BSN) dalam bentuk Standar Nasional Indonesia (SNI). Ada
beberapa parameter yang perlu ditetapkan, diantaranya adalah
penetapan bobot jenis, penetapan indeks bias, dan rotasi optik. Selain itu,
pemeriksaan komponen minyak atsiri secara kualitatif dapat dilakukan
dengan kromatografi lapis tipis, serta secara kuantitatif dapat dilakukan
dengan kromatografi gas-spektrometri massa (GC-MS).
PUSTAKA
Ditjen POM. 1979. Materia Medika Indonesia. Jilid III. Departemen
Kesehatan Republik Indonesia. 153-154.
Harborne, J.B. 1987. Metode Fitokimia. Terjemahan: Kosasih P. Penerbit
ITB. Bandung. 123 – 131.
Modul Praktikum 4 FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 36
LEMBAR KERJA PRAKTIKUM FARMAKOGNOSI-FARMASI BAHAN ALAM
FAKULTAS FARMASI-UNIVERSITAS PADJADJARAN
PRAKTIKUM 4 : ISOLASI DAN PENETAPAN KADAR MINYAK ATSIRI
NAMA MAHASISWA : .............................................................
NPM : .............................................................
KELOMPOK : .............................................................
NAMA TANAMAN : .............................................................
NAMA SIMPLISIA : .............................................................
PROSEDUR :
Isolasi Minyak Atsiri menggunakan Metode Destilasi Uap dan Air.
1. Siapkan simplisia yang akan ditetapkan kadar minyak atsirinya.
Simplisia yang digunakan adalah bentuk rajangan yang telah
dipotong-potong atau diris-iris hingga derajat halus tertentu
2. Timbang sejumlah tertentu simplisia di atas, kemudian masukkan ke
dalam tabung alat destilasi dan ditempatkan di atas saringan yang
sudah diisi aquades di bawah saringannya.
3. Pasang alat destilasi, kemudian isi buret dengan aquades hingga
penuh .
4. Lakukan destilasi dengan alat pemanas, atur pemanasannya hingga
destilasi berjalan lambat tetapi teratur. Destilasi dilakukan sekurang-
kurangnya 3 jam
5. Hentikan pemanasan, biarkan dingin, lalu volume minyak atsiri yang
terjadi dicatat
6. Hitung kadar minyak atsirinya.
Perhitungan kadar minyak atsiri :
Modul Praktikum 4 FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 37
HASIL PERCOBAAN
Berat simplisia : ………………………… g
Lama destilasi/perendaman : ………………………… jam
Volume minyak atsiri : ………………………… mL
Kadar minyak atsiri : ………………………… %
Spesifikasi minyak atsiri :
Warna : …………………………
Bau : …………………………
Rasa : ………………………..
Modul Praktikum 4 FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
PANDUAN PRAKTIKUM FARMAKOGNOSI 2020 Halaman 38
LEMBAR KERJA PRAKTIKUM FARMAKOGNOSI-FARMASI BAHAN ALAM
FAKULTAS FARMASI-UNIVERSITAS PADJADJARAN
PRAKTIKUM 4 : Pemeriksaan Pola KLT Minyak Atsiri
NAMA MAHASISWA : .............................................................
NPM : .............................................................
KELOMPOK : .............................................................
NAMA TANAMAN : .............................................................
NAMA SIMPLISIA : .............................................................
FASE GERAK : .............................................................
PEMBANDING : .............................................................
Pola Kromatografi Lapis Tipis
Sinar Tampak UV λ 254 nm UV λ 366 nm
Bercak Rf
1
2
3
4
5
6
7
Modul Praktikum 4 FAKULTAS FARMASI UNIVERSITAS PADJADJARAN
Anda mungkin juga menyukai
- Soal Praktikum Farmakognosi 1Dokumen2 halamanSoal Praktikum Farmakognosi 1Chemayanti SurbaktiBelum ada peringkat
- BUKU SEM 2 Praktikum Kimia Analisa Pertemuan Ke-1 Oleh Erma Yunita PDFDokumen29 halamanBUKU SEM 2 Praktikum Kimia Analisa Pertemuan Ke-1 Oleh Erma Yunita PDFNina WidhiBelum ada peringkat
- D-11 - Skrining Resep - Muhammad Faisal NajibDokumen12 halamanD-11 - Skrining Resep - Muhammad Faisal NajibFaisal NajibBelum ada peringkat
- Farmakognosi Jilid 2 PDFDokumen66 halamanFarmakognosi Jilid 2 PDFabubabubwww100% (1)
- Farmakognosi 11Dokumen15 halamanFarmakognosi 11ekaludiatiBelum ada peringkat
- Pengantar Farmasi Fisika 0Dokumen12 halamanPengantar Farmasi Fisika 0mardia ningsihBelum ada peringkat
- Biokimia (Farmasi)Dokumen11 halamanBiokimia (Farmasi)sariBelum ada peringkat
- Farmakognosi IDokumen19 halamanFarmakognosi ISandro WagutBelum ada peringkat
- (SAP) Farmakognosi IDokumen14 halaman(SAP) Farmakognosi IDhwie YhulianieBelum ada peringkat
- Antihistamin Antitusiv SteroidDokumen12 halamanAntihistamin Antitusiv Steroidrobiatul islamiahBelum ada peringkat
- MODUL PRAKTIKUM FARMAKOGNOSI 2019 EDIT 29122019 (Baru)Dokumen168 halamanMODUL PRAKTIKUM FARMAKOGNOSI 2019 EDIT 29122019 (Baru)Dini NurhalizaBelum ada peringkat
- FarmakognosiDokumen34 halamanFarmakognosisatria yudaBelum ada peringkat
- FarmakognosiDokumen53 halamanFarmakognosiRahmaBelum ada peringkat
- Analisis Kualitatif Simplisia Daun Nosi 2Dokumen25 halamanAnalisis Kualitatif Simplisia Daun Nosi 2putu sintya dewiBelum ada peringkat
- Rps SterilDokumen7 halamanRps SterilYusnitaUsmanBelum ada peringkat
- BAB 1 PendahuluanDokumen1 halamanBAB 1 PendahuluanNetty Desii SinurayaBelum ada peringkat
- DIKTAT PRAKTIKUM FARMAKOGNOSI NEW + Daftar IsiDokumen68 halamanDIKTAT PRAKTIKUM FARMAKOGNOSI NEW + Daftar IsiMochiiBelum ada peringkat
- Rps Fitoterapi Gasal 19-20Dokumen8 halamanRps Fitoterapi Gasal 19-20Shinta Dewi SiregarBelum ada peringkat
- Konsep KefarmasianDokumen17 halamanKonsep KefarmasianMeryzaBelum ada peringkat
- RPS 4 Praktikum FarmakognosiDokumen4 halamanRPS 4 Praktikum FarmakognosiRomadhiyana KisnosaputriBelum ada peringkat
- Standarisasi Simplisia Daun Kemiri PKL KLPK 1.2Dokumen38 halamanStandarisasi Simplisia Daun Kemiri PKL KLPK 1.2ade rafniBelum ada peringkat
- Lect04 Dasar Dasar Larutan Dan KelarutanDokumen23 halamanLect04 Dasar Dasar Larutan Dan Kelarutanheru ferdiansyahBelum ada peringkat
- Amylum FitoDokumen27 halamanAmylum FitoAgus Kaharap0% (1)
- Kisi-Kisi PAS Farmakognosi Kelas XIDokumen13 halamanKisi-Kisi PAS Farmakognosi Kelas XIAthiya Khairun ZandiaBelum ada peringkat
- Farmakognosi IIDokumen8 halamanFarmakognosi IIPoppy Siska IsabellaBelum ada peringkat
- Salep Kelas 10Dokumen70 halamanSalep Kelas 10Muhammad Anugrah ArahimBelum ada peringkat
- FructusDokumen17 halamanFructusYanche Patrisius50% (2)
- Farmakognosi 1.1Dokumen55 halamanFarmakognosi 1.1Rangga Mandela100% (1)
- Ketentuan Umum Farmakope IndonesiaDokumen23 halamanKetentuan Umum Farmakope IndonesiaYorry Chiristine PamanginBelum ada peringkat
- Diktat Praktikum Botani Farmasi 2020Dokumen61 halamanDiktat Praktikum Botani Farmasi 2020Mubharroq YuliusBelum ada peringkat
- Rencana Pelaksanaan Pembelajaran TpsoDokumen66 halamanRencana Pelaksanaan Pembelajaran TpsoGunawan NataBelum ada peringkat
- Analisa Tablet Piridoksin HCL TTTDokumen5 halamanAnalisa Tablet Piridoksin HCL TTTLiu Andi50% (2)
- Minyak AtsiriDokumen81 halamanMinyak Atsiriamelwd100% (1)
- Laporan Farmakognosi AmilumDokumen6 halamanLaporan Farmakognosi AmilumIta LwkBelum ada peringkat
- Kisi Kisi Semi SolidDokumen3 halamanKisi Kisi Semi SolidAlawiyah MuzaemaBelum ada peringkat
- Modul Praktikum Dasar Teknologi FarmasiDokumen24 halamanModul Praktikum Dasar Teknologi FarmasiLiana AgustiaBelum ada peringkat
- Industri FarmasiDokumen18 halamanIndustri Farmasidea sukmaBelum ada peringkat
- Makroskopik Dan Mikroskopik SimplisiaDokumen9 halamanMakroskopik Dan Mikroskopik SimplisiaNur HayatiBelum ada peringkat
- KK 7 SwamedikasiDokumen11 halamanKK 7 Swamedikasizahratul hayah, S.farm., Apt100% (3)
- Tumbuhan Obat Sebagai Dasar PengembanganDokumen15 halamanTumbuhan Obat Sebagai Dasar PengembanganAisyahkuriskaBelum ada peringkat
- Daftar Nama Simplisia MakroskopisDokumen1 halamanDaftar Nama Simplisia Makroskopischipyavianti50% (2)
- Modul Praktikum FitokimiaDokumen32 halamanModul Praktikum FitokimiaB-071 Sevia SusantriBelum ada peringkat
- ValerianDokumen6 halamanValerianidullrufaidahBelum ada peringkat
- Bab Ii Tinjauan Pustaka II.1 Definisi SimplisiaDokumen16 halamanBab Ii Tinjauan Pustaka II.1 Definisi SimplisiaherlinaBelum ada peringkat
- AlkaloidDokumen22 halamanAlkaloidAtiik AjalaahBelum ada peringkat
- FLOSDokumen7 halamanFLOSElviana DewiBelum ada peringkat
- Signa Bahasa Latin FarmasiDokumen2 halamanSigna Bahasa Latin FarmasiHenny IndraBelum ada peringkat
- TUGAS Ke-10. ILMU RESEP. NURUL ANNISADokumen6 halamanTUGAS Ke-10. ILMU RESEP. NURUL ANNISANURUL ANNISABelum ada peringkat
- SemenDokumen2 halamanSemenM'muZack D'ertoseBelum ada peringkat
- Pengembangan Obat OKDokumen26 halamanPengembangan Obat OKsuciBelum ada peringkat
- Buku Petunjuk Prakt Pengantar Farmasi KlinikDokumen21 halamanBuku Petunjuk Prakt Pengantar Farmasi KlinikDonifernandoBelum ada peringkat
- Resep 2Dokumen3 halamanResep 2RiskaBelum ada peringkat
- Laporan Praktikum Farmakognosi MikroskopikDokumen22 halamanLaporan Praktikum Farmakognosi MikroskopikChanica Aninditya100% (2)
- SalepDokumen35 halamanSalepariffatul lailatussholikhah100% (1)
- Farmakognosi..ppt 13.Dokumen12 halamanFarmakognosi..ppt 13.indrarizalBelum ada peringkat
- P L.M, S, S, M.P .,A: PillulaeDokumen15 halamanP L.M, S, S, M.P .,A: PillulaeBonita HerawatiBelum ada peringkat
- Modul Praktikum Farmakognosi Ganjil 22-23Dokumen70 halamanModul Praktikum Farmakognosi Ganjil 22-23Sahla TahtaBelum ada peringkat
- PPMPM Objek 1Dokumen29 halamanPPMPM Objek 1Ds MicinnaruBelum ada peringkat
- Petunjuk PRAKTIKUM METPEM Ganjil 2020 2021 New 11112020Dokumen27 halamanPetunjuk PRAKTIKUM METPEM Ganjil 2020 2021 New 11112020Pande Ayu LaksmiBelum ada peringkat
- Modul Praktikum Insilico KmmiDokumen24 halamanModul Praktikum Insilico Kmmilauren pangestuBelum ada peringkat
- Post Test Praktikum Uji Aktivitas Senyawa Herbal Secara Insilico - 2021Dokumen6 halamanPost Test Praktikum Uji Aktivitas Senyawa Herbal Secara Insilico - 2021lauren pangestuBelum ada peringkat
- Post Test Praktikum Uji Aktivitas Senyawa Herbal Secara Insilico - 2021Dokumen6 halamanPost Test Praktikum Uji Aktivitas Senyawa Herbal Secara Insilico - 2021lauren pangestuBelum ada peringkat
- Biofarm AkaDokumen47 halamanBiofarm Akalauren pangestuBelum ada peringkat
- Pre Test Prak. in Silico Dan ToksisitasDokumen3 halamanPre Test Prak. in Silico Dan Toksisitaslauren pangestuBelum ada peringkat
- Penilaian Posttest Prak 2Dokumen5 halamanPenilaian Posttest Prak 2lauren pangestuBelum ada peringkat
- Literatur GambarDokumen6 halamanLiteratur Gambarlauren pangestuBelum ada peringkat
- Cam PuranDokumen22 halamanCam Puranlauren pangestuBelum ada peringkat
- Reaksi Pewarnaan PatiDokumen1 halamanReaksi Pewarnaan Patilauren pangestuBelum ada peringkat
- Prosedur (Lauren)Dokumen1 halamanProsedur (Lauren)lauren pangestuBelum ada peringkat
- Format Laporan Praktikum FarmakognosiDokumen3 halamanFormat Laporan Praktikum Farmakognosilauren pangestu0% (1)
- Format JurnalDokumen1 halamanFormat Jurnallauren pangestuBelum ada peringkat
- B - 260110190095 - Lauren Pangestu - Tugas Farmakognosi SteroidDokumen3 halamanB - 260110190095 - Lauren Pangestu - Tugas Farmakognosi Steroidlauren pangestuBelum ada peringkat
- Format JurnalDokumen1 halamanFormat Jurnallauren pangestuBelum ada peringkat
- 251 497 1 SMDokumen5 halaman251 497 1 SMfirmanBelum ada peringkat
- Hermawati Dian JayantiDokumen61 halamanHermawati Dian Jayantilauren pangestuBelum ada peringkat
- Ok Tinjauan Ras HerbalDokumen10 halamanOk Tinjauan Ras HerbalCikw KuzhaBelum ada peringkat
- 324 1075 3 PBDokumen14 halaman324 1075 3 PBNur Asni NurBelum ada peringkat
- Skizofernia Inter FiraDokumen7 halamanSkizofernia Inter FiraSujanaBelum ada peringkat
- Descriptive Study of Two Antipsychotics Combination and Parkinsonism Syndromes in Paranoid Schizophrenia TreatmentDokumen6 halamanDescriptive Study of Two Antipsychotics Combination and Parkinsonism Syndromes in Paranoid Schizophrenia Treatmentlauren pangestuBelum ada peringkat
- Laporan Praktikum Kimia Analisis KLTDokumen9 halamanLaporan Praktikum Kimia Analisis KLTRastinahBelum ada peringkat
- 126760308201008051Dokumen51 halaman126760308201008051Anityo NugrohoBelum ada peringkat
- Lembar Kerja Pengenalan Alkes Dan BHPDokumen7 halamanLembar Kerja Pengenalan Alkes Dan BHPlauren pangestuBelum ada peringkat
- Kasus Depresi MHSW 2021Dokumen1 halamanKasus Depresi MHSW 2021lauren pangestuBelum ada peringkat
- 2546 5581 1 SM PDFDokumen6 halaman2546 5581 1 SM PDFdian oktavianiBelum ada peringkat
- MeningitisDokumen2 halamanMeningitislauren pangestuBelum ada peringkat
- Lauren Pangestu - DifusiDokumen10 halamanLauren Pangestu - Difusilauren pangestuBelum ada peringkat
- Pembahasan ResepDokumen3 halamanPembahasan Reseplauren pangestuBelum ada peringkat
- Lauren PangestuDokumen15 halamanLauren Pangestulauren pangestuBelum ada peringkat