Sistem Periodik Unsur
Diunggah oleh
tik Rivai0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
8 tayangan3 halamansistem periodik unsur
Judul Asli
SISTEM_PERIODIK_UNSUR
Hak Cipta
© © All Rights Reserved
Format Tersedia
DOCX, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen Inisistem periodik unsur
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
8 tayangan3 halamanSistem Periodik Unsur
Diunggah oleh
tik Rivaisistem periodik unsur
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 3
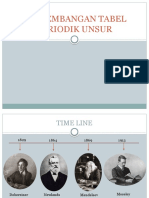
SISTEM PERIODIK UNSUR
SPU Modern terdiri atas 7 periode. Tiap-tiap
1). Pengelompokan atas dasar Logam dan Non Logam periode menyatakan jumlah / banyaknya kulit atom
v Dikemukakan oleh Lavoisier unsur-unsur yang menempati periode-periode
v Pengelompokan ini masih sangat sederhana, sebab antara tersebut.
unsur-unsur logam sendiri masih terdapat banyak
perbedaan. Nomor Periode = Jumlah Kulit Atom
2). Hukum Triade Dobereiner
Dikemukakan oleh Johan Wolfgang Dobereiner Jadi :
(Jerman). Jumlah unsur pada setiap periode :
Unsur-unsur dikelompokkan ke dalam kelompok Periode Jumlah Unsur Nomor Atom ( Z )
tiga unsur yang disebut Triade. 1 2 1–2
Dasarnya : kemiripan sifat fisika dan kimia dari 2 8 3 – 10
unsur-unsur tersebut. 3 8 11 – 18
Jenis Triade : 4 18 19 – 36
1. Triade Litium (Li), Natrium (Na) dan Kalium (K) 5 18 37 – 54
Unsur Massa Atom Wujud 6 32 55 – 86
Li 6,94 Padat 7 32 87 – 118
Na 22,99 Padat
K 39,10 Padat Catatan :
Massa Atom Na (Ar Na) = = 23,02 a) Periode 1, 2 dan 3 disebut periode pendek karena berisi
2. Triade Kalsium ( Ca ), Stronsium ( Sr ) dan relatif sedikit unsur
Barium ( Ba ) b) Periode 4 dan seterusnya disebut periode panjang
3. Triade Klor ( Cl ), Brom ( Br ) dan Iod ( I ) c) Periode 7 disebut periode belum lengkap karena belum
3). Hukum Oktaf Newlands sampai ke golongan VIII A.
v Dikemukakan oleh John Newlands (Inggris). d) Untuk mengetahui nomor periode suatu unsur
v Unsur-unsur dikelompokkan berdasarkan kenaikan massa berdasarkan nomor atomnya, Anda hanya perlu mengetahui
atom relatifnya (Ar). nomor atom unsur yang memulai setiap periode
v Unsur ke-8 memiliki sifat kimia mirip dengan unsur
pertama; unsur ke-9 memiliki sifat yang mirip dengan unsur Unsur-unsur yang memiliki 1 kulit (kulit K saja)
ke-2 dst. terletak pada periode 1 (baris 1), unsur-unsur yang
v Sifat-sifat unsur yang ditemukan berkala atau periodik memiliki 2 kulit (kulit K dan L) terletak pada
setelah 8 unsur disebut Hukum Oktaf. periode ke-2 dst.
H Li Be B C N O Contoh :
F Na Mg Al Si P S 9F = 2 , 7 periode ke-2
Cl K Ca Cr Ti Mn Fe 12Mg = 2 , 8 , 2 periode ke-3
Berdasarkan Daftar Oktaf Newlands di atas; unsur H, F dan Cl 31Ga = 2 , 8 , 18 , 3 periode ke-4
mempunyai kemiripan sifat. 2). Golongan
ü Sistem periodik terdiri atas 18 kolom vertikal yang disebut
4). Sistem Periodik Mendeleev (Sistem Periodik golongan
Pendek) ü Ada 2 cara penamaan golongan :
ü Dua ahli kimia, Lothar Meyer (Jerman) dan Dmitri a) Sistem 8 golongan
Ivanovich Mendeleev (Rusia) berdasarkan pada prinsip dari Menurut cara ini, sistem periodik dibagi menjadi 8 golongan
Newlands, melakukan penggolongan unsur. yaitu golongan utama (golongan A) dan 8 golongan transisi
ü Lothar Meyer lebih mengutamakan sifat-sifat kimia unsur (golongan B).
sedangkan Mendeleev lebih mengutamakan kenaikan massa b) Sistem 18 golongan
atom. Menurut cara ini, sistem periodik dibagi menjadi 18 golongan
ü Menurut Mendeleev : sifat-sifat unsur adalah fungsi yaitu golongan 1 sampai 18, dimulai dari kolom paling kiri.
periodik dari massa atom relatifnya. Artinya : jika unsur- ü Unsur-unsur yang mempunyai elektron valensi sama
unsur disusun menurut kenaikan massa atom relatifnya, ditempatkan pada golongan yang sama.
maka sifat tertentu akan berulang secara periodik. ü Untuk unsur-unsur golongan A sesuai dengan letaknya
ü Unsur-unsur yang memiliki sifat-sifat serupa ditempatkan dalam sistem periodik :
pada satu lajur tegak, disebut Golongan.
ü Sedangkan lajur horizontal, untuk unsur-unsur
berdasarkan pada kenaikan massa atom relatifnya dan
disebut Periode. Nomor Golongan = Jumlah Elektron Valensi
5). Sistem Periodik Modern (Sistem Periodik Panjang) ü Unsur-unsur golongan A mempunyai nama lain yaitu :
Dikemukakan oleh Henry G Moseley, yang 1. Golongan IA = golongan Alkali
berpendapat bahwa sifat-sifat unsur merupakan 2. Golongan IIA = golongan Alkali Tanah
fungsi periodik dari nomor atomnya. 3. Golongan IIIA = golongan Boron
4. Golongan IVA = golongan Karbon
Artinya : sifat dasar suatu unsur ditentukan oleh
5. Golongan VA = golongan Nitrogen
nomor atomnya bukan oleh massa atom relatifnya
6. Golongan VIA = golongan Oksigen
(Ar).
7. Golongan VIIA = golongan Halida / Halogen
8. Golongan VIIIA = golongan Gas Mulia
1. B. PERIODE DAN GOLONGAN DALAM SPU
1. C. SIFAT-SIFAT PERIODIK UNSUR
MODERN
Meliputi :
1). Periode
1). Jari-Jari Atom
Adalah lajur-lajur horizontal pada tabel periodik.
Adalah jarak dari inti atom sampai ke elektron di Semakin negatif harga afinitas elektron,
kulit terluar. semakin mudah atom tersebut menerima/menarik
Besarnya jari-jari atom dipengaruhi oleh besarnya elektron dan semakin reaktif pula unsurnya.
nomor atom unsur tersebut. Afinitas elektron bukanlah kebalikan dari energi
Semakin besar nomor atom unsur-unsur ionisasi.
segolongan, semakin banyak pula jumlah kulit Dalam satu golongan (dari atas ke bawah), harga
elektronnya, sehingga semakin besar pula jari-jari afinitas elektronnya semakin kecil.
atomnya. Dalam satu periode (dari kiri ke kanan), harga
Jadi : dalam satu golongan (dari atas ke bawah), jari-jari afinitas elektronnya semakin besar.
atomnya semakin besar. Unsur golongan utama memiliki afinitas elektron
Dalam satu periode (dari kiri ke kanan), nomor bertanda negatif, kecuali golongan IIA dan VIIIA.
atomnya bertambah yang berarti semakin Afinitas elektron terbesar dimiliki golongan VIIA (
bertambahnya muatan inti, sedangkan jumlah kulit halogen ).
elektronnya tetap. Akibatnya tarikan inti terhadap 5). Keelektronegatifan
elektron terluar makin besar pula, sehingga
Adalah kemampuan suatu unsur untuk menarik
menyebabkan semakin kecilnya jari-jari atom.
elektron dalam molekul suatu senyawa (dalam
Jadi : dalam satu periode (dari kiri ke kanan), jari-jari
ikatannya).
atomnya semakin kecil.
Diukur dengan menggunakan skala Pauling yang
2). Jari-Jari Ion besarnya antara 0,7 (keelektronegatifan Cs) sampai
v Ion mempunyai jari-jari yang berbeda secara nyata 4 (keelektronegatifan F).
(signifikan) jika dibandingkan dengan jari-jari atom Unsur yang mempunyai harga keelektronegatifan
netralnya. besar, cenderung menerima elektron dan akan
v Ion bermuatan positif (kation) mempunyai jari-jari yang membentuk ion negatif (anion).
lebih kecil, sedangkan ion bermuatan negatif (anion) Unsur yang mempunyai harga keelektronegatifan
mempunyai jari-jari yang lebih besar jika dibandingkan kecil, cenderung melepaskan elektron dan akan
dengan jari-jari atom netralnya. membentuk ion positif (kation).
Dalam satu golongan (dari atas ke bawah), harga
3). Energi Ionisasi ( satuannya = kJ.mol-1 ) keelektronegatifan semakin kecil.
ü Adalah energi minimum yang diperlukan atom netral Dalam satu periode (dari kiri ke kanan), harga
dalam wujud gas untuk melepaskan satu elektron sehingga keelektronegatifan semakin besar.
membentuk ion bermuatan +1 (kation). 6). Sifat Logam dan Non Logam
ü Jika atom tersebut melepaskan elektronnya yang ke-2
Sifat logam dikaitkan dengan keelektropositifan,
maka akan diperlukan energi yang lebih besar (disebut
yaitu kecenderungan atom untuk melepaskan
energi ionisasi kedua), dst.
elektron membentuk kation.
EI 1 < EI 2 < EI 3 dst
ü Dalam satu golongan (dari atas ke bawah), EI semakin Sifat logam bergantung pada besarnya energi
kecil karena jari-jari atom bertambah sehingga gaya tarik inti ionisasi ( EI ).
terhadap elektron terluar semakin kecil. Akibatnya elektron Makin besar harga EI, makin sulit bagi atom untuk
terluar semakin mudah untuk dilepaskan. melepaskan elektron dan makin berkurang sifat
ü Dalam satu periode (dari kiri ke kanan), EI semakin logamnya.
besar karena jari-jari atom semakin kecil sehingga gaya tarik Sifat non logam dikaitkan dengan
inti terhadap elektron terluar semakin besar/kuat. Akibatnya keelektronegatifan, yaitu kecenderungan atom
elektron terluar semakin sulit untuk dilepaskan. untuk menarik elektron.
Dalam satu periode (dari kiri ke kanan), sifat
4). Afinitas Elektron ( satuannya = kJ.mol-1 ) logam berkurang sedangkan sifat non logam
Adalah energi yang dilepaskan atau diserap oleh bertambah.
atom netral dalam wujud gas apabila menerima Dalam satu golongan (dari atas ke bawah), sifat
sebuah elektron untuk membentuk ion negatif logam bertambah sedangkan sifat non logam
(anion). berkurang.
Unsur logam terletak pada bagian kiri-bawah dalam
Beberapa hal yang harus diperhatikan : sistem periodik unsur, sedangkan unsur non logam
a) Penyerapan elektron ada yang disertai pelepasan terletak pada bagian kanan-atas.
energi maupun penyerapan energi. Unsur yang paling bersifat non logam adalah
b) Jika penyerapan elektron disertai pelepasan energi, unsur-unsur yang terletak pada golongan VIIA,
maka harga afinitas elektronnya dinyatakan dengan tanda bukan golongan VIIIA.
negatif.
c) Jika penyerapan elektron disertai penyerapan energi,
Unsur-unsur yang terletak pada daerah peralihan
maka harga afinitas elektronnya dinyatakan dengan tanda antara unsur logam dengan non logam disebut
unsur Metaloid ( = unsur yang mempunyai sifat
positif.
d) Unsur yang mempunyai harga afinitas elektron logam dan sekaligus non logam ). Misalnya : boron
dan silikon.
bertanda negatif, mempunyai daya tarik elektron yang
lebih besar daripada unsur yang mempunyai harga afinitas 7). Kereaktifan
elektron bertanda positif. Atau semakin negatif harga afinitas Kereaktifan bergantung pada kecenderungan unsur
elektron suatu unsur, semakin besar kecenderungan unsur untuk melepas atau menarik elektron.
tersebut untuk menarik elektron membentuk ion negatif Unsur logam yang paling reaktif adalah golongan
(anion). IA (logam alkali).
Unsur non logam yang paling reaktif adalah
golongan VIIA (halogen).
Dalam satu periode (dari kiri ke kanan), mula-
mula kereaktifan menurun, kemudian semakin
bertambah hingga golongan VIIA.
Golongan VIIIA merupakan unsur yang paling
tidak reaktif.
Anda mungkin juga menyukai
- Materi Kimia Kls X Semester 1 Bab 3Dokumen5 halamanMateri Kimia Kls X Semester 1 Bab 3-Nduuh Newbie-Belum ada peringkat
- Sistem Periodik UnsurDokumen40 halamanSistem Periodik UnsurFajrian FaridhoBelum ada peringkat
- Sistem PeriodiK UnsurDokumen19 halamanSistem PeriodiK UnsurRyan AsyhariBelum ada peringkat
- Sistem Periodik UnsurDokumen10 halamanSistem Periodik UnsurBintang Wahyu AjiBelum ada peringkat
- LKPD Polimer AnnaDokumen19 halamanLKPD Polimer AnnaAnonymous rr1bspu0OQ100% (2)
- Sejarah Perkembangan Sistem Periodik Unsur Dan Konfigurasi ElektronDokumen11 halamanSejarah Perkembangan Sistem Periodik Unsur Dan Konfigurasi ElektronVira FeverBelum ada peringkat
- Sistem Periodik Unsur KimiaDokumen21 halamanSistem Periodik Unsur KimiaYeni Khomaria100% (1)
- Bab 3 Sistim Periodik Unsur Sem1Dokumen5 halamanBab 3 Sistim Periodik Unsur Sem1nadnod620Belum ada peringkat
- Materi Kimia Kelas X Bab 3 PDFDokumen5 halamanMateri Kimia Kelas X Bab 3 PDFMohamad Nor AufaBelum ada peringkat
- Materi Kimia Kelas XI Bab 3Dokumen5 halamanMateri Kimia Kelas XI Bab 3Zoe.FiversBelum ada peringkat
- Adoc - Pub - Perkembangan Sistem Periodik UnsurDokumen9 halamanAdoc - Pub - Perkembangan Sistem Periodik UnsurPanji IndraBelum ada peringkat
- SIFAT_KEPERIODIKANDokumen16 halamanSIFAT_KEPERIODIKANNita NurBelum ada peringkat
- Materi kimia Kelas X Bab 3Dokumen10 halamanMateri kimia Kelas X Bab 3AnakLeta AnulBelum ada peringkat
- Bagi Materi Kimia Kelas X Bab 3Dokumen5 halamanBagi Materi Kimia Kelas X Bab 3Naeli Sururoh S.Pd.Belum ada peringkat
- Kimia Bab 2 Struktur AtomDokumen10 halamanKimia Bab 2 Struktur AtomdidinBelum ada peringkat
- MODUL Pembelajaran KimiaDokumen26 halamanMODUL Pembelajaran KimiaRosyid MahyudiBelum ada peringkat
- Ringkasan Materi SPUDokumen5 halamanRingkasan Materi SPUSiti SarwaniBelum ada peringkat
- MMMDokumen30 halamanMMMAnanda DwiBelum ada peringkat
- SP UnsurDokumen15 halamanSP UnsurIqis nisaBelum ada peringkat
- Materi Kimia Kelas XDokumen6 halamanMateri Kimia Kelas XYokoSimanjuntakBelum ada peringkat
- Sistem Periodik Unsur - KIMIA KELAS XDokumen6 halamanSistem Periodik Unsur - KIMIA KELAS XTabitha Maudy Charoline Ginting100% (1)
- Sistem Periodik Unsur, Struktur AtomDokumen36 halamanSistem Periodik Unsur, Struktur AtomMiftahul JannahBelum ada peringkat
- Sistem PeriodikDokumen21 halamanSistem PeriodikUmi Uminah100% (1)
- Tabel PeriodikDokumen32 halamanTabel PeriodikFransiskus Ricardo Adianto XI E SMA KarangturiBelum ada peringkat
- Struktur Tabel Periodik UnsurDokumen4 halamanStruktur Tabel Periodik UnsursindyBelum ada peringkat
- SPU_PERIODIKDokumen33 halamanSPU_PERIODIKMery Fitriani 2105110196Belum ada peringkat
- Sistem Periodik ModernDokumen6 halamanSistem Periodik ModernmahesBelum ada peringkat
- SISPERIODokumen5 halamanSISPERIONurul Fahmi zulkarnainBelum ada peringkat
- 6 LKS SpuDokumen4 halaman6 LKS SpuNadya RianasariBelum ada peringkat
- Sistem Periodik UnsurDokumen14 halamanSistem Periodik UnsuratikaBelum ada peringkat
- Tabel PeriodikDokumen28 halamanTabel PeriodikfrenaldoBelum ada peringkat
- SS4 Perkembangan Tabel Periodik UnsurDokumen13 halamanSS4 Perkembangan Tabel Periodik Unsurnur hidayantiBelum ada peringkat
- X Kimia KD 3.3 Sistem Periodik Unsur ZA 170923Dokumen12 halamanX Kimia KD 3.3 Sistem Periodik Unsur ZA 170923andiqiammulsyafiahBelum ada peringkat
- Struktur Atom dan Sifat PeriodikDokumen25 halamanStruktur Atom dan Sifat PeriodikDavid Julianto SiraitBelum ada peringkat
- Pertemuan 11. Sistem Periodik UnsurDokumen17 halamanPertemuan 11. Sistem Periodik UnsurAziz ZakiBelum ada peringkat
- Konfigurasi Elektron Dan Elektron ValensiDokumen32 halamanKonfigurasi Elektron Dan Elektron ValensiFeri ArifinBelum ada peringkat
- X Bab 2 - Sistem Periodik UnsurDokumen34 halamanX Bab 2 - Sistem Periodik UnsurZulkarnain ZulkarnainBelum ada peringkat
- Materi Kimia Dasar dan Sistem Periodik UnsurDokumen58 halamanMateri Kimia Dasar dan Sistem Periodik UnsurAtikatul MutmainahBelum ada peringkat
- Perkembangan Sistem Periodik UnsurDokumen22 halamanPerkembangan Sistem Periodik UnsurninizBelum ada peringkat
- SPU pptDokumen38 halamanSPU pptDyan SeptyanBelum ada peringkat
- Lembar Kerja Tugas KImia-Deriski X-4Dokumen2 halamanLembar Kerja Tugas KImia-Deriski X-4Deriski JanuarBelum ada peringkat
- Sistem Periodik UnsurDokumen6 halamanSistem Periodik UnsurAbdul Gaffar HadiBelum ada peringkat
- BARU PERKEMBANGAN TABEL PERIODIK UNSUR - PPT (Autosaved)Dokumen36 halamanBARU PERKEMBANGAN TABEL PERIODIK UNSUR - PPT (Autosaved)Samudra ArifBelum ada peringkat
- Strukturatomsistem PeriodikDokumen45 halamanStrukturatomsistem PeriodikErin FebrianBelum ada peringkat
- Periodisasi UnsurDokumen16 halamanPeriodisasi UnsurNur WahyuniBelum ada peringkat
- Sistem Periodik UnsurDokumen9 halamanSistem Periodik UnsurRindi Septiani DepariBelum ada peringkat
- Ringkasan Materi Sistem Periodik UnsurDokumen10 halamanRingkasan Materi Sistem Periodik UnsurYuyun Mustika SuryaniBelum ada peringkat
- 4.sistem Periodik UnsurDokumen24 halaman4.sistem Periodik Unsurelang bawanaBelum ada peringkat
- SPU Sistem Periodik UnsurDokumen7 halamanSPU Sistem Periodik UnsurRatna AvitasariBelum ada peringkat
- Modul SPUDokumen31 halamanModul SPUMubaid IsngariBelum ada peringkat
- Sistem Periodik UnsurDokumen3 halamanSistem Periodik UnsurSiska HafshariBelum ada peringkat
- Makalah SpuDokumen24 halamanMakalah SpuDhita LinchBelum ada peringkat
- (Template) Perkembangan Sistem Periodik Upaya Untuk Mengelompokkan UnsurDokumen11 halaman(Template) Perkembangan Sistem Periodik Upaya Untuk Mengelompokkan UnsurnovriBelum ada peringkat
- Sistem Periodik Unsur dan Sifat KepriodikannyaDokumen17 halamanSistem Periodik Unsur dan Sifat KepriodikannyaPUTRI FEBRIANTIBelum ada peringkat
- Wayan Lusi Oktaviana - 1913023016 - LKM 3 PRINSIP2 ANORGANIK PDFDokumen12 halamanWayan Lusi Oktaviana - 1913023016 - LKM 3 PRINSIP2 ANORGANIK PDFWayan Lusi OktavianaBelum ada peringkat
- Lecture Note Sesi 10 Sistem Periodik UnsurDokumen13 halamanLecture Note Sesi 10 Sistem Periodik UnsurberkasmengajardanangBelum ada peringkat
- Sistem Periodik UnsurDokumen30 halamanSistem Periodik UnsurSkuy SkyBelum ada peringkat
- Sistem Periodik Unsur KimiaDokumen3 halamanSistem Periodik Unsur KimiaMika FebrianiBelum ada peringkat
- Resume 15 - Sakira Molania Jacky - 21129302Dokumen21 halamanResume 15 - Sakira Molania Jacky - 21129302SedekahjariyahBelum ada peringkat
- P5 Daftar Hadir SiswaDokumen10 halamanP5 Daftar Hadir Siswatik RivaiBelum ada peringkat
- Pencemaran Lingkungan Dan SolusinyaDokumen6 halamanPencemaran Lingkungan Dan SolusinyaJskaBelum ada peringkat
- Analisis Dampak Pembangunan Hotel Terhadap Sanitasi Lingkungandi YogyakartaDokumen17 halamanAnalisis Dampak Pembangunan Hotel Terhadap Sanitasi Lingkungandi Yogyakartarindang santiagoBelum ada peringkat
- IKATAN KOVALENDokumen7 halamanIKATAN KOVALENtik RivaiBelum ada peringkat
- PTK Kimia Hidrokarbon 2Dokumen121 halamanPTK Kimia Hidrokarbon 2ꓰꓡꓡꓰꓠ-ꓓꓰꓖꓰꓠꓰꓣꓰꓢꓢ.100% (2)
- KimiaDokumen8 halamanKimiatik RivaiBelum ada peringkat
- Soal Dinamika SosialDokumen2 halamanSoal Dinamika Sosialtik RivaiBelum ada peringkat
- Hukum Dasar Kimia (Lavoisier, Proust, Dalton)Dokumen26 halamanHukum Dasar Kimia (Lavoisier, Proust, Dalton)tik RivaiBelum ada peringkat
- MediaDokumen8 halamanMediatik RivaiBelum ada peringkat
- IKATAN KOVALENDokumen7 halamanIKATAN KOVALENtik RivaiBelum ada peringkat
- Lamp. Peta KonsepDokumen1 halamanLamp. Peta Konseptik RivaiBelum ada peringkat
- Printable Idul Adha HomeducationDokumen10 halamanPrintable Idul Adha Homeducationindah susantiBelum ada peringkat
- Media 2Dokumen15 halamanMedia 2tik RivaiBelum ada peringkat
- Media Penguatan KonsepDokumen11 halamanMedia Penguatan Konseptik RivaiBelum ada peringkat
- KIMIA DASARDokumen25 halamanKIMIA DASARtik RivaiBelum ada peringkat
- Hidrokarbon SoalDokumen6 halamanHidrokarbon Soaltik RivaiBelum ada peringkat
- PolimerDokumen6 halamanPolimertik RivaiBelum ada peringkat
- Program Kerja Ekstra Bola VoliDokumen2 halamanProgram Kerja Ekstra Bola VoliChelsea WhiteBelum ada peringkat
- Soal Tugas Xi FDokumen3 halamanSoal Tugas Xi Ftik RivaiBelum ada peringkat
- Pola Hidup Sehat 1 10 PDFDokumen10 halamanPola Hidup Sehat 1 10 PDFGalih IrvandiBelum ada peringkat
- Ulangan IPADokumen6 halamanUlangan IPAtik RivaiBelum ada peringkat
- POLUSIDokumen8 halamanPOLUSItik RivaiBelum ada peringkat
- Manajemen PMRDokumen54 halamanManajemen PMRUbet ZubaidiBelum ada peringkat
- KIMIA DASARDokumen8 halamanKIMIA DASARtik RivaiBelum ada peringkat
- PROGRAM PASKIBRADokumen8 halamanPROGRAM PASKIBRAtik RivaiBelum ada peringkat
- English ClubDokumen9 halamanEnglish Clubtik RivaiBelum ada peringkat
- Surat Dukungan Kepala Sekolah Calon Peserta PPGPDokumen1 halamanSurat Dukungan Kepala Sekolah Calon Peserta PPGPWinoto AliaBelum ada peringkat
- HASIL PASDokumen9 halamanHASIL PAStik RivaiBelum ada peringkat
- Format PROGKER EXTRA 15Dokumen5 halamanFormat PROGKER EXTRA 15tik RivaiBelum ada peringkat