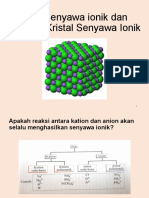
Kelompok 10
Diunggah oleh
Latoya WalkerDeskripsi Asli:
Judul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Kelompok 10
Diunggah oleh
Latoya WalkerHak Cipta:
Format Tersedia
Teori VSEPR adalah teori yang menduga bentuk molekul atau susunan geometrik dari pasangan elektron di sekitar
atom pusat sebagai akibat tolak-menolak aantara pasangan elektron. Jenis senyawa untuk membuktikan teori VSEPR adalah CF4 Bentuk Molekul adalah tetrahedral karena atom pusat C mengikat 4 pasangan elektron F. Tetrahedral memiliki empat sisi atau muka yang semuanya berupa segitiga sama sisi. Dalam molekul tetrahedral atom pusatnya terletak pada pusaat terahedron dan empat atom lainnya terletak pada sudut-sudut.sudut ikatannya 109,5. Ikatan pada senyawa CF4 adalah ikatan kovalen non polar, karena bentuk molekul pada CF4 adalah simeteris dan keelektronegatifan atau kerapatan elektron merata sehingga menyebabkan pusat muatan negatif berimpit dengan muatan positif. Hibridisasi pada CF4 adalah 1s2 2s2 2p2 Dengan menentukan hibridisasi pada C maka diperoleh bentuk molekul sp3 Menentukan jumlah Pasangan elektron bebas dan pasangan elektron terikat. CF4 1. Elektron valensi C 2. Jumlah atom F 3. Domain Elektron 4. PEB 5. PEI
6. Tipe ikatan 7. Bentuk Molekul
:4 :4 : 4+4/2= 4 : 4+4/0= 0 : 4-0= 4 :AX4 : Terahedral F
Anda mungkin juga menyukai
- Reaksi InterkalasiDokumen15 halamanReaksi InterkalasiRistya Redystia PurwodiningsihBelum ada peringkat
- Bab IiDokumen14 halamanBab IiElisa ManaluBelum ada peringkat
- Persentasi AnorDokumen5 halamanPersentasi AnorZellaBelum ada peringkat
- Kelompok 1 - Bentuk MolekulDokumen29 halamanKelompok 1 - Bentuk MolekulHeraBelum ada peringkat
- Sel ElektrokimiaDokumen6 halamanSel ElektrokimiaFarah CrisnadityaBelum ada peringkat
- Paper KonduktometriDokumen4 halamanPaper KonduktometriGhafur MagnaeBelum ada peringkat
- Kimia Koordinasi Bag I A PoncoDokumen17 halamanKimia Koordinasi Bag I A PoncoArdian FirmansyahBelum ada peringkat
- Menguasai Kimia Kuantum PDFDokumen62 halamanMenguasai Kimia Kuantum PDFRichardus Ngabut, S.Pd.,Gr.Belum ada peringkat
- Orbital MolekulDokumen21 halamanOrbital MolekulLhyna AlonelyBelum ada peringkat
- HibridisasiDokumen16 halamanHibridisasiHusnul KhotimahBelum ada peringkat
- Katalis OrganologamDokumen10 halamanKatalis Organologamronawati silabanBelum ada peringkat
- 1 - Laporan - Percobaan 1 - Novian Rico Saputra - Kimia - 1001Dokumen31 halaman1 - Laporan - Percobaan 1 - Novian Rico Saputra - Kimia - 1001Novian Rico SaputraBelum ada peringkat
- PERCOBAAN II (Reaksi Kimia Gejala Umum Dan Laju Reaksi)Dokumen30 halamanPERCOBAAN II (Reaksi Kimia Gejala Umum Dan Laju Reaksi)ade dosmariaBelum ada peringkat
- Proses Ekstraksi NatriumDokumen5 halamanProses Ekstraksi NatriumMuhammad FadlilahBelum ada peringkat
- MIRAERIDABASRI LAPORANMODUL4 Dikonversi PDFDokumen18 halamanMIRAERIDABASRI LAPORANMODUL4 Dikonversi PDFRiyanto WidodoBelum ada peringkat
- C3 IchiDokumen29 halamanC3 IchiSilky Amanda YuniarBelum ada peringkat
- Modul 5 Sik Tugas PendahuluanDokumen1 halamanModul 5 Sik Tugas PendahuluanElvina Laksmi KhairunisaBelum ada peringkat
- Ikatan Logam Serta Proses Pembentukan Dan ContohnyaDokumen4 halamanIkatan Logam Serta Proses Pembentukan Dan ContohnyaAl BaihaqiBelum ada peringkat
- Daftar PustakaDokumen2 halamanDaftar PustakawikaBelum ada peringkat
- Kunci JawabanDokumen4 halamanKunci Jawabanaripratama.aripBelum ada peringkat
- Bab 1.ikatan Kim2Dokumen25 halamanBab 1.ikatan Kim2andyBelum ada peringkat
- Rangkuman Kimia OrganikDokumen5 halamanRangkuman Kimia OrganikrinaBelum ada peringkat
- Lavoisier Mendapat Julukan Sebagai Bapak Kimia Modern Karena Menggolongkan Unsur Kimia Yang Dikenal Saat Itu Secara IlmiahDokumen5 halamanLavoisier Mendapat Julukan Sebagai Bapak Kimia Modern Karena Menggolongkan Unsur Kimia Yang Dikenal Saat Itu Secara IlmiahYuhanidha SitiBelum ada peringkat
- Muatan Formal AsambasaDokumen10 halamanMuatan Formal AsambasaAsty AnaBelum ada peringkat
- Laporan Praktikum Kimia FisikaDokumen29 halamanLaporan Praktikum Kimia FisikaL.a. Putu HendrayaniBelum ada peringkat
- Aldehida Dan KetonDokumen11 halamanAldehida Dan KetonAmaliatul KhusnaBelum ada peringkat
- Makalah Teori KuantumDokumen25 halamanMakalah Teori KuantumFarista Galuh SandraBelum ada peringkat
- Septia Adella 1301792 Analisis ButanaDokumen10 halamanSeptia Adella 1301792 Analisis Butanaseptia0% (1)
- Rangkuman Spektrokopi Massa JadiDokumen16 halamanRangkuman Spektrokopi Massa JadiChoYoorinBelum ada peringkat
- Struktur Elektronik AtomDokumen12 halamanStruktur Elektronik AtomMuh Nur FauziBelum ada peringkat
- Aplikasi Asam LewisDokumen4 halamanAplikasi Asam LewisazizatunnisaaBelum ada peringkat
- Ikatan KimiaDokumen37 halamanIkatan Kimiawahyu rahmadhanBelum ada peringkat
- Konstruksi Dan Operasi Sel VoltaDokumen2 halamanKonstruksi Dan Operasi Sel VoltaAlit Supriyana PutraBelum ada peringkat
- Katalis HomogenDokumen13 halamanKatalis HomogenArsendi NugrahaBelum ada peringkat
- p1 Dan p2 Panjang Ikatan EnergiDokumen15 halamanp1 Dan p2 Panjang Ikatan EnergiCut Khana MelianiBelum ada peringkat
- Kompleks Trigonal BipiramidalDokumen6 halamanKompleks Trigonal BipiramidalShinta PurnamasariBelum ada peringkat
- Makalah Tentang Simetri MolekulDokumen6 halamanMakalah Tentang Simetri MolekulDianKemalaAstutiBelum ada peringkat
- Spontanitas Dan Kesetimbangan1Dokumen15 halamanSpontanitas Dan Kesetimbangan1Alfiano FuadiBelum ada peringkat
- Materi Kekuatan LiganDokumen26 halamanMateri Kekuatan LiganNurul Rizki AriniBelum ada peringkat
- James E HuheeyDokumen235 halamanJames E HuheeyLulu Ciprutz Ajjah100% (2)
- Tugas Ikatan KimiaDokumen21 halamanTugas Ikatan KimiaアニタBelum ada peringkat
- ALKANADokumen2 halamanALKANASiti FatimahBelum ada peringkat
- Teori Molekul OrbitalDokumen19 halamanTeori Molekul OrbitalAiniRizkaBelum ada peringkat
- Soal Latihan 1Dokumen2 halamanSoal Latihan 1Hevliza TiaraBelum ada peringkat
- 5 HibridisasiDokumen28 halaman5 HibridisasiRikaRasti DestaMasyaBelum ada peringkat
- Handbook of Positive PsychologyDokumen36 halamanHandbook of Positive PsychologyIrene SatriawanBelum ada peringkat
- Laporan ElektrolisisDokumen7 halamanLaporan ElektrolisisLailatul BadriyahBelum ada peringkat
- Analitik 1 GaniDokumen102 halamanAnalitik 1 GaniMuhammad Hambari50% (2)
- Kimia KoordinasiDokumen4 halamanKimia KoordinasiEMardinusBelum ada peringkat
- 3-Bahan Ajar Sel VoltaDokumen21 halaman3-Bahan Ajar Sel VoltaDian MustikasariBelum ada peringkat
- Efek ComptonDokumen3 halamanEfek ComptonGhinaBelum ada peringkat
- Inti AtomDokumen30 halamanInti AtomMaulanaBelum ada peringkat
- Kristal Ionik Dan KovalenDokumen7 halamanKristal Ionik Dan KovalenRisna AmaliaBelum ada peringkat
- MolekulDokumen22 halamanMolekulridhoBelum ada peringkat
- Soal Dan PembahasanDokumen4 halamanSoal Dan PembahasanARIKABelum ada peringkat
- Muatan ParsialDokumen1 halamanMuatan ParsialAfif ZakariaBelum ada peringkat
- Pembuatan Bentuk - Bentuk MolekulDokumen5 halamanPembuatan Bentuk - Bentuk Molekulinsomnia jjangBelum ada peringkat
- Tugas KSMDokumen24 halamanTugas KSMUmmikalsum AminBelum ada peringkat
- H2ODokumen7 halamanH2OAIfa MIzumortBelum ada peringkat
- Bentuk Molekul Berdasarkan Teori Vsepr Dan HibridisasiDokumen11 halamanBentuk Molekul Berdasarkan Teori Vsepr Dan HibridisasiPutri Listiya SariBelum ada peringkat