BAB I Gas Ideal
BAB I Gas Ideal
Diunggah oleh
Aini MilawatiHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
BAB I Gas Ideal
BAB I Gas Ideal
Diunggah oleh
Aini MilawatiHak Cipta:
Format Tersedia
BAB I
GAS IDEAL DAN REAL GAS
1.1. Gas Ideal
1.1.1. Pendahuluan
Gas ideal dapat di peroleh dari teori kinetika gas dengan assumsi sebagai
berikut :
1. Gas terdiri dari partikel-partikel (atom-atom atau molekul-molekul) yang
jumlahnya sangat banyak
2. Volume sesungguhnya dari partikel-partikel gas dapat diabaikan
terhadap volume wadah sesungguhnya. Hal ini berarti partikel-partikel
gas dapat bergerak bebas.
3. Tidak ada interaksi (baik tarik-menarik atau tolak-menolak) antara
partikel-partikel, sehingga partikel-partikel bergerak dalam garis lurus
4. Terdapat tumbukan elastis antara partikel dengan partikel dan antara
partikel dengan dinding wadah. Hal ini berarti bahwa energi kinetik total
dan momentum garis ditetapkan sebelum dan sesudah tumbukan
5. Energi kinetik gas berbanding langsung dengan temperatur
Energi Internal dari real gas adalah fungsi dari tekanan berbanding dengan suhu.
tekanan meningkat diperoleh dari gaya antar molekul. jika gaya tidak ada, maka
tidak ada energi untuk mengubah jarak rata-rata intermolekul dan tidak ada energi
yang dibutuhkan untuk mengubah volume tekanan dalam gas pada suhu konstan.
Kita menarik kesimpulan bahwa tidak ada interaksi molekul, energi internal pada
gas tergantung pada suhu saja.
Jarak penyebaran partikel-partikel yang tak terhingga menyebabkan gaya
interaksi antar partikel mendekati nol. Pada kondisi ini gas dikatakan ideal.
Gas ideal adalah menyatakan hubungan antara tekanan temperature dan volume,
dengan persamaan :
pV = n.RT
atau p.
= R.T
Dimana :
^
p = Tekanan absolut gas
= Volum spesifik (Volume per mole atau massa)
V = Volume total gas
R = Tetapan gas
T = Temperatur absolut gas
n = mole gas
1.1.2. Hukum-Hukum Gas Ideal
Hukum-hukum
yang digunakan untuk menyatakan gas ideal adalah
sebagai berikut :
a. Hukum Boyle
Volume sejumlah massa gas pada temperatur konstan berbanding
terbalik dengan tekanan
V1 P2
V1.P1 V2 .P2
V2
P1
b. Hukum Charles
Volume sejumlah massa gas pada tekanan konstan berbanding lurus
dengan suhu mutlaknya
V1 T1
V2 T2
c. Hukum Gay Lussac
Tekanan sejumlah massa gas pada volume konstan berbanding lurus
dengan suhu mutlaknya
P1
T
1
P2 T2
d. Hukum Boyle-Gay Lussac
Gabungan dari persamaan Boyle dan Gay Lussac
P1V1
PV
2 2
T1
T2
e. Tetapan Gas
Jika digunakan 1 mole gas akan didapat harga tetapan gas dari
persamaan gas ideal (P,V,T dalam kondisi standar)
R
PV
T
Harga R tergantung dari system satuan yang dipakai
R = 8,314 m 3 .pa/molo K
0,08314 lt.bar/molo K
0,08206 lt.atm/molo K
R = 62,36 lt.mmhg/molo K
= 82,06 cm 3 .atm/molo K
= 0,7302 ft 3 .atm/lbmolo R
1.1.3. Aplikasi Hukum-Hukum Gas Ideal
Untuk menyelesaikan soal-soal dalam fase gas yang menyangkut V,P,T dapat
diselesaikan dengan persamaan :
PV
T
konstan
Untuk soal-soal yang menyangkut massa gas dapat diselesaikan dengan
persamaan gas ideal
pV = n.RT
Contoh Soal
1. Hitunglah volume (dalam liter) dari 100 gr Nitrogen pada 23oC dan tekanan 3
psig
Penyelesaian
Dik : massa Nitrogen = 100 gram
T = 23oC = 296oK
P = 3 psig
Dit : V ?
Jawab :
100 gr
Mole N2 = 28 gr/mol 3,57 mol
P absolut = Pgauge + P atmosfer
(1 P atm = 14,7 psi)
= 3 Psig + 14,7 psia
= 17,7 psia
tetapan gas R = 0,08206 liter.atm/mol.oK
= 0,08206 liter.(14,7 psia)/mol.oK
= 1,20628 liter.psia/mol.oK
maka :
V
(3,57 mol).(1,20628 liter.psia /mol o K).(296 K)
72,05 liter
17,7 psia
2. Sebuah silinder berisi 100 gr gas ideal (berat molekul = 40 gr/mol) pada 27 oC
dan tekanan 2 atm. Ketika dipindahkan silindernya jatuh dan menimbulkan
lekukan sehingga menurunkan volume silinder. Tetapi katup penahan silinder
tidak dapat menahan tekanan yang lebih besar dari 2 atm, sehingga 10 gram
gas bocor keluar.
a.
Hitung volume silinder sebelum dan sesudah terjadinya lekukan
b.
Bila katup sedikit bisa menahan tekanan berapa tekanan sesudah lekukan
temperatur tetap konstan
Penyelesaian :
dik :
Dit :
m gas = 100 gr
T = 27oC (300 K)
BM
P = 2 atm
= 40 gr/mol
a. V1(sebelum lekukan) dan V2 (sesudah lekukan)
b. P2 (bila tidak terjadi kebocoran pada saat terjadinya lekukan)
Jawab :
a. volume mula-mula dapat dihitung dari persamaan :
n.RT 100 gr (0,08206 dm 3 .atm/mol.K)(300 K)
3
30,79 dm
P1
40
gr/mol
2
atm
V1
massa sesudah lekukan (m2) = 100 10 = 90 gram
V2
n.RT
90 gr (0,08206 dm 3 .atm/mol.K)(300 K)
3
27,71 dm
P1
2 atm
40 gr/mol
b. bila tidak terjadi kebocoran, maka :
P2
P1V1
(2 atm)(30,79 dm 3 )
2,22 atm
V2
27,71 dm 3
3. Hituglah volume yang ditempati oleh 88 lb CO2 pada tekanan 32,2 ft H2O dan
suhu 15oC
Penyelesaian
kondisi 1
88 lb
ft3 pada
kondisi standar
Pada kondisi standar (kondisi 1)
kondisi 2
ft3 pada 32,2 ft H2O
dan 15oC
kondisi 2
P = 33,91 ft H2O
T = 273o K
Dengan menggunakan persamaan :
P1 T2 359,05 ft3 / lb mol
V2 V1
P2 T1 88 lb CO2
44 lb /lb mol CO2
^
p = 32,2 ft H2O
T = 273 + 15 = 288 oK
33,91 ft H 2O 288 K
3
798
ft
CO2
32,2
ft
H
O
273
K
Cara 2 :
Menggunakan persamaan gas ideal
Mencari harga R yang sesuai dengan konversi satuannya yang diukur
dalam keadaan standar
^
PV
T
dimana : V = 359,05 ft3/lb mol
P = 33,91 ft H2O
T = 273 K
(33,91)(359,05)
(ft )(H 2O)(ft 3 )
44,59
273
(lb mol)(K)
88 lb
n R.T 44 lb/lb mol 44,59(ft H 2O)(ft 3 )
o
3
o
V
288 K 798 ft CO 2 pada 15 C
o
P
32,2ft H 2O
(lb mol) ( K)
1.2. Campuran Gas Ideal
1.2.1. Tekanan dan Volume Parsial
Dalam campuran gas, molekul-molekul dari tiap komponen gas
terdistribusi
keseluruh volum ruangan dan tiap-tiap komponen gas tersebut
memberikan kontribusi pada tekanan total yang dihasilkan
a. Tekanan Parsial
Tekanan parsial adalah tekanan yang dihasilkan satu komponen gas, jika
hanya gas tersebut saja yang berada dalam ruangan dengan volume dan
suhu yang sama dengan campuran gas
Pi .Vtot n i .R.Ttot
Pi .Vtot
n .R.Ttot
i
Ptot .Vtot n tot .R.Ttot
Pi
n
n
i Pi Ptot i Pi yi .Ptot
Ptot n tot
n tot
dimana :
Pi = tekanan Parsial
yi = fraksi mol komponen I
b. Volume Parsial
Volume parsial adalah volume komponen murni satu komponen gas dalam
campuran apabila gas itu saja yang berada dalam ruangan dengan tekanan
dan suhu sama dengan campuran gas
Ptot .Vi n i .R.Ttot
Ptot .Vi
n .R.Ttot
i
Ptot .Vtot n tot .R.Ttot
Vi
n
n
i Vi Vtot i Vi y i .Vtot
Vtot n tot
n tot
Dimana :
Vi Volume parsial
yi fraksi mol komponen i
Hukum Dalton dan Amagat
Hukum Dalton
Tekanan total suatu campuran gas adalah jumlah dari tekanan-tekanan
parsial komponen-komponennya
Ptot = PA + PB + PC + .
Hukum Amagat
Volume total yang ditempati oleh campuran gas adalah jumlah dari volume
komponen-komponen murninya
Vtot = VA + VB + VC + ..
Contoh Soal
1. Suatu gas pada ruangan rapat dengan volume 1000 m3. dalam ruangan ini
mengandung udara ( 21% O2 dan 79% N2) pada 20oC dan tekanan total 1 atm
a.
Berapa volume parsial dari O2 dan N2
b.
Berapa tekanan parsial dari O2 dan N2
c.
Jika seluruh O2 dipindahkan dari ruangan dengan metode yang sama apa
yang akan terjadi pada tekanan total ruangan
Penyelesaian :
Dik : V gas = 1000 m3
T
= 20oC
p = 1atm
dalam ruangan terdapat 21% O2 dan 79% N2
Jawab :
Basis 1000 m3 dari udara pada 20oC dan 1 atm
a.
volume parsial dari O2 dan N2
Vi Vtot
Vi yi .Vtot
VO 2 Vtot
VN 2 Vtot
b.
n tot
nN2
n tot
VO 2 1000 m3
0,21
210 m 3 pada 20o C dan 1 atm
1
VN 2 1000 m3
0,79
790 m3 pada 20o C dan 1 atm
1
Tekanan Parsial dari O2 dan N2
Pi Ptot
ni
n tot
PO 2 Ptot
PN 2 Ptot
c.
nO2
ni
n tot
n O2
n tot
nN2
n tot
PO 2 1 atm
0,21
0,21 atm pada 1000 m3 dan 20o C
1
PN 2 1 atm
0,79
0,79 atm pada 1000 m 3 dan 20o C
1
Jika O2 seluruhnya dipindahkan dari ruangan maka akan mengalami
penurunan tekanan dalam ruangan menjadi 0,79 atm
1.2.2. Berat Molekul Dalam Campuran Gas
Berat molekul rata-rata dihitung dengan menggunakan mol campuran gas
sebagai dasar perhitungan
BM rata - rata
Berat
jumlah mol
contoh soal :
Hitunglah berat molekul rata-rata gas buang yang mempunyai komposisi (% w)
CO2
= 13,1 %
O2
= 7,7 %
N2
= 79,2 %
Penyelesaian :
Basis 100 mol gas campuran
CO2
= 13,1 mol
= 576 gr
O2
= 7,7 mol
= 246 gr
N2
= 79,2 mol
= 2218 gr
= 3040 gr
dalam 100 mol campuran gas terdapat 3040 gr
BM rata - rata
3040 gr
30,4 gr/mol
100 mol
1.2.3. Densitas Gas Campuran
Densitas gas campuran adalah massa tiap campuran tiap satuan volume
pada kondisi tekanan dan temperatur tertentu dengan menggunakan hukum gas
ideal
Contoh soal :
Hitunglah kerapatan dalam gr/lt campuran gas H2 dan O2 pada suhu 30oC
tekanan 740 mmHg, jika H2 = 11,1 % wt
Penyelesaian :
Dik : Tcamp = 30oC
Pcamp = 740 mmHg
massa H2 = 11,1 %wt
Dit : (kerapatan)
Jawab :
Basis 100 gr gas campuran
Massa H2 = 11,1 % x 100 gr = 11,1 gr
Mol H2
11,1 gr
= 2 gr/mol 5,55 mol
Massa O2 = (100 11,1)gr = 88,9 gr
88,9 gr
Mol O2 = 32 gr/mol 2,78 mol
Mol total = 5,55 + 2,78 = 8,33 mol
Volume (STP) = 22,4 lt/mol x 8,33 mol = 197,8 liter
V2 (Volume pada 740 mmHg dan 30oC) =
P1V1
PV
2 2
T1
T2
760 mmHg x 197,8 liter 740 mmHg x V2
273 K
303 K
V2 222,5 liter
100 gr
gr
kerapatan () = 222,5 lietr 0,39 liter
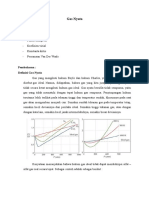
1.3. REAL GAS (GAS NYATA)
Pada suhu kamar dan tekanan 1 atm, pada umumnya gas mempunyai sifat
mendekati ideal, tetapi pada tekanan yang tinggi akan terjadi penyimpanganpenyimpangan sehingga persamaan gas ideal tidak dapat diterapkan secara
langsung tetapi memerlukan koreksi
Metode yang digunakan untuk menentukan gas real adalah :
a.
Menggunakan persamaan gas ideal (Equation of state)
b.
Dengan diagram kompresibilitas (Compressibility chart)
c.
Dengan estimasi sifat-sifat fisik
d.
Menggunakan data eksperimen
a) Equation of State
10
Pada temperatur tinggi dan tekanan rendah gas akan mendekati ideal.
Beberapa persamaan untuk menghitung gas real adalah
Persamaan Van Der Waals
a ^
P ^ Vb RT
V2
27 R2.T2 1RTc
a b
64 Pc 8 Pc
Redlich-Kwong
^
a
P V b RT
^ ^
T1/2.V (Vb)
R2.T2,5 RTc
a0,42748 b0, 86 4
Pc Pc
Benedict Webb-Rubin
11
P. V
B C D E
1 ^ 2 4 5
^
^
^
R.T
V V V V
2
Ao Co
B Bo 3 D c.. V
RT RT
2
a
a.
C b c .e V E
RT
RT
Soave-Redlich-Kwong
a' ^
P
V b RT
^ ^
V (V b)
R 2 .Tc
a 0,42748
Pc
1 k (1 Tr1 / 2
RTc
b 0,08664
Pc
k (0,480 1,574 0,176 2
b) Diagram Kompresibilitas
Untuk menghitung besaran-besaran yang menentukan keadaan suatu gas
(tekanan P, suhu T, dan Volume V) dapat dipakai diagram faktor
kompresibilitas
Faktor kompresibilitas adalah koefisien yang mengoreksi hukum gas ideal
agar dapat mendekati gas real sehingga persamaan akan terbentuk
P .V = Z.n.R.T
12
Dimana : Z = faktor kompresibilatas
Untuk menggunakan grafik perlu dihitung dahulu tekanan tereduksi (Pr) dan
suhu tereduksi (Tr) dengan persamaan berikut :
Tr =
T
Tc
Pr =
P
Pc
Dimana : Tc dan Pc adalah suhu kritis dan tekanan kritis
Dengan memplotkan tekanan reduksi (Pr) dengan temperatur reduksi (Tr) atau
volume reduksi (Vrc) akan didapat Z (factor kompresibilitas).
Selain menggunakan grafik faktor kompresibilitas dapat juga menggunakan
persamaan :
Virial Equation
Z 1
B.P
BPc Pr
1
..............1)
R.T
RTc Tr
BPc
Bo .B1................2)
RTc
Dengan menggabungkan persamaan 1 dan 2 didapat
Z 1 Bo
Pr
Pr
.B1
.3)
Tr
Tr
Hubungan Z dikembangkan oleh Pitzer dan Coworker didapat
Z = Zo + ZI.4)
Dengan menggabungkan persamaan 3 dan 4 didapat
Zo = 1 B
1
ZI = B
Pr
..5)
Tr
Pr
..6)
Tr
persamaan virial kedua adalah fungsi temperatur saja. B o dan BI adalah
fungsi suhu tereduksi saja
Bo = 0,083 -
0,422
Tr 1,6
BI = 0,139 -
0,172
Tr 4,2
1.3.1. Kondisi Kritis, Parameter Tereduksi dan Kompresibilitas
a. Kondisi Kritis
13
Tc = Batas temperatur dimana gas masih dapat dicairkan dengan
penekanan ) dibawah temperatur ini gas dapat dicairkan dengan
tekanan)
Pc = Tekanan yang dibutuhkan untuk mencairkan gas pada suhu Tc
Vc = Volume gas pada Tc dan Pc
b. Parameter Tereduksi
Tekanan Tereduksi (Pr)
Adalah perbandingan antara tekanan absolut dengan tekanan kritis
Pr =
P
Pc
Temperatur Tereduksi (Tr)
Adalah perbandingan suhu absolut dengan suhu kritis
Tr =
T
Tc
Contoh Soal :
1.
5 ft3 silender mengandung 50 lb propane berada disinar matahari yang
panas. Tekanan gauge menunjukan bahwa tekanannya adalah 665 psig.
Berapa suhu propane dalam silinder? Gunakan persamaan Van der Waals
665 psig
5 ft3
50 lb
C3H8
T?
Penyelesaian:
Basis : 50 lb propane
Dengan menggunakan persamaan Van Der Waals
14
a ^
P ^ V b RT
V2
atau
P n .a V n.b n.RT
V2
Nilai a dan b dapat dilihat pada tabel 3.4 (Himeblau)
a = 3,49 . 104 psia (ft3/lb mol)2
b = 1,45 ft3/lb mol
Pgauge = 665 psig
Pabsolut = Pg + Patm
= 665 + 14,7 = 679,7 psia
R = 10,73 psia .ft3/lb mol oR
Mol propane =
50 lb
1,136 mol
44 lb/lb mol
Maka :
2
4
679,7 (1,136) .3,49 .10 5 (1,136).(1,45) (1,136).(10,73).T
52
T 683o R atau 223o F
2.
Hitunglah volume molar dari n- butana pada 510oK dan 25 bar dengan
menggunakan :
a. persamaan gas ideal
b. Hubungan faktor kompresibilitas
c. Persamaan koefisien Virial
Penyelesaian :
a) Persamaan Gas Ideal
p.
= R.T
15
(83,14 cm 3 .bar/mol o K)(510o K)
1696,1 cm 3 / mol
25 bar
b) Dengan faktor kompresibilitas
dari appendix .B (JM Smith) di dapat Tc dan Pc
Tc = 425,1
Tr =
Pc = 37,96
510
1,2
425
25
Pr = 37,96 0,659
Dari harga Tr dan Pr didapat ZI dan Zo dengan menggunakan Tabel E1
dan E2 (JM.Smith)
ZI = 0,865 dan Zo = 0,038 sedangkan nilai = 0,2 (acentric Factor) dari
tabel B.1
Z = Zo + ZI
Z = 0,865 + 0,2. 0,038 = 0,873
PV = Z..R.T
(0,873)(83,14cm3 .bar/molo K )(510o K )
1480,7 cm3 /mol
25 bar
c) dengan Virial Koefisien
Z 1
B.P
BPc Pr
1
..............1)
R.T
RTc Tr
BPc
Bo .B1................2)
RTc
Bo = 0,083 -
0,422
Tr1,6
BI = 0,139 -
0,172
Tr 4,2
Maka :
Bo = 0,083 -
0,422
0,232
(1,2)1,6
BPc
-0,232 (0,2).(0,059 ) 0,22
RTc
BI = 0,139 -
0,172
0,059
(1,2) 4,2
16
Z 1 - 0,22
V=
0,659
0,879
1,2
(0,879)(83,14 cm 3 .bar/molo K )(510o K
1489,1 cm 3 /mol
25 bar
Harga V pada virial Koefisien lebih tinggi dari faktor kompresibilitas dan
data eksperiment di dapat V = 1480,7 cm3/mol
3.
Untuk menyimpan 1 lb-mol gas metana (CH4) pada tekanan 600 atm dan
suhu 122oF dibutuhkan bejana yang memenuhi syarat. Berapakan volume
baja tersebut bila di perhitungkan dengan metode :
a. Hukum gas Ideal
b. Persamaan Van Der Waals
c. Grafik Faktor Kompresibilitas
Penyelesaian :
a) Hukum Gas Ideal
PV = n.RT
P = 600 atm
T = 122oF = (122 + 460) = 582 oR
Mol metan = 1 lb mol
R = 0,73 atm ft3/lb mol oR
V=
(1 lb mol)(0,73 ft 3 .atm/molo R )(582o R
0,709 ft 3
600 atm
b) persamaan Van Der Waals
P n .a V n.b n.RT
V2
untuk mengitung V, maka harus di ubah ke bentuk persamaan pangkat 3
dalam V sebagai berikut :
n.b
n.RT 2 n 2 .a
n.a.b
V
V3 0
V
P
P
P
untuk harga a dan b dapat dilihat pada tabel 3.4 (Himeblau)
a = 2,25 .106 atm (cm3/mol)
3,353 . 10-5 ft 3
0,002205 lb mol
a = 2,25 . 106 atm (
b = 42,8 cm3/mol
ft 2
lb mol
577,3 atm
17
3,353 . 10 -5
ft 3
ft 3
0
,
651
b = 42,8
3
lb mol
2,205.10 lb mol
dengan harga R = 0,7302 ft3.atm/lb mol oR
persamaan menjadi :
1.0,7302(528) 2 12.577,3
1.(577,3).(0,651)
V
V3 0
V
600
600
600
V 3 1,359 V 2 0,962 V 0,626 0
1.0,651
dengan menggunakan trial and error didapat V = 1,0182 ft3
c) Dengan grafik Faktor Kompresibilitas
dari tabel (Himeblau) didapat harga :
Tc = 190,7 oK = 342.35oR
dan Pc =45,8 atm
582
1,7
342.35
Pr = 45,8 13,1
Tr =
600
Dari grafik didapat harga Z = 1,35
V=
(1,35)(1 lb mol)(0,73 ft 3 .atm/molo R )(582o R
0,95 ft 3
600 atm
Data eksperiment didapat V = 0,936 ft3/lb mol , kesalahan terkecil adalah
faktor kompresibilitas
SOAL SOAL LATIHAN
1.
Hitunglah tekanan pada 10 kg-mol ethane dalam tangki dengan volume
4,86 m3 pada suhu 300oK dengan menggunakan dua persamaan berikut ini :
a. Gas ideal
b. Soave-Redlich-Kwong
Bandingkan dengan jawabanmu, nilai yang benar adalah 34 atm
2.
Anda diminta untuk merancang tangki baja untuk mengisi CO2 pada suhu
290oK. Volume tangki adalah 10,4 m3, anda ingin menyimpan 460 kg CO2.
berapa tekanan yang akan ditimbulkan
CO2 ? Gunakan grafik factor
kompressibilitas.
3.
Sebuah tangki dengan volume 100 ft3 mengandung 95,1 lb-mole gas non
ideal dengan tekanan 1250 atm dan suhu 440oF. tekanan kritis yang
18
diketahui adalah 50 atm. Hitunglah temperatur kritis ? Gunakan grafik factor
kompressibilitas
4.
100 gram/min udara (21 % mol O2, sisanya N2) dicampur dengan aliran
CO2. aliran produk dianalisa dan ditemukan kandungan 56,7 wt % N2.
Hitunglah aliran volumetric dari umpan CO2 (liter (STP)/min) dan fraksi
mol dari aliran komponen produk ?
5.
Gunakan hokum gas ideal untuk menghitung spesifik volume dalam m 3/mol
dan densitas dalam kg/m3 dari hydrogen pada suhu 50oC dan tekanan
200 mmHg
6.
Suatu campuran gas ideal yang mengandung 40 % N2, 30 % CO, dan
30 % H2 dalam volume pada P = 2 atm (absolut) dan T = 65oC hitunglah :
7.
a.
Tekanan parsial dari tiap komponen
b.
Fraksi massa dari Nitrogen
c.
Densitas gas (gr/liter)
Gas proses mengalir dengan kecepatan 20.000 ft3/h pada tekanan 1 atm dan
suhu 200oF mengandung H2S dengan tekanan parsial 0,0294 psi. Gas
melewati scrubber dengan 92 % H2S dipindahkan. Hitunglah laju
pemindahan H2S dalam lbm/h
8.
50 pound CO2 yang berada pada 5 ft3 tangki. Batas aman dari tangki adalah
1600 psig. Gunakan factor kompressibilitas untuk menghitung temperatur
maksimum dari gas yang di izinkan ?
9.
Persamaan Van der Waals dengan konstanta a = 2,31 x 106
(atm)
(cm3/gr-mol)2 dan b = 44,9 cm3/gr-mol. Hitunglah volume per
gram-
mole jika gas mempunyai tekanan 90 atm dan suhu 373oK
10.
Hitunglah temperatur dari 2 mol gas dengan menggunakan persamaan van
der Waals dengan a = 1,35 x 10-6 m6(atm)(gr-mol-2), b = 0,0322 x 10-3 (m3)
(gr-mole-1) jika tekanan 100 kPa dan volume 0,0515 m3
19
Anda mungkin juga menyukai
- HK Pertama TermodinamikaDokumen30 halamanHK Pertama TermodinamikaNaufal Falih100% (1)
- Modul 3 Excel TerapanDokumen7 halamanModul 3 Excel Terapannabilla baliniBelum ada peringkat
- Keadaan Gas, Kelarutan, PengembunanDokumen37 halamanKeadaan Gas, Kelarutan, PengembunanKhazinatulBaitiaNazurah67% (3)
- Tugas KIMFIS 1Dokumen6 halamanTugas KIMFIS 1Aimatul Cholifah Sa'adaBelum ada peringkat
- Macam - Macam Panas Reaksi - Aulia Utami Herawati - 3335170023Dokumen5 halamanMacam - Macam Panas Reaksi - Aulia Utami Herawati - 3335170023aulia utamiBelum ada peringkat
- Kul1 Kesetimbangan & KespontananDokumen69 halamanKul1 Kesetimbangan & KespontananMuna Alfi ABelum ada peringkat
- Energi Bebas GibsDokumen9 halamanEnergi Bebas GibsOctovianus PasandaBelum ada peringkat
- Kegiatan 4 Kinetika KimiaDokumen25 halamanKegiatan 4 Kinetika KimiaHumayra Faja Syam100% (2)
- Pertemuan Ke 1 KFDokumen32 halamanPertemuan Ke 1 KFNasywa NailahBelum ada peringkat
- Laporan Tetap Praktikum Kimia Fisika Panas Pelarutan (HS) : Disusun OlehDokumen12 halamanLaporan Tetap Praktikum Kimia Fisika Panas Pelarutan (HS) : Disusun OlehAdhe Julian PertanandaBelum ada peringkat
- Pemrograman Pascal Dan Apliksi MatlabDokumen27 halamanPemrograman Pascal Dan Apliksi MatlabFairus RBelum ada peringkat
- Persamaan Keadaan Gas IdealDokumen13 halamanPersamaan Keadaan Gas IdealFebbi RahmadaniBelum ada peringkat
- Aplikasi DestilasiDokumen4 halamanAplikasi DestilasiNugraha Bayu Samodra100% (2)
- BAB I - Hasil Kali Kelarutan (KSP)Dokumen3 halamanBAB I - Hasil Kali Kelarutan (KSP)MFurqanulIkramBelum ada peringkat
- Lapres 03Dokumen11 halamanLapres 03Nur Rokhma SBelum ada peringkat
- Roy 2 KimfisDokumen2 halamanRoy 2 KimfisrizkiBelum ada peringkat
- Kimia Fisik Bab 2Dokumen12 halamanKimia Fisik Bab 2Bibiana Rume maranBelum ada peringkat
- Hukum I TermodinamikaDokumen53 halamanHukum I TermodinamikaSely Oktaviolita AsriBelum ada peringkat
- Diagram Terner BDokumen18 halamanDiagram Terner BErsa Nurul YarizsaBelum ada peringkat
- Aturan FasaDokumen5 halamanAturan FasaEva TrisnaBelum ada peringkat
- Makalah Energi Bebas GibbsDokumen3 halamanMakalah Energi Bebas GibbsAlmer Sudhiarta100% (1)
- Laporan Praktikum Volume Molal ParsialDokumen18 halamanLaporan Praktikum Volume Molal ParsialWhyna Hafid92% (13)
- Gas NyataDokumen10 halamanGas NyataYusuf EfendiBelum ada peringkat
- Persamaan Clausius-ClapeyronDokumen11 halamanPersamaan Clausius-ClapeyronLulu Ciprutz Ajjah100% (1)
- 13 - Kimia Fisika - KinetikaKimia - 13-Nop - 2013Dokumen41 halaman13 - Kimia Fisika - KinetikaKimia - 13-Nop - 2013Anonymous O1xkZIN100% (2)
- Volume Molal ParsialDokumen5 halamanVolume Molal ParsialJeremi StevenBelum ada peringkat
- Latihan Soal GravimetriDokumen2 halamanLatihan Soal GravimetriHayatul NikmahBelum ada peringkat
- Tuper 6 Rifqi Tubagus HilmiDokumen3 halamanTuper 6 Rifqi Tubagus HilmiRifqi Tubagus HilmiBelum ada peringkat
- Isomer IDokumen80 halamanIsomer IFha-fha Ie-fhiel FhaniZztsBelum ada peringkat
- 1 Kinetika KimiaDokumen13 halaman1 Kinetika KimiaWinda AlzamoriBelum ada peringkat
- LAPORAn Gas IdealDokumen17 halamanLAPORAn Gas IdealOkta Folorense Tobing100% (1)
- PANAS KELARUTAN DAN KSP-dikonversiDokumen30 halamanPANAS KELARUTAN DAN KSP-dikonversiaprilia kurnia putriBelum ada peringkat
- Aplikasi Percobaan 8 Dalam Kehidupan Sehari-Hari-1Dokumen6 halamanAplikasi Percobaan 8 Dalam Kehidupan Sehari-Hari-1Mona Maulina AriefBelum ada peringkat
- Fraksi MolDokumen12 halamanFraksi MolHardy Young HostelBelum ada peringkat
- Laporan Crude Oil Kelompok 3Dokumen30 halamanLaporan Crude Oil Kelompok 3Rizky MaulidiyaniBelum ada peringkat
- Soal Dan Pembahasan Fisika Gas Non IdealDokumen4 halamanSoal Dan Pembahasan Fisika Gas Non IdealMuhammad Reza Inazuma100% (3)
- Tugas MK KIMIA FISIKADokumen4 halamanTugas MK KIMIA FISIKABUDISATRIABelum ada peringkat
- Makalah Gas NyataDokumen12 halamanMakalah Gas NyataNita Sari100% (1)
- Penentuan Berat Molekul Berdasarkan Massa Jenis GasDokumen21 halamanPenentuan Berat Molekul Berdasarkan Massa Jenis GasskeptismeBelum ada peringkat
- LAPORAN PRAKTIKUM TermokimiaDokumen16 halamanLAPORAN PRAKTIKUM TermokimiaIlhamBelum ada peringkat
- Tugas 1 - Kelompok 13 - Kimia FisikaDokumen13 halamanTugas 1 - Kelompok 13 - Kimia FisikaNaurah Arika AzmiBelum ada peringkat
- Makalah Kelompok 12 - Energi Bebas Gibss Dan HelmholtzDokumen19 halamanMakalah Kelompok 12 - Energi Bebas Gibss Dan HelmholtzNurul KhairunnisaBelum ada peringkat
- TermodinamikaDokumen43 halamanTermodinamikaIfanFitrilFadilahBelum ada peringkat
- 1.2. Entropi Part 2Dokumen23 halaman1.2. Entropi Part 2SelviBelum ada peringkat
- Energi GibbsDokumen5 halamanEnergi Gibbsriska fitrianiBelum ada peringkat
- Kesetimbangan Fasa SoalDokumen2 halamanKesetimbangan Fasa SoalDony Angga Saputra100% (1)
- Maharani Fauzia Annur 1813441005 (Kuis Review Kurikulum Kimia)Dokumen20 halamanMaharani Fauzia Annur 1813441005 (Kuis Review Kurikulum Kimia)maharani fauzia annurBelum ada peringkat
- Kimia Fisika Keadaan CairanDokumen12 halamanKimia Fisika Keadaan CairanLcy JyjwdyBelum ada peringkat
- 1 MTK Konsep Neraca MasaDokumen23 halaman1 MTK Konsep Neraca MasaPermana PakpahanBelum ada peringkat
- Volume Molar PasrsialDokumen13 halamanVolume Molar Pasrsialnurika shintaBelum ada peringkat
- Rafly Nomor 13Dokumen1 halamanRafly Nomor 13rafly auliaBelum ada peringkat
- Makalah Kompleks Bu Beta1Dokumen50 halamanMakalah Kompleks Bu Beta1Manusia biasaBelum ada peringkat
- Translate Chapter 1-2Dokumen65 halamanTranslate Chapter 1-2KiptiyahBelum ada peringkat
- S 9 Mwue 1592863521Dokumen16 halamanS 9 Mwue 1592863521Lemon TeaBelum ada peringkat
- Gas Ideal Dan Non Ideal (Hanif)Dokumen27 halamanGas Ideal Dan Non Ideal (Hanif)Miraiko RoykoBelum ada peringkat
- Volume Molar GasDokumen12 halamanVolume Molar GasWempic Aulia FauziBelum ada peringkat
- Kimia Fisik 1Dokumen18 halamanKimia Fisik 1Joe NedBelum ada peringkat
- 1gas Dan Tekanan ParsialDokumen21 halaman1gas Dan Tekanan ParsialTeti SelfianaBelum ada peringkat
- PTK Kelompok 3Dokumen12 halamanPTK Kelompok 3Fadilah PiliangBelum ada peringkat
- Cetak Kartu Hasil Studi - Portal AkademikDokumen1 halamanCetak Kartu Hasil Studi - Portal AkademikYustinus Selis ToronBelum ada peringkat
- Klasifikasi MikrobiologiDokumen99 halamanKlasifikasi MikrobiologiYustinus Selis Toron100% (1)
- Democratic CitizenshipDokumen23 halamanDemocratic CitizenshipSiti AliyasihBelum ada peringkat
- Irisan KerucutDokumen43 halamanIrisan KerucutYustinus Selis ToronBelum ada peringkat
- P ZoybhDokumen4 halamanP ZoybhYustinus Selis ToronBelum ada peringkat