Modul 3 - Isolasi Dan Uji Biokimia - Novita - Rev2 Acc
Diunggah oleh
Novita Eka RahmawatiHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Modul 3 - Isolasi Dan Uji Biokimia - Novita - Rev2 Acc
Diunggah oleh
Novita Eka RahmawatiHak Cipta:
Format Tersedia
1
Laporan Resmi Praktikum Mikrobiologi Teknik
LAPORAN RESMI
ISOLASI MIKROORGANISME DARI SUATU CAMPURAN,
UJI BIOKIMIA, DAN UJI HIDROLISA
I. Tujuan
I.1 Isolasi Mikroorganisme dari Suatu Campuran
Tujuan dari percobaan isolasi mikroorganisme mempelajari isolasi
mikroorganisme dari suatu campuran dengan teknik cawan gores dan cawan tuang.
I.2 Uji Biokimia (Uji Oksidasi-Fermentasi)
Tujuan dari percobaan ini adalah mempelajari kemampuan mikroorganisme
dalam mengkatabolisme apakah berlangsung secara oksidatif atau fermentatif.
II. Data Pengamatan
II.1 Isolasi Mikroorganisme
II.1.1 Metode Cawan Gores
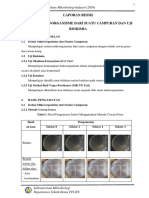
Tabel II.1 Hasil Pengamatan Isolasi Mikroorganisme dari Suatu Campuran
dengan Metode Cawan Gores Media NBA Setelah 24 Jam (Petri dish 1)
Bentuk koloni Hasil Pengamatan
dilihat dari: Sektor 0 Sektor I Sektor II Sektor III
Atas
Keseluruhan
Atas tepi
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
2
Laporan Resmi Praktikum Mikrobiologi Teknik
Permukaan
(samping)
Keterangan:
- Warna: Tidak ada
- Diameter: koloni dari
- Kepekatan: sel tunggal
- Configuration: yang tumbuh
- Margin: di sektor III
- Elevation:
Tabel II.2 Hasil Pengamatan Isolasi Mikroorganisme dari Suatu Campuran
dengan Metode Cawan Gores pada Media NBA Setelah 47 jam (Petri dish 1)
Bentuk koloni Hasil Pengamatan
dilihat dari: Sektor 0 Sektor I Sektor II Sektor III
Atas
Keseluruhan
Atas tepi
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
3
Laporan Resmi Praktikum Mikrobiologi Teknik
Permukaan
(samping)
Keterangan:
- Warna: Putih
- Diameter: 0.4 cm
- Kepekatan: Jarang
- Configuration: Round
- Margin: Regular
- Elevation: Raised
Tabel II.3 Hasil Pengamatan Isolasi Mikroorganisme dari Suatu Campuran
dengan Metode Cawan Gores pada Media NBA Setelah 24 Jam (Petri dish 2)
Bentuk koloni Hasil Pengamatan
dilihat dari: Sektor 0 Sektor I Sektor II Sektor III
Atas
Keseluruhan
Atas tepi
Permukaan
(samping)
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
4
Laporan Resmi Praktikum Mikrobiologi Teknik
Keterangan:
- Warna: Putih
- Diameter: 0.4 cm
- Kepekatan: Jarang
- Configuration: Round
- Margin: Regular
- Elevation: Raised
Tabel II.4 Hasil Pengamatan Isolasi Mikroorganisme dari Suatu Campuran
dengan Metode Cawan Gores pada Media NBA Setelah 47 jam (Petri dish 2)
Bentuk koloni Hasil Pengamatan
dilihat dari: Sektor 0 Sektor I Sektor II Sektor III
Atas
Keseluruhan
Atas tepi
Permukaan
(samping)
Keterangan:
- Warna: Putih
- Diameter: 1.2 cm
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
5
Laporan Resmi Praktikum Mikrobiologi Teknik
- Kepekatan: Jarang
- Configuration: Round
- Margin: Regular
- Elevation: Raised
II.1.2 Metode Cawan Tuang
Tabel II.5 Hasil Pengamatan Isolasi Mikroorganisme dari Suatu Campuran
dengan Metode Cawan Tuang pada Media NBA Setelah 24 Jam
Bentuk koloni Hasil Pengamatan
dilihat dari: Petri dish I Petri dish II Petri dish III
Atas
Keseluruhan
Atas tepi
Permukaan
(samping)
Keterangan:
- Warna: Putih
- Diameter: 0.3 cm
- Kepekatan: Jarang
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
6
Laporan Resmi Praktikum Mikrobiologi Teknik
- Configuration: Round
- Margin: Regular
- Elevation: Raised
Tabel II.6 Hasil Pengamatan Isolasi Mikroorganisme dari Suatu Campuran
dengan Metode Cawan Tuang pada Media NBA Setelah 47 jam
Bentuk koloni Hasil Pengamatan
dilihat dari: Petri dish I Petri dish II Petri dish III
Atas
Keseluruhan
Atas tepi
Permukaan
(samping)
Keterangan:
- Warna: Putih
- Diameter: 0.4 cm
- Kepekatan: Jarang
- Configuration: Round
- Margin: Regular
- Elevation: Raised
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
7
Laporan Resmi Praktikum Mikrobiologi Teknik
II.2 Uji Biokimia
II.2.1 Uji Oksidasi-Fermentasi
Tabel II.7 Hasil Pengamatan Uji Fermentasi-Oksidasi Mikroorganisme dengan
media Hugh and Leifson setelah 24 Jam
Nama Bakteri Terbuka Ditutup Parafin
Blanko
Nitrobacter
Lactobacillus
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
8
Laporan Resmi Praktikum Mikrobiologi Teknik
Tabel II.8 Hasil Pengamatan Uji Fermentasi-Oksidasi Mikroorganisme dengan
media Hugh and Leifson setelah 47 jam
Nama Bakteri Terbuka Ditutup Parafin
Blanko
Nitrobacter
Lactobacillus
III. Pembahasan
III.1 Isolasi Mikroorganisme
III.1.1 Metode Cawan Gores
Tujuan dari percobaan isolasi mikroorganisme dari suatu campuran dengan
metode cawan gores adalah untuk mempelajari cara cara mengisolasi
mikroorganisme dari suatu campuran dengan menggunakan teknik cawan gores.
Pada prinsipnya metode cawan gores adalah pengenceran biakan mikroorganisme
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
9
Laporan Resmi Praktikum Mikrobiologi Teknik
sehingga akan individu sel tunggal akan terpisah dari yang lainnya. Keunggulan
dari metode ini adalah kita bisa menghemat bahan dan waktu karena prosesnya
tidak lama dan tidak membutuhkan bahan yang banyak.
(Benson, 2001, hal. 82-86)
Langkah pertama yang dilakukan pada percobaan isolasi mikroorganisme
adalah mempersiapkan alat dan media untuk disterilisasi. Dua petri dish yang akan
digunakan pada bagian permukaan bawahnya dibagi menjadi empat sektor, yaitu
sektor 0, I, II, dan III seperti yang ditunjukkan pada gambar di bawah ini.
0
III II
Gambar III.1 Pembagian Sektor pada Petri dish
Kedua petri dish diisi dengan media nutrient broth agar (NBA) diusahakan
memenuhi seluruh luasan petri dish. Pengisian tidak terlalu penuh untuk memberi
kesempatan pada pertumbuhan bakteri, terutama yang memiliki elevasi
hemispherical atau umbonate. NBA merupakan media yang berasal dari ekstrak
daging. Media NBA terdiri dari 2 jenis, yaitu cair (nutrient broth) atau padat dengan
penambahan agar (nutrient agar). NBA cocok digunakan untuk kultur bakteri
karena kandungannya kaya protein yang sangat dibutuhkan bakteri dalam
pertumbuhannya.
Komposisi nutrient agar adalah sebagai berikut:
Peptone 5.0 g
Beef extract 3.0 g
Agar 15.0 g
Distilled water 1,000.0 ml
Komposisi nutrient broth adalah sebagai berikut:
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
10
Laporan Resmi Praktikum Mikrobiologi Teknik
Peptone 5.0 g
Beef extract 3.0 g
Distilled water 1,000.0 ml
(Prescott, 2002, hal. 446)
Kemudian petri dish dibungkus dengan kertas cokelat untuk mencegah air
dari autoclave yang masuk ke dalam petri dish dan mencegah kontaminasi. Bagian
kertas yang berada di luar adalah bagian yang licin. Bagian licin pada kertas cokelat
mengandung lilin, sehingga menghalangi uap air yang masuk ke dalam petri dish.
Selanjutnya petri dish yang telah berisi media dimasukkan ke dalam autoclave.
Sterilisasi dilakukan pada suhu 121oC selama kira-kira 20 menit.
Sterilisasi adalah penghilangan segala jenis kehidupan mikroorganime,
termasuk endosporanya, kecuali prion yang memiliki resistasi tinggi. Segala
sesuatu yang digunakan untuk sterilisasi disebut sterilant. Sterilisasi dengan
autoclave sangat efektif, ketika organisme dikontakkan langsung dengan uap panas
atau dengan sedikit liquid dengan suhu panas. Pada kondisi ini, uap dengan tekanan
sedikit di atas atmosfer (15 psig, 121oC) akan mematikan semua organisme beserta
endosporanya, selain prion.
(Tortora, 2010, hal 188)
Prion merupakan kependekan dari proteiaceous infectious particles. Prion
lebih kecil daripada virus dan mengandung DNA atau RNA. Prion dapat
menyebabkan penyakit neurodegenerative yang disebut spongiform
encephalopathies atau mad cow disease. Prion sangat resisten terhadap
penghilangan mikroorganisme dan tidak dapat dimatikan dengan dimasak pada
suhu tinggi. Tidak ada pengobatan bagi penyakit yang diakibatkan oleh prion dan
biasanya penyakit tersebut bersifat fatal dan dapat menyebabkan kematian.
(Morello, 2003, hal. 242)
Setelah petri dish berisi media disterilisasi, selanjutnya adalah
mendinginkan media hingga memadat dan membentuk agar. Lalu dilakukan
inokulasi dari suspensi berisi campuran B. Seluruh proses inokulasi dilakukan di
dalam incase sehingga dapat meminimalisir kontaminasi dan faktor lain dari
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
11
Laporan Resmi Praktikum Mikrobiologi Teknik
lingkungan karena dilakukan di ruangan tertutup dan terisolasi. Untuk
memindahkan mikroorganisme dari biakan ke media baru, digunakan kawat ose.
Sebelum digunakan, kawat ose dipanaskan terlebih dahulu di atas api hingga
membara pada bagian ujung hingga tengahnya. Tujuan dari pemanasan ini adalah
untuk sterilisasi kawat ose, dimana seluruh mikroorganisme akan mati apabila
terkena suhu tinggi. Kemudian kawat ose didiamkan beberapa saat supaya dingin,
karena suhu tinggi dapat membunuh bakteri pada biakan dan merusak media agar.
Petri dish dipanaskan sebentar pada bagian pinggirnya dengan api. Kawat ose
celupkan ke suspensi berisi campuran mikroorganisme. Setelah itu menggoreskan
kawat ose ke media pada petri dish. Kawat ose digoreskan dengan membentuk zig
zag pada kuadran 0. Hal ini bertujuan untuk memperbesar daerah inokulasi.
Setelah inokulasi di kuadran 0, kawat ose disterilkan kembali dengan
memanaskan menggunakan api kemudian ditunggu hingga dingin. Kemudian
menginokulasi kuadran I. Kawat ose digoreskan di kuadran 0 kemudian ditarik ke
kuadran I, sehingga ada mikroorganisme yang terambil dari kuadran 0 ke kuadran
I. Setelah itu menggores kuadran II dan kuadran III. Kawat ose harus selalu
disterilkan ketika berpindah kuadran untuk memastikan tidak ada mikroorganisme
yang terbawa kawat ose dari kuadran-kuadran sebelumnya yang dapat
memperbanyak jumlah koloni. Padahal yang diharapkan adalah jumlah koloni di
setiap kuadran lebih sedikit dari kuadran sebelumnya, sehingga pada kuadran
terakhir hanya terdapat beberapa koloni dari sel tunggal yang benar-benar terpisah
supaya dapat dibedakan mikroorganisme yang ada di dalam suatu campuran.
Gambar III.2 Penggoresan untuk Isolasi Bakteri
(Benson, 2003, hal 85)
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
12
Laporan Resmi Praktikum Mikrobiologi Teknik
Setelah digores, mulut petri dish dipanaskan sebentar dengan api. Pemanasan
petri dish hanya sebentar karena apabila terlalu lama dapat membunuh biakan yang
diinokulasi dan dapat menyebabkan agar leleh kembali. Setelah inokulasi selesai,
kawat ose dipanaskan kembali hingga membara lalu didinginkan. Setelah itu petri
dish dibungkus dengan kertas cokelat. Setelah inokulasi selesai, media baru yang
telah berisi inokulum dimasukkan ke dalam inkubator untuk diinkubasi. Inkubasi
berarti menyimpan kultur pada ruangan dengan temperatur yang dikontrol untuk
mendorong terjadinya pembelahan sel.
(Cowan, 2016, hal. 37)
Penyimpanan petri dish di inkubator dilakukan dengan terbalik untuk
mencegah uap air yang jatuh hingga menyentuh media. Uap air yang ada pada
media dapat menyebabkan pergerakan koloni mikroorganisme di dalam media dan
dapat merusak bakteri. Uap air berasal dari proses metabolisme mikroorganisme,
dimana terjadi pemecahan molekul besar menjadi molekul yang lebih kecil. Reaksi
metabolisme menghasilkan air dan ATP. Reaksi metabolisme adalah :
C6H12O6 + O2 CO2 + H2O + Energi
(Cowan, 2016, hal 179-180)
Proses inkubasi dilakukan selama 21 jam pada suhu 30 oC karena
merupakan suhu optimum dalam pertumbuhan mikroorganisme. Mikroorganisme
yang digunakan dalam percobaan merupakan contoh mikroorganisme mesophile,
dimana suhu optimum untuk tumbuh adalah di bawah 50oC.
(Tortora, 2010, hal. 158)
Gambar III.3 Rentang Temperatur untuk Pertumbuhan Mikroorganisme
(Waites, 2001, hal 33)
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
13
Laporan Resmi Praktikum Mikrobiologi Teknik
Selanjutnya dilakukan pengamatan terhadap pertumbuhan koloni bakteri
pada media. Pengamatan dilakukan pada 24 jam dan 47 jam. Pada pengamatan 24
jam, terlihat bahwa sudah ada koloni berwarna putih terutama di kuadran 0.
Pertumbuhan koloni semakin sedikit pada kuadran I dan II, dan belum ada
pertumbuhan koloni di kuadran III. Pada pengamatan 47 jam, kuadran 0 telah
dipenuhi koloni bakteri. Pada kuadran I dan II jumlah koloni lebih sedikit dibanding
kuadran 0. Sementara pada kuadran III hanya terdapat 1 koloni bakteri. Secara
umum, diameter pada pengamatan 47 jam lebih besar daripada pengamatan 24 jam.
Gambar III.4 Hasil Pengamatan Setelah 24 Jam pada Petri Dish 1 (Kiri) dan
Petri Dish 2 (Kanan)
Gambar III.5 Hasil Pengamatan Setelah 47 Jam pada Petri Dish 1 (Kiri) dan
Petri Dish 2 (Kanan)
Berdasarkan pengamatan yang telah dilakukan, dapat diketahui bahwa
bakteri murni tumbuh di kuadran III, yang menunjukan bahwa pada kuadran ini
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
14
Laporan Resmi Praktikum Mikrobiologi Teknik
bakteri telah terisolasi dari campuran mikroorganisme. Pada kuadran III hanya
terlihat 1 koloni bakteri, sehingga dapat teridentifikasi satu bakteri.
Berdasarkan literatur, morfologi dan ciri ciri dari bakteri Bacillus subtilis
dapat diidentifikasi melalui bentuk koloninya yang berbentuk kasar, tidak
transparan, menyebar, dan berwarna putih kusam.
(Breed, 1957, hal 620)
Bakteri Zymomonas mobilis memiliki ciri ciri yaitu, sel diplobasil,
berwarna putih, kondisi anaerob diperlukan untuk memfermentasi gula.
Zymomonas mobilis tidak tumbuh dengan baik pada media NBA. Zymomonas
mobilis membutuhkan kandungan gula untuk fermentasi, sementara NBA
menyediakan nutrisi protein (pepton).
(Breed, 1957, hal 199)
Kemungkinan lainnya, yaitu Escherichia coli mempunyai koloni pada
media agar yang berwarna putih hingga putih kekuningan, undulate, moist, dan
homogen.
(Breed, 1957, hal. 336)
Berdasarkan morfologinya, bakteri yang terisolasi pada cawan gores di
sektor III, baik pada petri dish 1 dan petri dish 2 lebih mengarah ke bakteri Bacillus
subtilis karena terdapat kesesuaian antara pengamatan dan literatur, yaitu koloni
berwarna putih kusam, kasar, dan tidak transparan.
Gambar III.6 (a) Bacillus subtilis pada Sheep Blood Agar Setelah Inkubasi 24
Jam (b) Setelah Inkubasi 47 Jam
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
15
Laporan Resmi Praktikum Mikrobiologi Teknik
Berikut adalah taksonomi dari Bacillus subtilis:
Domain : Bacteria
Kingdom : Monera
Phylum : Firmicutes
Class : Bacilli
Order : Bacillales
Family : Bacillaceae
Genus : Bacillus
Species : B. subtilis
(Leboffe, 2011, hal 25)
Untuk mengetahui mikroorganisme yang terdapat dalam campuran B, dapat
dilihat dari morfologi selain di sektor 3, yaitu pada sektor 1 dan 2. Pada sektor 1
dan 2 terdapat koloni bakteri berwarna putih kusam dengan bentuk irregular,
margin wavy, dan elevasinya raised. Berdasarkan literatur, koloni tersebut adalah
Bacillus subtilis. Apabila terdapat bakteri Escherichia coli pada campuran B,
seharusnya terdapat koloni lain yang berasal dari Escherichia coli pada petri dish.
Hal ini karena keadaan untuk hidup Escherichia coli mirip dengan Bacillus subtilis.
Kemungkinan campuran B berisi Zymomonas mobilis. Berdasarkan literatur
Zymomonas mobilis tidak tumbuh dengan baik pada media NBA. Selain itu,
Zymomonas mobilis termasuk bakteri anaerob dengan toleransi tertentu terhadap
oksigen. Dalam percobaan kondisinya adalah aerob, sehingga sangat kecil
kemungkinan Zymomonas mobilis untuk hidup. Sehingga Zymomonas mobilis tidak
terlihat pertumbuhan koloninya di petri dish.
(Breed, 1957, hal 199)
III.1.2 Metode Cawan Tuang
Tujuan dari percobaan isolasi mikroorganisme dari suatu campuran dengan
metode cawan tuang adalah untuk mempelajari cara cara mengisolasi
mikroorganisme dari suatu campuran dengan menggunakan teknik cawan tuang.
Pada prinsipnya metode cawan tuang sama dengan cawan gores yaitu dengan
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
16
Laporan Resmi Praktikum Mikrobiologi Teknik
pengenceran biakan mikroorganisme sehingga akan individu sel tunggal akan
terpisah dari yang lainnya. Keunggulan dari metode ini adalah tidak membutuhkan
banyak waktu dan keterampilan khusus dalam pengerjaannya, tetapi bahan yang
digunakan relatif lebih banyak daripada metode cawan gores.
Pada percobaan ini digunakan 3 tabung reaksi dan 3 petri dish. Ketiga
tabung reaksi diisi dengan media NBA hingga separuhnya. Kemudian tabung reaksi
diberi penyumbat yang terbuat dari kapas khusus yang mengandung lemak.
Penyumbat dari kapas agar udara tetap dapat masuk ke dalam tabung. Sementara
kandungan lemak pada kapas untuk mencegah masuknya uap air ke dalam tabung.
Aluminium foil tidak dapat digunakan untuk menutup tabung karena kandungan
logam dapat menghambat pertumbuhan mikroorganisme. Selain itu apabila ditutup
terlalu rapat dengan aluminium foil, udara tidak dapat masuk ke dalam tabung.
Sementara petri dish dibungkus dengan kertas cokelat untuk mencegah air
dari autoclave yang masuk ke dalam petri dish dan mencegah kontaminasi. Bagian
kertas yang berada di luar adalah bagian yang licin. Bagian licin pada kertas cokelat
mengandung lilin, sehingga menghalangi uap air yang masuk ke dalam petri dish.
Selanjutnya tabung reaksi dan petri dish yang telah berisi media dimasukkan ke
dalam autoclave. Sterilisasi dilakukan pada suhu 121oC selama kira-kira 20 menit.
Sterilisasi adalah penghilangan segala jenis kehidupan mikroorganime,
termasuk endosporanya, kecuali prion yang memiliki resistasi tinggi. Segala
sesuatu yang digunakan untuk sterilisasi disebut sterilant. Sterilisasi dengan
autoclave sangat efektif, ketika organisme dikontakkan langsung dengan uap panas
atau dengan sedikit liquid dengan suhu panas. Pada kondisi ini, uap dengan tekanan
sedikit di atas atmosfer (15 psig, 121oC) akan mematikan semua organisme beserta
endosporanya, selain prion.
(Tortora, 2010, hal 188)
Tabung reaksi berisi media didiamkan hingga suhunya mencapai suhu 50
o
C. Hal itu diperlukan karena mikroorganisme hanya dapat tumbuh dalam medium
agar pada kisaran suhu tertentu. Mayoritas mikroorganisme tergolong sebagai jenis
mesofil yang dapat tumbuh optimum pada suhu 200C 300C dan tidak dapat
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
17
Laporan Resmi Praktikum Mikrobiologi Teknik
tumbuh pada suhu sekitar diatas 50 0C. Penginokulasian harus dilakukan dengan
cepat sebelum media memadat. Apabila sebelum proses inokulasi media telah
memadat, maka perlu dipanaskan hingga media menjadi cair kembali.
(Waites, 2001, hal 33)
Selanjutnya dilakukan inokulasi dari suspensi berisi campuran
mikroorganisme. Seluruh proses inokulasi dilakukan di dalam incase sehingga
dapat meminimalisir kontaminasi dan faktor lain dari lingkungan karena dilakukan
di ruangan tertutup dan terisolasi. Untuk memindahkan mikroorganisme dari biakan
ke media baru, digunakan kawat ose. Sebelum digunakan, kawat ose dipanaskan
terlebih dahulu di atas api hingga membara pada bagian ujung hingga tengahnya.
Tujuan dari pemanasan ini adalah untuk sterilisasi kawat ose, dimana seluruh
mikroorganisme akan mati apabila terkena suhu tinggi. Kemudian kawat ose
didiamkan beberapa saat supaya dingin, karena suhu tinggi dapat membunuh
bakteri pada biakan dan merusak media agar.
Kawat ose dicelupkan ke suspensi berisi campuran mikroorganisme. Kapas
penyumbat pada tabung biakan dibuka dan ujung tabung dipanaskan dengan api
untuk sterilisasi. Setelah itu kawat ose yang telah berisi suspensi mikroorganisme
dicelupkan ke media pada tabung reaksi hingga mencapai dasarnya. mulut tabung
dipanaskan sebentar dengan api untuk membunuh mikroorganisme yang mungkin
tertinggal karena kawat ose menyentuh tabung. Setelah itu menutup tabung reaksi
dengan kapas penyumbat. Kapas penyumbat tidak boleh tertukar, untuk
menghindari kontaminasi apabila ada mikroorganisme yang tertinggal di kapas.
Setelah inokulasi selesai, kawat ose dipanaskan kembali hingga membara lalu
didinginkan untuk sterilisasi.
Tabung reaksi pertama yang telah diinokulasi harus diaduk dengan cara
memutarkan tabung reaksi diantara kedua telapak tangan hingga kekeruhannya
merata (homogen). Hal ini dimaksudkan agar bakteri tidak mengendap pada dasar
tabung reaksi. Pengadukan tidak boleh dilakukan dengan mengocok tabung reaksi
karena dapat menyebabkan sel-selnya mati dan terjadi penumpukan sel.
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
18
Laporan Resmi Praktikum Mikrobiologi Teknik
Dengan cara yang sama, memindahkan satu lup penuh biakan dari tabung
reaksi 1 ke dalam tabung reaksi 2, selanjutnya memindahkan satu lup penuh biakan
dari tabung reaksi 2 ke dalam tabung reaksi 3. Penginokulasian bakteri dari suspensi
biakan campuran dilakukan secara aseptik pada masing-masing tabung reaksi,
yakni dengan menggunakan kawat ose yang dipijarkan pada nyala api bunsen setiap
sebelum maupun setelah inokulasi pada masing-masing tabung reaksi. Hal ini
dilakukan agar tidak ada bakteri lain yang mengkontaminasi media. Lalu
menuangkan biakan dari tabung reaksi bernomor 1, 2, dan 3 masing-masing ke
dalam petri dish bernomor 1, 2, dan 3, Skema metode cawan tuang ditunjukkan
pada gambar dibawah ini.
Gambar III.7 Skema Percobaan Metode Cawan Tuang
(Benson, 2003, 86)
Setelah media pada petri dish memadat, petri dish dibungkus dengan kertas cokelat.
Kemudian dimasukkan ke dalam inkubator untuk diinkubasi. Inkubasi berarti
menyimpan kultur pada ruangan dengan temperatur yang dikontrol untuk
mendorong terjadinya pembelahan sel.
(Cowan, 2016, hal. 37)
Penyimpanan petri dish di inkubator dilakukan dengan terbalik untuk
mencegah uap air yang masuk hingga menyentuh media. Uap air yang ada pada
media dapat menyebabkan pergerakan koloni mikroorganisme di dalam media dan
dapat merusak bakteri. Proses inkubasi dilakukan selama 47 jam pada suhu 30 oC
karena merupakan suhu optimum dalam pertumbuhan mikroorganisme.
Mikroorganisme yang digunakan dalam percobaan merupakan contoh
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
19
Laporan Resmi Praktikum Mikrobiologi Teknik
mikroorganisme mesophile, dimana suhu optimum untuk tumbuh adalah di bawah
50oC.
(Tortora, 2010, hal. 158)
Selanjutnya dilakukan pengamatan terhadap pertumbuhan koloni bakteri
pada media. Pengamatan dilakukan pada 24 jam dan 47 jam. Pada pengamatan 24
jam, terlihat bahwa sudah ada koloni berwarna putih terutama di petri dish 1.
Pertumbuhan koloni semakin sedikit pada petri dish 2, dan hanya terdapat satu
koloni di petri dish 3. Pada pengamatan 47 jam, petri dish 1 telah dipenuhi koloni
bakteri. Pada petri dish 2 jumlah koloni lebih sedikit dibanding petri dish 1, namun
diameternya lebih besar. Sementara pada petri dish 3 terdapat 2 koloni bakteri
dengan morfologi yang berbeda.
Gambar III.8 Hasil Pengamatan pada Petri dish 1 setelah 24 jam (kiri) dan 47
jam (kanan)
Berdasarkan pengamatan, pada petri dish 1 terdapat 2 koloni bakteri dengan
bentuk yang berbeda. Koloni pertama berwarna putih kusam, bulat, dan dengan
elevasi raised. Sementara koloni yang lainnya berwarna putih kekuningan, bulat,
dengan elevasi raised tetapi berukuran lebih kecil dan terlihat moist. Berdasarkan
morfologi ini, dapat diprediksi bahwa masing-masing koloni berasal dari sel
tunggal yang berbeda, yaitu koloni pertama dari Bacillus subtilis sementara yang
lain dari Eschericia coli. Berdasarkan literatur, morfologi dan ciri ciri dari bakteri
Bacillus subtilis dapat diidentifikasi melalui bentuk koloninya yang berbentuk
kasar, tidak transparan, menyebar, dan berwarna putih kusam.
(Breed, 1957, hal 620)
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
20
Laporan Resmi Praktikum Mikrobiologi Teknik
Bakteri Zymomonas mobilis memiliki ciri ciri yaitu, sel diplobasil,
berwarna putih, kondisi anaerob diperlukan untuk memfermentasi gula.
Zymomonas mobilis tidak tumbuh dengan baik pada media NBA. Zymomonas
mobilis membutuhkan kandungan gula untuk fermentasi, sementara NBA
menyediakan nutrisi protein (pepton).
(Breed, 1957, hal 199)
Kemungkinan lainnya, yaitu Escherichia coli mempunyai koloni pada
media agar yang berwarna putih hingga putih kekuningan, undulate, moist, dan
homogen.
(Breed, 1957, hal. 336)
Gambar III.9 Hasil Pengamatan pada Petri dish 2 setelah 24 jam (kiri) dan 47
jam (kanan)
Berdasarkan pengamatan, pada petri dish 2 terdapat 2 koloni bakteri dengan
bentuk yang berbeda. Koloni pertama berwarna putih kusam, bulat, dan dengan
elevasi raised. Sementara koloni yang lainnya berwarna putih kekuningan, bulat,
dengan elevasi raised tetapi berukuran lebih kecil dan terlihat moist. Berdasarkan
morfologi ini, dapat diprediksi bahwa masing-masing koloni berasal dari sel
tunggal yang berbeda, yaitu koloni pertama dari Bacillus subtilis sementara yang
lain dari Eschericia coli.
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
21
Laporan Resmi Praktikum Mikrobiologi Teknik
Gambar III.10 Hasil Pengamatan pada Petri dish 3 setelah 24 jam (kiri) dan
47 jam (kanan)
Berdasarkan pengamatan pada petri dish ketiga, koloni pertama berwarna
putih kusam, bulat, dan dengan elevasi raised. Sementara koloni yang lainnya
berwarna putih kekuningan, bulat, dengan elevasi raised tetapi berukuran lebih
kecil dan terlihat moist. Berdasarkan morfologi ini, dapat diprediksi bahwa masing-
masing koloni berasal dari sel tunggal yang berbeda, yaitu koloni pertama dari
Bacillus subtilis sementara yang lain dari Eschericia coli. Dapat disimpulkan
bahwa campuran A berisi Bacillus subtilis dan Escherichia coli.
B. subtilis
E. coli
Gambar III.11 Hasil pengamatan setelah 47 jam metode cawan tuang
Gambar III.12 (Kiri) Koloni Escherichia coli (Kanan) Koloni Bacillus subtilis
(www.hardydiagnostics.com)
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
22
Laporan Resmi Praktikum Mikrobiologi Teknik
II.2 Uji Biokimia (Uji Oksidasi-Fermentasi)
Tujuan dari percobaan ini adalah mempelajari kemampuan mikroorganisme
dalam mengkatabolisme apakah berlangsung secara oksidant atau fermentatif.
Bakteri yang digunakan adalah Nitrobacter dan Lactobacillus.
Langkah pertama dari uji ini mensterilkan tabung reaksi yang akan
digunakan dengan alkohol 70%. Alkohol efektif untuk membunuh bakteri dan
jamur, tetapi tidak dengan endospore dan virus yang tidak mempunyai envelope.
Mekanisme alkohol digunakan sebagai desinfektan karena alkohol menyebabkan
denaturasi protein, dapat merusak membran dan melarutkan lemak, termasuk
komponen lemak penyusun lapisan pelindung pada virus. Alkohol cukup baik
dalam membunuh mikroorganisme dan mudah menguap serta tidak meninggalkan
residu.
(Tortora, 2010, hal. 197)
Setelah tabung reaksi sudah disterilisasi, media Hugh and Leifson steril
ditambahkan ke dalam masing-masing tabung reaksi. Media Hugh and Leifson
mengandung gula dan pepton dengan rasio tinggi untuk memberi kesempatan basa
yang dihasilkan dari pepton akan menetralisir asam lemah yang dihasilkan dari
oksidasi karbohidrat. Biasanya di dalam media Hugh and Leifson ditambahkan
bromtymol blue yang berwarna kuning pada pH 6.0 dan hijau pada pH 7.1 sebagai
indicator. Sementara kandungan agar yang rendah menjadikan Hugh and Leifson
sebagai media semi-solid yang memberi kesempatan pada mikroorganisme untuk
berpindah tempat.
(Leboffe, 2011, hal 89-90)
Kemudian menginokulasikan biakan menggunakan kawat ose ke dalam
masing masing tabung. 2 tabung untuk Nitrobacter, 2 tabung Lactobacillus.
Sementara 2 tabung reaksi lainnya untuk blanko. Menginokulasi mikroorganisme
harus dilakukan di dalam incase karena percobaan yang kita lakukan bersifat
aseptic. Selanjutnya salah satu dari tabung yang telah diinokulasi masing masing
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
23
Laporan Resmi Praktikum Mikrobiologi Teknik
Nitobacter, Lactobacillus, dan blanko ditambah dengan parafin sebanyak kurang
lebih sampai 1 cm. Setelah itu diinkubasi pada suhu sekitar 30oC. Sehingga masing-
masing bakteri mempunyai sampel anaerobik dan aerobik.
Mikroorganisme yang memiliki metabolisme oksidatif akan mengoksidasi
karbohidrat secara langsung menjadi piruvat dan kemudian mengubahnya menjadi
CO2 dan energy dihasilkan dari siklus Krebs dan transport electron, dimana molekul
anorganik seperti oksigen berperan sebagai penerima elektron terakhir. Fermentasi
juga mengubah karbohidrat menjadi piruvat, tetapi menggunakannya untuk
memghasilkan satu atau lebih asam. Mikroorganisme fermentatif dapat
diidentifikasi dengan tes ini melalui test keasaman.
(Leboffe, 2011, hal 89-90)
Mikroorganisme yang bersifat oksidatif, maka akan terjadi perubahan warna
media, yaitu media yang tidak tertutup parafin sedangkan untuk mikroorganisme
yang bersifat fermentatif, akan terjadi perubahan warna media baik yang tertutup
parafin maupun yang tidak tertutup. Sementara mikroorganisme yang tidak
mempunyai metabolisme gula tidak akan berubah warna atau bahkan berubah
warna menjadi biru karena kebasaan yang dihasilkan dari degadrasi asam amino.
(Leboffe, 2011, hal 89-90)
Berdasarkan percobaan yang telah dilakukan, Nitrobacter berubah warna
menjadi keseluruhan kuning ketika dalam kondisi anaerobik, tetapi hanya sedikit
berubah warna pada keadaan aerobik. Berdasarkan literatur, Nitrobacter bersifat
aerobik dan oksidatif karena dapat mengoksidasi nitrat menjadi nitrit. Namun pada
hasil percobaan yang telah dilakukan menunjukkan bahwa pada kondisi aerobik
hanya sedikit perubahan warnanya menjadi warna hijau muda. Hal ini dikarenakan
ketika inokulasi kawat ose terlalu panas, sehingga mematikan bakteri yang akan
diinokulasi. Akibatnya jumlah bakteri yang hidup di tabung aerobik sedikit,
sehingga tidak terlihat perubahan warnanya.
(Breed, 1957, hal 72)
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
24
Laporan Resmi Praktikum Mikrobiologi Teknik
Pada Lactobacillus, terjadi perubahan warna, namun tidak pada seluruh
bagian media baik pada kondisi aerobik maupun anaerobik. Hal ini menunjukkan
bahwa Lactobacillus merupakan bakteri yang oksidatif dan fermentatif.
Lactobacillus merupakan bakteri yang dapat mengubah glukosa dan heksosa
aldehid sejenis, karbohidrat yang dapat menghasilkan glukosa, dan polyhydroxy
alkohol menjadi asam laktat dengan homofermentasi atau menjadi asam laktat dan
asam asetat, alkohol dan karbon dioksida dengan heterofermentasi. Nitrat tidak
dapat direduksi kecuali dalam kondisi tertentu dengan Lactobacillus plantarum.
Bakteri ini secara umum bersifat mikroaerofilik atau anaerobik. Meskipun
anaerobik, bakteri ini masih memiliki toleransi terhadap oksigen di udara sehingga
pada percobaan pada kondisi aerobik maupun anaerobik bakteri dapat hidup.
(Breed, 1957, hal 542)
Jawaban Pertanyaan
III. A. Isolasi Mikroorganisme dari Suatu Campuran
1. Bagaimanakah keadaan media pembanding (blanko)? Apakah
kegunaannya?
Kegunaan dari blanko ini adalah sebagai pembanding keadaan media yang
tidak terdapat mikroorganisme dan yang terdapat mikroorganisme (yang
telah diinokulasi).
(Tortora, 2010, hal 254)
2. Setelah melakukan isolasi bakteri dengan metode cawan gores, pada
daerah manakah bakteri terisolasi? Bandingkan dengan media
pembanding!
Pada isolasi mikroorganisme dengan metode cawan goeres,
mikroorganisme terisolasi sempurna pada kuadran III karena pada kuadran
ini merupakan penggoresan yang terakhir. Suspensi biakannya paling encer
sehingga koloni bakteri yang tumbuh paling sedikit daripada kuadran yang
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
25
Laporan Resmi Praktikum Mikrobiologi Teknik
lain. Media pembanding tetap steril atau tidak ada mikroorganisme yang
tumbuh.
(Benson, 2001, hal. 82)
3. Apakah pada permukaan agar yang tidak digores tampak koloni?
Jelaskan! (Jika terdapat ataupun tidak)
Pada permukaan agar yang tidak digores terdapat mikroorganisme. Hal ini
menunjukkan bahwa media agar yang digunakan telah terkontaminasi
mikroorganisme yang tidak diinginkan. Hal ini mengindikasikan bahwa
media yang kita gunakan sewaktu proses inokulasi di dalam incase telah
terkontaminasi oleh mikroorganisme. Hal ini dimungkinkan terjadi karena
tidak adanya batasan antar tiap sektor yang menghalangi bakteri tumbuh
menyebar ke sektor yang tidak digores, dan juga kepadatan populasi dalam
sektor asal menyebabkan bakteri mencari nutrisi dan lahan yang cukup
untuk tumbuh dan berkembang.
(Benson, 2001, hal.39)
4. Apakah keunggulan dan kekurangan dari kedua metode di atas?
Teknik Cawan Gores
- Keunggulan : pengerjaan lebih cepat sehingga dapat menghemat
waktu dan bahan.
- Kekurangan : lebih sulit karena membutuhkan keterampilan yang
baik dalam menggores.
Teknik Cawan Tuang
- Keunggulan : tidak membutuhkan keterampilan yang tinggi untuk
mendapatkan hasil yang baik. Selain itu, mikroorganisme yang
tumbuh dan dapat tersebar merata pada media agar.
- Kekurangan : memerlukan waktu yang lama dan bahan yang
banyak.
(Benson, 2001, hal. 82-86)
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
26
Laporan Resmi Praktikum Mikrobiologi Teknik
III. B. Uji Biokimia
1. Sebutkan media yang digunakan pada beberapa tes berikut !
a) Produksi Butanediol
b) Hidrolisis kanji
c) Hidrolisis lemak
d) Hidrolisis kasein
a) Produksi Butanediol : Media MR VP
b) Hidrolisis kanji : Media Kanji
c) Hidrolisis lemak : Media NBA (Nutrient Broth Agar)
d) Hidrolisis kasein : Media kasein agar
(Tortora, 2010, hal. 160)
2. Pilihlah nama nama reagent yang digunakan tes tersebut !
a) Voges Proskauer Test
b) Catalase Test
c) Hidrolisis Kanji
Voges Proskauer Test : A. Reagen Barrit
Catalase Test : C. Hidrogen Peroksida
Hidrolisis Kanji : B. Grams iodine
(Tortora, 2010, hal. 161)
3. Enzim enzim apa saja yang terlibat pada reaksi reaksi berikut dan
sebutkan pula produk hasil hidrolisisnya ?
a) Hidrolisis kasein
b) Hidrolisis kanji
c) Hidrolisis lemak
d) Hidrolisis gelatin
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
27
Laporan Resmi Praktikum Mikrobiologi Teknik
a) Hidrolisis kasein : kaseinase ( kasein asam amino)
b) Hidrolisis kanji : - amylase (polisakarida monosakarida)
c) Hidrolisis lemak : lipase ( lemak asam lemak dan gliserol)
d) Hidrolisis gelatin : gelatinase (gelatin asam amino)
(Tortora, 2010, hal. 116)
4. Apakah perbedaan Methyl Red Test dengan Voges Proskauer Test ?
Perbedaan Methyl-Red Test Voges-Proskauer Test
Fungsi Uji untuk menentukan Uji untuk menentukan
adanya fermentasi asam terbentuknya asam organik
campuran berupa asetil metil karbinol
Indikator Reagent Methyl-Red Reagent Barrit
(Naphtol+KOH)
Hasil test positif Warna merah Warna merah muda
Hasil test Warna kuning Warna kuning
negative
Alasan terjadi Uji MR dan uji VP digunakan untuk menentukan apa
perubahan produk akhir terjadi ketika uji degradasi glukosa oleh
warna organisme. Bila indikator pH metil merah
ditambahkan ke media asam akan menjadi warna
merah (uji MR positif). Reagen yang digunakan untuk
uji VP adalah Barrit A (alpha-napthol) dan Barrit B
(kalium hidroksida). Ketika reagen ditambahkan ke
media kaldu yang mengandung asetil metil karbinol,
warna akan berubah menjadi merah muda (tes VP
positif).
5. Apakah manfaat enzim enzim tersebut (soal nomor 3) pada
mikroorganisme ?
a) Kaseinase
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
28
Laporan Resmi Praktikum Mikrobiologi Teknik
b) Amylase
c) Lipase
d) Gelatinase
a) Kaseinase : untuk menghidrolisis kasein menjadi asam amino
b) Amylase : untuk menguraikan polisakarida menjadi
monosakarida
c) Lipase : untuk menghidrolisis lemak menjadi asam lemak
dan gliserol
d) Gelatinase : untuk menguraikan gelatin menjadi asam amino
(Tortora, 2010, hal. 116)
IV. Kesimpulan
IV.1 Isolasi Mikroorganisme dari Suatu Campuran
1. Isolasi mikroorganisme dapat dilakukan dengan metode cawan gores
maupun cawan tuang.
2. Pada metode cawan gores, mikroorganisme yang dapat diisolasi adalah
Bacillus subtilis.
3. Pada metode cawan tuang, mikroorganisme tidak dapat diisolasi karena
terdapat 2 mikroorganisme yaitu Bacillus subtilis dan Escherichia coli.
IV.2 Uji Biokimia (Uji Oksidasi-Fermentasi)
Berdasarkan percobaan yang telah dilakukan, dapat disimpulkan bahwa:
1. Nitrobacter tidak menunjukkan sifat aerobik karena pada percobaan aerobik
tidak berubah warna
2. Lactobacillus bersifat oksifatif-fermentatif sesuai dengan literatur
Daftar Pustaka
Benson. 2001. Microbiological Applications Laboratory Manual 8th Edition. The
McGraw Hill
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
29
Laporan Resmi Praktikum Mikrobiologi Teknik
Breed, Robert S., Murray, E.G.D., Sith, Nathan R. 1957. Bergey Manual of
Determinative Bacteriology 7th Edition. US: The Williams & Wilkins
Company
Cowan, Marjorie Kelly, et. al. 2016. Microbiology Fundamentals A Clinical
Approach Second Edition. New York: McGraw Hill
Leboffe, Michael J., Pierce, Burton E. 2011. A Photographic Atlas for the
Bicrobiology Laboratory 4th Edition. US: Morton Publishing Company
Morello, Josephine A. Granato, Paul A. Mizer, Helen Eckel. 2003. Laboratory
Manual and Workbook in Microbiology 7th Edition. The McGraw Hill
Company.
Prescott. Harley. 2002. Laboratory Exercises in Microbiology 5th Edition. The
McGraw Hill Company
Tortora, Gerard J., Funke, Berdell R. Case, Christine L. 2010. Microbiology an
Introduction 10th Edition. US: Benjamin Cummings.
Waites, Michael J. et.al. 2001. Industrial Microbiology An Introduction. Oxford:
Blackwell Science Ltd
www.catalog.hardydiagnostics.com/cp_prod/Content/hugo/TrypticSoyAgar.htm
Diakses pada 2 April 2016 pukul 19.20
Laboratorium Mikrobiologi Teknik
Jurusan Teknik Kimia FTI-ITS
Anda mungkin juga menyukai
- LKPD BioteknologiDokumen8 halamanLKPD Bioteknologinaqsya007Belum ada peringkat
- Biokim LapDokumen20 halamanBiokim LapKevin EsmunaldoBelum ada peringkat
- Inokulasi Mikroorganisme & Penggunaan MikroskopDokumen19 halamanInokulasi Mikroorganisme & Penggunaan MikroskopFarkhan ApriadiBelum ada peringkat
- Modul 1 - Inokulasi Dan Mikroskop - Novita - Rev2 AccDokumen23 halamanModul 1 - Inokulasi Dan Mikroskop - Novita - Rev2 AccNovita Eka RahmawatiBelum ada peringkat
- Laporan Resmi Modul 1Dokumen27 halamanLaporan Resmi Modul 1NaufalBelum ada peringkat
- Laporan Pratikum ISOLASI MIKROORGANISME DARI SUATU CAMPURAN DAN UJI BIOKIMIA.Dokumen10 halamanLaporan Pratikum ISOLASI MIKROORGANISME DARI SUATU CAMPURAN DAN UJI BIOKIMIA.Kelvin Letare SBelum ada peringkat
- Lapres Mikro Modul IIDokumen14 halamanLapres Mikro Modul IIyuzansaBelum ada peringkat
- Uji Desinfektan Dan Thermal Death TimeDokumen23 halamanUji Desinfektan Dan Thermal Death TimeAditiya RamadhanBelum ada peringkat
- Lapres 2Dokumen15 halamanLapres 2alifahfajrinBelum ada peringkat
- MikrobiologiDokumen22 halamanMikrobiologiadithimatekk 99Belum ada peringkat
- Isolasi Mikroorganisme Dan Penggunaan Mi PDFDokumen20 halamanIsolasi Mikroorganisme Dan Penggunaan Mi PDFRegina Elshaddai TimangBelum ada peringkat
- Cawan Gores & ofDokumen7 halamanCawan Gores & ofAmelia DjafaarBelum ada peringkat
- Laporan Resmi 1Dokumen11 halamanLaporan Resmi 1dayuvinkyBelum ada peringkat
- Modul 3Dokumen16 halamanModul 3Afifatul JannahBelum ada peringkat
- Jurnal Mikrobiologi InokulasiDokumen19 halamanJurnal Mikrobiologi InokulasinovaBelum ada peringkat
- Laporan Praktikum Inokulasi MikroorganismeDokumen17 halamanLaporan Praktikum Inokulasi MikroorganismeAfifatul JannahBelum ada peringkat
- LAPORAN RESMI Desinfektan TDT DinnyDokumen23 halamanLAPORAN RESMI Desinfektan TDT DinnyFathia Syahranti100% (1)
- Lapres Modul 2 - Fahmi Reza W. (2313100123)Dokumen21 halamanLapres Modul 2 - Fahmi Reza W. (2313100123)Fahmi Reza WijanarkoBelum ada peringkat
- Petunjuk Praktikum Mikrobiologi PDFDokumen43 halamanPetunjuk Praktikum Mikrobiologi PDFTantri RatnasariBelum ada peringkat
- Modul 5. Melakukan Analisis MikrobiologiDokumen89 halamanModul 5. Melakukan Analisis MikrobiologiNeiya MasykurBelum ada peringkat
- Pengaruh Desinfektan Dan Antiseptik Terhadap Pertumbuhan BakteriDokumen23 halamanPengaruh Desinfektan Dan Antiseptik Terhadap Pertumbuhan BakteriNiswatun ChasanahBelum ada peringkat
- Template Laprak 2Dokumen8 halamanTemplate Laprak 2smbfst. uinmalangBelum ada peringkat
- Lapres Mikro Modul 1 - GladysElvinaAntou - 02211740000030Dokumen14 halamanLapres Mikro Modul 1 - GladysElvinaAntou - 02211740000030Gladys ElvinaBelum ada peringkat
- Uji AntibakteriDokumen9 halamanUji AntibakteriThree ManurungBelum ada peringkat
- Desinfektan Dan Thermal Death TimesDokumen20 halamanDesinfektan Dan Thermal Death TimesChazza Moet100% (1)
- Nabilla Zahra Ap1 Mikrobiologi TM 3Dokumen10 halamanNabilla Zahra Ap1 Mikrobiologi TM 3NABILLA ZAHRABelum ada peringkat
- Lapres Uji Biokimia MilaDokumen17 halamanLapres Uji Biokimia MilaChristopher Endika Purba GirsangBelum ada peringkat
- Isolasi Bakteri Dan Uji BiokimiaDokumen14 halamanIsolasi Bakteri Dan Uji BiokimiaHaris Pratama100% (1)
- Uji Desinfektan Dan Thermal Death TimeDokumen12 halamanUji Desinfektan Dan Thermal Death TimeHaris PratamaBelum ada peringkat
- Budi Santoso - 200209121 - 20B1 - Mikro Tipe3Dokumen5 halamanBudi Santoso - 200209121 - 20B1 - Mikro Tipe3Tatiana Siska WardaniBelum ada peringkat
- B13 Made Aryduta Sutasoma (020.06.0049) Praktikum Mikrobio Respi 2Dokumen25 halamanB13 Made Aryduta Sutasoma (020.06.0049) Praktikum Mikrobio Respi 2DutaSSBelum ada peringkat
- Bioteknologi YoghurtDokumen4 halamanBioteknologi YoghurtSerly PerdaniBelum ada peringkat
- LP BioteknologiDokumen4 halamanLP Bioteknologiongky greenBelum ada peringkat
- LKPD 2. Praktikum Virtual Mitosis Pada Ujung Akar BawangDokumen2 halamanLKPD 2. Praktikum Virtual Mitosis Pada Ujung Akar BawangRafi Not Good.Belum ada peringkat
- Lembar Kerja Mikro Blok 8 KuDokumen6 halamanLembar Kerja Mikro Blok 8 KuannaBelum ada peringkat
- Bioteknologi Produksi MetabolitDokumen12 halamanBioteknologi Produksi MetabolitimamaptBelum ada peringkat
- 08f-Bagian VIIIf FAKULTAS TEKNOBIOLOGI PDFDokumen14 halaman08f-Bagian VIIIf FAKULTAS TEKNOBIOLOGI PDFYonatan AdiBelum ada peringkat
- Isolasi Mikroorganisme Dan Uji BiokimiaDokumen34 halamanIsolasi Mikroorganisme Dan Uji BiokimiaSelvi Amelia VBelum ada peringkat
- Peranan Positif Dan Negatif BioteknologiDokumen4 halamanPeranan Positif Dan Negatif BioteknologiHakki Ahdika SiregarBelum ada peringkat
- Laporan Praktikum Mikrobiologi NitrifikasiDokumen13 halamanLaporan Praktikum Mikrobiologi NitrifikasiAlmeira AdefiaBelum ada peringkat
- Laprak Mikrobiologi Umum Acara 4Dokumen13 halamanLaprak Mikrobiologi Umum Acara 4Dimitri Widi512Belum ada peringkat
- Laporan Praktikum Mikrobia Tanah Acara 1Dokumen16 halamanLaporan Praktikum Mikrobia Tanah Acara 1Rinaldi KomendangiBelum ada peringkat
- Silabusbiotek PDFDokumen4 halamanSilabusbiotek PDFkoleksi paulusBelum ada peringkat
- Modul TTV Sains F5Dokumen146 halamanModul TTV Sains F5Karisma Diana50% (2)
- Week 6 Microbial Growth 2022Dokumen70 halamanWeek 6 Microbial Growth 2022Rivaldi Di CaprioBelum ada peringkat
- Laporan Praktikum Mikrobiologi Tempe Dan TapeDokumen33 halamanLaporan Praktikum Mikrobiologi Tempe Dan TapealipiahBelum ada peringkat
- 3-LKPD 3.7-1-Apakah Bioteknologi ItuDokumen7 halaman3-LKPD 3.7-1-Apakah Bioteknologi ItumayaBelum ada peringkat
- Isolasi MikroorganismeDokumen31 halamanIsolasi MikroorganismearwindarBelum ada peringkat
- Mikrobiologi Tanah PDFDokumen15 halamanMikrobiologi Tanah PDFChrista GabrielaBelum ada peringkat
- LKPD 1-Identifikasi Produk BioteknologiDokumen3 halamanLKPD 1-Identifikasi Produk BioteknologiPuji AstutikBelum ada peringkat
- Lembar Kerja Peserta Didik BioDokumen6 halamanLembar Kerja Peserta Didik BioNuril channelBelum ada peringkat
- Laprak Ke 4 InaDokumen8 halamanLaprak Ke 4 InaKKN 75 JuniyarBelum ada peringkat
- Spesifikasi Bactec FX40Dokumen2 halamanSpesifikasi Bactec FX40tuanfatur0% (1)
- Pertemuan 1a. Pengantar Semester Genap 2021 2022Dokumen23 halamanPertemuan 1a. Pengantar Semester Genap 2021 2022MnemosyneBelum ada peringkat
- MODUL6Dokumen11 halamanMODUL6Nursinta DewiBelum ada peringkat
- Mikrobiologi Umum - Puja Rania Taj Nacia - 195100100111054Dokumen1 halamanMikrobiologi Umum - Puja Rania Taj Nacia - 195100100111054RaniaBelum ada peringkat
- MIKROBIOLOGIDokumen75 halamanMIKROBIOLOGIKilang MinyakBelum ada peringkat
- Modul TTV Bio F4Dokumen229 halamanModul TTV Bio F4Karisma DianaBelum ada peringkat
- LKPD BioteknologiDokumen6 halamanLKPD Bioteknologialmalikbhaqi29Belum ada peringkat
- Modul 4 - Oligodinamik Dan TDT - Novita - Rev3 AccDokumen29 halamanModul 4 - Oligodinamik Dan TDT - Novita - Rev3 AccNovita Eka RahmawatiBelum ada peringkat
- CoverDokumen1 halamanCoverNovita Eka RahmawatiBelum ada peringkat
- Modul 3 - CoverDokumen3 halamanModul 3 - CoverNovita Eka RahmawatiBelum ada peringkat
- Modul 1 - CoverDokumen5 halamanModul 1 - CoverNovita Eka RahmawatiBelum ada peringkat
- Laporan Praktikum Mikrobiologi Teknik - Turbidimetri Dan Counting Chamber - NovitaDokumen16 halamanLaporan Praktikum Mikrobiologi Teknik - Turbidimetri Dan Counting Chamber - NovitaNovita Eka RahmawatiBelum ada peringkat