Laporan Spu PDF
Diunggah oleh
Dewi Kurniawati PutriHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Laporan Spu PDF
Diunggah oleh
Dewi Kurniawati PutriHak Cipta:
Format Tersedia
Search
Laporan
DownloadSPU !
Uploaded by rizky
' 0 ratings · 155 views · 10 pages
Document Information (
spu
Original Title
laporan SPU
Copyright
Download !
© © All Rights Reserved
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
PERCOBAAN V Jumat, 06 November 2015
SISTEM PERIODIK UNSUR
I. TUJUAN
Facebook
1. Twitter
Mengenal unsur halogen dan ion halida.
2. Mempelajari kekuatan oksidasi relatif unsur-unsur.
3. Mempelajari keperiodikan sifat logam-logam alkali dan alkali tanah.
%
II. DASAR TEORI
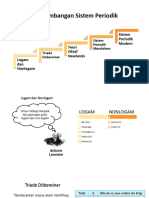
Skema klasifikasi unsur-unsur serupa yang dikenal sekarang ditemukan secara
terpisah dan hampir serempak oleh dimitri Mendeleev dan lohar mayer pada tahun 1869.
“Jika unsur disusun berdasarkan kenaikan bobot atom, seperangkat sifat akan terulang
secara berkala. Tabel berkala ialah penataan unsur-unsur dalam 12 baris mendatar dan 8
kolom tegak (golongan). Kedelapan golongan kemudian dibagi lagi menjadi sub
Did you golongan
find this yangdocument
sesuai, secarauseful?
obyektif perlu ditinggalkan beberapa ruang kosong bagi
unsur-unsur yang belum ditemukan pada waktu itu dan dibuat praduga mengenai bobot
atom yang belum diketahui secara pasti. (Petrucci, 1987: 245)
Kira-kira 80 unsur diklasifikasikan sebagai logam yang melipuuti beberapa dari
setiap grup, kecuali VIII A, VII A dan mungkin VI A. logam-logam ini berada disebelah
kiri dan tengah tabel berkala. Dalam reaksi kimia dengan nonlogam, atom logam
cenderung menyumbangkan elektron, dan membentuk kation keelektronegatifannya
rendah, kebanyakan diantaranya kurang dari 2,0. Selanjutnya unsur non logam, yang
Is this content inappropriate? Report this Document
terdiri dari kira-kira selusin unsur-unsur yang relatif umum dan penting, ditambah gas
mulia, berada disebelah kanan pada tabel priodik, kecuali hidrogen. Atom dari non
logam cenderung menerima elektron, dan membentuk anion dalam reaksi kimia dengan
logam. Selain itu nonlogam juga non logam juga mudah bereaksi satu sama lain dengan
membentuk ikatan kovalen misalnya dalam SO 3, CO2 dan H2O. keelektronegatifannya
dari kebanyakan non logam berkisar dari sekitar 2,4 ke atas. Selanjutnya Metoloid atau
unsur perbatasan, memperlihatkan baik sifat logam maupun sifat non logam sampai
tingkat tertentu, biasanya ia bertindak sebagai penyumbang elektron dengan non logam,
dan sebagai penerima elektron dengan logam. Unsur-unsur ini terletak berdekatan
dengan garis zig-zag (seperti tangga) dalam tabel berkala, seperti B, Si,Ge, Ar, Sb, Tc
termasuk dalam kelas ini. Keelektornigatifan unsur garis batas ini, berkisar antara 1.8
dan 2.1 (Keenan, dkk., 1984: 149)
Jari-jari alam adalah jarak dari inti sampai ke suatu tempat yang mempunyai
peluang untuk menemukan elektro dikulit terluarnya. Jari-jari atau suatu logam adalah
setengah jarak anatara dua inti pada atom-atom ayang berdekatan. Untuk unsur-unsur
yang berupa molekul diatomik, jari-jari atomnya adalah setengah jarak antara inti dua
Improve Your Experience *
Rating will help us to suggest even better
related documents to all of our readers!
' Useful
) Not useful
atom dalam molekul tertentu. Adapun faktor-faktor yang mempengaruhi yang
mempengaruhinya adalah keragaman ukuran atom dalam satu golongan pada sistem
priodik unsur, makin besar ukuran atomya. Yang kedua adalah keragaman ukuran atom
dalam satu periode yaitu jari-jari atom semakin menurun dari kiri kekanan dalam satu
periode. (Petrucci 1987:251).
Energi ionisasi adalah energi minum yang diperlukan untuk melepaskan satu
elektron dari atom berwujud gas pada keadaan dasarnya. Semakin besar energi ionisasi
makin sukar untuk melepaskan elektronnya (Chang, 2004: 239).
Afinitas electron kemampuan untuk menerima satu atau lebih electron, yaitu
negatif dari perubahan energi yang terjadi ketikan suatu electron diterima oleh
atom suatu unsure dalam keadaan gas. Pola kecenderungan keseluruhannya adalah
meningkatkatnya kecenderungan dalam menerima electron (yaitu, nilai afinitas electron
menjadi semakin positif) dari kiri kanan dalam satu periode. (Chang, 2004: 243).
Elektronegativitas memberikan kemampuan suatu atom dalam bersaing
mendapatkan electron, dengan atom lain yang berkaitan electronnegativitas berikatan
dengan energy ionisasi dan afinitas electron karena besaran ini memcerminkan
kemampuan atom melepaskan atau memperoleh sebuah elektron. Sebagai patokan kasar,
logam mempunai electron negativitas kurang dari 2, metalloid kira-kira sama dengan 2
dan bukan logam lebih besar dari 2. (Petrucci,1987: 258).
Beberapa sifat fisika penting dari unsur grup I A dan II A. unsur dari kedua
keluarga ini meiliki kilap keperekan logam yang khas, pada permukaan yang baru
dipotong. (tetapi ini cepat menghitam setelah tersingkap terhadap udara). Unsur-unsur ini
juga meliliki daya hantar (konduktifitas) listrik danpanas yang tinggi yang adalah khas
logam. Beberapa titik lelehnya yang relatif rendah rapatannya yang relatif rendah
dankelunakannya. Ciri khas yang paling mencolok dari logam akali dan akali tanah-
tanahan adalah kereaktifannya yang luar biasa besar. Pada unsur alkali jari-jari atom dari
litrum ke fransium semakin besar dikarenakan bertambahnya jumlah kulit electron.
Sedangkan energy ionisasinya dari keelektronegatifannya dari ltium ke fransium
semakin berkurang. Logam-logam alkali hanya memiliki satu malam tingkat oksidasi
yaitu +1. Titik leleh dan titik didih alkali tanah dari litium ketransium semakin menurun
bagitu pula gelang daya hantar listrik panas. Kecuali pada natrium. Reaksi antara
logamalkali dengan air membentuk basa dengan gas hidrogen. Dengan semakin
bertambahnya nomor atom, reaksi berlangsung semakin hebat.
Contoh: 2Na(s) + 2H2O(ℓ) → 2NaOH(aq)+ H2(g).
Pada alkali tanah dari atas kebawah dalam sestem periodik jari-jari atom secara
beraturan meningkat, sedangkan energi ionisai dan keelektronegatifannya menurun. Titik
didih dan titik lelehnya cenderung menurun dari berilium ke barium. Pada alkali dan
alkali tanah terdapat tes nyala logam yaitu untuk menentukan warna-warna unsure.
Logam alkali dan alkali tanah adalah zat pereduksi yang sangat kuat karena bagi mudah
kehilangan elektron. Logam alkali tanah bereaksi dahsyat dengan air: kalsium, strosium
dan barium bereaksi kurang dahsyat tidak satupun dari unsure-unsur alkali dan alkali
tanah terdapat didalam keadaan unsure. Semua unsure alkali terdapat dalam senyawa
alam sebagai ion-ion positif (positif satu) : sedangkan unsure alkali tanah terdapat
sebagai ion dipositif (positif dua). (keenan, dkk., 1984: 151)
Empat dari dalam group VII A, flour, klor, brom dan iod dikenal sebagai unsure
keluarga halogen. Sifat umum yang Nampak jelas pada halogen yaitu bahwa setiap sifat
tertentu berubah dengan teratur dari satu unsure keunsur berikutnya. Selanjutnya pada
kenaikan titik didih dan titik leleh dengan bertambahnya nomor atom, dijelaskan dengan
fakta bahwa molekul-molekul yang lebih besar mempunyai gaya tarik –menarik van der
wals yang lbih besar. Sedfangkan iod penting lemah. Jari-jari atom dari F ke At semakin
bertambah sedangkan energy ionisasi keelektronigatifan dan afinitas semakin berkurang
dari F ke At. Reaktivitas flour yang lebih besar disbanding dengan klor. Keempat unsure
grup VII A, semuanya sengat merangsang sekli terhadap hidung dan tenggorokan
(keenan, dkk., 1984: 228)
III. ALAT DAN BAHAN
Alat Bahan
NO Nama Alat Jumlah NO Bahan Jumlah
1 Tabung reaksi 10 1 Lautan NaF, 10mL
2 Rak tabung reaksi 1 NaCl, NaBr, dan
3 Pinggan 1 NaI
penguapan 2 Larutan brom 1mL
4 Gelas kimia 3 3 Larutan Iod 1mL
500mL 4 Larutan kanji 1mL
5 Gelas ukur 10mL 1 5 Larutan CCl4 1mL
6 Pipet tetes 5 6 Larutan AgNO3 1mL
7 Kawat nikom 1 7 Larutan natrium 1mL
tiosulfonat
8 Logam Na, Mg, 1 butir
Ca
9 Larutan pekat 10mL
LiCl, NaCl,
MgCl2, BaCl2,
SrCl2
10 Ca(NO3)2 1mL
11 Ba(NO3)2 1mL
12 Sr(NO3)2 1mL
13 (NH4)2C2O4 1mL
14 K2CrO4 1mL
15 (NH4)2SO4 1mL
16 Larutan metil 5mL
merah
IV. PROSEDUR
1. Pengenalan golongan alkali dan alkali tanah
Reaksi dengan air
! Secarik kertas saring diapungkan diatas permukaan air dalam pinggan
penguapan. Lalu sepotong kecil logam Natrium dijepit dan diletakkan di atas
kertas itu. Harus diperhatikan bahwa logam Natrium tidak dipegang dengan
tangan dan tidak dekat dengan tempat reaksi. Setelah reaksi selesai, air di dalam
pinggan tersebut diperiksa dengan satu tetes fenolftalein dan dicatan
perubahannya yang terjadi.
! Sepotong logam Magnesium dibersihkan dengan amplas. Kemudian logam
Magnesium tersenut dimasukkan ke dalam air. Lalu ditunggu beebrapa menit
dan airnya diperiksa dengan fenolftalein. Lalu dicatat perubahan yang terjadi.
Reaksi nyala
! Kawat nikrom dibersihkan dengan cara mencelupkannya ke dalam larutan HCl
pekat, kemudia kawat nikrom tersebut dipanaskan dalam nyla api. Pekerjaan
tersebut diulangi sampai tampak warna lain dalam nyla (kawat yang bersih tidak
mengubah warna nyala). Kemudian kawat nikrom dicelupkan ke dalam larutan
NaCl pekat dan warnanya diperiksa dalam nyala. Dengan cara yang sama warna
nyala MgCl2, dan BaCl2, diperiksa.
Kelarutan senyawa logam alkali tanah
! Ke dalam tabung reaksi berturut-turut dimasukkan 1 mL larutan Ca(NO 3)2 0,1
M dan 1 mL larutan Ba(NO 3)2 0,1 M. ke dalam masing-masing tabung reaksi
tersebut ditetesi larutan (NH4)2C2O2 sampai terbentuk endapan. Jumlah tetes
endapan dicatat sampai terbentuk endapan.
! Seperti pada langkah di atas, dilakukan pekerjaan tetapi larutan
(NH4)2C2O2 dengan larutan K2CrO4 0,1 M
2. Pengenalan Halogen
Di tambahkan beberapa tetes larutan kanji ke dalam larutan iod, catat warna yang
terjadi.
V. PENGAMATAN
NO REAKSI PERLAKUAN HASIL PENGAMATAN
1 Reaksi dengan air. Logam Natrium Logam natrium memutar di
Reaksi antara Na diletakkan diatas kertas atas permukaan air dan
dengan air. saring yang disimpan menghasilkan asap. Lalu
diatas permukaan air. Natrium menimbulkan api
dan gas. Setelah di tetesi
metil merah, air berubah
warna menjadi warna
kuning.
2 Reaksi dengan air. Sepotong Magnesium Timbul gelembung
Reaksi antara dimasukkan ke dalam gelembung halus di
Magnesium dengan gelas kimia yang berisi potongan magnesium dan
air. air. pada air tidak terjadi
perubahan warna. Setelah di
tetesi metil merah, ternyata
terjadi perubahan warna
pada air menjadi
kekuningan.
3 Reaksi nyala. Sebuah kawat di Ketika kawat dimasukkan
Kawat nikrom bersihkan dahulu dengan kedalam NaCl pekat lalu
dimasukkan ke dalam cara mencelupkan ke kawat dipanaskan, terjadi
larutan NaCl pekat dalam larutan HCl lalu di perubahan warna pada nyala
lalu di bakar. panaskan. Setelah kawat api menjadi warna kuning.
dibersihkan, kawat
dimasukkan kedalam
larutan NaCl pekat lalu
kawat dipanaskan.
4 Reaksi nyala. Sebuah kawat di Ketika kawat dimasukkan
Kawat nikrom bersihkan dahulu dengan kedalam NaCl pekat lalu
dimasukkan ke dalam cara mencelupkan ke kawat dipanaskan, terjadi
larutan MgCl2 pekat dalam larutan HCl lalu di perubahan warna pada nyala
lalu di bakar. panaskan. Setelah kawat api menjadi warna putih.
dibersihkan, kawat
dimasukkan kedalam
larutan MgCl2 pekat lalu
kawat dipanaskan.
5 Reaksi nyala. Sebuah kawat di Ketika kawat dimasukkan
Kawat nikrom bersihkan dahulu dengan kedalam NaCl pekat lalu
dimasukkan ke dalam cara mencelupkan ke kawat dipanaskan, terjadi
larutan BaCl2 pekat dalam larutan HCl lalu di perubahan warna pada nyala
lalu di bakar. panaskan. Setelah kawat api menjadi warna hijau.
dibersihkan, kawat
dimasukkan kedalam
larutan BaCl2 pekat lalu
kawat dipanaskan.
6 Larutan Ba(NO3)2 Masukkan 1mL larutan Ketika Ba(NO3)2 ditambah
ditambah larutan Ba(NO3)2 ke dalam (NH4)2C2O4 menghasilkan
(NH4)2C2O4 tabung reaksi, lalu endapan putih yang terjadi
larutan tersebut ditetesi pada saat 10 kali penetesan
larutan (NH4)2C2O4. (NH4)2C2O4
7 Larutan CaCl2 Masukkan 1mL larutan Ketika CaCl2 ditambah
ditambah larutan CaCl2 ke dalam tabung (NH4)2C2O4 tidak
(NH4)2C2O4 reaksi, lalu larutan menghasilkan endapan,
tersebut ditetesi larutan namun warna larutan
(NH4)2C2O4. berwarna putih.
8 Larutan BaCl2 Masukkan 1mL larutan Ketika BaCl2 ditambah
ditambah larutan BaCl2 ke dalam tabung (NH4)2C2O4 menghasilkan
(NH4)2C2O4 reaksi, lalu larutan endapan putih kekuningan
tersebut ditetesi larutan setelah 10 kali penetesan
(NH4)2C2O4. (NH4)2C2O4.
9 Larutan Ba(NO3)2 Masukkan 1mL larutan Ketika Ba(NO3)2 ditambah
ditambah larutan Ba(NO3)2 ke dalam (NH4)2SO4 menghasilkan
(NH4)2SO4 tabung reaksi, lalu endapan putih setelah 8 kali
larutan tersebut ditetesi penetesan (NH4)2SO4.
larutan (NH4)2SO4.
10 Larutan BaCl2 Masukkan 1mL larutan Ketika BaCl2 ditambah
ditambah larutan BaCl2 ke dalam tabung (NH4)2SO4 tidak
(NH4)2SO4 reaksi, lalu larutan menghasilkan endapan
tersebut ditetesi larutan walaupun telah 20 kali
(NH4)2SO4. penetesan.
11 Larutan CaCl2 Masukkan 1mL larutan Ketika CaCl2 ditambah
ditambah larutan CaCl2 ke dalam tabung (NH4)2SO4 tidak
(NH4)2SO4 reaksi, lalu larutan menghasilkan endapan
tersebut ditetesi larutan walaupun telah 20 kali
(NH4)2SO4. penetesan.
12 Larutan Ba(NO3)2 Masukkan 1mL larutan Ketika Ba(NO3)2 ditambah
ditambah larutan Ba(NO3)2 ke dalam K2CrO4 menghasilkan
K2CrO4. tabung reaksi, lalu endapan berwarna kuning
larutan tersebut ditetesi setelah 10 kali penetesan
larutan K2CrO4. K2CrO4.
13 Larutan BaCl2 Masukkan 1mL larutan Ketika BaCl2 ditambah
ditambah larutan BaCl2 ke dalam tabung K2CrO4 menghasilkan
K2CrO4. reaksi, lalu larutan endapan berwarna kuning
tersebut ditetesi larutan setelah 8 kali penetesan.
K2CrO4.
14 Larutan CaCl2 Masukkan 1mL larutan Ketika CaCl2 ditambah
ditambah larutan CaCl2 ke dalam tabung K2CrO4 menghasilkan
K2CrO4. reaksi, lalu larutan endapan berwarna kuning
tersebut ditetesi larutan setelah 10 kali penetesan.
K2CrO4.
15 Reaksi pengenalan Yodium sebanyak 2 mL Larutan iod berubah warna
halogen. ditetesi larutan amilum. menjadi warna hitam atau
Iod ditambah larutan ungu tua setelah ditetesi
kanji. amilum sebanyak 5 tetes.
Persamaan reaksi yang mungkin terjadi:
! Natrium dengan Air
Na (s) + 2H2O (l) → 2NaOH (aq) + H2 (g)
! Magnesium dengan air
Mg (s) + 2H2O (l) → Mg(OH)2 (aq) + H2 (g)
! Reaksi nyala
NiCr (s) + 4NaCl (aq) + 2O2 (g) → NiCl (s) + CrCl2 (s) + 4NaO (aq)
NiCr (s) + 2MgCl2 (aq) + 2O2 (g) → NiCl (s) + CrCl2 (s) + 2MgO (aq)
NiCr (s) + 2BaCl2 (aq) + 2O2 (g) → NiCl (s) + CrCl2 (s) + 2BaO (aq)
! Kelarutan senyawa logam alkali tanah
Ba(NO3)2 (aq) + (NH4)2C2O4 (aq) → BaC2O4 (s) + 2NH4C2O4 (aq)
CaCl2 (aq) + (NH4)2C2O4 (aq) → 2NH4Cl (aq) + CaC2O4 (s)
BaCl2 (aq) + (NH4)2C2O4 (aq) → 2NH4Cl (aq) + BaC2O4 (s)
Ba(NO3)2 (aq) + (NH4)2SO4 (aq) → BaSO4 (s) + 2NH4NO3 (aq)
BaCl2 (aq) + (NH4)2SO4 (aq) → 2NH4Cl (aq) + BaSO4 (s)
CaCl2 (aq) + (NH4)2SO4 (aq) → 2NH4Cl (aq) + CaSO4 (s)
Ba(NO3)2 (aq) + K2CrO4 (aq) → BaCrO4 (s) + 2KNO3 (aq)
BaCl2 (aq) + K2CrO4 (aq) → 2KCl(aq) + BaCrO4 (s)
CaCl2 (aq) + K2CrO4 (aq) → 2KCl(aq) + CaCrO4 (s)
! Reaksi pengenalan halogen
I2 (aq) + amilum (aq) → senyawa kompleks berwarna hitam (aq)
Analisis data
! CaCl2 0,1 M 1mL
!"# .&'.( 0,1 .111.1
Gram = = = 0,011 gram CaCl 2
1000 1000
! Ba(NO3)2 0,1 M 1mL
!"# .&'.( 0,1 .261.1
Gram = = = 0,026 gram Ba(NO 3)2
1000 1000
! (NH4)2SO4 0,1M 2mL
!"# .&'.( 0,1 .126.2
Gram = = = 0,025 gram (NH 4)2SO4
1000 1000
! Ca(NO3)2 0,1M 1mL
!"# .&'.( 0,1 .164.1
Gram = = = 0,016 gram Ca(NO 3)2
1000 1000
! (NH4)2C2O4 0,1M 2mL
!"# .&'.( 0,1 .224.2
Gram = = = 0,044 gram (NH 4)2C2O4
1000 1000
! K2CrO4 0,1M 2,5mL
!"# .&'.( 0,1 .246.2,5
Gram = = = 0,061 gram K2CrO4
1000 1000
VI. PEMBAHASAN
Reaksi antara logam natrium dengan air menghasilkan basa dan gas hidrogen.
Untuk menguji kandungan basanya, maka larutan hasil reaksi ditetesi dengan metil
merah. Setelah ditetesi metil merah larutannya berubah menjadi warna kuning yang
menandakan bahwa larutan tersebut adalah larutan basa. Kereaktifan logam alkali
terhadap air sangat kuat. Dari reaksi itu, melibatkan pergantian hidrogen dari air oleh
logam Na untuk membentuk suatu basa kuat dan disertai dengan pelepasan gas
hidrogen. Pada reaksi antara logam Mg dengan air maka terbentuk gelembung-
gelembung kecil pada batang Mg. Reaksi ini menghasilkan basa karena pada saat
ditetesi metil merah, warna larutan berubah menjadi warna kekuningan. Gelembung-
gelembung yang dihasilkan dari reaksi Mg dengan air disebabkan oleh pelepasan gas
hidrogen. Magnesium agak lambat apabila bereaksi dengan air, hal itu disebabkan
jari-jari atom logam alkali tanah lebih kecil sehingga energi pengionan lebih besar.
Hal ini yang menyebabkan logam magnesium membentuk gelembung-gelembung
kecil dalam air.
Untuk reaksi antara logam Na dengan air, logam alkali (contoh disini Na) mempunyai
massa jenis lebih rendah dari air. Akibatnya, logam tersebut mengapung di atas
permukaan air. Logam alkali sangat reaktif terhadap air dan reaksinya bersifat
eksplosif disertai nyala, itulah sebabnya pada percobaan yang dilakukan, natriu
bergerak memutar dan menghasilkan api serta asap.
Pada percobaan reaksi nyala, digunakan senyawa yang mengandung unsur
alkali dan alkali tanah yaitu NaCl, MgCl 2, dan BaCl 2. Pada saat kawat nikrom (NaCr)
dimasukkan kedalam NaCl lalu dibakar, nyala ali yang dihasilkan menjadi warna
kuning. Hal ini sesuai berdasarkan teori bahwa logam Na berwarna kuning. Ketika
kawat Nikrom (NaCr) dimasukkan ke dalam MgCl 2 lalu dibakar, nyala api yang
dihasilkan berwarna putih. Hal ini sesuai berdasarkan teori bahwa logam Mg
berwarna putih. Ketika kawat nikom dimasukkan kedalam larutan BaCl 2 lalu dibakar,
nyala api yang dihasilkan menjadi warna hijau. Hal ini sesuai berdasarkan teori bahwa
logam Ba berwarna hijau.
Suatu unsur ketika di lakukan uji nyala bisa menghasilkan warna tertentu, hal ini
disebabkan karena apabila suatu senyawa dipanaskan akan terurai menghasilkan
unsur unsur penyusunnya dalam wujud gas atau uap. Warna nyala yang dihasilkan
dari pergerakan elektron-elektron dalam ion-ion logam yang terdapat dalam senyawa.
Masing-masing perpindahan elektron ini, melibatkan sejumlah senyawa energi
tertentu yang dilepaskan sebagai energi cahaya, dan masing masing memiliki warna
tertentu.
Pada percobaan kelarutan senyawa logam alkali tanah, ketika Ba(NO 3)2
ditambahkan dengan (NH4)2C2O4 menghasilkan endapan putih, karena dikromat sukar
larut dengan Ba2+. Ketika CaCl2 ditambahkan (NH4)2C2O4 seharusnya menghasilkan
endapan, tetapi mungkin terdapat kesalahan penglihatan oleh praktikan sehingga
dalam percobaan tidak menghasilkan endapan.
Senyawa Ba2+ dan Ca2+ akan menghasilkan endapan ketika bereaksi dengan SO 42-.
Ketika BaCl2 dan CaCl2 direaksikan dengan (NH4)2 SO4 seharusnya menghasilkan
endapan, namun pada percobaan tidak menghasilkan endapan. Hal tersebut bisa
terjadi mungkin karena praktikan melakukan kesalahan dalam penglihatan.
Senyawa Ba2+ dan Ca2+ akan menghasilkan endapan berwarna kuning jika direaksikan
dengan CrO4-, karena senyawa kromat adalah senyawa yang sukar larut, kecuali
dengan logam alkali dan amonia.
Pada percobaan larutan Iod ditetesi larutan kanji terjadi perubahan warna
larutan dari coklat menjadi ungu tua. Warna ungu tersebut berasal dari amilum.
Larutan Iod adalah unsur halogen, karena cara kerja dari larutan kanji/amilum adalah
apabila suatu larutan ditetesi larutan kanji/amilum, warna larutan berubah menjadi
ungu tua maka larutan tersebut adalah unsur halogen.
VII. KESIMPULAN
1. Pengenalan unsur halogen dan ion halida dapan dipelajari dengan menggunakan
larutan amilum. Apabila suatu larutan ditetesi suatu larutan amilum, warna
berubah menjadi biru tua, maka larutan tersebut mengandung unsur halogen.
Contohnya adalah pada pengujan iod. Larutan iod berwarna cokelat akan berubah
menjadi warna biru/ungu tua apabila ditetesi larutan kanji.
2. Kekuatan oksidasi relatif unsur-unsur halogen memiiki enam tingkat oksidasi,
kecuali Flourin yang hanya memiliki dua macam tingkat oksidasi 0 dan -1. Selain
unsur Flourin , memiliki tingkat oksidasi +1, +3, +5, dan +7.
3. Keperiodikan sifat-sifat logam-logam alkali dan alkali tanah dapat diuji dengan
reaksi nyala yang akan menimbulkan warna khas dari unsur-unsur tersebut.
Seperti Na berearna orange, Mg berwarna putih/transparan, dan Ba berwarna
kuning kehijauan. Selain dengan uji nyala, dapat juga dengan uji kelarutan
senyawa logam alkali dan alkali tanah yang digunakan untuk mjengetahui seberpa
besar tingkat kelarutan dari logam alkali dan alkali tanah. pad unsur-unsur ini,
jari-jari atom logam deari atas ke bawah semakin besar sedangkan energi ionisasi
dan keelektronegatifannya semakin kecil dari atas ke bawah.
VIII. DAFTAR PUSTAKA
! Chang, Raymond. 2005. Konsep-konsep inti. Jakarta: Erlangga.
! Chang, Raymond. 2005. Kimia Dasar. Jakarta: Erlangga.
! Fitria. 2011. Golongan alkali tanah.
http://fitria-nff.blogspot.co.id/2011/08/golongan-alkali-tanah.html diakses
tanggal 30 Oktober 2015. Pukul 18.00 WIB.
! Keenan, Charles w. Donald C keteinfeltes dan Jesse H Wood. 1996. Ilmu kimia
untuk universitas. Jakarta: Erlangga.
! Wardhani, Sri. 2009. Unsur-unsur golongan 1A.
http://ww.chem-is-try.co.id diakses tanggal 30 Oktober 2015. Pukul 20.00 WIB.
Share this document
" # $ % &
You might also like
PERCOBAAN VIII REAKSI
KESETIMBANGAN
Astrid Alasa
REAKSI REDOKS
mu2gammabunta
makalah pengantar
kebudayaan.docx
Misran Muhsin
Magazines Podcasts
Sheet Music
PERCOBAAN I Unsur Alkali
Tanah.pdf
Meitri Wulandari Kohar
Soal Farmasi X
Haris Supriatna
Laporan Kimia Anorganik I
Pembuatan Kalsium Sulfat Dari
Batu Gamping
ernanda
Tugas 2 - Minyak Atsiri
Handy Dinar Astiansyah
Makalah Laboratorium
Mikrobiologi
Anidia Rasmi
Tugas Pendahuluan l1 Hukum
KirchoR
Like This
Iman Islam Ihsan, Islam dan
Sains, Islam dan Penegakan
Hukum, Amar Ma'ruf dan Na…
Cynthia
Mungkar,Claudia Tamara
Fitnah Akhir Zaman.
40+ Contoh Soal Latihan UN
Matematika SD + Kunci
Jawaban
Ps Diraja
Kata Pengantar
rizky
Show more
About Support
About Scribd Help / FAQ
Press Accessibility
Our blog Purchase help
Join our team! AdChoices
Contact us Publishers
Invite friends
Social
GiKs
Scribd for enterprise Instagram
Twitter
Legal
Facebook
Terms Pinterest
Privacy
Copyright
Cookie Preferences
Get our free apps
Books • Audiobooks • Magazines • Podcasts •
Sheet Music • Documents • Snapshots • Directory
Language: English
Copyright © 2021 Scribd Inc.
What is Scribd? +
Millions of titles at your fingertips
Home Only Rp70,000/month.
Books Cancel anytime. Documents
Audiobooks
Anda mungkin juga menyukai
- LAPORAN Kimia 2 FixDokumen23 halamanLAPORAN Kimia 2 FixLeny SuryaniBelum ada peringkat
- Laporan Sistem Periodik UnsurDokumen10 halamanLaporan Sistem Periodik UnsurNovi HardiyantiBelum ada peringkat
- Laporan Praktikum Kimia DasarDokumen17 halamanLaporan Praktikum Kimia DasarHelmi Fauzi100% (1)
- Makalah Tentang Unsur Kimia Gol 1a, 2a Dan 3aDokumen18 halamanMakalah Tentang Unsur Kimia Gol 1a, 2a Dan 3aAmarasinthia PutriBelum ada peringkat
- Sistem Periodik UnsurDokumen40 halamanSistem Periodik UnsurFajrian FaridhoBelum ada peringkat
- Sifat Sifat Unsur ADokumen19 halamanSifat Sifat Unsur ARavenBelum ada peringkat
- Tugas 2 Kimia Dasar Dosen Pengampu: Dr. Rugaiyah Andi Arfah, M.SiDokumen8 halamanTugas 2 Kimia Dasar Dosen Pengampu: Dr. Rugaiyah Andi Arfah, M.SiAndi Erisya Magfirah AsnawiBelum ada peringkat
- MAKALAH Kimia DasarDokumen35 halamanMAKALAH Kimia DasarNurul Adinda0% (1)
- Sistem Periodik UnsurDokumen18 halamanSistem Periodik UnsurBudi Bahtiar Bin NananBelum ada peringkat
- GAJAHDokumen12 halamanGAJAHJoan destalino destalinoBelum ada peringkat
- Sistem Periodik UnsurDokumen18 halamanSistem Periodik UnsurBudi Bahtiar Bin NananBelum ada peringkat
- PPTsistem Periodik Unsur-IinDokumen18 halamanPPTsistem Periodik Unsur-IinMichel IskandarBelum ada peringkat
- KIMIADokumen18 halamanKIMIANur AnnisahBelum ada peringkat
- Laporan Lengkap Kimia Unsur Ass 2Dokumen16 halamanLaporan Lengkap Kimia Unsur Ass 2WAHYU YAHYA SAPUTRABelum ada peringkat
- Sistem Periodik UnsurDokumen14 halamanSistem Periodik UnsurWahyudiBaenlahBelum ada peringkat
- Pertemuan 1 (Tabel Periodik) - 1Dokumen23 halamanPertemuan 1 (Tabel Periodik) - 1jay yeolBelum ada peringkat
- Kimia Unsur 1Dokumen8 halamanKimia Unsur 1LirofiatillahBelum ada peringkat
- Unsur UtamaDokumen54 halamanUnsur UtamasittimurliaBelum ada peringkat
- Bab 3 Sistem Periodik UnsurDokumen17 halamanBab 3 Sistem Periodik UnsurhindarnantoBelum ada peringkat
- Sifat Keperiodikan Unsur (KIMIA)Dokumen23 halamanSifat Keperiodikan Unsur (KIMIA)MFurqanulIkramBelum ada peringkat
- Sistem Periodik UnsurDokumen18 halamanSistem Periodik UnsurBenazir Amalia FirduausyBelum ada peringkat
- Modul Materi LCCDokumen39 halamanModul Materi LCCalmasriwulandariBelum ada peringkat
- Bab 3Dokumen17 halamanBab 3zaskyalatifahBelum ada peringkat
- Bab II Sifat-Sifat UnsurDokumen22 halamanBab II Sifat-Sifat UnsurLm PradinotoBelum ada peringkat
- Rangkuman Kimia - Raihan Rafi Rizqullah - 270110190032 - Kelas BDokumen5 halamanRangkuman Kimia - Raihan Rafi Rizqullah - 270110190032 - Kelas BRaihan RafiBelum ada peringkat
- Sifat Periodik UnsurDokumen40 halamanSifat Periodik Unsuremiliolukman34Belum ada peringkat
- Sifat Fisik Dan KimiaDokumen11 halamanSifat Fisik Dan KimiaNur MutmainnahBelum ada peringkat
- Sistem Periodik UnsurDokumen16 halamanSistem Periodik UnsursaidahBelum ada peringkat
- (Fiix) Makalah Ikatan Kimia Dan Tabel PeriodikDokumen21 halaman(Fiix) Makalah Ikatan Kimia Dan Tabel PeriodikSyahreza MuslihBelum ada peringkat
- Tabel PeriodikDokumen23 halamanTabel Periodikcutepika7Belum ada peringkat
- 2-Kereaktifan Logam AlkaliDokumen8 halaman2-Kereaktifan Logam AlkaliMirrah AfinaBelum ada peringkat
- Kelompok 3 Soal Alkali 4.1 - 4.5Dokumen9 halamanKelompok 3 Soal Alkali 4.1 - 4.5Khaeriani100% (1)
- Desain Proyek.11Dokumen8 halamanDesain Proyek.11Humaira PutriBelum ada peringkat
- Ppt. Logam Alkali Golongan 1 ADokumen79 halamanPpt. Logam Alkali Golongan 1 AAnanda Dian Yustikarini100% (2)
- Bab 3Dokumen21 halamanBab 3Niha NurmalaBelum ada peringkat
- Sistem Periodik UnsurDokumen11 halamanSistem Periodik UnsurCHakun 1999Belum ada peringkat
- AlkaliDokumen16 halamanAlkaliMahendra PuguhBelum ada peringkat
- Laporan Praktikum Kimia - SpuDokumen11 halamanLaporan Praktikum Kimia - SpuAfrina Dearny DamanikBelum ada peringkat
- Kimia Unsur 1Dokumen28 halamanKimia Unsur 1Risang Bagasworo100% (1)
- Percobaan Sifat-Sifat UnsurDokumen11 halamanPercobaan Sifat-Sifat UnsurImma HayasukiBelum ada peringkat
- Sifat Sifat Unsur Nabila 11Dokumen16 halamanSifat Sifat Unsur Nabila 11Nabila AngreaniBelum ada peringkat
- Praktikum 10 - Sistem Periodik UnsurDokumen8 halamanPraktikum 10 - Sistem Periodik UnsurFaraah BadarBelum ada peringkat
- Tugas KimiaDokumen18 halamanTugas Kimia「RL」 RoseBelum ada peringkat
- Sistem PeriodikDokumen29 halamanSistem PeriodikMuh AnugrahBelum ada peringkat
- GAJAHDokumen19 halamanGAJAHJoan destalino destalinoBelum ada peringkat
- Periodisitas KimiaDokumen44 halamanPeriodisitas KimiaAinun JariyahBelum ada peringkat
- Popi Anggriani - 21.71.024341 - Laporan Ke 6 Praktikum Identifikasi Reaksi KimiaDokumen20 halamanPopi Anggriani - 21.71.024341 - Laporan Ke 6 Praktikum Identifikasi Reaksi KimiaJoan destalino destalinoBelum ada peringkat
- Konfigurasi Elektron Dan Elektron ValensiDokumen32 halamanKonfigurasi Elektron Dan Elektron ValensiFeri ArifinBelum ada peringkat
- Laporan SPUDokumen10 halamanLaporan SPUrizkyBelum ada peringkat
- Sistem PeriodikDokumen4 halamanSistem PeriodikDiyah AnjayyBelum ada peringkat
- Tipus Sifat Unsur-1Dokumen6 halamanTipus Sifat Unsur-1RhmaBelum ada peringkat
- Sifat Periodik UnsurDokumen14 halamanSifat Periodik Unsurmichealalvaro37Belum ada peringkat
- Sejarah Perkembangan Tabel Periodik Unsur Dan Sifat-Sifat Yang Ada Pada Tabel Periodik UnsurDokumen6 halamanSejarah Perkembangan Tabel Periodik Unsur Dan Sifat-Sifat Yang Ada Pada Tabel Periodik UnsurNuril idha0% (1)
- Makalah Unsur Dan SenyawaDokumen16 halamanMakalah Unsur Dan SenyawaDarmawan Setiadi100% (1)
- Kelimpahan UnsurDokumen14 halamanKelimpahan UnsurUlya Lutfa ZulfianaBelum ada peringkat
- Sistem Periodik UnsurDokumen27 halamanSistem Periodik Unsuralfaadvertising68100% (1)
- Kimia AnorDokumen2 halamanKimia AnorYANTIBelum ada peringkat
- Sifat-Sifat UnsurDokumen34 halamanSifat-Sifat UnsurMasitahBelum ada peringkat
- Definisi Alkali TanahDokumen13 halamanDefinisi Alkali TanahscribddewiBelum ada peringkat