Buffer Tambahan
Diunggah oleh
Vic Tantri0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
7 tayangan7 halamanHak Cipta
© © All Rights Reserved
Format Tersedia
PPT, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PPT, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
7 tayangan7 halamanBuffer Tambahan
Diunggah oleh
Vic TantriHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PPT, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 7
Funtianak, 21 Desember 2012
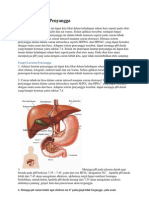
Peranan Larutan Penyangga
Dalam Tubuh Makhluk Hidup
Kebanyakan reaksi-reaksi biokimia dalam tubuh makhluk
hidup hanya dapat berlangsung pada pH tertentu. Oleh
karena itu, cairan tubuh harus merupakan larutan
penyangga agar pH senantiasa konstan ketika metabolisme
berlangsung. Dalam keadaan normal, pH dari cairan tubuh
termasuk darah kita adalah 7,35 – 7,5. Walaupun sejumlah
besar ion H+ selalu ada sebagai hasil metabolisme dari zat-
zat, tetapi keadaan setimbang harus selalu dipertahankan
dengan jalan membuang kelebihan asam tersebut. Hal ini
disebabkan karena penurunan pH sedikit saja menunjukkan
keadaan sakit.
Larutan penyangga sangat berperan dalam kehidupan sehari-
hari. Beberapa fungsi larutan penyangga dalam kehidupan
dapat kalian pelajari pada uraian di bawah ini.
pH darah tubuh manusia berkisar antara 7,35-7,45. pH
darah tidak boleh kurang dari 7,0 dan tidak boleh melebihi
7,8 karena akan berakibat fatal bagi manusia. Organ yang
paling berperan untuk menjaga pH darah adalah paru-paru
dan ginjal. Kondisi di mana pH darah kurang dari 7,35
disebut asidosis. Faktor-faktor yang mempengaruhi
terjadinya kondisi asidosis antara lain penyakit jantung,
penyakit ginjal, kencing manis, dan diare yang terus-
menerus. Sedangkan kondisi di mana pH darah lebih dari
7,45 disebut alkolosis. Kondisi ini disebabkan muntah yang
hebat, hiperventilasi (kondisi ketika bernafas terlalu cepat
karena cemas atau histeris pada ketinggian). Untuk
menjaga pH darah agar stabil, di dalam darah terdapat
beberapa larutan penyangga alami, yaitu:
Penyangga hemoglobin
Oksigen merupakan zat utama yang diperlukan oleh sel tubuh yang
didapatkan melalui pernapasan. Oksigen diikat oleh hemoglobin di
dalam darah, di mana O2 sangat sensitif terhadap
pH. Reaksi kesetimbangan yang terjadi dapat dituliskan sebagai berikut.
HHb+ + O2
⇄ H+ + HbO2
Produk buangan dari tubuh adalah CO2-
yang di dalam
tubuh bisa membentuk senyawa H 2CO3 yang nantinya akan
terurai menjadi H+ dan HCO3-. Penambahan H+ dalam tubuh
akan mempengaruhi pH, tetapi hemoglobin yang telah
melepaskan O2 dapat mengikat H+ membentuk asam
hemoglobin(HHb+).
Penyangga karbonat
Penyangga karbonat juga berperan dalam
mengontrol pH darah. Reaksi kesetimbangannya
adalah:
H+(aq) + HCO3-(aq)
⇄ H2CO3(aq)
⇄ H2O(aq) + CO2(aq)
Perbandingan molaritas HCO3- terhadap H2CO3
yang diperlukan untuk mempertahankan pH
darah 7,4 adalah 20:1. Jumlah HCO3
-
yang relatif jauh lebih banyak itu dapat
dimengerti karena hasil-hasil metabolisme yang
diterima darah lebih banyak bersifat asam.
Penyangga fosfat
Penyangga fosfat merupakan penyangga yang berada di
dalam sel. Penyangga ini adalah campuran dari asam lemah
H2PO4- dan basa konjugasinya, yaitu HPO42-. Jika dari proses
metabolisme sel dihasilkan banyak zat yang bersifat asam,
maka akan segera bereaksi dengan ion HPO 42-
HPO42-(aq) + H+(aq) ⇄ H2PO4-(aq)
Dan jika proses metabolism sel menghasilkan senyawa yang
bersifat basa, maka ion OH- akan bereaksi dengan H2PO4-.
H2PO4-(aq) + OH-(aq) ⇄ HPO42-(aq) + H2O(l)
Sehingga perbandingan [H2PO4- ] / [HPO42-] selalu tetap dan
akibatnya pH larutan tetap.Penyangga ini juga ada di luar
sel, tetapi jumlahnya sedikit. Selain itu, penyangga fosfat
juga berperan sebagai penyangga urin.
Apabila mekanisme pengaturan pH dalam tubuh gagal, seperti dapat
terjadi selama sakit, sehingga pH darah turun di bawah 7,0 atau naik ke
atas 7,8, dapat menyebabkan kerusakan permanen pada organ tubuh
atau bahkan kematian.
Faktor-faktor yang dapat menyebabkan keadaanasidosis (penurunan
pH) adalah penyakit jantung, penyakit ginjal, diabetes mellitus (penyakit
gula), diare yang terus menerus, atau makanan berkadar protein tinggi
dalam jangka waktu lama. Keadaan asidosis sementara dapat terjadi
karena olahraga intensif yang dilakukan terlalu lama.
Alkalosis (peningkatan pH darah) dapat terjadi sebagai akibat muntah
yang hebat, hiperventilasi (bernapas terlalu berlebihan, kadang-kadang
karena cemas atau histeris atau berada di ketinggian). Suatu penelitian
yang dilakukan terhadap para pendaki gunung yang mencapai puncak
Everest (8.848 m) tanpa oksigen tambahan menunjukkan pH darah
mereka berada di antara 7,7–7,8. Hiperventilasi diperlukan untuk
mengatasi tekanan oksigen yang amat rendah (kira-kira 43 mmHg) di
tempat setinggi itu.
Anda mungkin juga menyukai
- Makalah Keseimbangan Asam BasaDokumen45 halamanMakalah Keseimbangan Asam BasaNhoPhie Destian Viana100% (2)
- ASAM BASADokumen8 halamanASAM BASALinda AriasihBelum ada peringkat
- LARUTAN BUFFERDokumen14 halamanLARUTAN BUFFERRizki AdistaBelum ada peringkat
- Hubungan Hco3 Dengan PH DarahDokumen20 halamanHubungan Hco3 Dengan PH DarahDinda Nur AidaBelum ada peringkat
- Makalah Sistem Buffer TubuhDokumen9 halamanMakalah Sistem Buffer TubuhMaulyda Nurul FaizahBelum ada peringkat
- Sistem Buffer Pada Tubuh ManusiaDokumen3 halamanSistem Buffer Pada Tubuh ManusiaAgil CrBelum ada peringkat
- Larutan Penyangga Dalam Tubuh ManusiaDokumen4 halamanLarutan Penyangga Dalam Tubuh ManusiaMirna HariatiBelum ada peringkat
- Fungsi Larutan PenyanggaDokumen4 halamanFungsi Larutan Penyanggarafi_17Belum ada peringkat
- KimiaDokumen2 halamanKimiaPaskal StevanezBelum ada peringkat
- Fungsi Larutan Buffer Pada Tubuh ManusiaDokumen2 halamanFungsi Larutan Buffer Pada Tubuh ManusiaNidaIdzniBelum ada peringkat
- Paper Metabolik AlkalosisDokumen11 halamanPaper Metabolik AlkalosisAnonymous YwnFebtBelum ada peringkat
- Larutan PenyanggaDokumen3 halamanLarutan Penyanggadevilbath15Belum ada peringkat
- pH Darah ManusiaDokumen10 halamanpH Darah ManusiaRizky Fachrian RidloBelum ada peringkat
- Tugas Perbaikan PKMBDokumen23 halamanTugas Perbaikan PKMBgusti ayuBelum ada peringkat
- KimiaDokumen2 halamanKimiaRanti RahmawatiBelum ada peringkat
- Artikel PH Darah Dan Jaringan TubuhDokumen4 halamanArtikel PH Darah Dan Jaringan TubuhAdeTiyasWidyawatiBelum ada peringkat
- pH REGULASIDokumen5 halamanpH REGULASIDani IbrahimBelum ada peringkat
- Makalah Asam BasaDokumen27 halamanMakalah Asam Basanzi_eX6943100% (2)
- Fungsi Larutan PenyanggaDokumen4 halamanFungsi Larutan PenyanggaNur Desi YaniBelum ada peringkat
- Latar Belakang AlkalosisDokumen2 halamanLatar Belakang AlkalosisVreeq VreechaBelum ada peringkat
- Interpretasi Asam Basa IgdDokumen11 halamanInterpretasi Asam Basa Igdarik iskandarBelum ada peringkat
- Fungsi Larutan Penyangga Dalam Kehidupan SehariDokumen8 halamanFungsi Larutan Penyangga Dalam Kehidupan SehariDusfirah MajidBelum ada peringkat
- Larutan Penyangga dalam Kehidupan Sehari-hariDokumen6 halamanLarutan Penyangga dalam Kehidupan Sehari-hariSevriadyBelum ada peringkat
- Fungsi Larutan PenyanggaDokumen2 halamanFungsi Larutan PenyanggacindyokhotanBelum ada peringkat
- Peranan Larutan Penyangga Dalam Tubuh Mahluk HidupDokumen1 halamanPeranan Larutan Penyangga Dalam Tubuh Mahluk HidupNada AlfiBelum ada peringkat
- pH DarahDokumen25 halamanpH DarahIntan RensiskaBelum ada peringkat
- RPP Larutan PenyanggaDokumen9 halamanRPP Larutan PenyanggaBurhan CfBelum ada peringkat
- Keseimbangan Asam Basa Dalam Tubuh Dan BiolistrikDokumen32 halamanKeseimbangan Asam Basa Dalam Tubuh Dan Biolistrikputrianisepti154Belum ada peringkat
- Asam Basa TubuhDokumen15 halamanAsam Basa TubuhRizka VeliaBelum ada peringkat
- Keseimbangan Asam Basa (Referat)Dokumen13 halamanKeseimbangan Asam Basa (Referat)Virza Chairunnisa LatuconsinaBelum ada peringkat
- Fungsi Larutan PenyanggaDokumen3 halamanFungsi Larutan PenyanggaleajulianaBelum ada peringkat
- BIOKIMIADokumen60 halamanBIOKIMIAYuna Pratiwi100% (2)
- Aplikasi Larutan PenyanggaDokumen6 halamanAplikasi Larutan PenyanggaMariati AbdullahBelum ada peringkat
- Aplikasi Larutan Buffer PDFDokumen6 halamanAplikasi Larutan Buffer PDFYuliaDelestiBelum ada peringkat
- Respirasi dan Keseimbangan Asam BasaDokumen11 halamanRespirasi dan Keseimbangan Asam BasaWidia PangestikaBelum ada peringkat
- Haidar Makalah Larutan PenyanggaDokumen8 halamanHaidar Makalah Larutan Penyanggadewi netBelum ada peringkat
- KimiabufferDokumen5 halamanKimiabufferDewita Fajar RianiBelum ada peringkat
- HiperkalemiaDokumen74 halamanHiperkalemiaYudiatmaBelum ada peringkat
- Tugas Kelompok Dasar2 KMBDokumen10 halamanTugas Kelompok Dasar2 KMBMaulida nurlizaBelum ada peringkat
- Keseimbangan Asam Basa PPT NewDokumen23 halamanKeseimbangan Asam Basa PPT NewMaya Putri HaryantiBelum ada peringkat
- Kesemibangan Asam BasaDokumen38 halamanKesemibangan Asam BasaAhmad Dailah SudrajatBelum ada peringkat
- Wrap Up DiareDokumen26 halamanWrap Up Diarenorasaputri100% (1)
- Keseimbangan Asam Basa PPT NewDokumen23 halamanKeseimbangan Asam Basa PPT NewZayed NorwantoBelum ada peringkat
- Asam BasaDokumen24 halamanAsam BasaApriyani laila MaddatuBelum ada peringkat
- AGDDokumen10 halamanAGDAisyah ArrosyadaBelum ada peringkat
- Laporan Pendahuluan Ketidak Seimbangan Asam BasaDokumen24 halamanLaporan Pendahuluan Ketidak Seimbangan Asam BasaAbdul LatiifBelum ada peringkat
- Konsentrasi H+ Dan PH Cairan Tubuh Normal Serta Perubahan Yang Terjadi Pada Asidosis Dan AlkalosisDokumen2 halamanKonsentrasi H+ Dan PH Cairan Tubuh Normal Serta Perubahan Yang Terjadi Pada Asidosis Dan AlkalosisMasDhedotBelum ada peringkat
- Fungsi Larutan Penyangga Dalam Tubuh Makhluk HidupDokumen4 halamanFungsi Larutan Penyangga Dalam Tubuh Makhluk HidupAlvinFloppeeBelum ada peringkat
- UNTUK ARTIKEL KIMIA LARUTAN PENYANGGADokumen5 halamanUNTUK ARTIKEL KIMIA LARUTAN PENYANGGAAndinifth100% (2)
- Ilmu Dasar Keperawatan Khasbi HusainDokumen25 halamanIlmu Dasar Keperawatan Khasbi HusainHusain BankBelum ada peringkat
- Makalah Asam Basa Dan EKGDokumen27 halamanMakalah Asam Basa Dan EKGYuliana BawenduBelum ada peringkat
- Materi Uts BesokDokumen37 halamanMateri Uts BesokLiendah AruMiBelum ada peringkat
- Anatomi Fisologi Asam BasaDokumen29 halamanAnatomi Fisologi Asam BasaPriscilla AnandaBelum ada peringkat
- Apa Sih Buffer Dan ManfaatnyaDokumen2 halamanApa Sih Buffer Dan ManfaatnyaElinira SubandiBelum ada peringkat
- Point 8 Dan 9Dokumen2 halamanPoint 8 Dan 9Deski juliandaBelum ada peringkat
- Kunci Jawaban LKPD Pertemuan 2Dokumen2 halamanKunci Jawaban LKPD Pertemuan 2Asnita dahibaBelum ada peringkat
- Keseimbangan Asam BasaDokumen26 halamanKeseimbangan Asam BasaVrimaBelum ada peringkat
- TUGAS FISIOLOGI Asam Basa ElektrolitDokumen13 halamanTUGAS FISIOLOGI Asam Basa Elektrolit02 APH Komang AnggariniBelum ada peringkat
- Bab 10Dokumen63 halamanBab 10ST. Fatimah KadirBelum ada peringkat
- BufferDokumen16 halamanBufferVic TantriBelum ada peringkat
- Seleksi Essay FixDokumen4 halamanSeleksi Essay FixVic TantriBelum ada peringkat
- Seleksi Essay FixDokumen4 halamanSeleksi Essay FixVic TantriBelum ada peringkat
- Debat Kefarmasian FixDokumen4 halamanDebat Kefarmasian FixVic TantriBelum ada peringkat
- Pce FixDokumen4 halamanPce FixVic TantriBelum ada peringkat