Laporan Resmi Perc 1 Rifqi
Diunggah oleh
RifQi Mizan Aulawi67%(3)67% menganggap dokumen ini bermanfaat (3 suara)
4K tayangan14 halamanHak Cipta
© Attribution Non-Commercial (BY-NC)
Format Tersedia
DOCX, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Attribution Non-Commercial (BY-NC)
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
67%(3)67% menganggap dokumen ini bermanfaat (3 suara)
4K tayangan14 halamanLaporan Resmi Perc 1 Rifqi
Diunggah oleh
RifQi Mizan AulawiHak Cipta:
Attribution Non-Commercial (BY-NC)
Format Tersedia
Unduh sebagai DOCX, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 14
PERCOBAAN I
PENENTUAN RUMUS MOLEKUL SENYAWA KOMPLEKS
I. TUJUAN
Mempelajari pembuatan dan penentuan molekul senyawa kompleks besi (II) Oksalat
II. PENDAHULUAN
Alhamdulillah Puji Syukur kehadiran Allah SWT. Karena Sang Khaliq lah
percobaan kali ini bisa dilakukan. Dengan kekuatan yang telah Allah SWT. Berikan dan
ilmu yang telah Allah ridhoi maka banyak penemuan-penemuan yang muncul di Alam
Semesta ini.
-EE}4O -4:4N ;}g)` .4^g14:gN
+OE4uO>-47 LOE;O4O ;}g)` 4^gLgN
+OE4u^U44 }g` ^^-. VUgN ^g)
65. Lalu mereka bertemu dengan seorang hamba di antara hamba-hamba Kami,
yang telah Kami berikan kepadanya rahmat dari sisi Kami, dan yang telah Kami ajarkan
kepadanya ilmu dari sisi Kami[886].
Salah satunya yaitu Ilmu Kimia. Dengan banyak penemuan maka banyak pula
permasalahan yang timbul. Maka dari itu Perlu adanya pembuktian mengenai
penemuan-penemuan tersebut. Dengan demikian Pembuktian yang akan dilakukan
pada perconaan ini adalah mengenai Penentuan Rumus Molekul Senyawa Kompleks.
Reaksi antara dua molekul stabil atau lebih dapat menghasilkan produk reaksi
yang stabil dengan sifat karakteristik . Sebagai contoh komplek amina akan terbentuk
jika amina direaksikan dengan kobalt (II) klorida. Hakekat struktur senyawa kordinasi
adalah transfer elaktron yang terjadi antara ligan dan molekul atau ion logam. Dalam
bentuk paling sederhana, ikatan koordinasi terbentuk oleh transfer pasangan elektron
dari ligan atau molekul ke ion logam.
Molekul netral atau ion-ion yang bertindak sebagai ligan harus memiliki
pasangan elektron sunyi. Senyawa koordinasi paIing sederhana akan terbentuk dengan
ikatan sigma antara antara suatu ligan dengan molekul atau ion logam. Beberapa
senyawa komplek dikenal dimana ikatan sigma dan ikatan phi dari orbital 2p pada
oksigen memberi konstribusi pada seluruh ikatan. Dalam ligan yang lain seperti karbon
monoksida dan nitroksida, konstribusi dari ikatan phi berperan dalam seluruh ikatan.
Maka dari itu percobaan ini dilakukan.
III. DASAR TEORI
Senyawa kompleks dapat merupakan senyawa kompleks netral atau senyawa
kompleks ionik. Senyawa kompleks ionik terdiri atas ion positif (kation) dan ion negative
(anion), dimana salah satu atau kedua ion tersebut dapat merupakan ion kompleks. Dalam
pembentukan senyawa kompleks, atom logam atau ion logam disebut sebagai atom pusat,,
sedangkan atom yang dapat mendonorkan elektronnya ke atom logam atau ion logam
disebut atom donor. Ion dan molekul netral memiliki atom-atom donor yang disebut
dengan ligan. Atom pusat senyawa kompleks dapat merupakan unsur-unsur transisi atau
unsur-unsur logam utama. Atom pusat suatu senyawa kompleks dapat memiliki bilangan
oksidasi yang harganya positif, nol atau negatif. (Effendy, 2007).
Secara umum senyawa pembentukannya melibatkan pembentukan ikatan kovalen
koordinasi yang dapat pula dianggap sebagai senyawa koordinasi. Dalam konteks yang
lebih khusus, senyawa koordinasi adalah senyawa yang pembentukannya melibatkan
pembentukan ikatan kovalen koordinasi antar ion logam atau atom logam dengan atom
nonlogam. Pada awal perkembangannya, senyawa koordinasi disebut dengan senyawa
kompleks karena pembentukannya sulit untuk dijelaskandengan konsep valensi atau teori
ikatan kimia yang ada. Istilah senyawa koordinasi setelah Wemer menjelaskan bahwa ligan-
ligan terkoordinasi pada atom pusat terletak pada posisi tertentu. Fakta-fakta eksperimen
baru menunjukan banyak senyawa kompleks yang sangat sulit dijelaskan pembentukannya
denag teori yang ada, sehingga dimasa kini tampak istilah senyawa kompleks atau
kompleks cenderung lebih banyak dipakai dibandingkan senyawa koordinasi.(Vogel,1990).
Bilangan koordinasi menyatakan jumlah ruang yang tersedia sekitar atom atau ion
pusat biasa disebut dengan bulatan koordinasi yang masing-masing dapat dihuni satu ligan
(monodentat). Susunan logam-logam sekitar ion pusat adalah simetris. Menurut Lewis teori
tentang ikatan-ikatan kimia didasarkan atas pembentukan pasangan elektron, menerangka
pembentukan kompleks terjadi karena penyumbangan suatu pasangan elektron seluruhnya
oleh atom ligan kepada atom pusat. Ikatan datif kadang dinyatakan dengan sebuah anak
panah yang menunjukan arah penyumbangan elektron. Teori medan ligan menjelaskan
pembentukan kompleks atas dasar medan elektrostastik yangn diciptakan oleh lilgan-ligan
yang terkoordinasi sekeliling bulatan sebelah dalam dari atom pusat. Medan ligan
menyebabkan penguraian tingkatan energi bilangan orbital d atom pusat , yang lalu
menghasilakan enrgi untuk menstabilkan kompleks tersebut (energy stabilisasi medan
ligan). Salah satu fenomena yang paling umum terjadi bila ion kompleks terbentuk adalah
perubahan warna dalam larutan. Beberapa contoh adalah :
Cu
2+
+ 4NH
3
[Cu(NH
3
)
4
]
2+
Biru biru tua gelap
Fe
2+
+ 6CN
-
[Fe(CN)
6
]
4-
Hijau muda kuning
Ni
2+
+ 6NH
3
[Ni(NH
3
)
6
]
2+
Hijau biru
Fe
3+
+ 6F
-
[FeF
6
]
3-
Kuning tak berwarna (Vogel, 1990).
Ion kompleks dalam larutan terbentuk secara bertahap. Pembentukan kompleks
oktahedral satu ion logam dalam pelarut air dengan suatu ligan berlangsung melalui
mekanisme reaksi substitusi. Reaksi substitusi ion logam dengan masing-masing ligan
monodentat, bidentat atau tridentat berturut-turut terdiri dari enam, tiga dan dua tahap.
Sebagai contoh, ion logam dalam pelarut air membentuk kompleks [M(H
2
O)
6
]
n+
. Pada saat
ke dalam larutan ditambahkan ligan monodentat tidak bermuatan maka terjadi reaksi:
[M(H
2
O)
6
]
n+
+ L [M(H
2
O)
5
L]
n+
+ H
2
O
Reaksi tersebut terus berlangsung hingga keenam H
2
O tersubstitusi dan dihasilkan
kompleks [ML
6
]
n+
. Apabila ligan yang ditambahkan merupakan ligan bidentat maka reaksi
terdiri dari tiga tahap. Pada setiap tahap dua molekul H
2
O disubstitusi oleh satu ligan
bidentat hingga pada akhir reaksi diperoleh kompleks [ML
3
]
n+
(Kristian. H, 2003).
Kompleks dengan satu ion logam pusat dikenal sebagai kompleks inti tunggal
(mononuklir). Salah satu kompleks mononuklir yang banyak diteliti adalah kompleks Fe(II)
dengan ligan C
14
H
10
N
2
(2,(2-pyridyl)quinoline = pq) misalnya [Fe(pq)
2
(ClO
4
)
2
],
[Fe(pq)
2
(ClO
4
)
2
].H
2
O, [Fe(pq)
2
(H
2
O)Br]Br.H
2
O, [Fe(pq)
2
(NCS)
2
], [Fe(pq)
3
](ClO
4
)
2
1
,
[Fe(pq)
3
](ClO
4
)
2
.H
2
O
2
, [Fe(pq)Cl
2
]
3
. Ligan pq merupakan ligan bidentat turunan bpy (2,2-
bipyridine = C
10
H
8
N
2
) yang dihasilkan dari substitusi benzo dalam posisi cis. Ligan pq sangat
menarik karena pada beberapa kasus menghasilkan kekuatan medan sedang yang dapat
memberikan efek spin crossover (Effendy, 2007).
Rumus molekul menentukan jumlah eksak atom-atom dari setiap unsur di dalm unit
terkecil suatu zat. Dalam pembahasan tentang molekul, setiap contoh diberikan bersama
dengan rumus molekulnya dalam di dalam tanda kurung. Jadi H
2
adalah rumus molekul
untuk hydrogen,O
2
adalah oksigen dan H
2
O adalah air. Angka subskrip menandai jumlah
atom suatu unsur yang ada dalam molukul itu. Dalam H
2
O tidak ada subskrip untuk O,
karena hanya ada satu oksigen dalam stu molekul air., dan angka satu dihilangkan dari
rumus. Perhatikan bahwa oksigen O
2
dan ozon O
3
adalah alotrop dari oksigen. Alotrop
adalah salah satu dari dua atau lebih dari dua bentuk lain dari unsur (Chang, 2003).
Besi dengan kemurnian yang tinggi tersedia sebagai standar primer. Besi dilarutkan
dalam larutan asam dan pada proses pelarutan besi (III) direduksi menjadi besi (II). Jika
kemudian larutan itu dititrasi dengan permanganat. Suatu larutan mangan (II) sulfat, asam
sulfat dan asam fosfat yang disebut larutan pencegah dapat ditambahkan ke dalam larutan
asam dari besi sebelum dititrasi dengan permanganate. Asam fosfat menurunkan
konsentrasi ion besi (III) dengan pembentukan kompleks, sehingga membantu untuk
memaksa agar reaksi brjalan lengjap dan juga menghilangkan warna kuning yang terdapat
pada besi (III) dalm media asam. Kompleks fosfat tidak berwarna dan titik akhir akan
menjadi lebih jelas (Day dan Underwood, 2002 ).
Besi dialam ditemukan sebagai unsur kimia ke sepuluh paling banyak. Hal ini
menyumbang kepada medan magnet bumi. Beberapa komleksi besi juga memiliki sifat
magnet. senyawa kompleks Fe(II)-Cr(III) dengan ligan oksalat memiliki rumus kimia
[(C
6
H
9
)
4
N][Fe
II
Cr
III
(C
2
O
4
)
3
].H
2
O. Ligan oksalat pada kompleks tersebut berfungsi sebagai
jembatan antra ion besi (II) dengan khrom (III). Kompleks tersebut berwarna hijau
kekuningan dan bersifat paramagnet pada temperatur ruang. Pengukuran suseptibilitas
pada temperatur 80-300K menghasilkan peningkatan suseptibilitas pada temperatur makin
rendah yang menunjukkan kompleks yang terbentuk bersifat feromagnet (Effendy, 2007).
Titrasi redoks melibatkan reaksi oksidasi dan reduksi antara titrant dan analit.Titrasi
redoks banyak dipergunakan untuk penentuan kadar logam atau senyawa yang bersifat
sebagai oksidator atau reduktor. Aplikasi dalam bidang industri misalnya penentuan sulfite
dalam minuman anggur dengan menggunakan iodine, atau penentuan kadar alkohol
dengan menggunakan kalium dikromat. Beberapa contoh yang lain adalah penentuan asam
oksalat dengan menggunakan permanganate, penentuan besi(II) dengan serium(IV), dan
sebagainya. Karena melibatkan reaksi redoks maka pengetahuan tentang penyetaraan
reaksi redoks memegang peran penting, selain itu pengetahuan tentang perhitungan sel
volta, sifat oksidator dan reduktor juga sangat berperan. Dengan pengetahuan yang cukup
baik mengenai semua itu maka perhitungan stoikiometri titrasi redoks menjadi jauh lebih
mudah (Day dan Underwood, 2002 ).
Contoh titrasi redoks yang terkenal adalah iodimetri, iodometri, permanganometri
menggunakan titrant kalium permanganat untuk penentuan Fe
2+
dan oksalat, Kalium
dikromat dipakai untuk titran penentuan Besi(II) dan Cu(I) dalam CuCl. Bromat dipakai
sebagai titrant untuk penentuan fenol, dan iodida (sebagai I
2
yang dititrasi dengan
tiosulfat), dan Cerium(IV) yang bisa dipakai untuk titrant titrasi redoks penentuan
ferosianida dan nitrit (Day dan Underwood, 2002 ).
Titik akhir titrasi dalam titrasi redoks dapat dilakukan dengan mebuat kurva titrasi
antara potensial larutan dengan volume titrant, atau dapat juga menggunakan indicator.
Dengan memandang tingkat kemudahan dan efisiensi maka titrasi redoks dengan indicator
sering kali yang banyak dipilih. Beberapa titrasi redoks menggunakan warna titrant sebagai
indicator contohnya penentuan oksalat dengan permanganate, atau penentuan alkohol
dengan kalium dikromat (Day dan Underwood, 2002 ).
Permanganometri adalah titrasi yang dilakukan berdasar reaksi kalium
permanganat (KMnO
4
). Reaksi ini di fokuskan pada reaksi oksidasi dan reduksi ang terjadi
antar KMnO
4
dengan bahan baku tertentu. Kalium permanganat merupakan zat coklat tua
yang menghasilkan larutan ungu bila dilaritkan dalam air. Kalium permanganat merupakan
pengoksid kuat yang bekerja berlainan menurut pH dari medium dan merupakan larutan
standar sekunder. Oleh sebab itu larutan KMnO
4
harus distandarisasi agar larutan menjadi
standar primer. Dalam larutan asam ion permanganat direduksi menurut proses lima
elektron, bila bilangan oksidasi mangan di ubah dari +7 ke +2 adalah
MnO
4
-
+ 8H
+
+ 5e Mn
2+
+ 4H
2
O (Oxtoby, 2001)
Kalium permanganat dapat bertindak sebagai indikator pada umumnya titrasi
dilakukan dalam suasana asam, karena akan lebih mudah mengamati titik akhir titrasinya.
Permananat bereaksi secara cepat dengan banyak reagen pereduksi namun beberapa
reaksi membutuhkan pemanas dan pengadukan atau penggunaan sebuah katalis untuk
mempercepat laju reaksi. (Anonim,2009).
Reaksi yang paling lazim dijumpai dalam laboratorium pengantar adalah reaksi
dalam larutan yang sangat asam. Permanganate bereaksi dengan cepat dengan banyak zat
pereduksi menurut reaksi 1,namun salah satu zat memerlukan pemanasan atau katalis
untuk mempercepat reaksi. Seandainya reaksi itu tidak lambat, akan dijumpai lebih banyak
kesulitan dalm menggunakan reagensia. Misalnya permanganate merupakan zat pengoksid
yang cukup kuat untuk mengoksidasi Mn(II) menjadi MnO
2
menurut persamaan :
3Mn
2+
+ 2MnO
4
-
+ 2 H
2
O 5MnO
(s)
+ 4H
+
Sedikit kelebihan permangant yang ada pada titik akhir suatu titrasi telah cukup
untuk menimbulkan pengandapan MnO
2.
Dalam persiapan larutan permanganat harus
dilakukan tindakan pencegahan khusus dengan cara pemanasan untuk memusnahkan zat
pereduksi dan penyaringan lewat kaca masir ( filter tak mereduksi) untuk menyingkirkan
MnO
2
dan agar proses oksidasi lebih cepat (Day dan Underwood, 2002 ).
Persamaan redoks yang berimbang haruslah dicari beberapa elektron yang
dilepaskan oleh zat pereduksi dan diambil zat pengoksid. Hal tersebut dapat diketahui
dengan mudah apabila persamaan reaksi setengah sel dari sistem redoks yang dilibatkan
itu telahdiketahui, contohnya adalah
H
2
O
2
O
2
+ 2H
+
+ 2e
Dan MnO
4
-
+ 8H
+
+ 5e Mn
2+
+4H
2
O
(1)
Dapatlah dengan segera nampak bahwa 5 hidrogen peroksida akan melepaskan 10
elektron yang kemudian akan diambil 2 ion permanganat. Dari angka persamaan ini dapat
berimbang dengan sangat mudah. (Oxtoby, 2001)
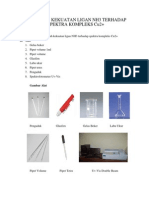
IV. ALAT DAN BAHAN
1. Alat-alat
a. Pipet ukur 25mL
b. Pipet ukur 1mL
c. Gelas piala 150 mL
d. Pengaduk gelas
e. Pembakar spiritus dan tripot
f. Gelas arloji besar
g. Sendok sungu
h. Buret
i. Statif
j. Corong gelas
k. Erlenmeyer
l. Termometer
m. Pinset
n. Penyaring Buchner
o. Glass wool
2. Bahan bahan
a. Ammonium besi (II) sulfat
b. Serbuk seng
c. Kalium permanganate
d. Aseton
e. Asam sulfat 2M
f. Kristal asam oksalat
g. Akuades
9
V. CARA KERJA
4 gram ammonium
besi(II) sulfat
12,5 mL Akuades
0,5 mL asam sulfat
2M
2.5 gram kristal
asam oksalat
Larutan besi (II)
15 mL akuades
Larutan asam
oksalat
dididihkan
Endapan yang
terbentuk disaring
Dicuci dengan air panas
Dicuci dengan aseton
Endapan dikeringkan
Tentukan rendemen
0,2 gram rendemen
10 mL asam sulfat 2M
Tentukan kadar besi,oksalat dan air
Dicuci dengan H
2
SO
4
2M
m
Disaring dengan glass wool
Dididihkan larutan dengan 2
gram serbuk seng 10 menit
Dititrasi dengan KMnO
4
Dititrasi dengan KMnO
4
10
VI. PEMBAHASAN
Penentuan Rumus Molekul Senyawa Kompleks merupakan judul yang akan di
bahas pada percobaan kimia anorganik 2 kali ini, yang bertujuan mempelajari
pembuatan dan penentuan molekul senyawa kompleks besi (II) oksalat. Awal mula
percobaan ini yaitu menyiapkan larutan besi(II)oksalat yang dibuat dengan
dilarutkannya ammonium besi(II)sulfat dengan di tambahkannya akuades beserta
sedikit asam sulfat 2 M. Setelah itu membuat larutan asam oksalat dengan cara
melarutkan Kristal asam oksalat dengan beberapa mL akuades. Ditambahkannnya asam
sulfat pada pembuatan larutan besi(II) yaitu bertujuan agar larutan besi (II) oksalat
bersifat asam sama dengan asam oksalat jadi agar sama-sama asamnya serta yang
paling urgen yaitu karena besi merupakan zat reduksi yang lemah, sehingga jika
ditambah dengan asam oksalat maka akan mudah direduksi oleh permanganate.
Kemudian kedua larutan tersebut dicampurkan, dan akan terbentuk suatu
endapan dan warna kuning. Endapan tersebut adalah Fe
2
C
2
O
4.
Dan warna kuning yang
dihasilkan adalah suatu bukti bahwa telah terbentuknya ion Fe
3+
. Setelah kedua larutan
tersebut di campur lalu didihkan. Fungsi didihkan yaitu agar ketika dititrasi akan
diperoleh hasil yang maksimal karena titrasi akan maksimal apabila dipanaskan dan Fe
akan maksimal pada suhu yang berkisar 40-60
o
C.
Setelah melalui proses dididihkan maka proses selanjutnya yaitu penyaringan
endapan yang terbentuk, tidak lain yaitu endapan Fe
2
C
2
O
4
. Penyaringan dilakukan
menggunakan penyaringan Buchner. Ketika disaring menggunakan penyaring Buchner
residu yang telah tertangkap dicuci dengan 2 kali pencucian. Pencucian pertama
menggunakan air panas dan pencucian kedua menggunakan larutan aseton. Pencucian
bertujuan untuk membersihkan senyawa-senyawa organik.
Kemudian Endapan atau residu dikeringkan di dalam alat pengering. Tujuan
pengeringan yaitu untuk menghilangkan sisa-sisa air yang masih ada dalam residu tetapi
suhu yang digunakan tidak lebih dari suhu titik lebur residua atau Fe
2
C
2
O
4
. Setelah
11
melalui beberapa waktu dalam proses pengeringan kemudian ditentukan rendemenya.
Hasil rendemen di ambil beberapa gram dan di larutkan dengan beberapa mL asam
sulfat 2M. Kemudian dititrasi menggunakan larutan standar kalium permanganat sampai
titik ekivalen tercapai. Titrasi menggunakan kalium permanganate dikarenakan kalium
permanganate merupakan oksidator kuat.
Setelah dititrasi kemudian hasil titrasi tersebut di dididihkan dengan
menambahkan beberapa gram serbuk seng selama durasi waktu 10 menit.
Ditambahkannya serbuk seng karena seng (III) mereduksi Besi (III) menjadi Besi (II).
Kemudian sambil menunggu proses, disiapkannya corong yang pada mulut
corong telah di modifikasi menggunakan glass woll sebagai penyaring. Pemasangan
glass woll sangatlah hati-hati karena glass woll terbuat dari serabut-serabut gelas yang
dapat membahayakan kesehatan karena glass woll dapat terhirup sehingga
mengganggu proses pernapasan pada paru-paru bahkan dapat menimbulkan kematian,
maka perlu dipakainya masker untuk melindungi hidung. Setelah itu larutan disaring
menggunakan corong yang telah dimodifikasi tadi dan dicuci menggunakan larutan
H
2
SO
4
. 2M. kemudian dititrasi lagi menggunakan KMnO
4
. Dengan melalui berbagai
proses tadi maka dapat ditentukannya kadar besi, oksalat dan air.
VII. KESIMPULAN
Pembuatan serta penentuan molekul senyawa komplek besi (II) oksalat dapat
dilakukan dengan cara titrasi menggunakan larutan standart KMnO
4
, mengetahui rumus
empiris serta massa molar dari senyawa tersebut.
Rumus yang terbentuk yaitu [FeC
2
O
4
]. 2 H
2
O dengan perbandingan rumus
empirisnya 1 : 1 : 2
12
VIII. DAFTAR PUSTAKA
Effendy, Ph.D.2007 . Prespektif Baru Kimia Koordinasi Jilid 1. Bayumedia Publising.
Malang
Khopkar. S.M. 2008 . Konsep Dasar Kimia Analitik. UI Press. Jakarta
Underwoood, David . W. 2001. Analisis Kimia Kuantitatif Edisi keenam. Erlangga : Jakarta
Vogel. 1985. Analisis Anorganik Kuantitatif Makro dan Semimakro Edisi Edisi ke Lima. PT
Kalman Media Pusaka : Jakarrta.
Mengetahui Yogyakarta, 04 April 2011
Asisten Praktikan,
Andika Fajar Setiawan Rifqi Mizan AUlawi
13
IX. LAMPIRAN
PERHITUNGAN
1. Titrasi I
0,2 gram sampel KMnO4 V Titrasi = 6,4 mL
2. Titrasi II
Larutan Titrasi II + Zn KMnO4 V Titrasi = 1,7 mL
3. Penentuan Kadar Besi
Mgrek Fe = m grek MnO4
mmol Fe x n Fe = mmol MnO4
-
x n MnO4
-
mmol Fe x 1 = 0,1 x 1,7 mL x 5
mmol Fe = 0,85/1 = 0,85 mmol
4. Penentuan Kadar C2O4
2-
Mgrek C2O4
2-
= m grek MnO4
mmol C2O4
2-
x n C2O4
2-
= mmol MnO4
-
x n MnO4
-
mmol C2O4
2-
x 2 = 0,1 x (6,4-1,7) mL x 5
mmol C2O4
2-
= 0, x 4,7 mL x 5
mmol C2O4
2-
= 1,175 mmol
5. Penentuan kadar air
Kadar air = massa sampel massa Fe massa C2O4
2-
= 200 mg (mmol Fe x Ar Fe) (mmol C2O4
2-
x Mr C2O4
2-
)
= 200 mg ( 0,85 x 55,9) - (1,175 mmol x 88)
= 200 mg 47,51 103,4
= 49,09 mg
14
Mmol air =
Mol Fe : Mol C2O4
2-
: mol H2O
0,85 : 1,175 : 2,73 mmol
1 : 1 : 2
Anda mungkin juga menyukai
- Penetapan Rumus Molekul Senyawa KompleksDokumen9 halamanPenetapan Rumus Molekul Senyawa KompleksNonong IsdayantiBelum ada peringkat
- Pembuatan Garam Kompleks Tetra Amin TembagaDokumen14 halamanPembuatan Garam Kompleks Tetra Amin TembagayennioctaBelum ada peringkat
- Percobaan 17Dokumen8 halamanPercobaan 17Risa ImanurisaBelum ada peringkat
- Laporan Pengaruh Kekuatan Ligan Nh3 Terhadap Spektra Kompleks Cu2Dokumen10 halamanLaporan Pengaruh Kekuatan Ligan Nh3 Terhadap Spektra Kompleks Cu2Anggia Putri Gustami50% (2)
- Laporan Praktiku Cis Trans Kalium Dioksalato Diakuo Kromat (III)Dokumen11 halamanLaporan Praktiku Cis Trans Kalium Dioksalato Diakuo Kromat (III)Nadia YulisaBelum ada peringkat
- Laporan Akhir Anor 3Dokumen8 halamanLaporan Akhir Anor 3GinaMaulia100% (2)
- Pembuatan Garam Kompleks Dan Garam RangkapDokumen14 halamanPembuatan Garam Kompleks Dan Garam RangkapAnggia Putri Gustami0% (1)
- Laporan Anorganik Sintesis Senyawa Koordinasi Kalium Trioksalato FeratDokumen12 halamanLaporan Anorganik Sintesis Senyawa Koordinasi Kalium Trioksalato FeratYasendi AnakriBelum ada peringkat
- Percobaan Pengaruh Kekuatan Ligan Terhadap Spektra Kompleks Tembaga (II)Dokumen17 halamanPercobaan Pengaruh Kekuatan Ligan Terhadap Spektra Kompleks Tembaga (II)Tri PebriantiBelum ada peringkat
- Heksaminakobalt (III) TrikloridaDokumen15 halamanHeksaminakobalt (III) TrikloridaFadhil Kardani Lagawi PutraBelum ada peringkat
- Laporan Kimia Anorganik I Reaksi Senyawa Kompleks EtilendiaminDokumen4 halamanLaporan Kimia Anorganik I Reaksi Senyawa Kompleks Etilendiaminernanda100% (6)
- Objek 1 FixDokumen24 halamanObjek 1 FixFauziah AnnisaBelum ada peringkat
- Laporan Pembuatan Cis Dan Trans-KaliumdiaoksalatodiakuokromatDokumen16 halamanLaporan Pembuatan Cis Dan Trans-KaliumdiaoksalatodiakuokromatYuli Astuti X TigaBelum ada peringkat
- Pembuatan Garam Kompleks Dan Garam Rangkap Dari TembagaDokumen7 halamanPembuatan Garam Kompleks Dan Garam Rangkap Dari TembagaDWI ARIF SBelum ada peringkat
- Laporan Akhir Percobaan Soda KostikDokumen13 halamanLaporan Akhir Percobaan Soda KostikAnonymous EXYGIzYp100% (1)
- Penentuan Komposisi Ion KompleksDokumen6 halamanPenentuan Komposisi Ion KompleksDian Agus SetyawatiBelum ada peringkat
- TugasDokumen3 halamanTugasnilaBelum ada peringkat
- Laporan Praktikum Kimia Anorganik I KoordinasiDokumen12 halamanLaporan Praktikum Kimia Anorganik I Koordinasiokta fatma wita75% (4)
- Stabilisasi Dan Isolasi Senyawa TembagaDokumen4 halamanStabilisasi Dan Isolasi Senyawa TembagaMuhammad Nashih Ulwan0% (1)
- Kompleks Inert Dan LabilDokumen9 halamanKompleks Inert Dan LabilSarmila EkaBelum ada peringkat
- Teori Medan KristalDokumen12 halamanTeori Medan KristalYendro Try SaturaBelum ada peringkat
- Kompleks TetrahedralDokumen25 halamanKompleks TetrahedralArdiansyah DrkBelum ada peringkat
- Anor Obj 1Dokumen23 halamanAnor Obj 1Humaira FaradillaBelum ada peringkat
- Lapres Kekuatan Medan LiganDokumen27 halamanLapres Kekuatan Medan LiganifaBelum ada peringkat
- Kekuatan Medan LiganDokumen12 halamanKekuatan Medan LiganDamon NealBelum ada peringkat
- 2.kinetika Dan Mekanisme Reaksi Senyawa KompleksDokumen18 halaman2.kinetika Dan Mekanisme Reaksi Senyawa KompleksrabiantiBelum ada peringkat
- Keseimbangan Senyawa Koordinasi AnorganikDokumen15 halamanKeseimbangan Senyawa Koordinasi AnorganikRizki Wardani100% (1)
- Laporan Kekuatan Medan LiganDokumen20 halamanLaporan Kekuatan Medan LiganMetta Sari Kedele50% (2)
- Kimia Anorganik TawasDokumen8 halamanKimia Anorganik TawasGusty DyanoBelum ada peringkat
- Yasendi Anakri - !903112495 - Sintesis Senyawa Koordinasi Kalium Trioksalato FeratDokumen14 halamanYasendi Anakri - !903112495 - Sintesis Senyawa Koordinasi Kalium Trioksalato FeratMuhammad RafiBelum ada peringkat
- Mekanisme Reaksi Anorganik DanPengarah TransDokumen12 halamanMekanisme Reaksi Anorganik DanPengarah TransHakamBelum ada peringkat
- Kompleks WernerDokumen5 halamanKompleks WernerAmanda PujiastutiBelum ada peringkat
- Pko CannizaroDokumen5 halamanPko CannizaroSepti Nur Diana100% (2)
- Makalah Bab Disosiasi Dan Substitusi LiganDokumen17 halamanMakalah Bab Disosiasi Dan Substitusi LiganRifki SolihatunBelum ada peringkat
- Pembuatan Garam Kompleks Dan Garam RangkapDokumen14 halamanPembuatan Garam Kompleks Dan Garam RangkapErwinda PrimaBelum ada peringkat
- (Fotokimia Reduksi Ion Besi (III) )Dokumen27 halaman(Fotokimia Reduksi Ion Besi (III) )shellavalentina77100% (2)
- Sintesis Kalium NitratDokumen11 halamanSintesis Kalium NitratCorinne SandersBelum ada peringkat
- Embuatan Garam Kompleks Tetra Amin Tembaga (Ii)Dokumen19 halamanEmbuatan Garam Kompleks Tetra Amin Tembaga (Ii)Ade NurBelum ada peringkat
- Jurnal ElektrogravimetriDokumen1 halamanJurnal ElektrogravimetriRahmawati Nirmala SariBelum ada peringkat
- Reduksi Fotokimia Garam Besi (III) - Gustin Lestiani - 1817011035-DikonversiDokumen5 halamanReduksi Fotokimia Garam Besi (III) - Gustin Lestiani - 1817011035-DikonversiGustin LestianiBelum ada peringkat
- Laporan Praktikum Kimia Fisik E-2 Kelarutan Timbal BalikDokumen22 halamanLaporan Praktikum Kimia Fisik E-2 Kelarutan Timbal BalikCatia Julie Aulia100% (1)
- Kimia KomputasiDokumen8 halamanKimia KomputasiAnnisa Aulia RahmahBelum ada peringkat
- Laporan Praktikum Kimia Anorganik I - Percobaan VIII (Pembuatan Kalium Trioksalato Aluminat)Dokumen13 halamanLaporan Praktikum Kimia Anorganik I - Percobaan VIII (Pembuatan Kalium Trioksalato Aluminat)lyraBelum ada peringkat
- Pembuatan Cis-Trans Kalium Dioksalatodiakuokromat (III)Dokumen15 halamanPembuatan Cis-Trans Kalium Dioksalatodiakuokromat (III)rabianti100% (1)
- Pembuatan Natrium Peroksoborat - 2Dokumen6 halamanPembuatan Natrium Peroksoborat - 2saudagar_minang72100% (1)
- Laporan Anorganik Penentuan Komposisi Senyawa Kompleks PDFDokumen5 halamanLaporan Anorganik Penentuan Komposisi Senyawa Kompleks PDFFadila Rizka Aini100% (3)
- Kimia Koordinasi Teori Medan KristalDokumen22 halamanKimia Koordinasi Teori Medan KristalSetyani100% (1)
- Entalpi Dan Entropi PeleburanDokumen15 halamanEntalpi Dan Entropi PeleburanFavian Ferris100% (1)
- Tetraamintembaga II SulfatDokumen17 halamanTetraamintembaga II SulfatKhunaz Miligh Ci'Mommye0% (1)
- Pembuatan Garam Kompleks Dan Garam RangkapDokumen19 halamanPembuatan Garam Kompleks Dan Garam RangkapMuhamad Zaky90% (10)
- Makalah Kimia Anorganik 2Dokumen24 halamanMakalah Kimia Anorganik 2Yiyi Qyudi100% (1)
- Bundelan Unit 5 Pentuan BilkorDokumen25 halamanBundelan Unit 5 Pentuan BilkorWalny NichaBelum ada peringkat
- Kompleks Koordinasi Dan Pembentukan Senyawa KompleksDokumen16 halamanKompleks Koordinasi Dan Pembentukan Senyawa KompleksNurmala Mulyani100% (2)
- Laporan KompleksDokumen16 halamanLaporan KompleksOnoBelum ada peringkat
- Senyawa Dan Ion KompleksDokumen8 halamanSenyawa Dan Ion KompleksChendi M. BatasBelum ada peringkat
- Senyawa KompleksDokumen9 halamanSenyawa Komplekszaamulfah100% (1)
- Laptep Kiman Kelompok 2Dokumen16 halamanLaptep Kiman Kelompok 2Adelia190498Belum ada peringkat
- Senyawa KompleksDokumen30 halamanSenyawa Kompleksana ulfaBelum ada peringkat
- Laporan Prak Kiman 2 Pembuatan Senyawa KoordinasiDokumen15 halamanLaporan Prak Kiman 2 Pembuatan Senyawa KoordinasiFazita FauBelum ada peringkat
- Kimia Analisis Ion KompleksDokumen7 halamanKimia Analisis Ion KompleksyantoBelum ada peringkat
- Form. Surat Permohonan Penggantian KTM (Dokumen1 halamanForm. Surat Permohonan Penggantian KTM (RifQi Mizan AulawiBelum ada peringkat
- Surat Pernyataan Kebenaran Dokumen Cpns Kemenko Polhukam Unggah Portal SSCN OkDokumen1 halamanSurat Pernyataan Kebenaran Dokumen Cpns Kemenko Polhukam Unggah Portal SSCN OkRifQi Mizan AulawiBelum ada peringkat
- Dok Surat Bebas PustakaDokumen1 halamanDok Surat Bebas PustakaRifQi Mizan AulawiBelum ada peringkat
- Form KRS 20172Dokumen2 halamanForm KRS 20172RifQi Mizan AulawiBelum ada peringkat
- Homework Value ChainDokumen3 halamanHomework Value ChainRifQi Mizan AulawiBelum ada peringkat
- Surat Pernyataan SSCN PDFDokumen1 halamanSurat Pernyataan SSCN PDFPangeran BerantakanBelum ada peringkat
- Soal Statistik KimiaDokumen1 halamanSoal Statistik KimiaRifQi Mizan AulawiBelum ada peringkat
- CCR RouterOS v6Dokumen42 halamanCCR RouterOS v6RifQi Mizan AulawiBelum ada peringkat
- Bahan AjarDokumen1 halamanBahan AjarRifQi Mizan AulawiBelum ada peringkat
- Panduan Teknis Ver 6.2 Lampiran KomplitDokumen45 halamanPanduan Teknis Ver 6.2 Lampiran KomplitRifQi Mizan AulawiBelum ada peringkat
- Percobaan 4 ResmiDokumen16 halamanPercobaan 4 ResmiRifQi Mizan AulawiBelum ada peringkat
- TA Pendidikan AgamaDokumen12 halamanTA Pendidikan AgamaRifQi Mizan AulawiBelum ada peringkat
- Glosarium KerajinanDokumen3 halamanGlosarium KerajinanRifQi Mizan AulawiBelum ada peringkat
- Fuel Cell 2Dokumen8 halamanFuel Cell 2Susanto SulistyoBelum ada peringkat
- Chang22 Polimer Organik-Sintetik Dan AlamiDokumen6 halamanChang22 Polimer Organik-Sintetik Dan AlamiRifQi Mizan AulawiBelum ada peringkat