Kimia Industri
Diunggah oleh
AasNurhasanah0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
92 tayangan18 halamanDokumen tersebut merupakan diktat praktikum kimia bahan industri yang berisi 6 percobaan, di antaranya adalah (1) pengolahan kaolin menjadi aluminium sulfat, (2) pembuatan kieselguhr dari limbah abu layang, (3) pengolahan batu gamping menjadi kalsium oksida bebas impuritis, (4) pemurnian garam dapur, (5) pembuatan silikagel dari limbah kaolin, dan (6) pembuatan kalsium sulfat dari batu
Deskripsi Asli:
kimia
Judul Asli
Praktikum Kimia Bahan Industri
Hak Cipta
© © All Rights Reserved
Format Tersedia
PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniDokumen tersebut merupakan diktat praktikum kimia bahan industri yang berisi 6 percobaan, di antaranya adalah (1) pengolahan kaolin menjadi aluminium sulfat, (2) pembuatan kieselguhr dari limbah abu layang, (3) pengolahan batu gamping menjadi kalsium oksida bebas impuritis, (4) pemurnian garam dapur, (5) pembuatan silikagel dari limbah kaolin, dan (6) pembuatan kalsium sulfat dari batu
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
92 tayangan18 halamanKimia Industri
Diunggah oleh
AasNurhasanahDokumen tersebut merupakan diktat praktikum kimia bahan industri yang berisi 6 percobaan, di antaranya adalah (1) pengolahan kaolin menjadi aluminium sulfat, (2) pembuatan kieselguhr dari limbah abu layang, (3) pengolahan batu gamping menjadi kalsium oksida bebas impuritis, (4) pemurnian garam dapur, (5) pembuatan silikagel dari limbah kaolin, dan (6) pembuatan kalsium sulfat dari batu
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 18
DIKTAT PRAKTIKUM
KIMIA BAHAN INDUSTRI
Disusun Oleh :
Staf Dosen Lab. Kimia Anorganik
PROGRAM D-III ANALIS KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS BRAWIJAYA
MALANG
2009
2
Materi Praktikum Kimia Bahan Industri
PERCOBAAN I
PENGOLAHAN KAOLIN MENJADI ALUMINIUM SULFAT
PERCOBAAN II
PEMBUATAN KIESELGUHR DARI LIMBAH ABU LAYANG
PERCOBAAN III
PENGOLAHAN BATU GAMPING MENJADI
KALSIUM OKSIDA BEBAS IMPURITIS
PERCOBAAN IV
PEMURNIAN GARAM DAPUR
PERCOBAAN V
PEMBUATAN SILIKAGEL DARI LIMBAH KAOLIN
PERCOBAAN VI
PEMBUATAN KALSIUM SULFAT DARI BATU GAMPING
3
PERCOBAAN I
PENGOLAHAN KAOLIN MENJADI ALUMINIUM SULFAT
Pendahuluan
Alumina merupakan senyawa oksida yang mempunyai banyak kegunaan,
diantaranya sebagai adsorben, support katalis, atau sebagai bahan pembuatan
keramik dan logam aluminium. Untuk pembuatan logam Al dan bahan pembuatan
keramik biasanya diperlukan kemurnian yang tinggi.
Alumina yang mempunyai kemurnian tinggi biasanya diperoleh dari proses
sintesis dengan menggunakan bahan organik sebagai sumber Al. Proses ini
memerlukan biaya yang sangat mahal. Suatu upaya telah dilakukan untuk
mendapatkan alumina yang mempunyai kemurnian tinggi dan biaya cukup murah
dengan mengolah mineral kaolin menjadi aluminium sulfat yang kemudian
mengkalsinasi bahan tersebut menjadi alumina.
Kaolin merupakan mineral yang keberadaannya cukup berlimpah di
Indonesia. Kaolin terutama mengandung silika (45%) dan alumina (38,5%).
Kandungan lain adalah feri oksida (0,98%), kalsium oksida (0,49%), natrium oksida
(0,48%), serta bahan lain yang habis dengan pembakaran (13,78%).
Dalam percobaan ini kaolin diolah dengan menggunakan larutan asam sulfat
untuk mendapatkan aluminium sulfat sebagai bahan dasar pembuatan alumina yang
relatif murni. Senyawa tersebut diperoleh sebagai hidratnya, yaitu Al2(SO4)3.18H2O.
Tujuan Percobaan
Mempelajari cara pembuatan aluminium sulfat dari mineral kaolin.
Alat dan Bahan
a. Alat-alat yang digunakan
- Peralatan refluks
- Gelas kimia 250 mL
- Pipet tetes
4
- Gelas arloji
- Sendok spatula
- Seperangkat alat pengaduk magnetik
- Corong gelas
- Erlenmeyer 250 mL
b. Bahan-bahan yang digunakan
- Mineral kaolin yang sudah dikalsinasi pada 800
0
C.
- Larutan asam sulfat 1 M
- Etanol
Cara Kerja
a. 10 gram kaolin yang sudah dikalsinasi direfluks dengan larutan asam sulfat 1 M
sebanyak 100 mL pada 80
0
C selama 1 jam.
b. Hasil yang diperoleh disaring dan filtratnya dipekatkan sampai volume larutan
tinggal setengahnya.
c. Filtrat tersebut ditambahkan ke dalam etanol (100 mL) setetes demi setetes
sambil terus diaduk (dengan pengaduk magnetik). Hentikan tetesan bila tidak
terbentuk endapan lagi.
d. Saring endapan yang diperoleh dan cuci dengan air.
e. Keringkan di udara
f. Timbang dan tentukan titik lelehnya (cocokkan dengan data direference).
Tugas :
1. Dari komponen oksida yang terdapat dalam kaolin, oksida yang mana saja yang
larut dalam asam sulfat?
2. Oksida-oksida yang terlarut dalam larutan asam sulfat akan membentuk senyawa
sulfat. Dari senyawa sulfat tersebut, yang mana yang tetap larut dalam etanol ?
5
PERCOBAAN II
PEMBUATAN KIESELGUHR DARI LIMBAH ABU LAYANG
Pendahuluan
Silika ditemukan di alam dalam berbagai bentuk kristal (contoh : quartz,
trimidit, dan kristobalit) dan juga sebagai silika amorf (kieselguhr). Silika amorf
tersebut mempunyai daya adsorpsi yang besar. Silika amorf dapat dipreparasi
dengan cara menandapkan larutan natrium silikat dengan menambahkan asam
(misalnya HCl) sehingga terbentuk silika hidrat. Jika silika hidrat tersebut dipanaskan
sehingga terbentuk anhidratnya, maka anhidrat tersebut akan berpotensi sekali
sebagai zat pengering (drying agent).
Abu layang merupakan limbah dari pembakaran batu bara yang banyak
mengandung silika. Dalam praktikum ini akan dibuat silika amorf dari limbah
tersebut.
Tujuan Percobaan
Memahami cara pembuatan silika amorf (kieselguhr) dari limbah abu layang.
Alat dan Bahan
a. Alat-alat yang digunakan :
- Gelas kimia 250 mL
- Corong buchner
- Erlenmeyer berleher cabang
- Pengaduk gelas
- Cawan penguap
- Gelas kimia plastik
- Tabung reaksi
- Gelas arloji
b. Bahan-bahan yang digunakan :
- Abu layang yang sudah ditanur pada 800
0
C selama 1 jam
6
- Larutan asam sulfat 1 M
- Larutan NaOH 5 M
- Larutan HCl 1:1
- Larutan KCNS 1 M
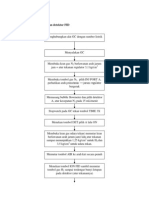
Cara Kerja :
1. Timbang 2 gram abu layang hasil kalsinasi dan masukkan ke dalam gelas kimia
250 mL, kemudian tambahkan dengan 50 mL asam sulfat 1 M. Aduk larutan
selama 15 menit.
2. Saring dan cuci padatannya dengan akuades. Pindahkan padatan tersebut ke
wadah plastik.
3. Tambahkan larutan natrium hidroksida sedikit demi sedikit sambil terus diaduk
sampai semua padatan tersebut larut.
4. Tambahkan larutan asam klorida sedikit demi sedikit sampai terbentuk endapan.
Teruskan penambahan sampai tidak terlihat adanya pembentukan endapan lagi.
5. Saring dengan corong buchner. kemudian cuci sampai netral (tes air cuciannya
dengan kertas lakmus biru).
6. Keringkan padatan tersebut dalam oven pada 100
0
C.
7. Setelah dingin, timbang padatan yang diperoleh.
8. Lakukan uji impuritis dengan cara mengambil sedikit padatan hasil sintesis dan
tetesi dengan larutan KCNS 1M.
Tugas :
1. Abu layang terutama mengandug silika, alumina, kalsium oksida, dan feri oksida.
Dari keempat oksida tersebut manakah yang larut dalam asam sulfat 1 M?
2. Oksida yang diperoleh dari hasil pencucian dengan asam sulfat dilarutkan dengan
larutan NaOH. Tuliskan reaksinya !
3. Untuk mendapatkan silika amorf, silika yang terlarut dalam larutan NaOH
diendapkan dengan penambahan asam. Tuliskan reaksinya !
4. Untuk menguji impurities, bagaimanakah hasil penambahan larutan KCNS ?
7
PERCOBAAN III
PENGOLAHAN BATU GAMPING MENJADI
KALSIUM OKSIDA BEBAS IMPURITIS
Pendahuluan
Batu gamping (CaCO3) merupakan salah satu mineral yang berlimpah di
Indonesia. Mineral tersebut dapat dipanaskan sehingga menghasilkan kalsium oksida
atau biasa dikenal sebagai kapur tohor. Kapur tohor ini selain biasa digunakan
sebagai bahan bangunan juga bermanfaat sebagai bahan untuk pemurnian nira dalam
industri pembuatan gula merah. Dalam aplikasi sebagai bahan pemurni nira
diperlukan kapur tohor yang bebas impuritis terutama silika dan magnesium oksida.
Dalam percobaan ini akan dilakukan pengolahan terhadap batu gamping di pasaran
dan diolah lagi menjadi kalsium oksida yang relatif bebas impuritis silika dan
magnesium oksida.
Tujuan Percobaan
Memahami proses pengolahan batu gamping menjadi kalsium oksida.
Alat dan Bahan
a. Alat-alat yang dipergunakan :
- Gelas kimia 150 mL
- Gelas kimia 100 mL
- Cawan penguapan porselin
- Gelas arloji
- Pengaduk gelas
- Corong gelas
- Erlenmeyer
b. Bahan-bahan yang dipergunakan :
- Batu gamping
- Larutan natrium karbonat 5 M
8
- Akuades
Cara Kerja
a. Ditimbang 10 gram batu gamping dan panaskan dalam tanur pada 900
0
C selama
0,5 jam kemudian didinginkan.
b. Timbang 5 gram padatan hasil penanuran tsb dan larutkan dalam 100 mL
akuades. Saring jika terdapat endapan dan ambil filtratnya.
c. Filtrat dipekatkan hingga 25 mL kemudian didinginkan.
d. Tambahkan larutan natrium karbonat 5 M sedikit demi sedikit (dengan pipet
tetes) hingga terbentuk endapan. Penambahan ini dihentikan apabila tetesan
natrium karbonat tidak memberikan endapan lagi.
e. Saring dan cuci sampai air pencuci netral.
f. Keringkan endapan di dalam oven pada 100
0
C, setelah itu pindahkan ke tanur dan
panaskan pada 900
0
C selama 1 jam.
g. Timbang padatan yang diperoleh dan hitung prosentase hasilnya.
Uji Kemurnian
1. Ambil sedikit padatan produk yang diperoleh dan letakkan dalam tabung reaksi.
Tambahkan akuades secukupnya, apakah ada endapannya ?
2. Uji titik leleh.
9
PERCOBAAN IV
PEMURNIAN GARAM DAPUR
Pendahuluan
Kelimpahan natrium klorida di alam sangat besar sebagai garam batuan atau
halit. Kelimpahan garam tersebut juga terdapat di air laut dengan konsentrasi rata-
rata 3%, sedang di laut mati sekitar 7,2%. Struktur kristal natrium klorida berbentuk
kubus transparan dengan kisi-kisi sederhana, mempunyai titik leleh 804
0
C dan dapat
diuapkan pada suhu tinggi.
Garam NaCl dialam masih banyak mengandung pengotor, NaCl murni dapat
diperoleh dengan cara mengalirkan gas HCl dalam larutan garam NaCl tidak murni,
karena pengaruh ion sejenis maka NaCl terendapkan.
Tujuan Percobaan
Pemurnian garam dapur kasar dengan menggunakan gas hidrogen klorida
hasil reaksi antara NaCl dengan H2SO4.
Alat dan Bahan
a. Alat-alat yang dipergunakan
- Erlenmeyer alas bulat 500 mL
- Erlenmeyer 250 mL
- Gelas kimia 500 mL
- Corong pisah
- Corong
- Slang Mika
- Pengaduk gelas
- Gabus
- Lampu bunsen
- Ring besi
- Kertas saring
- Melting point apparatus
10
- Statif
b. Bahan-bahan yang dipergunakan
- Garam dapur kasar
- Asam sulfat pekat
- Asam klorida pekat
- Akuades
Cara Kerja
a. Buatlah larutan jenuh garam dapur dengan cara melarutkan 45 g garam dapur
kasar dalam 100 mL air.
b. Panaskan larutan tersebut sambil diaduk.
c. Saring larutan dalam keadaan panas kemudian tempatkan dalam gelas kimia 500
mL (D).
d. Tempatkan 50 g garam dapur kasar dalam labu (B) dan tambahkan 10 mL
akuades.
e. Tuangkan sebanyak 45 mL H2SO4 pekat dalam corong pisah (A).
f. Tuangkan 20 mL HCl pekat ke dalam erlenmeyer (C).
g. Setelah diperkirakan tidak ada sambungan yang bocor, teteskan asam sulfat pekat
dari A ke B, bila perlu dipanaskan dengan api kecil.
h. Gas yang timbul akan mengalir ke C, setelah mengalami pencucian, gas akan
mengalir melalui corong ke labu D, beberapa lama kemudian akan terbentuk
kristal NaCl murni.
i. Keringkan kristal yang terbentuk dan timbang hasilnya.
Uji Hasil
- Uji titik leleh garam NaCl yang diperoleh dan bandingkan dengan titik leleh
NaCl murni.
11
PERCOBAAN V
PEMBUATAN SILIKAGEL DARI LIMBAH KAOLIN
Pendahuluan
Silika ditemukan didalam berbagai bentuk kristal (contoh : quarsa, trimidit
dan kristobalit) selain itu juga sebagai silika amorf. Silika amorf tersebut mempunyai
daya adsorpsi yang besar. Silika amorf dapat dipreparasi dengan cara mengendapkan
larutan natrium silikat dengan menambahkan asam misalnya HCl, sehingga terbentuk
silika hidrat. Jika silika hidrat tersebut dipanskan sehingga terbentuk anhidratnya,
maka anhidrat tersebut akan berpotensi sekali sebagai zat pengering.
Tujuan Percobaan
Memahami cara pembuatan silika gel dari limbah kaolin.
Alat dan Bahan
a. Alat yang dipergunakan
- 2 buah gelas kimia 250 mL
- Corong Buchner
- Erlenmeyer leher cabang
- Pengaduk gelas
- Cawan pengisap
- Gelas kimia plastik
- Tabung reaksi
- Gelas arloji
b. Bahan yang dipergunakan
- Kaolin yang sudah dikalsinasi
- Larutan asam sulfat 1M
- Larutan natrium hidroksida 5 M
- Larutan HCl 1:1
- Larutan KSCN 1 M
12
Cara Kerja
- Timbang 2 g kaolin hasil kalsinasi dan masukkan ke dalam gelas kimia 250 mL
dan tambahkan dengan 50 mL asam sulfat 1M.
- Aduk selama 15 menit
- Saring dan cuci padatannya dengan akudes.
- Pindahkan padatan tersebut ke gelas kimia plastik
- Tambahkan larutan natrium hidroksida sedikit demi sedikit sambil terus
diaduk sampai semua padatan tersebut larut.
- Tambahkan larutan asam klorida sedikit demi sedikit sampai terbentuk
endapan. Teruskan penambahan sampai tidak terlihat adanya pembentukan
endapan lagi.
- Saring dengan saringan Buchner
- Cuci sampai netral, kemudian tes cuciannya dengan kertas lakmus biru.
- Keringkan padatan tersebut dalam oven pada temperatur 100
0
C.
- Setelah dingin, timbang padatan yang diperoleh.
- Lakukan uji impuritis dengan cara mengambil sedikit demi sedikit padatan
hasil sintesis dan tetesi dengan larutan KSCN
13
PERCOBAAN VI
PEMBUATAN KALSIUM SULFAT DARI BATU GAMPING
Pendahuluan
Gamping banyak terdapat di Indonesia. Gamping mempunyai rumus kimia
CaCO3 dengan impuritis silika, besi dan magnesium. Salah satu penggunaan batu
gamping adalah digunakan untuk pembuatan bahan kimia, diantaranya kalsium
sulfat.
Tujuan Percobaan
Untuk mempelajari cara pembuatan kalsium sulfat dari batu gamping.
Alat dan Bahan
a. Alat-alat yang dipergunakan
- Oven
- Melting point
- Tanur
- Buret
- Ayakan 100 mesh
- Gelas kimia 250 mL
- Gelas ukur 100 mL
- Satu set penyaring vacum
- Tabung reaksi
- Sendok tula
- Mortar
- Neraca analitik
- Gelas arloji
- Erlenmeyer 250 mL
b. Bahan-bahan yang dipergunakan
- Batu gamping
- Asam sulfat
14
- Aquades
- Kalium tiosianat
Cara Kerja
- Timbang 2,0 g batu gamping yang sudah ditumbuk halus (kira-kira 100 mesh),
kemudian dipanaskan dalam tanur pada 900
0
C selama 1 jam.
- Rendamlah serbuk hasil pentanuran dengan 50 mL akuades selama 10 menit
sambil diaduk, kemudian saring dan ambil filtratnya.
- Pekatkan larutan dengan cara menguapkan larutan tapi jangan sampai
terbentuk endapan (bila terbentuk, hentikan pemanasan dan tambah setetes
demi setetes akuades sampai larut lagi).
- Tambahkan setetes demi setetes asam sulfat pekat sambil diaduk hingga
terbentuk kristal jarum. Bantu dengan pendinginan bila perlu atau
penambahan sedikit etanol.
- Saring endapan yang terbentuk kemudian keringkan.
- Timbang kristal yang terbentuk
Uji Hasil
a. Uji titik leleh
Bandingkan dengan titik leleh pada literatur
b. Uji Kimiawi
Larutkan sedikit kristal hasil sintesa dalam asam sulfat dan tetesi dengan KCNS 1
M. Lihat apakah ada perubahan warna ?
TUGAS
1. Apa fungsi pentanuran? Tulis persamaan reaksinya !
2. Pada saat ditambah akuades, impuritis apa yang tidak larut ? Tulis persamaan
reaksi untuk impuritis dan gamping
15
--------------------------------------
16
PERCOBAAN VI
PEMBUATAN KALSIUM KLORIDA DARI BATU GAMPING
Pendahuluan
Kalsium adalah logam yang lunak, tetapi sedikit lebih keras dari pada timah,
mudah ditempa dan ditekan. Oleh karena logam ini didapatkan dalam bentuk
persenyawaan yang mengandung nitrogen, sehingga untuk memperolehnya logam
kalsium murni sangat sulit. Biasanya untuk mendapatkan logam kalsium dengan jalan
elektrolisa terhadap leburan kalsium klorida murni.
Logam kalsium sangat reaktiv, bereaksi dengan halogen dan hidrogen masing-
masing membentuk senyawa halidanya dan hidridanya.
Ca +Cl2 CaCl2
Ca +H2 CaH2
Pada temperatur tinggi, kalsium mereduksi sebagian besar logam, maka kalsium
banyak dipakai sebagai reduktor dalam pembuatan logam-logam Cu, Fe, Ni dan Pb.
Dan juga dipakai untuk membuat logam campuran.
Kalsium klorida banyak terdapat pada Tachydrite. Secara teknis kalisum klorida
diperoleh dari hasil samping dari pembuatan Natrium bikarbonat dengan proses
solvay. Dapat juga diperoleh dengan jalan melarutkan (Ca(OH)2) atau CaCO3 dalam
HCl.
Kalsium klorida dalam bentuk anhidrous banyak digunakan sebagai bahan pengering.
Sifat kalsium klorida adalah asam sehingga kalsium klorida juga dapat mempercepat
terjadinya proses korosi pada besi.
Tujuan Percobaan
Untuk mempelajari cara pembuatan kalsium klorida dari batu gamping.
Alat dan Bahan
c. Alat-alat yang dipergunakan
- Oven
17
- Melting point
- Tanur
- Buret
- Ayakan 100 mesh
- Gelas beker 250 mL
- Gelas ukur 100 mL
- Satu set penyaring vacum
- Tabung reaksi
- Sendok tula
- Mortar
- Neraca analitik
- Gelas arloji
- Erlenmeyer 250 mL
d. Bahan-bahan yang dipergunakan
- Batu gamping
- Asam klorida
- Aquades
- Indikator pp
- Asam sulfat
- Natrium hidroksida
- Asam oksalat
- Kalium tiosianat
- Kalsium klorida
Cara Kerja
- Timbang 5,0 g batu gamping yang sudah ditumbuk halus (kira-kira 100 mesh),
kemudian ditanur pada suhu 900
0
C selama 1 jam.
- Rendamlah serbuk hasil penanuran dengan 50 mL akuades selama 10 menit.
Saring dan diambil filtratnya.
- Ditambahkan HCl pekat 25 mL
- Sating endapan yang terbentuk
- Keringkan kristal yang terbentuk dan ditimbang
18
Uji Hasil
c. Uji titik leleh
Bandingkan dengan titik leleh pada literatur
d. Uji Kimiawi
Larutkan sedikit kristal hasil sintesa dalam asam sulfat dan tetesi dengan KCNS 1
M. Lihat ada perubahan warna.
Anda mungkin juga menyukai
- Makalah CaSO4Dokumen13 halamanMakalah CaSO4limaduaBelum ada peringkat
- Laporan Praktikum Kimia Organik Sintesis Asam Oksalat Dari Sekam PadiDokumen7 halamanLaporan Praktikum Kimia Organik Sintesis Asam Oksalat Dari Sekam PadiRizky WidyastariBelum ada peringkat
- Pembuatan Kalsium Oksalat HidratDokumen19 halamanPembuatan Kalsium Oksalat HidratAfhryma Ezha0% (1)
- Laporan Praktikum Kimia Anorganik Pembuatan Silika Gel PDFDokumen5 halamanLaporan Praktikum Kimia Anorganik Pembuatan Silika Gel PDFRizky Widyastari100% (1)
- Resume KALSIUM SULFAT PADA BATU GAMPINGDokumen2 halamanResume KALSIUM SULFAT PADA BATU GAMPINGuly ghaningBelum ada peringkat
- Hidrolisis Metil Salisilat Punya InyolDokumen10 halamanHidrolisis Metil Salisilat Punya InyolSiapa SajaBelum ada peringkat
- Sintesis Kloropentaamin Nikel SulfatDokumen13 halamanSintesis Kloropentaamin Nikel SulfatNurul Hasana AkmarBelum ada peringkat
- PEMBENTUKAN KALSIUM SULFATDokumen6 halamanPEMBENTUKAN KALSIUM SULFATRahmi Dini GunawatiBelum ada peringkat
- Penetapan Kadar KalsiumDokumen11 halamanPenetapan Kadar KalsiumTika LovCom SepriantiBelum ada peringkat
- Pembuatan Asam Oksalat Dari Sekam PadiDokumen6 halamanPembuatan Asam Oksalat Dari Sekam PadiReza FalepiBelum ada peringkat
- Pembuatan Asam OksaladDokumen2 halamanPembuatan Asam Oksaladsubagyo 2018Belum ada peringkat
- Objek 7Dokumen17 halamanObjek 7Riefkyansyah PutraBelum ada peringkat
- Laporan Sementara Praktikum Anorganik IDokumen7 halamanLaporan Sementara Praktikum Anorganik IMarena ThalitaBelum ada peringkat
- KALSULFDokumen9 halamanKALSULFNuning SubowoBelum ada peringkat
- Analisis Kualitatif Batuan Dengan KalsiumDokumen5 halamanAnalisis Kualitatif Batuan Dengan KalsiumAldo Andrian PangestuBelum ada peringkat
- Batu GampingDokumen2 halamanBatu GampingPutri PpaBelum ada peringkat
- Pembuatan Kalsium Sulfat Dari Batu GampingDokumen13 halamanPembuatan Kalsium Sulfat Dari Batu GampingNandha Van SolangBelum ada peringkat
- Laporan Praktikum Kimia Anorganik I1Dokumen14 halamanLaporan Praktikum Kimia Anorganik I1Nur AmaliaBelum ada peringkat
- Laporan Praktikum Pembuatan TawasDokumen11 halamanLaporan Praktikum Pembuatan TawasANNISA ZAHRA RAMADHANBelum ada peringkat
- Pembuatan CaSO4Dokumen10 halamanPembuatan CaSO4rahmadanBelum ada peringkat
- Pembuatan Kalsium Oksalat HidratDokumen18 halamanPembuatan Kalsium Oksalat HidratSalmi SepriantiBelum ada peringkat
- ALUMUNIUM SULFATDokumen14 halamanALUMUNIUM SULFATRomy Muchamad Rizky100% (1)
- Asam OksalatDokumen4 halamanAsam OksalatShofia RahmiBelum ada peringkat
- Diktat Praktikum 1Dokumen19 halamanDiktat Praktikum 1putriadriasalsabilaBelum ada peringkat
- Lap. Limbah I ADokumen41 halamanLap. Limbah I ANuhiyahBelum ada peringkat
- Embuatan Garam Kompleks Tetra Amin Tembaga (Ii)Dokumen19 halamanEmbuatan Garam Kompleks Tetra Amin Tembaga (Ii)Ade NurBelum ada peringkat
- Laporan Pembuatan Tawas FIXDokumen23 halamanLaporan Pembuatan Tawas FIXAnonymous vjTWskvBelum ada peringkat
- Larutan Kimia PraktikumDokumen16 halamanLarutan Kimia PraktikumAri Rizki ChucoBelum ada peringkat
- Kalsium SulfatDokumen4 halamanKalsium SulfatKATYABelum ada peringkat
- Sintesis Kristal AlumDokumen5 halamanSintesis Kristal AlumFajar RizkiBelum ada peringkat
- Sophia Az-Zahro S - 104221015 - Do Dan Nilai PermanganatDokumen11 halamanSophia Az-Zahro S - 104221015 - Do Dan Nilai PermanganatfiaBelum ada peringkat
- Batu Gamping'Dokumen6 halamanBatu Gamping'Melan Enggal DwiartiBelum ada peringkat
- Pemanfaatan SdmeDokumen3 halamanPemanfaatan Sdmeputri ariskaBelum ada peringkat
- 5 - 6107222991291025964 (1) - DikompresiDokumen6 halaman5 - 6107222991291025964 (1) - Dikompresiathira jihadi160Belum ada peringkat
- Laporan PraktikDokumen6 halamanLaporan PraktikDinda Ristiani PutriBelum ada peringkat
- LAPORAN TETAP Tawas AlumuniumDokumen11 halamanLAPORAN TETAP Tawas AlumuniumYunika Marsyah putriBelum ada peringkat
- Tawas Potassium KromiumDokumen13 halamanTawas Potassium KromiumAyu AnggrainiBelum ada peringkat
- Pembuatan Kalsium Sulfat Dari Batu GampiDokumen6 halamanPembuatan Kalsium Sulfat Dari Batu GampilimaduaBelum ada peringkat
- laprak5anor_1Dokumen6 halamanlaprak5anor_1Efrin SitumorangBelum ada peringkat
- Pembuatan Tawas Dari Aluminium FoilDokumen6 halamanPembuatan Tawas Dari Aluminium Foilmashfufatul ilmaBelum ada peringkat
- Asam OksalatDokumen4 halamanAsam OksalatMuhamad Laksmana WibowoBelum ada peringkat
- Laporan Percobaan Anorganik KalsiumDokumen25 halamanLaporan Percobaan Anorganik KalsiumTresia Anita SariBelum ada peringkat
- Asam OksalatDokumen15 halamanAsam OksalatFujian RatuBelum ada peringkat
- Laporan Pengolahan Limbah Analisa Kualitatif Air Proses TekstilDokumen56 halamanLaporan Pengolahan Limbah Analisa Kualitatif Air Proses Tekstilfasya yakarimaBelum ada peringkat
- Taman Kimia InteraktifDokumen16 halamanTaman Kimia Interaktifkarim kasmudinBelum ada peringkat
- Kalsium Sulfat (Makalah)Dokumen23 halamanKalsium Sulfat (Makalah)indriani debora100% (1)
- P-3. PermanganometriDokumen3 halamanP-3. PermanganometriBela YuniBelum ada peringkat
- Panduan Analisis Senyawa KompleksDokumen20 halamanPanduan Analisis Senyawa KompleksIman Yoshua Kurniawan PurbaBelum ada peringkat
- Latihan Soal GravimetriDokumen1 halamanLatihan Soal GravimetriAfny Surya Fadhillatul ChairBelum ada peringkat
- Pembuatan Natrium HidroksidaDokumen19 halamanPembuatan Natrium HidroksidakholiqBelum ada peringkat
- Silika Gel Limbah KacaDokumen7 halamanSilika Gel Limbah KacaNisa Mutia PaniBelum ada peringkat
- Pembuatan Tawas Dari Limbah Alumunium FoilDokumen13 halamanPembuatan Tawas Dari Limbah Alumunium FoilNaufal SyariefBelum ada peringkat
- Kimia Fisik 2Dokumen15 halamanKimia Fisik 2Milda Nurmalia SopaBelum ada peringkat
- Bella Permatasari - Pretest Kimia 1 Titrasi Redok1Dokumen4 halamanBella Permatasari - Pretest Kimia 1 Titrasi Redok1Bella PermatasariBelum ada peringkat
- Penuntun Teknik Pengolahan Rumput LautDokumen8 halamanPenuntun Teknik Pengolahan Rumput LautFachreza FarhamBelum ada peringkat
- Pembuatan Tawas (Alum) Dari Aluminium FoilDokumen4 halamanPembuatan Tawas (Alum) Dari Aluminium FoilPutri Dewi Mailya FatimahBelum ada peringkat
- Bahan Kimia HalusDokumen10 halamanBahan Kimia HalusRiskaBelum ada peringkat
- Pembuatan Kalium Aluminium Sulfat2Dokumen9 halamanPembuatan Kalium Aluminium Sulfat2Muhammad Syarif HidayatullahBelum ada peringkat
- Neraca Massa Tanpa Reaksi Kimia - 2Dokumen11 halamanNeraca Massa Tanpa Reaksi Kimia - 2AasNurhasanah100% (2)
- Cuso4 JadiDokumen14 halamanCuso4 JadiAasNurhasanahBelum ada peringkat
- Koligatif LarutanDokumen17 halamanKoligatif LarutanAasNurhasanahBelum ada peringkat
- PolariDokumen2 halamanPolariAasNurhasanahBelum ada peringkat
- Langkah Kerja GCDokumen5 halamanLangkah Kerja GCAasNurhasanahBelum ada peringkat
- PolariDokumen2 halamanPolariAasNurhasanahBelum ada peringkat
- Kesetimbangan IonDokumen23 halamanKesetimbangan IonAasNurhasanahBelum ada peringkat
- Kurva SpektrofotometriDokumen2 halamanKurva SpektrofotometriAasNurhasanahBelum ada peringkat
- 02 Dasar Dasar Instrumentasi Proses3Dokumen75 halaman02 Dasar Dasar Instrumentasi Proses3Chory AinurrivaBelum ada peringkat
- Bab 1-2 PDFDokumen22 halamanBab 1-2 PDFwakasensei99Belum ada peringkat
- Sifat Koligatif LarutanDokumen18 halamanSifat Koligatif LarutanAasNurhasanah100% (1)