Pengenceran Larutan
Diunggah oleh
ihwan ramadhanDeskripsi Asli:
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Pengenceran Larutan
Diunggah oleh
ihwan ramadhanHak Cipta:
Format Tersedia
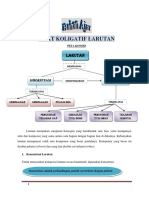
Pengenceran Larutan
Larutan didefinisikan sebagai campuran yang homogen antara 2 macam zat
ataupun lebih. Larutan terdiri dari pelarut dan zat terlarut. Umumnya zat terlarut
jumlahnya lebih sedikit dibanding pelarut. Sedangkan pelarut bisa berupa air
ataupun cairan organik seperti metanol, etanol, aseton dan lain-lain.
Pengenceran pada prinsipnya hanya menambahkan pelarut saja, sehingga jumlah
mol zat terlarut sebelum pengenceran sama dengan jumlah mol zat terlarut
sesudah pengenceran. Dengan kata lain jumlah mmol zat terlarut sebelum
pengenceran sama dengan jumlah mmol zat terlarut sesudah penegenceran atau
jumlah gr zat terlarut sebelum pengenceran sama dengan jumlah gr zat terlarut
sesudah pengenceran.
Rumus sederhana pengenceran sebagai berikut :
M1V1 = M2V2
M1 = Molaritas larutan sebelum pelarutan
V1 = Volume larutan sebelum pelarutan
M2 = Molaritas larutan sesudah pelarutan
V2 = Volume Molaritas larutan sesudah pelarutan
Misal jika kita akan membuat 500 ml HCl 2 M menggunakan HCl 4 M maka
penggunaan rumus pengencerannya adalah 4 M x V1 = 2 M x 500 ml
maka V1 = 250 ml, artinya ambil HCl 4 M sebanyak 250 ml addkan dengan air
hingga 500 ml. Sedang pada praktek pengencerannya : masukkan air dulu sebanyak
kurang dari 250 ml baru ditambahkan 250 ml HCl 4 M lalu tinggal diaddkan dengan
air hingga batas labu takar 500 ml. Praktek perlakuan seperti ini dimaksudkan agar
tidak menimbulkan letupan untuk pengenceran asam pekat.
Prinsip Cara Mengencerkan
1. Lakukan perhitungan pengenceran
2. Masukan larutan pekat ke labu takar (dengan pemipetan)
3. Tambahkan pelarut sampai leher labu takar
4. Gojok hingga homogen
5. Tambahkan pelarut sampai batas
6. Tutup dan gojok lagi
Alat Pengenceran
Labu takar berbagai ukuran
Cara pengenceran larutan bisa menggunakan alat pipet atau labu takar.
Penggunaan labu takar akan lebih tepat dalam penaraan volume. Bila
menggunakan labu takar, rawat alat dengan cara mencuci dengan sabun lunak
dan bilas dengan air kran diikuti akuades. Kemudian biarkan kering sebelum
digunakan kembali. Pengeringan labu takar jangan didalam oven.
Pembacaan Miniskus
1. Letakkan labu takar pada tempat datar
2. Posisi mata sejajar dengan tanda batas
3. Untuk bentuk cekung, batas bawah cekungan tepat pada garis batas (misal
air)
4. Untuk cembung, batas atas cembungan tepat pada garis batas (misal Hg)
Beberapa satuan konsentrasi
Jika membuat campuran konsentrasi yang berbeda, rumusnya seperti ini :
Fraksi mol (X) : perbandingan jumlah mol suatu zat dalam larutan terhadap
jumlah mol seluruh zat dalam larutan.
Kemolaran (M) : jumlah mol zat terlarut dalam per liter larutan.
Kemolalan (m) : jumlah mol zat terlarut dalam per 1000 gram penaraan
bobot pelarut.
Kenormalan (N) : jumlah grek zat terlarut dalam perlliter larutan.
Persentase (%) : jumlah gram zat terlarut dalam tiap 100 ml larutan atau
100 gr penaraan bobot.
Untuk persentase, rumus perhitungan begini :
gram zat terlarut x 100 %
% = ------------------------------
gram larutan
(jika satuannya % b/b) ; (baca : persen berat per berat)
macam satuan persen lain :
% b/v (berat per volume)
% v/b (volume per berat)
% v/v (volume per volume)
X = mol suatu zat : mol seluruh zat
M = mol : liter = mmol : ml
M = (1000 : p) X (gram : BM)
N = grek : liter = mgrek : ml
Grek = mol x jumlah H+ atau OH-
Larutan Elektrolit
Definisinya adalah suatu zat yang jika dilarutkan ke dalam air akan terurai menjadi
ion-ion (terionisasi) sehingga dapat menghantarkan listrik.
Elektrolit kuat akan terurai seluruh zat menjadi ion-ion (terionisasi sempurna)
sedang elektrolit lemah tidak mampu menguraikan seluruh zat dalam air menjadi
ion-ion artinya hanya terionisasi sebagian saja.
Contoh elektrolit kuat antara lain asam-asam kuat ( asam halogen, HNO3, H2SO4 ),
basa-basa kuat ( basa alkali, Sr(OH)2, Ba(OH)2 ). Untuk bentuk garam, hampir
semuanya merupakan elektrolit kuat. Salah satu ciri dari elektrolit kuat adalah
mempunyai reaksi berkesudahan (berlangsung sempurna ke arah kanan).
Sedang untuk elektrolit lemah contohnya adalah asam-asam lemah, basa-basa
lemah. Untuk garam yang tergolong elektrolit lemah adalah garam merkuri (II).
Elektrolit lemah mempunyai reaksinya kesetimbangan (elektrolit hanya terionisasi
sebagian).
V1 M1 + V2M2
M camp = -------------------
V1 + V2
(http://lansida.blogspot.com/2010/10/pengenceran-larutan.html)
Anda mungkin juga menyukai
- OPTIMASI PENGENCERANDokumen8 halamanOPTIMASI PENGENCERANIsmail Nur20% (5)
- Molalitas Dan Fraksi MolDokumen12 halamanMolalitas Dan Fraksi MolAbimanyu KartodikromoBelum ada peringkat
- 5 Jurnal KimiaDokumen28 halaman5 Jurnal KimiaGarry Yonathan ManurungBelum ada peringkat
- Normalitas, Molaritas Dan MolalitasDokumen10 halamanNormalitas, Molaritas Dan MolalitasboelloversBelum ada peringkat
- Pengenceran LarutanDokumen3 halamanPengenceran LarutanRezza PachruraziBelum ada peringkat
- Molaritas, Normalitas, Dan Pengenceran LarutanDokumen6 halamanMolaritas, Normalitas, Dan Pengenceran LarutanNOVA LINDA Y SINAGABelum ada peringkat
- Faktor PengenceranDokumen8 halamanFaktor Pengencerandiah ayu romadhaniBelum ada peringkat
- Perhitungan Molaritas Dan Molalitas Larutan DariDokumen31 halamanPerhitungan Molaritas Dan Molalitas Larutan DariElizabetz Erma100% (1)
- Cara Mengencerkan Larutan dan Rumus PengenceranDokumen3 halamanCara Mengencerkan Larutan dan Rumus PengenceranJoshua Robinson0% (1)
- Tugas Kimia Larutan Dan Koloid (Repaired)Dokumen35 halamanTugas Kimia Larutan Dan Koloid (Repaired)edisBelum ada peringkat
- 1-Kimia LarutanDokumen17 halaman1-Kimia LarutanZhe' Fitheighta HalizaizzaluphnoorsaypanjogerBelum ada peringkat
- Perberdaan MOLARITAS, MOLALITASDokumen8 halamanPerberdaan MOLARITAS, MOLALITASHendri FirmansyahBelum ada peringkat
- Pembuatan LarutanDokumen23 halamanPembuatan LarutanIrvandar NurviandyBelum ada peringkat
- Larutan Dan KelarutanDokumen64 halamanLarutan Dan KelarutanDangsony DangBelum ada peringkat
- Larutan Dan Kelarutan Part 1Dokumen58 halamanLarutan Dan Kelarutan Part 1unarimaBelum ada peringkat
- 3.larutan&cairan Tubuh ManusiaDokumen37 halaman3.larutan&cairan Tubuh ManusiaRendy AlamsyahBelum ada peringkat
- p12 - Larutan Elektrolit - NonelektrolitDokumen36 halamanp12 - Larutan Elektrolit - NonelektrolitichaBelum ada peringkat
- Bab 3 LarutanDokumen16 halamanBab 3 LarutanniaaparamitaBelum ada peringkat
- SOLUTIONSDokumen33 halamanSOLUTIONSFAUZAN HANIF AL FIKRI FAUZAN HANIF AL FIKRIBelum ada peringkat
- JENIS LARUTANDokumen5 halamanJENIS LARUTANUlylhilmiBelum ada peringkat
- LarutanDokumen22 halamanLarutanDika Virga Saputra100% (1)
- JUDUL Pembuatan LarutanDokumen18 halamanJUDUL Pembuatan LarutanDiana DewiBelum ada peringkat
- Kimia LarutanDokumen47 halamanKimia LarutanMuhammad Syendi AriansyahBelum ada peringkat
- Makalah Larutan Dan KonsentrasiDokumen7 halamanMakalah Larutan Dan KonsentrasiTri Pramana UtamaBelum ada peringkat
- Kelompok 1 Farmasi Fisika 3 Farm 2Dokumen12 halamanKelompok 1 Farmasi Fisika 3 Farm 2muhammad iqbalBelum ada peringkat
- Laporan 2 Pembuatan LarutanDokumen17 halamanLaporan 2 Pembuatan LarutanReynold Kevin0% (2)
- Tugas GamtekDokumen12 halamanTugas GamtekYuma ChaniagoBelum ada peringkat
- 8345 4.larutanDokumen16 halaman8345 4.larutanImam AbdurokhimBelum ada peringkat
- Larutan & KonsentrasiDokumen34 halamanLarutan & KonsentrasiDiluc KurniawanBelum ada peringkat
- MEMAHAMI KONSENTRASI LARUTANDokumen10 halamanMEMAHAMI KONSENTRASI LARUTANA.zhalzhabilla azzahrah AzzahrahBelum ada peringkat
- La RutanDokumen34 halamanLa Rutanwiratgoru69Belum ada peringkat
- KIMIA LARUTANDokumen17 halamanKIMIA LARUTANmonicarizkiBelum ada peringkat
- LarutanDokumen18 halamanLarutanYildi Rae AsgarBelum ada peringkat
- Modul Praktikum OSEKIM-1Dokumen20 halamanModul Praktikum OSEKIM-1Juanda FerdinalBelum ada peringkat
- Larutan Non ElektrolitDokumen167 halamanLarutan Non ElektrolitWinda Regita PratiwiBelum ada peringkat
- Larutan ALIDokumen20 halamanLarutan ALISelvi WoiyaBelum ada peringkat
- KONSENTRASIDokumen20 halamanKONSENTRASIIneffable classBelum ada peringkat
- Mol LarutanDokumen11 halamanMol LarutanmahardikaBelum ada peringkat
- MAKALAHDokumen14 halamanMAKALAHFiqri Ihsan FadhillahBelum ada peringkat
- SIFAT KOLIGATIFDokumen9 halamanSIFAT KOLIGATIFvivianBelum ada peringkat
- 1.larutan 1Dokumen43 halaman1.larutan 1SAMINUR FAUZANBelum ada peringkat
- 05 - Larutan KimiaDokumen28 halaman05 - Larutan KimiaPandu HariyantoBelum ada peringkat
- Materi Tiga: Sifat Larutan dan Kesetimbangan IonDokumen16 halamanMateri Tiga: Sifat Larutan dan Kesetimbangan Ionneneng rohayatiBelum ada peringkat
- Materi Konsentrasi LarutanDokumen11 halamanMateri Konsentrasi LarutanLeisha MireldaBelum ada peringkat
- Larutan Dan KelarutanDokumen34 halamanLarutan Dan KelarutanunarimaBelum ada peringkat
- Definisi Larutan, 24 OktoberDokumen27 halamanDefinisi Larutan, 24 OktoberHam KhoirunnisaBelum ada peringkat
- Modul Kimia IIDokumen287 halamanModul Kimia IIDhea SandrinaBelum ada peringkat
- KIMIA DASARDokumen25 halamanKIMIA DASARFahri AbdanBelum ada peringkat
- Laprak Kimia Cara Menyatakan KonsentrasiDokumen15 halamanLaprak Kimia Cara Menyatakan KonsentrasiDwitri AlyaniBelum ada peringkat
- Bab 6 LarutanDokumen30 halamanBab 6 LarutanWelly AnggrainiBelum ada peringkat
- Kel 9 Kimia UmumDokumen32 halamanKel 9 Kimia UmumTheresia LubisBelum ada peringkat
- Buku KF PDFDokumen166 halamanBuku KF PDFNovianti HABelum ada peringkat
- Pembuatan LarutanDokumen25 halamanPembuatan LarutanIvva KajalBelum ada peringkat
- Bab 9 LabDokumen7 halamanBab 9 LabPratiwi Devi KurniasihBelum ada peringkat
- 2 Konstr Larutan1Dokumen16 halaman2 Konstr Larutan1rezamaulanaBelum ada peringkat
- LarutanDokumen18 halamanLarutanDominik Dwi SatyaBelum ada peringkat
- Larutan 1 1Dokumen22 halamanLarutan 1 1Destria MaheswariBelum ada peringkat
- Lapres PEMBUATAN LARUTANDokumen23 halamanLapres PEMBUATAN LARUTANFebri Nanda PriantiningtiasBelum ada peringkat
- 1 TM Definisi Etika Bisnis Dan Komunikasi Bisnis2Dokumen22 halaman1 TM Definisi Etika Bisnis Dan Komunikasi Bisnis2Ikke CaponteBelum ada peringkat
- 010 SKKD Teknik Transmisi Tenaga Listrik BK FpupDokumen3 halaman010 SKKD Teknik Transmisi Tenaga Listrik BK Fpupihwan ramadhanBelum ada peringkat
- 4 Sistem Pernapasan ManusiaDokumen18 halaman4 Sistem Pernapasan Manusiaihwan ramadhanBelum ada peringkat
- ID Perancangan Dan Pembuatan Alat MonitorinDokumen8 halamanID Perancangan Dan Pembuatan Alat Monitorinihwan ramadhanBelum ada peringkat
- Dasar Teori Modul 1 KebreDokumen17 halamanDasar Teori Modul 1 Kebreihwan ramadhanBelum ada peringkat
- OPTIMASI PLTADokumen27 halamanOPTIMASI PLTAihwan ramadhanBelum ada peringkat
- Dasar Gambar TeknikDokumen117 halamanDasar Gambar TeknikMelly Chandra FrayektiBelum ada peringkat
- Diagnosis Peralatan Tegangan Tinggi dan Smart GridDokumen49 halamanDiagnosis Peralatan Tegangan Tinggi dan Smart Gridihwan ramadhanBelum ada peringkat
- Surat Pengantar Dari FakultasDokumen1 halamanSurat Pengantar Dari Fakultasihwan ramadhanBelum ada peringkat
- 09.1 Klasifikasi Motor Listrik DC PDFDokumen31 halaman09.1 Klasifikasi Motor Listrik DC PDFVidsvara PutraBelum ada peringkat
- Menerapkan k3Dokumen90 halamanMenerapkan k3MaNk ANuBelum ada peringkat
- PDF Metadata 20211692Dokumen1 halamanPDF Metadata 20211692ihwan ramadhanBelum ada peringkat
- Report TextDokumen3 halamanReport Textihwan ramadhanBelum ada peringkat
- Materi DescriptiveDokumen2 halamanMateri DescriptiveAyhuwrBelum ada peringkat
- Tugas Lingkugan IwanDokumen14 halamanTugas Lingkugan Iwanihwan ramadhanBelum ada peringkat
- RedoksDokumen3 halamanRedoksihwan ramadhanBelum ada peringkat
- Diposkan Oleh Shaquille Jabbar Di 05Dokumen14 halamanDiposkan Oleh Shaquille Jabbar Di 05ihwan ramadhanBelum ada peringkat
- Golongan Dan IdentifikasiDokumen2 halamanGolongan Dan Identifikasiihwan ramadhanBelum ada peringkat
- Bab 1Dokumen8 halamanBab 1ihwan ramadhanBelum ada peringkat
- Surat Pernyataan Deka MaulanaDokumen2 halamanSurat Pernyataan Deka Maulanaihwan ramadhanBelum ada peringkat
- Bab 1Dokumen8 halamanBab 1ihwan ramadhanBelum ada peringkat
- Pengertian ImanDokumen3 halamanPengertian Imanihwan ramadhanBelum ada peringkat
- Konsep Ketuhanan Dan Keimanan DalamDokumen5 halamanKonsep Ketuhanan Dan Keimanan Dalamihwan ramadhanBelum ada peringkat
- Files 891699533456Dokumen65 halamanFiles 891699533456ihwan ramadhanBelum ada peringkat
- CoverDokumen13 halamanCoverUlil AmriBelum ada peringkat