Macam Konsentrasi Larutan (Kimia
Diunggah oleh
Ria JelitaDeskripsi Asli:
Judul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
Macam Konsentrasi Larutan (Kimia
Diunggah oleh
Ria JelitaHak Cipta:
Format Tersedia
Nama : Ria Jelita Simangunsong
Nim : 4121131018
Kelas : Kimia Dik’B 2012
Macam Macam Konsentrasi Larutan (Kimia)
1. FRAKSI MOL
Fraksi mol adalah perbandingan antara jumlah mol suatu komponen dengan jumlah
mol seluruh komponen yang terdapat dalam larutan.
Fraksi mol dilambangkan dengan X.
𝑚𝑜𝑙 𝑧𝑎𝑡
X = 𝑚𝑜𝑙 𝑡𝑜𝑡𝑎𝑙
Contoh:
Suatu larutan terdiri dari 3 mol zat terlarut A dan 7 mol zat terlarut B. maka:
𝑚𝑜𝑙 𝑧𝑎𝑡 𝑚𝑜𝑙 𝑧𝑎𝑡
XA = 𝑚𝑜𝑙 𝑡𝑜𝑡𝑎𝑙 XB = 𝑚𝑜𝑙 𝑡𝑜𝑡𝑎𝑙
3 7
X = 3+7 X = 7+3
X = 0,3 X = 0,7
Maka : XA + XB = 0,3 + 0,7
=1
2. PERSENTASE
Persentase menyatakan gram zat terlarut dalam 100 gram larutan.
𝑔𝑟𝑎𝑚 𝑧𝑎𝑡
% = 𝑔𝑟𝑎𝑚 𝑙𝑎𝑟𝑢𝑡𝑎𝑛 x 100%
Contoh:
Larutan gula 5% dalam air, artinya: dalam 100 gram larutan terdapat :
𝑔𝑟𝑎𝑚 𝑧𝑎𝑡
% gula = 𝑔𝑟𝑎𝑚 𝑙𝑎𝑟𝑢𝑡𝑎𝑛 x 100%
5
% gula = 100 x 100%
% gula = 5 𝑔𝑟𝑎𝑚, maka : air = 100 – 5 = 95 gram
3. MOLALITAS (m)
Molalitas menyatakan jumlah mol zat terlarut dalam tiap kilogram pelarut atau dalam
1000 gram pelarut.
𝑚𝑜𝑙 𝑧𝑎𝑡 100 𝑔𝑟
m= atau m = x 𝑚𝑟
𝑘𝑔 𝑝
Contoh:
Hitunglah molalitas 4 gram NaOH (Mr = 40) dalam 500 gram air!
100 𝑔𝑟
m = 𝑝 x 𝑚𝑟
100 4
m= x 40
500
m = 0,2 m
4. MOLARITAS (M)
Molaritas menyatakan jumlah mol zat terlarut dalam 1 liter larutan.
𝑚𝑜𝑙 𝑧𝑎𝑡 100 𝑔𝑟
M= atau M = x 𝑚𝑟
𝐿 𝑚𝑙
Contoh:
Berapakah molaritas 9.8 gram H2SO4 (Mr= 98) dalam 250 ml larutan?
𝑚𝑜𝑙 𝑧𝑎𝑡
M=
𝐿
0,1 𝑚𝑜𝑙
M= 0,25 𝑙
M = 0,4 M
5. NORMALITAS (N)
Normalitas menyatakan jumlah mol ekivalen zat terlarut dalam 1 liter larutan.
Contoh :
Untuk asam, 1 mol ekivalennya sebanding dengan 1 mol ion H+.
Untuk basa, 1 mol ekivalennya sebanding dengan 1 mol ion OH-.
Hubungan Antara Normalitas dan Molaritas adalah :
N = M x valensi
6. Parts Per Million (ppm)
PPM didefenisikan sebagai satuan yang mirip persentase. Bila persentase gram zat
terlarut per 100 g larutan, maka ppm gram terlarut per sejuta gram larutan.
𝑚𝑎𝑠𝑠𝑎 𝑧𝑎𝑡 (𝑚𝑔)
PPM = 𝑣𝑜𝑙𝑢𝑚𝑒 (𝐿)
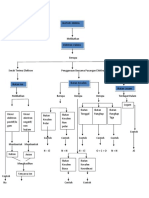
Hubungan antara satuan-satuan konsentrasi, yaitu :
M % m
Xt
Pengenceran larutan V1M1 = V2M2
Dimana : V1 = volume sebelum pengenceran
V2 = volume sesudah pengenceran
M1 = konsentrasi sebelum pengenceran
M2 = konsentrasi sudah pengenceran
V1M1+ V2M2…
Pencampuran larutan sejenis, mcamp = V1+V2…
Ada empat kuantitas yang menjelaskan konsentrasi, yaitu :
1. Konsentrasi massa
Konsentrasi massa didefinisikan sebagai massa suatu konstituen dibagi dengan
volume campuran :
2. Konsentrasi molar
Konsentrasi molar didefinisikan sebagai jumlah konstituen dibagi dengan
volume campuran :
3. Konsentrasi hitung
Konsentrasi hitung didefinisikan sebagai jumlah entitas konstituen dalam
campuran dibagi dengan volume campuran :
4. Konsentrasi volume
Konsentrasi volume didefinisikan sebagai volume konsetituen dibagi dengan
volume campuran :
Anda mungkin juga menyukai
- Perberdaan MOLARITAS, MOLALITASDokumen8 halamanPerberdaan MOLARITAS, MOLALITASHendri FirmansyahBelum ada peringkat
- Konsentrasi Larutan-64843822Dokumen3 halamanKonsentrasi Larutan-64843822annhysaa putriBelum ada peringkat
- Materi Konsentrasi LarutanDokumen11 halamanMateri Konsentrasi LarutanLeisha MireldaBelum ada peringkat
- Sifat Koligatif LarutanDokumen16 halamanSifat Koligatif LarutanRiysan OctyBelum ada peringkat
- Molar Molal Normalitas Fraksi Mol FixDokumen15 halamanMolar Molal Normalitas Fraksi Mol FixTiara ZabrinaBelum ada peringkat
- Bab 2 LarutanDokumen16 halamanBab 2 Larutannurhikmah_88Belum ada peringkat
- untuk Presentasi Kelompok X Marketing 1Dokumen19 halamanuntuk Presentasi Kelompok X Marketing 1Fabian RBelum ada peringkat
- Normalitas, Molaritas Dan MolalitasDokumen10 halamanNormalitas, Molaritas Dan MolalitasboelloversBelum ada peringkat
- Konsentrasi Larutan - Kimia XIIDokumen13 halamanKonsentrasi Larutan - Kimia XIIcigrttes aftrsxBelum ada peringkat
- Fraksi MolDokumen2 halamanFraksi MolMikhel AndersonBelum ada peringkat
- Sifat Koligatif Larutan Kelompok 4 XII IPA 3Dokumen9 halamanSifat Koligatif Larutan Kelompok 4 XII IPA 325. Qonita QotrunnadaBelum ada peringkat
- Bahan AjarDokumen15 halamanBahan AjarLinus LusiBelum ada peringkat
- KONSENTRASI LARUTANDokumen23 halamanKONSENTRASI LARUTANdiana irantoBelum ada peringkat
- KADAR ZATDokumen7 halamanKADAR ZATPutu Kuniari Komang SuniaBelum ada peringkat
- Konsentrasi LarutanDokumen28 halamanKonsentrasi LarutanYunia Qonitatin Al Masyani100% (3)
- Konsep Larutan1Dokumen26 halamanKonsep Larutan1riskyfadhilkamsyahBelum ada peringkat
- Konstentrasi LarutanDokumen18 halamanKonstentrasi Larutanrotul aliyahBelum ada peringkat
- KADAR ZAT DALAM CAMPURANDokumen11 halamanKADAR ZAT DALAM CAMPURANChiara Azra CendaniBelum ada peringkat
- MOLARITASDokumen4 halamanMOLARITASDale Carter50% (2)
- Modul IV (Larutan)Dokumen8 halamanModul IV (Larutan)Bakatotestboo100% (1)
- Modul 1 Sifat Koligatif Larutan - PendahuluanDokumen4 halamanModul 1 Sifat Koligatif Larutan - PendahuluanIlhamBelum ada peringkat
- Satuan Konsentrasi LarutanDokumen4 halamanSatuan Konsentrasi LarutanElva Rizky Auliya Virmanda IIBelum ada peringkat
- Konsentrasi LarutanDokumen24 halamanKonsentrasi LarutanJANANU SAVABelum ada peringkat
- Larutan 1 1Dokumen22 halamanLarutan 1 1Destria MaheswariBelum ada peringkat
- D. KonsentrasiDokumen18 halamanD. KonsentrasiChrisnaALBelum ada peringkat
- Konsentrasi LarutanDokumen21 halamanKonsentrasi LarutanPriyatiBelum ada peringkat
- A - 079 - Fitrida Anggraini - Tugas Kimia DasarDokumen5 halamanA - 079 - Fitrida Anggraini - Tugas Kimia DasarFaza MailalBelum ada peringkat
- Paket - 4 Laju ReaksiDokumen20 halamanPaket - 4 Laju ReaksiRohmat AliBelum ada peringkat
- SIFAT KOLIGATIFDokumen26 halamanSIFAT KOLIGATIFRegina NernereBelum ada peringkat
- Kadar ZatDokumen33 halamanKadar ZatRatih NirmaBelum ada peringkat
- Kelompok 3 Pembuatan Reagensia (REVISI)Dokumen11 halamanKelompok 3 Pembuatan Reagensia (REVISI)Emir Zacky MaulanaBelum ada peringkat
- Konsentrasi LarutanDokumen1 halamanKonsentrasi LarutanJulia MärðhìyåBelum ada peringkat
- Pertandingan PersahabatanDokumen5 halamanPertandingan PersahabatanAkbar HidayatBelum ada peringkat
- Kompetensi DasarDokumen46 halamanKompetensi DasarIta Pardede67% (6)
- STOIKIOMETRIDokumen10 halamanSTOIKIOMETRIDwi Layla RahmawatiBelum ada peringkat
- 1.sifat Koligatif LarutanDokumen13 halaman1.sifat Koligatif Larutanpololo.luwuBelum ada peringkat
- Sifat KoligatifDokumen2 halamanSifat KoligatifDenise LieBelum ada peringkat
- Konsentrasi LarutanDokumen3 halamanKonsentrasi LarutanSyarifah Humaira Al'mudhirBelum ada peringkat
- LKS Sifat Koligatif Larutan 1 BaruDokumen4 halamanLKS Sifat Koligatif Larutan 1 Barumimmaamalia13Belum ada peringkat
- InjeksiDokumen9 halamanInjeksisri ulandaryBelum ada peringkat
- Kimia Analisa Minggu IDokumen10 halamanKimia Analisa Minggu IsheilaBelum ada peringkat
- Mol LarutanDokumen11 halamanMol LarutanmahardikaBelum ada peringkat
- Tugas Makalah Sifat Koligatif SukrisnoDokumen22 halamanTugas Makalah Sifat Koligatif SukrisnoSukrisno SyukriBelum ada peringkat
- KONSENTRASI LARUTANDokumen11 halamanKONSENTRASI LARUTANmarta SandiBelum ada peringkat
- Tugas GamtekDokumen12 halamanTugas GamtekYuma ChaniagoBelum ada peringkat
- Stoikiometri PDFDokumen21 halamanStoikiometri PDFYuliaAndrianaBelum ada peringkat
- Konsentrasi LarutanDokumen13 halamanKonsentrasi LarutanHarimau 2Belum ada peringkat
- MEMAHAMI KONSENTRASI LARUTANDokumen10 halamanMEMAHAMI KONSENTRASI LARUTANA.zhalzhabilla azzahrah AzzahrahBelum ada peringkat
- Materi 10, Perhitungan Konsentrasi, Agus Sudrajat, S.si, M.TDokumen6 halamanMateri 10, Perhitungan Konsentrasi, Agus Sudrajat, S.si, M.TnurmaauliaBelum ada peringkat
- StoikiometriDokumen20 halamanStoikiometriCut riska WatiBelum ada peringkat
- Materi Sifat Koligatif Larutan Kelas XIIDokumen30 halamanMateri Sifat Koligatif Larutan Kelas XIIMaharani PutriBelum ada peringkat
- KONSEP POKOK SIFAT KOLIGATIF LARUTANDokumen25 halamanKONSEP POKOK SIFAT KOLIGATIF LARUTANAnonymous ZwkjFokJNCBelum ada peringkat
- STOIKIOMETRI LARUTANDokumen22 halamanSTOIKIOMETRI LARUTANyunus fairvryBelum ada peringkat
- Kimia DasarDokumen5 halamanKimia DasarFebronia VionaBelum ada peringkat
- Ringkasan Kimdas PDFDokumen18 halamanRingkasan Kimdas PDFAgustina BerlianaBelum ada peringkat
- LKPD Kimia 2Dokumen11 halamanLKPD Kimia 2Nadya AjaBelum ada peringkat
- 1laporan PengenceranDokumen5 halaman1laporan PengencerannikojoeBelum ada peringkat
- 4 KonsentrasiLarutan PDFDokumen19 halaman4 KonsentrasiLarutan PDFRicko SaputraBelum ada peringkat
- X Ipa Kel 3Dokumen5 halamanX Ipa Kel 3Ria JelitaBelum ada peringkat
- Kisi-Kisi Soal Ipa KLS 7 Kurikulum 2013Dokumen6 halamanKisi-Kisi Soal Ipa KLS 7 Kurikulum 2013karel_mewal77% (35)
- Ipa 9Dokumen6 halamanIpa 9Ria JelitaBelum ada peringkat
- PKDokumen11 halamanPKRia JelitaBelum ada peringkat
- Bu HeniDokumen6 halamanBu HeniRia JelitaBelum ada peringkat
- Bu HeniDokumen6 halamanBu HeniRia JelitaBelum ada peringkat
- KNBDokumen4 halamanKNBRia JelitaBelum ada peringkat
- Kompetensi Dasar IPA SMK Mawar SaronDokumen2 halamanKompetensi Dasar IPA SMK Mawar SaronRia JelitaBelum ada peringkat
- Kim XDokumen3 halamanKim XRia JelitaBelum ada peringkat
- X Ipa Kel 3Dokumen5 halamanX Ipa Kel 3Ria JelitaBelum ada peringkat
- Ipa 9Dokumen6 halamanIpa 9Ria JelitaBelum ada peringkat
- Fis XDokumen5 halamanFis XRia JelitaBelum ada peringkat
- Artikel Ai Mahmud 1Dokumen16 halamanArtikel Ai Mahmud 1m_billahBelum ada peringkat
- Kim XDokumen3 halamanKim XRia JelitaBelum ada peringkat
- X Ipa Kel 3Dokumen5 halamanX Ipa Kel 3Ria JelitaBelum ada peringkat
- X Ipa Kel 4Dokumen14 halamanX Ipa Kel 4Ria JelitaBelum ada peringkat
- X Ipa Kel 4Dokumen14 halamanX Ipa Kel 4Ria JelitaBelum ada peringkat
- Cerpen NoviDokumen3 halamanCerpen NoviRia JelitaBelum ada peringkat
- Macam Konsentrasi Larutan (KimiaDokumen4 halamanMacam Konsentrasi Larutan (KimiaRia JelitaBelum ada peringkat
- Bus 1 (Kelas 8) : Nama Guru: 1. Bu Berliana 2. Pak Adhi 3. Bu Teti 4. Lause Meliyanto 5. Bu RiaDokumen4 halamanBus 1 (Kelas 8) : Nama Guru: 1. Bu Berliana 2. Pak Adhi 3. Bu Teti 4. Lause Meliyanto 5. Bu RiaRia JelitaBelum ada peringkat
- Susunan Kepanitiaan Pensi Mawar SaronDokumen2 halamanSusunan Kepanitiaan Pensi Mawar SaronRia JelitaBelum ada peringkat
- Cerpen NoviDokumen3 halamanCerpen NoviRia JelitaBelum ada peringkat
- Bidang Kimia: Olimpiade Sains Nasional Ke IiiDokumen43 halamanBidang Kimia: Olimpiade Sains Nasional Ke IiiRia JelitaBelum ada peringkat
- Peta Konsep Ikatan KimiaDokumen2 halamanPeta Konsep Ikatan KimiaRia JelitaBelum ada peringkat
- Gambar 2Dokumen1 halamanGambar 2Ria JelitaBelum ada peringkat
- H2S Dapat Dioksidasi Oleh KMnO4 Menghasilkan Antara Lain K2SO4 Dan MnO2Dokumen11 halamanH2S Dapat Dioksidasi Oleh KMnO4 Menghasilkan Antara Lain K2SO4 Dan MnO2Ria JelitaBelum ada peringkat
- Peta Konsep Ikatan KimiaDokumen2 halamanPeta Konsep Ikatan KimiaRia Jelita100% (1)
- Lagu KebaktianDokumen2 halamanLagu KebaktianRia JelitaBelum ada peringkat
- YesDokumen1 halamanYesRia JelitaBelum ada peringkat