ADR (Adverse Drug Reaction)
Diunggah oleh
gembul0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
54 tayangan21 halamanDokumen tersebut membahas tentang reaksi obat tidak diinginkan (ADR), yang didefinisikan sebagai reaksi obat yang berbahaya dan tidak diharapkan akibat dosis obat normal. ADR dapat berupa reaksi tipe A, yang berlebihan dari efek farmakologis obat, atau reaksi tipe B yang aneh dan tidak terkait dengan dosis. Faktor-faktor seperti polifarmasi, jenis kelamin, penyakit, usia, ras
Deskripsi Asli:
adverse drug reaction
Hak Cipta
© © All Rights Reserved
Format Tersedia
PPTX, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniDokumen tersebut membahas tentang reaksi obat tidak diinginkan (ADR), yang didefinisikan sebagai reaksi obat yang berbahaya dan tidak diharapkan akibat dosis obat normal. ADR dapat berupa reaksi tipe A, yang berlebihan dari efek farmakologis obat, atau reaksi tipe B yang aneh dan tidak terkait dengan dosis. Faktor-faktor seperti polifarmasi, jenis kelamin, penyakit, usia, ras
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PPTX, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
54 tayangan21 halamanADR (Adverse Drug Reaction)
Diunggah oleh
gembulDokumen tersebut membahas tentang reaksi obat tidak diinginkan (ADR), yang didefinisikan sebagai reaksi obat yang berbahaya dan tidak diharapkan akibat dosis obat normal. ADR dapat berupa reaksi tipe A, yang berlebihan dari efek farmakologis obat, atau reaksi tipe B yang aneh dan tidak terkait dengan dosis. Faktor-faktor seperti polifarmasi, jenis kelamin, penyakit, usia, ras
Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PPTX, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 21
ADR (Adverse Drug Reaction)
Reaksi Obat Tidak Dikehendaki /
Diinginkan
Tahoma Siregar, MSi., Apt.
Definisi ADR (WHO)
• Reaksi obat tidak diinginkan sebagai respon
terhadap suatu obat yang berbahya dan tidak
diharapkan serta terjadi pada dosis lazim yang
digunakan oleh manusia untuk tujuan profilaksis,
diagnosis maupun terapi.
ADR
• Reaksi obat yang tidak diinginkan (ADR) umumnya
dapat dikelompokkan menjadi dua kelompok
utama, yaitu ;
– Reaksi tipe A (augmented) adalah reaksi yang
muncul berlebihan dimana reaksi ini terkait
dengan dosis obat yang diminum.
– Reaksi tipe B (bizzare) adalah reaksi yang aneh
dan tidak terkait sama sekali dengan dosis.
Ciri reaksi tipe A dan B adalah sebagai berikut ;
Tipe A Tipe B
Dapat diramalkan dari efek Tidak dapat diramalkan
farmakologinya
Tergantung dosis Jarang tergantung dosis
Morbiditas tinggi Morbiditas rendah
Mortalitas rendah Mortalitas tinggi
Pengurangan dosis dapat Penghentian obat, adalah cara
menangani masalah penanganannya
Angka kejadian tinggi Angka kejadian rendah
Raeksi tipe A
• Reaksi tipe A adalah kerja farmakologis
normal, tetapi meningkat.
• Reaksi tipe A dibedakan menjadi ;
–Reaksi primer, contoh ; Bradikardi oleh
penghambat adrenoreseptor beta.
–Reaksi sekunder, contoh ; mulut kering oleh
antidepresan trisiklik (aktivitas
antimuskariniknya).
Reaksi tipe B
Contoh ;
• Hemolisis oleh metildopa atau trombositopenia
oleh penghambat ACE (agiotensin Converting
Enzyme Inhibitors) terjadi tanpa terkait dengan
dosis, namun berkaitan dengan sistem metabolisme
dengan sistem imun tubuh
• Syok anafilatik oleh antibiotika, Hipertermia oleh
anestesi, Anemia aplastik oleh kloramfenikol.
Terjadi pada individu rentan terhadap obat
tersebut.
Identifikasi ADR
• Perlu diperhatikan bahwa sulit membuktikan suatu
obat mempunyai hubungan penyebab dengan
gejala yang dialami pasien.
• Informasi yang diperlukan dan bagaimana
menggunakannya dalam mengembangkan sebuah
kesimpulan tentang gejala yang tampak.
Faktor-faktor yang mempengaruhi ADR
yaitu ;
– Polifarmasi
– Jenis kelamin
– Kondisi penyakit
– Usia
– Ras
– Polimorfisa genetika
Faktor-faktor yang mempengaruhi ADR
Polifarmasi
• Polifarmasi sering pada penderita geriatri, beberapa penyakit sekaligus. Risiko ADR pada
pasien ini meningkat
Jenis kelamin
• ADR lebih sering pada wanita. Contoh akibat digoksin, captopril dan heparin. Kelainan sel
darah oleh penggunaan fenilbutazon dan kloramfenikol lebih sering pada wanita
Kondisi penyakit
• Adanya penyakit lain dapat mempengaruhi farmakokinetik atau kepekaan jaringan.
Gangguan ginjal dan hati akan meningkatkan risiko ADR. Keadaan hamil dan setelah
persalinan dapat mempengaruhi respon obat
Usia
• Lanjut usia lebih sering risiko ADR, karena sering mendapatkan obat, terjadi perubahan
farmakokinetika.
• Neonatus, khususnya prematur, risiko tinggi ADR karena metabolisme dan distribusi obat
belum berkembang sempurna
Ras dan Polimorfisa genetika
• Perbedaan ras dan genetika dapat mempengaruhi proses pengobatan. Contoh, laju
metebolisme obat dapat berbeda pada perbedaan ras dan genetika. Misalnya orang negro di
Amerika dan orang mediteranian mempunyai risiko hemolisis yang lebih tinggi bila
menggunakan obat sulfon (dapson), 4-kuinolon (siprofloksasin, ofloksasin, asam nalidiksat),
antimalaria (primakuin, kuinin) dan aspirin, karean ras tersebut sering mengalami defisiensi
enzim glukosa-6 posfat dehidrogenase (G6PD).
KRITERIA UNTUK IDENTIFIKASI ADR
• Gejala ADR diduga ?
– Buat rincian pengobatan, termasuk penggunaan obat
bebas (over the counter) serta obat tradisional
– Pertanyaan yang perlu diajukan untuk identifikasi ADR
adalah waktu, dosis, sifat permasalahan, pengalaman,
penghentian, keterulangan.
IDENTIFIKASI ADR
Waktu
• Kapan ADR muncul ? Apakah sesaat meminum obat
atau setelah lama. Bila sesaat meminum obat mudah
dikenali (contoh ; anafilaksis, orang dengan kelainan
enzim yang minum obat), tetepi bila muncul telah lama
seperti beberapa minggu-bulan atau lama setelah
dihentikan, hubungan antara obat dengan ADR
menjadi lebih sulit ditentukan (contoh ; kanker,
retinopati oleh klorokuin). Benzodiazepin setelah
dihentikan dapat terjadi gejala putus obat (withdrawal
syndrome) ditandai insomnia, ansietas, kehilangan
nafsu makan dan penurunan berat badan, tremor,
berkeringat, telinga mendengung dan gangguan
persepsi.
IDENTIFIKASI ADR
Dosis
• Apakah dosis terlalu besar ? Apakah pemakaian
obat kedua meningkatkan kadar obat pertama
didalam darah, misalnya teofilin + simetidin
(penghambat enzim).
IDENTIFIKASI ADR
Sifat permaasalahan
• Apakah ciri sifat ADR sama dengan kerja
farmakologi obat tersebut. Membantu identifikasi
tipe ADR.
IDENTIFIKASI ADR
Pengalaman
• Apakah reaksi mirip yang pernah dilaporkan
dipustaka? Pustaka memuat ADR antara lain AHFS
Drug Information, Martindale, BNF,. Tentu mungkin
saja timbul ADR yang teramati belum pernah
dilaporkan / tercatat dipustaka.
• Bila ada ADR yang teramati tentu saja farmasis /
tenaga kesehatan lain dapat melaporkan ke Badan
POM.
IDENTIFIKASI ADR
Penghentian (dechalenge) & Keterulangan
(rechalenge)
• Bila obat dihentikan apakah ADR teratasi?
Bagaimana bila obat yang menyebabkan ADR suatu
saat dipakai lagi apakah ADR muncul kembali?.
Apabila muncul kembali ADR dapat dikatakan ada
hubungan pemakaian obat dengan ADR. Setelah
penghentian tidak selalu ADR terhenti, sebab ada
efek yang irreversibel.
MENGGUNAKAN INFORMASI UNTUK MENGIDENTIFIKASI ADR
• Metode rasional menetapkan kemungkinan adanya
ADR. Pendekatan yang sistematik adalah
menggunakan algoritma. Algoritma yang dapat
dipakai antara lain algoritma FDA, lihat gambar /
bagan.
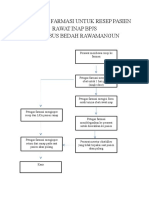
Algoritma ADR, Ibuprofen dengan gejala dispepsia
Masalah Kesehatan
Minum Ibuprofen selama 1 tahun
Gejala dispepsia
Hentikan
Gejala Kurang-Hilang
Konsumsi lagi
Gejala dispepsia muncul kembali
• Kesimpulan : terdapat hubungan yang sangat tinggi
antara pemakaian obat dan gejala yang muncul
Pencegahan ADR
1. Jangan menggunakan obat bila tidak diindikasikan
dengan jelas. Wanita hamil menggunakan obat bila
benar-benar diperlukan.
2. Alergi dan idiosinkrasi adalah penyebab penting ADR,
tanyakan pasien apakah pernah mengalami.
3. Penggunaan obat sendiri / swamedikasi ditanyakan
sebab dapat terjadi interaksi
4. Usia, penyakit hati, ginjal, faktor genetik pasien harus
diketahui.
5. Jika mungkin dengan obat yang telah dikenal, waspada
dengan obat baru.
6. Jika mungkin terjadi ADR serius, hati-hati.
Penanganan ADR
• Pengawasan obat setelah dipasarkan (post
marketing sureveilance / PMS)
• Metode PMS antara lain laporan kasus, penelitian
kohort, dan penelitian kasus kontrol. Farmasis lebih
terkait dengan pelaporan spontan.
Pelaporan Spontan ADR
• Mengapa reaksi obat tidak diinginkan perlu
dilaporkan, antara lain karena
– fase uji klinik, subjek terlalu kecil dibanding pemakai
obat, sehingga memungkinkan timbul reaksi yang tidak
terdeteksi selama uji klinis
– Anak-anak, wanita hamil, lanjut usia dan pasien
komplikasi umumnya tidak dilibatkan dalam uji klinik
• Pelaporan spontan dapat dilakukan melalui ; jurnal,
dilaporkan ke produsennya, secara lokal ke rumah
sakit, atau nasional ke BPOM dengan metode
pelaporan melalui formulir monitoring efek
samping obat (MESO)
TERIMA KASIH
Anda mungkin juga menyukai
- Swamedikasi D-2Dokumen4 halamanSwamedikasi D-2Fitria NurcahyaniBelum ada peringkat
- 12 CPD Dan ResertifikasiDokumen42 halaman12 CPD Dan ResertifikasiEdy SusiloBelum ada peringkat
- Soal UTS BU AlfinaDokumen5 halamanSoal UTS BU Alfinadewi assyah raniBelum ada peringkat
- Kelompok 6 - Penarikan, Pemusnahan, Pelaporan, Evaluasi Mutu PelayananDokumen18 halamanKelompok 6 - Penarikan, Pemusnahan, Pelaporan, Evaluasi Mutu PelayananAlika DitaBelum ada peringkat
- DTSR APOTEK WARASMORODokumen1 halamanDTSR APOTEK WARASMOROtitinBelum ada peringkat
- Layanan Klinis FarmasiDokumen4 halamanLayanan Klinis FarmasiDwi MulyaningsihBelum ada peringkat
- KONSELING OBATDokumen28 halamanKONSELING OBATnelly silitongaBelum ada peringkat
- A - Meitriyana Monita - Tabel Rencana Peningkatan Kemampuan Diri Sebagai AptDokumen2 halamanA - Meitriyana Monita - Tabel Rencana Peningkatan Kemampuan Diri Sebagai AptMeitriyana MonitaBelum ada peringkat
- Laporan PKPA Industri SRDokumen28 halamanLaporan PKPA Industri SRshelfinarara100% (1)
- NAVAL DRINK EFFERVESCENTDokumen68 halamanNAVAL DRINK EFFERVESCENTMuchamad Indung HikmawanBelum ada peringkat
- CDOB2019Dokumen69 halamanCDOB2019Daud Abadi100% (2)
- Makalah Fartis Kajian KlinisDokumen16 halamanMakalah Fartis Kajian KlinissoniawardaBelum ada peringkat
- Makalah Swamedikasi HemoroidDokumen25 halamanMakalah Swamedikasi HemoroidAfriance 24Belum ada peringkat
- SEJARAH SOHODokumen43 halamanSEJARAH SOHODita Putri Widyantoro0% (1)
- Tugas Undang Undang Dan Etika Kefarmasian Kelompok 3Dokumen27 halamanTugas Undang Undang Dan Etika Kefarmasian Kelompok 3UlfahBelum ada peringkat
- Harga dan PajakDokumen11 halamanHarga dan PajakArisandi NiarBelum ada peringkat
- TUGAS BU VITA Skor NaranjoDokumen4 halamanTUGAS BU VITA Skor Naranjoputra pratamaBelum ada peringkat
- 11,12 Prilaku AsertifDokumen55 halaman11,12 Prilaku AsertifWahyuni ayu lestariBelum ada peringkat
- OBAT ANTIBIOTIKA GENERASI KETIGADokumen6 halamanOBAT ANTIBIOTIKA GENERASI KETIGAAri Anggara100% (1)
- PCD MesoDokumen33 halamanPCD MesoervianaBelum ada peringkat
- Gambaran Penggunaan Obat Gastritis Pada Pasien Rawat Jalan Di Salah Satu Rumah Sakit Di Provinsi RiauDokumen5 halamanGambaran Penggunaan Obat Gastritis Pada Pasien Rawat Jalan Di Salah Satu Rumah Sakit Di Provinsi RiauelpakahiiBelum ada peringkat
- Arti Logo Dan Warna Lingkaran Pada Kemasan ObatDokumen12 halamanArti Logo Dan Warna Lingkaran Pada Kemasan ObatSoesi R. Setiawan100% (1)
- LAPORAN PKPA RSUDDokumen176 halamanLAPORAN PKPA RSUDnugrah_angrainiBelum ada peringkat
- Kasus 2 PBF BUDI Revisi DoneDokumen10 halamanKasus 2 PBF BUDI Revisi DoneNabila CahayaBelum ada peringkat
- Farmakoterapi Lanjut Kelompok 1Dokumen21 halamanFarmakoterapi Lanjut Kelompok 1emiks0917Belum ada peringkat
- BPJS Rawamangun Farmasi Pelayanan RanapDokumen1 halamanBPJS Rawamangun Farmasi Pelayanan RanapNila Permata Sari S.Si,AptBelum ada peringkat
- Uts Manajemen Farmasi Profesi ApotekerDokumen9 halamanUts Manajemen Farmasi Profesi ApotekerDesak SukmaBelum ada peringkat
- Modul Apotek Aveola Care (Post 6)Dokumen21 halamanModul Apotek Aveola Care (Post 6)Septian SuryoBelum ada peringkat
- SOP SwamedikasiDokumen5 halamanSOP SwamedikasiAni HistiqomahBelum ada peringkat
- Materi Permenkes 1148 & 34,30 A 21Dokumen31 halamanMateri Permenkes 1148 & 34,30 A 21Agum RahayuBelum ada peringkat
- ANGELYN wASUGAI (N014192088)Dokumen4 halamanANGELYN wASUGAI (N014192088)angelyn wasugaiBelum ada peringkat
- Tugas Khusus PBFDokumen20 halamanTugas Khusus PBFfitria lavitaBelum ada peringkat
- Farmasi SWOTDokumen18 halamanFarmasi SWOTElfrida HaznaBelum ada peringkat
- OPTIMASI ASAM URATDokumen13 halamanOPTIMASI ASAM URATLia lischeBelum ada peringkat
- Kelompok 5 - RPF-ASF - Kelas ADokumen28 halamanKelompok 5 - RPF-ASF - Kelas AAlifahBelum ada peringkat
- Compounding Dan DispensingDokumen14 halamanCompounding Dan DispensingDeccy MawonBelum ada peringkat
- Uas CND Bu Anita Pspa 34: Apoteker Menerima Dan Diminta Meracik Resep Berikut Untuk Pasien GeriatriDokumen9 halamanUas CND Bu Anita Pspa 34: Apoteker Menerima Dan Diminta Meracik Resep Berikut Untuk Pasien GeriatriR144septi fatmawatiBelum ada peringkat
- Compounding Dan DispensingDokumen44 halamanCompounding Dan DispensingnuriasatrianaBelum ada peringkat
- UU 30 AprilDokumen23 halamanUU 30 AprilRoa Mpoa100% (1)
- Jurnal Prak 4 - Kelompok 4 (Salep Clobetasol Propionate) - 1Dokumen24 halamanJurnal Prak 4 - Kelompok 4 (Salep Clobetasol Propionate) - 1Candra Fajar ArfahBelum ada peringkat
- Kasus 4Dokumen8 halamanKasus 4Vivi aja 2Belum ada peringkat
- FARMAKOTERAPI LANJUTAN Kel 2-1Dokumen29 halamanFARMAKOTERAPI LANJUTAN Kel 2-1putri sandyBelum ada peringkat
- BUD_DEFINISIDokumen4 halamanBUD_DEFINISIWisda YulihartiBelum ada peringkat
- DRPDokumen15 halamanDRPAulia Rachmadhini FaizBelum ada peringkat
- OPTIMALISASI RESEPDokumen9 halamanOPTIMALISASI RESEPdeviBelum ada peringkat
- Review Jurnal Interaksi ObatDokumen11 halamanReview Jurnal Interaksi ObatRizcy annastasyaBelum ada peringkat
- Kasus Pak WiddDokumen7 halamanKasus Pak WiddPardon MeBelum ada peringkat
- Peran Apoteker Dalam Hal Promotif Dan Rehabilitatif Penyakit HipertensiDokumen1 halamanPeran Apoteker Dalam Hal Promotif Dan Rehabilitatif Penyakit HipertensiAynita KurniawanBelum ada peringkat
- OWADokumen3 halamanOWAisabellaRamdhaBelum ada peringkat
- FI Pak WayanDokumen11 halamanFI Pak WayanRachmaBelum ada peringkat
- Mengelola Pasokan ObatDokumen18 halamanMengelola Pasokan ObatFerdyan Wana SaputraBelum ada peringkat
- Laporan PKPA Puskesmas Purbaratu TasikmalayaDokumen82 halamanLaporan PKPA Puskesmas Purbaratu TasikmalayaTami AtiBelum ada peringkat
- Contoh Lporan Pkpa RsDokumen143 halamanContoh Lporan Pkpa Rshema rianaBelum ada peringkat
- PTO dan DRP untuk Pasien dengan Multi PenyakitDokumen15 halamanPTO dan DRP untuk Pasien dengan Multi PenyakitSinta LestariBelum ada peringkat
- Farmakoekonomi 2-1Dokumen12 halamanFarmakoekonomi 2-1Yunike NgantungBelum ada peringkat
- 11 - Contoh Analisis SWOT-dikonversiDokumen8 halaman11 - Contoh Analisis SWOT-dikonversiArdhi aBelum ada peringkat
- BAB 1 PENDAHULUANDokumen6 halamanBAB 1 PENDAHULUANRita AndiyaniBelum ada peringkat
- KAUSUS GANGGUAN TULANG Dan KASUS GASTRITIS, KONSTIPASIDokumen12 halamanKAUSUS GANGGUAN TULANG Dan KASUS GASTRITIS, KONSTIPASIAndry IrfaniBelum ada peringkat
- Kuliah 10-11 ADR (Adverse Drug Reaction)Dokumen34 halamanKuliah 10-11 ADR (Adverse Drug Reaction)Laras Haryan LBelum ada peringkat
- Kuliah 10-11, ADR (Adverse Drug Reaction)Dokumen36 halamanKuliah 10-11, ADR (Adverse Drug Reaction)Fitri Utami Rizky50% (2)
- Kti Nissi - 2Dokumen10 halamanKti Nissi - 2gembulBelum ada peringkat
- Contoh Obat LasaDokumen3 halamanContoh Obat LasagembulBelum ada peringkat
- SirsakDokumen16 halamanSirsakgembulBelum ada peringkat
- Interaksi ObatDokumen24 halamanInteraksi ObatgembulBelum ada peringkat
- INTERAKSI OBAT EKSKRESIDokumen17 halamanINTERAKSI OBAT EKSKRESIgembulBelum ada peringkat
- Kuesioner StatistikDokumen1 halamanKuesioner StatistikgembulBelum ada peringkat
- Cover AmpisilinDokumen1 halamanCover AmpisilingembulBelum ada peringkat
- Pengertian Dan Konsep Epid KeslingDokumen12 halamanPengertian Dan Konsep Epid KeslinggembulBelum ada peringkat
- FarmokognosiDokumen16 halamanFarmokognosigembulBelum ada peringkat
- Kuesioner StatistikDokumen1 halamanKuesioner StatistikgembulBelum ada peringkat
- Obat KardiovaskularDokumen50 halamanObat KardiovaskulargembulBelum ada peringkat
- Makalah k3rsDokumen39 halamanMakalah k3rsgembulBelum ada peringkat
- Proses Munculnya Dan Cara Menghilangkan JerawatDokumen6 halamanProses Munculnya Dan Cara Menghilangkan JerawatgembulBelum ada peringkat
- Tugas Farmakologi P2KDokumen24 halamanTugas Farmakologi P2KgembulBelum ada peringkat
- KOSMETOLOGIDokumen56 halamanKOSMETOLOGIgembulBelum ada peringkat
- Tugas AgamaDokumen6 halamanTugas AgamagembulBelum ada peringkat
- BAB - Dapus AmpisilinDokumen18 halamanBAB - Dapus AmpisilingembulBelum ada peringkat
- Pedoman Interpretasi Data Klinik (Kemenkes, 2011)Dokumen97 halamanPedoman Interpretasi Data Klinik (Kemenkes, 2011)Jamaluddin Ahmad0% (1)
- KULITDokumen19 halamanKULITgembulBelum ada peringkat
- JerawatDokumen21 halamanJerawatRia MardianaBelum ada peringkat
- Tugas Keaneka Ragaman Hayati Mamalia LautDokumen14 halamanTugas Keaneka Ragaman Hayati Mamalia LautgembulBelum ada peringkat
- Imunologi KankerDokumen14 halamanImunologi KankergembulBelum ada peringkat
- Instalasi Pengolahan AirDokumen14 halamanInstalasi Pengolahan AirgembulBelum ada peringkat
- Bilirubin Albumin PDFDokumen6 halamanBilirubin Albumin PDFmidori_verde29Belum ada peringkat
- INTERAKSI EKSRESIDokumen12 halamanINTERAKSI EKSRESIgembulBelum ada peringkat
- Interaksi Obat Pada Fase EkskresiDokumen25 halamanInteraksi Obat Pada Fase EkskresigembulBelum ada peringkat
- Sel Darah MerahDokumen17 halamanSel Darah MerahgembulBelum ada peringkat
- Proposal Pendirian Industri Farmasi ObatDokumen8 halamanProposal Pendirian Industri Farmasi ObatgembulBelum ada peringkat
- Defisiensi ImunDokumen18 halamanDefisiensi ImungembulBelum ada peringkat
- Tugas Farmakoterapi Lanjutan - KontrasepsiDokumen19 halamanTugas Farmakoterapi Lanjutan - KontrasepsigembulBelum ada peringkat