Sifat Zat Padat, Cair, Gas
Diunggah oleh
SRIAYU NURIANI 400 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
4 tayangan19 halamanJudul Asli
SIFAT ZAT PADAT, CAIR ,GAS
Hak Cipta
© © All Rights Reserved
Format Tersedia
PPTX, PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PPTX, PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
4 tayangan19 halamanSifat Zat Padat, Cair, Gas
Diunggah oleh
SRIAYU NURIANI 40Hak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PPTX, PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 19
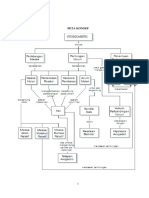
PENDAHULUAN
1. Wujud Zat (The state of matter)
2. Bentuk fisik (physical state)
3. Gaya (force)
4. Energi (energy)
5. Tekanan (pressure)
6. Suhu (Temperatur)
7. Jumlah za (amount substance)
8. Konsentrasi (concentration)
9. Stokiometri reaksi (Reaction stoichiometry)
1. Wujud zat (the state of matter)
• Gas (gas) adalah zat yang mengisi seluruh wadah.
• Cair (liquid) adalah zat yang punya permukaan dan
mengisi bagian bawah wadah.
• Padat (solid) adalah zat yang mempertahankan
bentuknya.
• Gas terdiri atas partikel yg selalu bergerak tak
beraturan. Partikel selalu bergerak dan
berbenturan dengan partikel lain, jarak antar
partikel cukup jauh sehingga interaksinya
sangat lemah.
• Cair terdiri atas partikel yg berdekatan dan
bisa saling melewati. Interaksi antar partikel
lebih intensif.
• Padat terdiri atas partikel yg berdekatan tapi
tidak bebas bergerak.
2. Keadaan fisik (physical state)
• Menjelaskan zat berkaitan dengan bentuk fisik
(gas, cair dan padat), volume, tekanan, suhu
dan jumlahnya.
• 1 kg gas hidrogen di dalam wadah volum 10
dm3 pada tekan tertentu dan suhu tertentu
adalah contoh satu keadaan (state).
• 1 kg gas hidrogen di dalam wadah 5 dm3
disebut punya keadaan (state) berbeda.
• Dua sampel zat dlm keadaan sama (the same state)
hanya jika massa, volum, tekanan dan suhu sama.
• Untuk melihat lebih detail keadaan suatu zat perlu ada
definisi untuk massa (mass), volum (volume), Gaya
(force), suhu (temperature) dan jumlah zat.
• Harus diingat bahwa massa (mass) dan berat (weight)
adalah dua besaran berbeda.
• Massa (kg) adalah ukuran kuantitas zat tidak
bergantung lokasi. Sedangkan berat (N) adalah gaya yg
dihasilkan oleh suatu benda bergantung pada gravitasi
lokasi.
• Volum (dm3) adalah ukuran tiga dimensi ruang yg
ditenpati benda.
3. Gaya (force)
• Gaya adalah kuantitas ‘vektor’ kuantitas yg punya arah
dan besaran.
Gaya = massa x percepatan F = m.a
• Percepatan benda jatuh bebas di permukaan bumi
adalah 9,81 ms-1 jadi besaran gaya yang bekerja pada
benda 1 kg adalah;
F = 1 kg . 9,81 ms-1 = 9,8 kgms-1 = 9,81 N (newton)
• Pada saat benda sejauh jarak tertentu (s) melawan gaya,
ini disebut ada kerja (work) yang dilakuka oleh benda.
Kerja = gaya x jarakW = F.s
• Untuk mengangkat benda yg punya massa 1 kg di
permukaan bumi ke arah vertikal 1 meter dibutuhkan
kerja (work) sebesar;
• W = F.s = 9,81 N x 1 m = 9,81 Nm = 9,81 joule
• Jadi dibutuhkan kerja 9,81 Juntuk mengangkat massa
1 kg vertikal sejarak 1 m di atas permukaan bumi.
4. Energi (energy)
• Energi adalah kapasitas/kemampuan untuk
melakukan kerja.
Pegas (sring) yg tertekan penuh punya
lebih banyak energi daripada pegas yang
setengah tertekan.
Benda panas punya lebih banyak eneri
daripada benda dingin.
• Satuan energi adalah joule (J), 1 J = 1 kgm2s-1
• Energi kinetik, Ek, adalah energi benda yg disebabkan
oleh gerakan. Benda massa, m, bergerak pada
kecepatan, v, maka benda punya energi kinetik;
Ek = ½ mv2
• Energi potensial, Ep, adalah energi benda yg
disebabkan oleh posisi/letak. Massa, m, pada
ketinggian, h, punya energi potensial;
Ep = mgh
• Total energi benda adalah jumlah energi kinetik dan
energi potensial. Jika tidak ada gaya lain yg bekerja
pada benda maka total energi benda konstan. Ini yg
disebut dengan hukum kekekalan energi.
5. Tekanan (pressure)
• Tekanan , P, adalah gaya, F, dibagi luas area, A.
tekanan=gaya/area P=F/A
• Tekanan atmosfer setara dengan beban 1kg logam
pada area 1 cm2.
• Tekanan dalam air laut pada kedalaman 100m
tekanan10 kali lebih besar daripada di permukaan
air.
• Satuan SI untuk tekanan adalah pascal (Pa)
1 Pa = 1 Nm-2 = 1 kgm-1s-2
pascal, Pa 1 Pa = 1 Nm-2
bar 1 bar = 105 Pa
Atmosfer, atm 1 atm = 101325 Pa = 1,01325 bar
Torr, 760 torr = 1 atm
• Barometer adalah alat untuk mengukur tekanan atmosfer
• Tekanan atmosfer ditentukan oleh ketinggian merkuri (Hg) di
dalam tabung kapiler;
P=ρgh dimana ρ adalah densitas, ρ=m/V
• Berapa tekanan yg disebabkan oleh air yg berada di dalam kolom
silinder ketinggian h, luas area silinder, A?
P=F/A F=mg m=ρhAg
P=mg/A P=ρhAg/A P=ρhg
6. Suhu (temperature)
• Suhu, T, adalah keadaan suatu benda yg menentukan
kearah mana energi akan mengalir bila bersentuhan
dengan benda lain.
• Energi mengalir dari benda bersuhu tinggi ke benda
bersuhu rendah. Bila dua beda tersebut suhunya
sama, maka tidak ada energi mengalir, ini disebut
dengan kesetimbangan termal.
• Suhu diukur dengan skala Celcius atau Kelvin.
T (Kelvin) = Ө (oCelcius) + 273,15
7. Jumlah zat (amount of substance)
• Jumlah zat dinyatakan dengan satuan mol.
• 1 mol zat/partikel adalah samadengan jumlah atom pada
12 g karbon-12.
• Jumlah partikel pada 12g karbon-12 adalah;
molsampel
jumlah.zat
massasatuatom
12 g 23 1
1mol 6,022 x10 mol
1,99265x10 23
• 6,022 x 10- 23 adalah konstanta Avogadro, simbol NA
• Jumlah partikel = jumlah zat x jumlah partikel per mol
N (partikel) = n (mol) x NA (partikel/mol)
• Massa sampel = jumlah zat x massa molar
m (g) = n (mol) x M (g/mol)
• Untuk mengetahui jumlah atom C di dalam 21,5 g karbon,
diketahui massa molar karbon 12,01 g/mol. Gunakan rumus
m 21,5 g
nC 1
1,79mol
M C 12,01gmol
Soal 1. Berapa jumlah molekul H2O di dalam 10 gram air?
8. Konsentrasi (concentration)
• Konsentrasi molar (molaritas) adalah jumlah
zat terlarut di dalam volum larutan yg
diketahui. n mol
MJ J
mol.dm 3
V dm3
Soal 2. 0,282 g glukosa, C6H12O6 dilarutkan di
dalam 250 cm-3 air. Berapa konsentrasi
molar larutan gula tersebut?
• Molalitas (molality) adalah jumlah zat dibagi massa
pelarut.
molsampel nsampel mol
molalitas
massa pelarut m pelarut kg
• Fraksi mol adalah rasio jumlah zat terlarut terhadap
jumlah zat pelarut.
molsampel nsampel mol
fraksimol
mol pelarut n pelarut mol
Soal 3. Berapa fraksi mol molekul glukosa
C6H12O6 di dalam larutan 0,140 M
glukosa?
Soal 4. Hitung fraksi mol sukrosa C12H22O11 di
dalam larutan 1,22 M sukrosa?
9. Stoichiometry
• Reaksi kimia harus setimbang (balance),
artinya jumlah atom harus sama pada sisi
reaktan dan sisi produk dari suatu reaksi.
CH4(g)+2O2(g)CO2(g)+2H2O(l)
• Stoichiometric coefficient adalah angka pengali
pda setiap molekul.
Soal 5. Hitung massa karbondioksida yang
dihasilkan dari pembakaran 22 gram gas
metana dengan udara berlebihan!
Anda mungkin juga menyukai
- Analisa Kadar Proksimat Pada Susu Bubuk PDFDokumen30 halamanAnalisa Kadar Proksimat Pada Susu Bubuk PDFSRIAYU NURIANI 40Belum ada peringkat
- Pengertian StoikiometriDokumen24 halamanPengertian StoikiometriWidyaBelum ada peringkat
- Konsep MolDokumen31 halamanKonsep MolPaskaBelum ada peringkat
- GgdukdfkgfDokumen97 halamanGgdukdfkgfkhafifah nanda permata sari100% (2)
- StoikiometriDokumen31 halamanStoikiometriSyalomita SihiteBelum ada peringkat
- Kimia Modul 1 - 4Dokumen10 halamanKimia Modul 1 - 4KelvinBelum ada peringkat
- StoikiometriDokumen33 halamanStoikiometriRiad DericsBelum ada peringkat
- STOIKIOMETRI BaruDokumen17 halamanSTOIKIOMETRI BarufahrulBelum ada peringkat
- Makalah StokiometriDokumen17 halamanMakalah StokiometriNona Tri AuliaBelum ada peringkat
- StokiometriDokumen29 halamanStokiometriLa AdenBelum ada peringkat
- Ramba 1-2Dokumen24 halamanRamba 1-227. SYAHRIN AZRIL IZULKHAQUEBelum ada peringkat
- Teori Energi KinetikDokumen18 halamanTeori Energi KinetikPopy ElismawatiBelum ada peringkat
- 3 - Proses Dan Variabel ProsesDokumen46 halaman3 - Proses Dan Variabel ProsesAnnisa IstiqomahBelum ada peringkat
- STOIKIOMETRIDokumen55 halamanSTOIKIOMETRINurul Aini100% (1)
- Resume Kosep MolDokumen3 halamanResume Kosep MolDwi PutriBelum ada peringkat
- StoikiometriDokumen33 halamanStoikiometriShendi SuryanaBelum ada peringkat
- KIMIA DASAR (Materi 4)Dokumen10 halamanKIMIA DASAR (Materi 4)rizkyfahlevi75Belum ada peringkat
- Modul 1 Kimia TeknikDokumen12 halamanModul 1 Kimia Teknikdes100% (1)
- STOIKIOMETRIDokumen40 halamanSTOIKIOMETRIAzmy Almas DalilaBelum ada peringkat
- Konsep MolDokumen4 halamanKonsep Molmarheaven888Belum ada peringkat
- @bab Iii StoikiometriDokumen24 halaman@bab Iii StoikiometriYoga AfdhBelum ada peringkat
- RPP Konsep MolDokumen17 halamanRPP Konsep MolfrengkiBelum ada peringkat
- WUJUD ZAT (Kelompok I Dan II)Dokumen65 halamanWUJUD ZAT (Kelompok I Dan II)Gigih Adi PambudiBelum ada peringkat
- Laporan KimiaDokumen13 halamanLaporan KimiaDwi Junita SariBelum ada peringkat
- 2 StoikiometriDokumen26 halaman2 StoikiometriMarni MarniBelum ada peringkat
- 02 StoikiometriDokumen20 halaman02 StoikiometriNur PadilaBelum ada peringkat
- StoikiometriDokumen33 halamanStoikiometriNaila syabina RachmiBelum ada peringkat
- StoikiometriDokumen35 halamanStoikiometriRevaldo AlfianBelum ada peringkat
- Stoikiometri KimiaDokumen66 halamanStoikiometri KimiaNikodemus SianturiBelum ada peringkat
- Filsafat Kimia Konsep MolDokumen17 halamanFilsafat Kimia Konsep MolFikriyanti WardaniBelum ada peringkat
- Persamaan Kimia StoikiometriDokumen30 halamanPersamaan Kimia StoikiometriErlinaBelum ada peringkat
- Wujud ZatDokumen37 halamanWujud ZatSeiei NashikinoBelum ada peringkat
- Bab 6 - Hukum Dasar Ilmu Kimia Dan Perhitungan Kimia 2Dokumen37 halamanBab 6 - Hukum Dasar Ilmu Kimia Dan Perhitungan Kimia 2Iskandar ZulBelum ada peringkat
- ATK Hari 1-1Dokumen52 halamanATK Hari 1-1Lilis Suryani PBelum ada peringkat
- Kimia FarmasiDokumen47 halamanKimia FarmasiNur HasanahBelum ada peringkat
- StoikiometriDokumen34 halamanStoikiometricicilia wolleyBelum ada peringkat
- Stoikiometri Klmpok 5Dokumen9 halamanStoikiometri Klmpok 5Wuena PinariaBelum ada peringkat
- MODUL Stoikiometri Berbasis SETSDokumen30 halamanMODUL Stoikiometri Berbasis SETSSeptry Nurjaya NingsihBelum ada peringkat
- Resume Kimia Nur Isyams S.I.DDokumen3 halamanResume Kimia Nur Isyams S.I.DPatria WibowoBelum ada peringkat
- Kimia Dasar PendahuluanDokumen61 halamanKimia Dasar PendahuluanAprilia MedatuaBelum ada peringkat
- Laporan Kimia Kalor ReaksiDokumen12 halamanLaporan Kimia Kalor Reaksimariapardede66Belum ada peringkat
- Fania 250324Dokumen14 halamanFania 250324msyahrulramdan050199Belum ada peringkat
- StoikiometriDokumen34 halamanStoikiometriYusufBelum ada peringkat
- Ringkasan Stoikiometri - Kelompok 3Dokumen23 halamanRingkasan Stoikiometri - Kelompok 3Ilham ArasyidBelum ada peringkat
- Konsep MolDokumen4 halamanKonsep MolNur-RGSBelum ada peringkat
- Lanjutan Makalah KimiaDokumen11 halamanLanjutan Makalah KimiaSteven ChoBelum ada peringkat
- StoikiometriDokumen14 halamanStoikiometriSatriani Erie ArdikallBelum ada peringkat
- Rangkuman Materi StoikiometriDokumen6 halamanRangkuman Materi StoikiometriSNurjanahBelum ada peringkat
- Sec.4 Kimia SM2Dokumen5 halamanSec.4 Kimia SM2huangchasonBelum ada peringkat
- Konsep MolDokumen44 halamanKonsep MolFarij AbdurrohmanBelum ada peringkat
- Tugas 1.2. Bahan Ajar Stoikiometri - Nurma Yunita - Imam SamodraDokumen28 halamanTugas 1.2. Bahan Ajar Stoikiometri - Nurma Yunita - Imam SamodraSMA ABBSBelum ada peringkat
- LKPD - Massa MolarDokumen4 halamanLKPD - Massa MolarrahimaBelum ada peringkat
- Wujud Zat Dan Kesetimbangan FasaDokumen61 halamanWujud Zat Dan Kesetimbangan FasaXiumin KimBelum ada peringkat
- StoikiometriDokumen27 halamanStoikiometriAgnes klon TsuBelum ada peringkat
- Sifat-Sifat Zat Cair OkDokumen24 halamanSifat-Sifat Zat Cair OkHendrik SimamoraBelum ada peringkat
- Konsep Mol PDFDokumen5 halamanKonsep Mol PDFMuhammad ImamBelum ada peringkat
- Teori Kinetik Gas - RDokumen34 halamanTeori Kinetik Gas - Rnapitupuludaniel930Belum ada peringkat
- StoikiometriDokumen30 halamanStoikiometriadi ranggaBelum ada peringkat
- 3 StoikiometriDokumen30 halaman3 Stoikiometrifajar gumelarBelum ada peringkat
- FisikaDokumen34 halamanFisikarizky raizinBelum ada peringkat
- LaktutosaDokumen10 halamanLaktutosaSRIAYU NURIANI 40Belum ada peringkat
- Maltosa (Biokimia)Dokumen11 halamanMaltosa (Biokimia)SRIAYU NURIANI 40Belum ada peringkat
- Sukrosa Tugas 1 BiokimiaDokumen9 halamanSukrosa Tugas 1 BiokimiaSRIAYU NURIANI 40Belum ada peringkat
- Polisakarida Kelompok 7Dokumen22 halamanPolisakarida Kelompok 7SRIAYU NURIANI 40Belum ada peringkat
- Kelompok 4 - Laporan Obat Dan Makanan PDFDokumen72 halamanKelompok 4 - Laporan Obat Dan Makanan PDFSRIAYU NURIANI 40Belum ada peringkat
- BAB II-Pengembilan SampelDokumen21 halamanBAB II-Pengembilan SampelSRIAYU NURIANI 40Belum ada peringkat
- Bahaya Yang Dapat Timbul Saat Berada Di LaboratoriumDokumen9 halamanBahaya Yang Dapat Timbul Saat Berada Di LaboratoriumSRIAYU NURIANI 40Belum ada peringkat
- 2-3 - Dimensi Dan SatuanDokumen10 halaman2-3 - Dimensi Dan SatuanSRIAYU NURIANI 40Belum ada peringkat