RPP 16 Lesson Plan Redox
Diunggah oleh
Debbylia AnggrainyJudul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
RPP 16 Lesson Plan Redox
Diunggah oleh
Debbylia AnggrainyHak Cipta:
Format Tersedia
RENCANA PELAKSANAAN PEMBELAJARAN
(RPP)
Sekolah : SMA Negeri 1 Purwadadi
Mata Pelajaran : Kimia
Kelas/Semester : X/2
Materi Pokok : Reaksi Oksidasi Reduksi
Sub Materi : Perkembangan Konsep Reaksi Oksidasi-Reduksi
Alokasi waktu : 6 × 45 menit
A. KOMPETENSI INTI
1. Menghayati dan mengamalkan ajaran agama yang dianutnya
2. Menghayati dan mengamalkan perilaku jujur, disiplin, tanggung jawab, peduli (gotong
royong, kerjasama, toleran, damai), santun, responsif dan pro-aktif dan menunjukkan
sikap sebagai bagian dari solusi atas berbagai permasalahan dalam berinteraksi secara
efektif dengan lingkungan sosial dan alam serta dalam menempatkan diri sebagai
cerminan bangsa dalam pergaulan dunia
3. Memahami, menerapkan, menganalisis pengetahuan faktual, konseptual, prosedural
berdasarkan rasa ingintahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan
humaniora dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban
terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada
bidang kajian yang spesifik sesuai dengan bakat dan minatnya untuk memecahkan
masalah
4. Mengolah, menalar, dan menyaji dalam ranah konkret dan ranah abstrak terkait dengan
pengembangan dari yang dipelajarinya di sekolah secara mandiri, dan mampu
menggunakan metoda sesuai kaidah keilmuan
B. KOMPETENSI DASAR DAN INDIKATOR
1.1 Menyadariadanya keteraturan struktur partikel materi sebagai wujud kebesaran Tuhan
YME dan pengetahuan tentang struktur partikel materi sebagai hasil pemikiran kreatif
manusia yang kebenarannya bersifat tentatif
2.1 Menunjukkan perilaku ilmiah (memiliki rasa ingin tahu, disiplin, jujur, objektif,
terbuka,mampu membedakan fakta dan opini,ulet, teliti, bertanggung jawab, kritis,
kreatif, inovatif, demokratis, komunikatif ) dalam merancang dan melakukan percobaan
serta berdiskusi yang diwujudkan dalam sikap sehari-hari
Indikator:
2.1.1 Menunjukkan sikap rasa ingin tahu dalam melakukan percobaan
2.1.2 Menunjukkan sikap tanggung jawab selama percobaan berlangsung
2.1.3 Menunjukkan sikap jujur dalam mengumpulkan dan mengomunikasikan data
hasil percobaan
2.1.4 Menunjukkan sikap komunikatif dalam menyampaikan data hasil percobaan
3.9 Menganalisis perkembangan konsep reaksi oksidasi-reduksi serta menentukan bilangan
oksidasi atom dalam molekul atau ion
Indikator:
3.9.1 Menganalisis beberapa reaksi yang termasuk reaksi oksidasi atau reduksi
berdasarkan keterlibatan oksigen
MGMP KIMIA Page 1
3.9.2 Mengelompokkan reaksi yang termasuk reaksi oksidasi atau reduksi berdasarkan
keterlibatan oksigen dari beberapa data reaksi oksidasi dan reduksi
3.9.3 Menjelaskan pengertian reaksi oksidasi dan reaksi reduksi berdasarkan
keterlibatan oksigen
3.9.4 Menjelaskan konsep reaksi oksidasi-reduksi berdasarkan keterlibatan elektron
melalui percobaan
3.9.5 Menjelaskan konsep reaksi oksidasi-reduksi berdasarkan perubahan bilangan
oksidasi melalui percobaan
4.9Merancang, melakukan, dan menyimpulkan serta menyajikan hasil percobaan reaksi
oksidasi-reduksi
Indikator:
4.9.1 Mengemukakan kesimpulanreaksi oksidasi-reduksi berdasarkan keterlibatan
oksigen dari data beberapa reaksi oksidasi dan reduksi
4.9.2 Melakukan percobaan reaksi oksidasi-reduksi berdasarkan konsep keterlibatan
elektron
4.9.3 Mengemukakan kesimpulan hasil percobaan reaksi oksidasi-reduksi berdasarkan
konsep keterlibatan elektron
4.9.4 Melakukan percobaan reaksi oksidasi-reduksi berdasarkan konsep perubahan
bilangan oksidasi
4.9.5 Mengemukakan kesimpulan hasil percobaan reaksi oksidasi-reduksi berdasarkan
konsep perubahan bilangan oksidasi
C. TUJUAN PEMBELAJARAN
Setelah proses mencari informasi dengan mengidentifikasi, mengamati, menanya,
berdiskusi, dan melaksanakan diharapkan peserta didik dapat:
2.1.1.1 Menunjukkan sikap rasa ingin tahu dalam melakukan percobaan
2.1.2.1 Menunjukkan sikap tanggung jawab selama percobaan berlangsung
2.1.3.1 Menunjukkan sikap jujur dalam mengumpulkan dan mengomunikasikan data
hasil percobaan
2.1.4.1 Menunjukkan sikap komunikatif dalam menyampaikan data hasil percobaan
3.9.1.1 Menganalisis beberapa reaksi yang termasuk reaksi oksidasi atau reduksi
berdasarkan keterlibatan oksigen dari beberapa data reaksi oksidasi-reduksi
melalui diskusi kelompok
3.9.2.1 Mengelompokkan reaksi yang termasuk reaksi oksidasi atau reduksi
berdasarkan keterlibatan oksigen dari beberapa data reaksi oksidasi dan reduksi
melalui diskusi kelompok
3.9.3.1 Menjelaskan pengertian reaksi oksidasi dan reaksi reduksi berdasarkan
keterlibatan oksigen melalui diskusi kelompok
3.9.4.1 Menjelaskan konsep reaksi oksidasi-reduksi berdasarkan keterlibatan elektron
melalui percobaan
3.9.5.1 Menjelaskan konsep reaksi oksidasi-reduksi berdasarkan perubahan bilangan
oksidasi melalui percobaan
MGMP KIMIA Page 2
4.9.1.1 Mengemukakan kesimpulanreaksi oksidasi-reduksi berdasarkan keterlibatan
oksigen dari data beberapa reaksi oksidasi dan reduksi melalui diskusi
kelompok
4.9.2.1 Melakukan percobaan reaksi oksidasi-reduksi berdasarkan konsep keterlibatan
elektron
4.9.3.1 Mengemukakan kesimpulan hasil percobaan reaksi oksidasi-reduksi
berdasarkan konsep keterlibatan elektron dari data hasil percobaan
4.9.4.1 Melakukan percobaan reaksi oksidasi-reduksi berdasarkan konsep perubahan
bilangan oksidasi
4.9.5.1 Mengemukakan kesimpulan hasil percobaan reaksi oksidasi-reduksi
berdasarkan konsep perubahan bilangan oksidasi
D. MATERI PEMBELAJARAN
1. Materi Pra-syarat
a. Persamaan reaksi kimia
b. Ciri-ciri reaksi kimia
2. Materi Inti
a. Faktual
Konsep reaksi oksidasi dan reduksi mengalami perkembangan dari masa ke masa
sesuai cakupan konsep yang dijelaskan. Reaksi reduksi dan oksidasi banyak terjadi di
dalam kehidupan sehari-hari, misalnya reaksi pembakaran, proses apel membusuk,
fotosintesis dan perkaratan besi.Pada awalnya konsep reaksi oksidasi-reduksi ini hanya
didefinisikan dari sudut pandang keterlibatan oksigen saja.Namun selanjutnya, ternyata
ada reaksi yang termasuk reaksi oksidasi-reduksi, yang tidak melibatkan
oksigen.Kemudian berkembanglah konsep reaksi oksidasi-reduksi berdasarkan
keterlibatan elektron.
Dua konsep reaksi oksidasi-reduksi di atas pada awalnya memandang reaksi oksidasi
dan reduksi tidak terjadi beriringan, seolah terpisah. Padahal pada kenyataannya, setiap
reaksi oksidasi akan beriringan dengan reaksi reduksi. Sehingga muncullah konsep yang
lebih luas yang mampu menjelaskan hal ini.Yaitu konsep reaksi oksidasi-reduksi
berdasarkan perubahan bilangan oksidasi.
b. Konseptual
Berdasarkan konsep keterlibatan oksigen, reaksi oksidasi didefinisikan sebagai reaksi
pengikatan/pengikatan suatu zat dengan oksigen.
Contoh reaksi oksidasi :
C(s) + O2(g) 3CO2(g)
Cu(s) + O2(g) CuO(s)
S(s) + O2(g) SO2(g)
N2(g) + O2(g) 2NO(g)
Pada reaksi di atas C mengalami oksidasi membentuk CO2. Demikian juga Cu, S,
dan N2 berturut-turut mengalami oksdiasi menjadi CuO, SO2, dan NO.
Sebaliknya reaksi pelepasan oksigen oleh suatu zat disebut reaksi reduksi. Adapun contoh
reaksi reduksi
KClO3 + 6Li(s) KCl(s) + 3Li2O(g)
2 H2O2(l) 2H2O(l) + O2(g)
MGMP KIMIA Page 3
Fe2O3(s) + C 2Fe(s) + 3CO2(g)
Al2O3(s) + 3Mg(s) 2Al(s) + 3MgO(g)
Pada reaksi diatas, KClO3 tereduksi menjadi KCl dan melepaskan oksigen. Demikian juga
pada H2O2, Fe2O3 dan Al2O3 tereduksi menjadi H2O, Fe dan Al serta melepaskan
oksigen.Konsep selanjutnya yang berkembang adalah berdasarkan keterlibatan elektron.
Di zaman yang modern ini, kita manusia semakin dimanjakan dengan berbagai
macam bentuk kemudahan.Contoh yang paling sederhana adalah remote kontrol untuk
TV, AC, dan lain-lainnya.Sejatinya, baterailah yang menjadikan barang-barang tersebut
mempunyai nilai guna sehingga bisa menjalankan fungsinya.
Betapa berpangaruhnya peranan baterai dalam kehidupan modern saat ini, utamanya
bagi mereka orang-orang yang hidup diperkotaan yang serba praktis.Sesungguhnya jika
kita meninjau lebih jauh dan lebih dalam, sebenarnya komponen zat kimia-lah yang
berpengaruh besar dibalik fenomena ini.Tanpa kehadirannya, apalah arti sebuah
smartphone, android dan gadget lainnya jika penyuplai energi pendukungnya tidak ada.
Fungsi dari baterai identik dengan fungsi accumulator atau lebih dikenal dengan
istilah aki yang terdapat pada kendaraan bermotor seperti sepeda motordan mobil.
Dua komponen penting seperti baterai dan aki merupakan salah satu bentuk
penerapan reaksi kimia dalam menghasilkan energi listrik. Reaksi kimia yang dimaksud
adalah reaksi oksidasi-reduksi (selanjutnya disebut reaksi redoks).Terjadinya reaksi redoks
juga dapat ditiknjau berdasarkan keterlibatan elektron pada reaksi tersebut.Elektron inilah
yang pada akhirnya menghantarkan arus listrik.
Konsep Reksi Redoks Berdasarkan Keterlibatan Elektron
Konsep redoks yang melibatkan transfer elektron berkembang setelah diketahui
adanya elektron dalam atom dan reaksi pembentukan senyawa ion (lihat kembali topik
ikatan ion). Sehingga, konsep reaksi redoks tidak hanya melibatkan oksigen dan hidrogen
saja.Tetapi, juga dapat ditinjau dari keterlibatan elektron.
Dalam konsep reaksi redoks berdasarkan keterlibatan elektron, reaksi pelepasan
elektron dinamakan reaksi oksidasi, sedangkan reaksi pengikatan elektron dinamakan
reaksi reduksi.
Reaksi Redoks yang Melibatkan Elektron
Gambar B1. Reaksi logam Zn dengan larutan CuSO4
Keterangan:
Gambar (1) : logam Zn dicelupkan kedalam larutan CuSO4 (biru terang)
Gambar (2) : logam Zn terkikis seiring terbentuknya logam Cu (merah) pada
permukaan lempeng logam Zn yang tercelup.
MGMP KIMIA Page 4
Gambar (3) : ion Cu2+ dalam larutan CuSO4 perlahan-lahan akan berkurang karena
tereduksi membentuk logam Cu yang ditandai dengan memudarnya warna larutan yang
sekaligus menandakan logam Zn telah teroksidasi membentuk ion Zn2+ yang tak berwarna.
Reaksi Oksidasi adalah reaksi yang disertai dengan kenaikan bilangan oksidasi
Reaksi Reduksi adalah reaksi yang disertai dengan penurunan bilangan oksidasi
Pada reaksi antara logam Zn dengan larutan CuSO4, logam Zn mengalami reaksi
oksidasi dengan melepaskan dua elektronnya sehingga membentuk ion Zn2+, sedangkan
ion Cu2+ pada larutan CuSO4 mengalami reaksi reduksi dengan mengikat 2 elektron dan
membentuk logam Cu. Penggabungan kedua proses itu dinamakan reaksi redoks.
Reaksi redoks yang terjadi antara logam Zn dan ion Cu2+ (dalam larutan CuSO4)
sebagai berikut:
Zn (s) → Zn2+(aq) + 2e- (setengah reaksi oksidasi)
Cu (aq) + 2e → Cu (s)
2+ -
(setengah reaksi reduksi)
Zn (s) + Cu2+ (aq) → Zn2+ (aq) + Cu (s) (reaksi redoks)
Pada reaksi tersebut, dua elektron dilepaskan oleh logam Zn kemudian diterima oleh
ion Cu2+.Oleh karena itu, peristiwa reaksi oksidasi selalu disertai peristiwa reaksi
reduksi.Dalam hal ini terjadi serah-terima elektron antara logam Zn dengan ion Cu2+. Pada
setiap persamaan reaksi, massa dan muatan harus setara antara ruas kanan/reaktan dan ruas
kiri/produk (akan dibahas lebih jauh pada materi “Persamaan Reaksi”)
Reaksi Oksidasi-reduksi merupakan pokok bahasan yang penting dalam ilmu
kimia. Dalam kehidupan sehari-hari, reaksi ini dapat kita jumpai pada reaksi
perkaratan pakuseperti yang terlihat pada gambar di bawah ini:
Gambar : Fenomena reaksi oksidasi-reduksi yang terjadi
pada reaksi perkaratan paku
Dengan memperhatikan perubahan bilangan oksidasi, maka:
Di dalam reaksi redoks terdapat zat-zat yang bertindak sebagai pereduksi (reduktor)
dan pengoksidasi (oksidator).
Reduktor adalah zat yang di dalam reaksi oksidasi-reduksi mengalami oksdasi dan
menyebabkan zat yang lain mengalami reduksi
Oksidator adalah zat yang di dalam reaksi oksidasi-reduksi mengalami reduksi dan
Contoh menyebabkan
: zat yang lain mengalami oksidasi
1. Reaksi oksidasi-reduksi yang terjadi pada proses perkaratan besi. Besi (Fe) berwarna
silver mengalami oksidasi menjadi besi berwarna coklat (Fe2O3) seperti yang terlihat
pada gambar :
MGMP KIMIA Page 5
Fe (s) + 3O2 (g) + 6 H2O (l) → 2Fe2O3 .3H2O (s)
Oksidator : O2
0 (Oksidasi) +3
Reduktor : Fe
0 (Reduksi) -2
2. Reaksi oksidasi-reduksi yang terjadi antara logam Zn dengan H2SO4
0 +1+6-2 +2+6-2 0 (biloks)
Zn (s) + H2SO4 (aq) → ZnSO4 (aq) + H2 (g)
Oksidator : H2SO4
0 (Oksidasi) +2
-1 (Reduksi) 0 Reduktor : Zn
c. Prosedural
Untuk mengetahui adanya keterlibatan oksigen dalam reaksi redoks bisa kita lihat
dalam reaksinya dilakukan dengan cara
C(s) + O2(g) CO2(g)
Cu(s) + O2(g) 2CuO(s)
S(s) + O2(g) SO2(g)
2KClO3 +6 Li(s) 2KCl(s) + 3Li2O(g)
2 H2O2(l) 2H2O(l) + O2(g)
2Al2O3(s) + 3Mg(s) 4Al(s) + 3MgO(g)
Pada reaksi a, unsur C mengalami oksidasi menjadi CO2, pada reaksi b, unsur Cu
mengalami oksidasi mengalami oksidasi menjadi CuO, dan unsur S mengalami oksidasi
menjadi SO2, dari reaksi a,b dan c karena melibatkan dan mengikat oksigen, diketahui
bahwa oksidasi adalah reaksi yang mengikat oksigen. Pada reaksi d, senyawa KClO3
mengalami reduksi menjadi KCl(s) dan Li2O. Reaksi e, senyawa H2O2 tereduksi menjadi
H2O dan O2, dan reaksi f mengalami reduksi menjadi Al dan MgO. Dari reaksi d,e dan f
dikarenakan melibatkan dan melepaskan oksigen diketahui bahwa reduksi adalah reaksi
yang melepaskan oksigen
3. Materi Pengayaan
Materi pengayaan berkaitan dengan kontekstual atau materi makro yang dapat siswa
temukan pada kehidupan sehari-hari. Materi pengayaan diberikan melalui wacana yang
diharapkan dapat mengandung nilai kehidupan. Berikut beberapa wacana reaksi oksidasi-
reduksi yang berkaitan dengan nilai yang akan ditanamkan.
Berikut beberapa wacana yang berkaitan dengan adanya reaksi oksidasi-reduksi
berdasarkan bilangan oksidasi yang berkaitan dengan nilai yang akan ditanamkan.
1) Penanaman Nilai Rasa Ingin Tahu
Sering terdengar besi berkarat. Pertanyaan yang muncul yakni ”mengapabesi
(Fe) bisa mengalami perkaratan?
Berdasarkan gambar yang telah diperlihatkan, siswa diharapkan mampu
membangkitkan rasa ingin tahu dengan mengkaji literatur yang berkaitan dengan
fenomena materi reaksi oksidasi-reduksi yang terjadi pada besi.
2) Penanaman Nilai Kritis
MGMP KIMIA Page 6
Jika dikaji lebih lanjut lagi, Fe bersifat elektropositif (mudah melepaskan
elektron) sehingga bilangan oksidasinya bertanda positif.
Fe dapat memiliki biloks 2, 3, 4, dan 6.Hal ini disebabkan karena perbedaan energi
elektron pada subkulit 4s dan 3d cukup kecil, sehingga elektron pada subkulit 3d juga
terlepas ketika terjadi ionisasi selain elektron padasubkulit 4s.
3) Penanaman Nilai Komunikatif
Logam murni besi sangat reaktif secarakimiawi sehingga mudah berkarat (terkorosi),
khususnya di udara yang lembab.
4) Penanaman Nilai Religius
Selain uraian yang telah dikemukakan, reaksi oksidasi-reduksi juga terjadi di dalam
tubuh, misalnya pada proses pencernaan makanan selain itu juga reaksi oksidasi-
reduksi mempunyai peranan antara lain pada baterai, penyetruman akumulator,
pemutihan pakaian, ekstraksi logam besi dan daur ulang perak.
E. STRATEGI PEMBELAJARAN
Model : Inkuiri
Pendekatan : Saintifik (5M)
Metode : Praktikum dan diskusi
F. MEDIA DAN SUMBER BELAJAR
1. Media
a. LKS (Lembar Kerja Siswa) Reaksi oksidasi dan reduksi
b. Alat tulis menulis (spidol, whiteboard, penghapus, buku tulis, pulpen)
c. Slide power point
d. Alat dan bahan praktikum:
1) Gelas kimia 50 mL
2) Gelas ukur 25 mL
3) Pipit tetes
4) Ampelas
5) Larutan CuSO4 0,5 M
6) Logam Zn
7) Pita Magnesium (Mg) 1 cm 0,3 gram
8) Larutan Asam Klorida (HCl)1 M 5 mL
9) Tabung Reaksi 1 buah
10) Spatula/ pinset 1buah
11) Korek api Secukupnya
2. Sumber Belajar
LKS, modul, dan buku referensi:
Jauhari, J.M.C. dan M. Rachmawati. 2009. Kimia 2 (SMA dan MA untuk kelas X).
Jakarta : Esis.
Sunarya, Y dan Agus Setiabudi.2009.Mudah dan Aktif Belajar Kimia I: Untuk Kelas
X SMA/MA. Jakarta: Pusat Perbukuan Departemen Pendidikan Nasional.
MGMP KIMIA Page 7
Utami, B.2009. Kimia untuk SMA/MA Kelas X. Jakarta : Pusat Perbukuan
DEPDIKNAS.
MGMP KIMIA Page 8
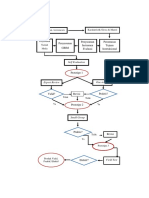
G. LANGKAH-LANGKAH PEMBELAJARAN
Pertemuan Pertama 3× 45 menit
Indikator Tahap Kegiatan Kegiatan Siswa Nilai Alokasi
Waktu
Pertemuan Pertama 1. Siswa menjawab salam pembuka yang diucapkan oleh guru
1.1.1 Kegiatan Awal 2. Siswa berdoa sebelum memulai proses pembelajaran Religius 5’
Etika Pendahuluan 3. Siswa menginformasikan temannya yang tidak hadir
4. Siswa duduk secara berkelompok sesuai arahan guru di pertemuan
sebelumnya
2.1.4 Pertanyaan 1. Siswa diajukan pertanyaan apersepsi sebelum memasukikegiatan inti Komunikatif 5’
Apersepsi pembelajaran
G: Masih ingatkah kalian, apakah ciri-ciri terjadinya reaksi kimia?
S: Perubahan warna, terjadi endapan, adanya gas, perubahan suhu
G: Dalam kehidupan sehari-hari sering kita melihat perkaratan pada besi,
perkaratan pada besi merupakan salah satu reaksi redoks
2. Siswa menyimakmotivasi mengenai pentingnya materi redoks yang akan
dipelajari dalam kehidupan
G: Adanya perkaratan besi dalam kehidupan sehari sangat merugikan
kita, perkaratan besi merupakan contoh dari reaksi redoks.
G: Menurut anda, apa salah satu komponen terpenting dari sebuah
ponsel?
3. Siswa menyimak penjelasan mengenai tujuan pembelajaran yang akan
dicapai melalui tayangan slide
MGMP KIMIA Page 9
2.1.1 G: Nah, hari ini kita akan memelajari reaksi redoks berdasarkan konsep Rasa ingin
Pertanyaan motivasi yang lain. Ini tujuan pembelajaran yang diharapkan bisa kita capai. tahu
Untuk itu, seperti yang disampaikan minggu lalu. Silakan duduk secara
berkelompok untuk melaksanakan diskusi dan praktikum untuk
memelajari materi kita kali ini
4. Siswa duduk secara berkelompok untuk melaksanakan diskusi dan
praktikum
2.1.1 Kegiatan Inti 1. Siswa mengambil LKS untuk dikerjakan secara berkelompok. Rasa ingin 30’
1. Mengamati 2. Siswa diberikanfenomenaberupa reaksi perkaratan besi tahu
3. Siswa mengamati beberapa contoh reaksi redoks tanpa melebitkan
Oksigen dan Hidrogen yang terdapat pada LKS yang telah dibagikan
atau pada slideyang ditampilkan.
2Na (s) + Cl2 (g) → 2NaCl (s)
Mg (s) + Cl2 (g) → MgCl2 (s)
2Na (s) + S (s) → Na2S (s)
2.1.1 2. Menanyakan 1. Siswa menanyakan fenomena yang dituliskan dalam LKS Rasa ingin
S: Mengapa besi bisa berakarat? tahu
S: Berdasarkan konsep redoks, termasuk oksidasi ataukah reduksi?
2.1.2 3. Mengumpulkan 1. Siswa diberikan beberapa reaksi redoks berdasarkan keterlibatan oksigen Tanggung
Data 2. Siswa diminta untuk menganalisis reaksi oksidasi dan reduksi jawab
berdasarkan keterlibatan oksigen
2.1.3 4. Mengasosiasi 1. Siswa diminta untuk menjawab pertanyaan di LKS, kemudian mencari Jujur
persamaan dari contoh-contoh reaksi yang diberikan
2.1.4 5. 1. Siswa mengemukakan pendapatnya dalam diskusi kelompok untuk Komunikatif
Mengkomu menjawab pertanyaan-pertanyaan yang ada di LKS
nikasikan 2. Siswa dari masing-masing kelompok secara acak diminta untuk
mempresentasikan hasil kerja kelompoknya
3. Siswa perwakilan dari masing-masing kelompok mempresentasikan
MGMP KIMIA Page 10
hasil diskusi kelompok tentang “Reaksi redoks berdasarkan keterlibatan
oksigen”.
4. Setelah perwakilan dari masing-masing kelompok mempresentasikan
jawabannya, guru memberi penguatan atau memberikan kesimpulan
yang jelas dari pertanyaan-pertanyaan yang ada di LKS, agar tidak ada
miskonsepsi, melengkapi jawaban yang kurang lengkap, dan memberi
kesimpulan dengan jawaban yang benar.
5. Setelah perwakilan dari masing-masing kelompok selesai
mempresentasikan hasil diskusinya, siswa lain boleh bertanya tentang
hal-hal yang belum dimengerti terkait materi yang dipresentasikan.
** Pada saat guru membimbing diskusi kelompok, guru sambil menilai :
Rasa ingin tahu dalam menjawab LKS
kerjasama siswa dalam kelompok
Sikap komunikatif dalam menarik kesimpulan saat diskusi
6. Siswa melanjutkan kegiatan dengan melakukan praktikum
Mengumpulkan Data - Siswa merancang percobaan (dibimbing oleh guru) untuk mengamati 90’
reaksi antara logam Zn dengan ion Cu2+ (dalam larutan CuSO4) dengan
memperhatikan LKS yang disediakan untuk masing-masing kelompok.
- Siswa mengumpulkan informasi mealalui buku pelajaran atau mencari
sumber belajar lainnya melalui internet.
- Siswa mengamati keadaan fisik (warna) dari Zn dan larutan CuSO4.
- Siswa melakukan percobaan reaksi redoks.
- Siswa mengamati dan mencatat hasil percobaan.
- Siswa mengerjakan LKS yang berisi soal-soal terkait dengan percobaan
yang telah dilakukan secara berkelompok.
Siswa menuliskan reaksi yang terjadi.
- Siswa mendiskusikan hasil percobaan bersama anggota kelompoknya
masing-masing.
MGMP KIMIA Page 11
Siswa menyimpulkan definisi konsep reaksi redoks berdasarkan
keterlibatan elektron.
3.9.1 Kegiatan Akhir 1. Siswa diberikan umpan balik terhadap proses dan hasil pembelajaran 5’
3.9.2 2. Siswa dibimbing untuk menyimpulkan hasil diskusi materi yang
3.9.3 dipelajari dengan memberikan pertanyaan-pertanyaan berikut
”Baiklah, sekarang saatnya kita menyimpulkan pembelajaran kita
pada hari ini.”
”Coba jelaskan pengertian dari reaksi Oksidasi dan reaksi Reduksi ?”
3. Guru menginformasikan rencana kegiatan pembelajaran untuk kegiatan
berikutnya.
”Baiklah, hari ini, kita sudah membahas Redoks berdasarkan
keterlibatan oksigen dan elektron. Pada pertemuan selanjutnya kita akan
membahas reaksi redoks berdasarkan peruabhan bilangan oksidasi”
4. Guru melakukan kegiatan tindak lanjut dengan pemberian tugas individu
yang berhubungan dengan reaksi redoks berdasarkan keterlibatan
oksigen
Guru menutup pertemuan dengan salam.
MGMP KIMIA Page 12
Pertemuan Kedua 3× 45 menit
Alokasi
Tahapan Kegiatan Kegiatan Siswa Nilai
Waktu
Kegiatan Awal - Siswa menjawab salam pembuka yang diucapkan oleh guru
- Siswa berdoa sebelum memulai proses pembelajaran
1. Etika Pendahuluan - Siswa menginformasikan temannya yang tidak hadir Religius 5 Menit
- Siswa menjawab pertanyaan guru terkait materi bilangan oksidasi yang telah
2. Apersepsi dipelajari pada pertemuan sebelumnya - Rasa ingin tahu 5 Menit
- Memotivasi siswa dengan memberikan suatu fenomena yaitu perkaratan pada besi - Religius
Nah hal ini diberikan sebagai pengantar kita masuk materi terkait dengan percobaan
reaksi redoks , dengan harapan ketika kalian telah melakukan percobaan, kalian
mampu menjelasklan kenapa besi bisa berkarat.
- Siswa memperhatikan tujuan pembelajaran yang ingin dicapai.
- Siswa mengatur kelompoknya masing-masing yang terdiri dari 4 orang.
Kegiatan Inti
1. Mengamati Siswa mengamati alat dan zat-zat yang akan digunakan dalam praktikum - Teliti 5 Menit
MGMP KIMIA Page 13
2. Menanya Siswa bertanya, apa yang terjadi jika zat tersebut direaksikan? - Rasa ingin tahu
5 menit
3. Mengumpulkan - Siswa melakukan percobaan (dibimbing guru) untukmenyelidiki terjadinya reaksi - Kerjasama 40
data reduksi-oksidasi berdasarkan bilangan oksidasi dengan memperhatikan LKS yang - Jujur Menit
disediakan.
- Siswa melakukan percobaan reaksi reduksi-oksidasi pada larutan.
- Siswa mencatat data hasil percobaan reaksi reduksi-oksidasi pada tabel hasil
pengamatan.
4. Mengasosiasi - Siswa melakukan diskusi kelompok untuk membahas terjadinya reaksi reduksi- - Kritis 40 menit
oksidasi serta menentukan zat yang bertindak sebagai reduktor dan oksidator.
5. - Tiap-tiap kelompok/perwakilan kelompok mempresentasikan hasil diskusi - Komunikatif 20
Mengkomunikasikan kelompoknya tentang terjadinya reaksi reduksi-oksidasi pada percobaan Menit
Kegiatan Akhir - Guru memberikan penguatan terkait kesimpulan yang telah dipaparkan oleh masing- - Tanggung jawab 10
masing kelompok/perwakilan kelompok. Menit
- Memberikan tugas kepada siswa untuk mempelajari materi selanjutnya.
- Berdoa dan salam penutup.
MGMP KIMIA Page 14
H. PENILAIAN HASIL PEMBELAJARAN
1. Mekanisme dan prosedur
Penilaian dilakukan dari proses dan hasil. Penilaian proses dilakukan melalui kegiatan praktikum dan diskusi. Sedangkan penilaian hasil
dilakukan melalui tes tertulis.
2. Bentuk Instrumen, Instrumen dan Pedoman Penskoran
a. Bentuk : Soal uraian
b. Instrumen : Terlampir
MENGETAHUI, Bandung, Februari 2016
Guru Mata Pelajaran
Dra. Hj Ika Yudiwastika, M.P.Kim Setia Rahmawan
196008221986032003 1200583
MGMP KIMIA Page 15
I. LAMPIRAN
LAMPIRAN I
KISI-KISI INSTRUMEN PENILAIAN PENGETAHUAN
KD INDIKATOR BUTIR SOAL RANAH KUNCI JAWABAN SKOR
3.9 3.9.1 Menganalisis reaksi Perhatikan reaksi-reaksi C4 a. Oksidasi
oksidasi dan reduksi oksidasi dan reaksi reduksi b. Reduksi
berdasarkan keterlibatan berikut ini! kemudian c. Reduksi
oksigen identifikasi manakah yang d. Oksidasi
termasuk reaksi oksidasi e. Oksidasi
atau reaksi reduksi
berdasarkan keterlibatan
oksigen !
a. 2Ba(s) + O22BaO(s)
25
b. 2Na2O(s) 4Na(s)
+ O2(g)
c. 2HgO(s)
2Hg(l) + O2(g)
d. 2Mg(s) + O2(g)
2MgO(s)
e. 2Ca(s) + O2(g)
2CaO(s)
3.9.2 Menjelaskan pengertian reaksi Jelaskan pengertian Oksidasi adalah reaksi yang mengalami pengikatan
oksidasi dan reaksi reduksi oksidasi dan reduksi oksigen
berdasarkan keterlibatan berdasarkan keterlibatan C2 Reduksi adalah reaksi yang mengalami pelepasan 20
oksigen oksigen ? oksigen
MGMP KIMIA Page 16
JENJANG
KD INDIKATOR BUTIR SOAL KUNCI JAWABAN SKOR
KOGNITIF
3.9 3.9.1 Menjelaskan konsep 1. Tuliskan reaksi C3 1. Ca2+ + 2e-→ Ca 2
reaksi oksidasi-reduksi reduksi pada ion Ca2+
berdasasrkan berdasarkan konsep
keteribatan elektron keterlibatan elektron!
melalui percobaan. 2. Tuliskan reaksi C3 2. 2Na + Cl2→ 2NaCl 3
oksidasi dan reduksi Oksidasi : 2Na → 2Na+ + 2e-
jika Na direskasikan Reduksi : Cl2 + 2e-→ 2Cl-
dengan gs Cl2!
4.9 4.9.1. Merancang percobaan 5. Kemukakan alasan 3. Sebelum direaksikan dengan larutan CuSO4,
reaksi oksidasi-reduksi anda, mengapa logam Zn terlebih dahulu diampelas untuk
berdasarkan konsep sebelum direaksikan membersihkannya dari partikel-partikel
keterlibatan elekron. dengan larutan C4 pengganggu/pengotor yang ada pada permukaan 5
CuSO4, logam Zn logam Zn.
harus diamplas
terlebih dahulu.
4.9.2. Melakukan 6. Mengapa pada reaksi 4. Karena pada larutan CuSO4, ion Cu2+ yang
percobaan reaksi logam Zn dengan memberikan warna biru perlahan-lahan akan habis
oksidasi-reduksi CuSO4 larutan yang tereduksi membentuk logam Cu yang melekat
berdasarkan konsep mulanya berwarna C4 pada logm Zn. 5
keterlibatan elektron. biru perlahan berubah
memudar? Tuliskan
reaksi yang terjad!
4.9.3. Mengemukakan 1. Tuliskan tiga contoh 5. Cu + Cl2→ CuCl2
kesimpulan hasil reaksi redoks C4 Oksidasi : Cu → Cu2+ + 2e- 9
percobaan reaksi bedasarkan konsep Reduksi : Cl2 + 2e-→ 2Cl-
MGMP KIMIA Page 17
JENJANG
KD INDIKATOR BUTIR SOAL KUNCI JAWABAN SKOR
KOGNITIF
oksidasi-reduksi keterlibatan elektron Ca + F2→ CaF2
berdasarkan konsep selain dari contoh Oksidasi : Ca → Ca2+ + 2e-
keterlibatan elektron yang telah diberikan, Reduksi : F2 + 2e-→ 2F-
kemudin tentukan zat 2Ag + Cl2→2AgCl2
yang mengalami Oksidasi : 2Ag → 2Ag+ + 2e-
reaksi oksidasi dan Reduksi : Cl2 + 2e-→ 2Cl-
reduksi!
JUMLAH 24
Kompetensi Indikator Evaluasi Jenjang Kognitif/ Skor
MGMP KIMIA Page 18
dasar No Soal
3.9Menganalisis 3.9.1 Berdasarkan data hasil percobaan di bawah ini, tentukanlah bilangan oksidasi
perkembangan Menentukan masing-masing unsur, reaksi reduksi dan reaksi oksidasinya, serta zat yang C3 100
konsep reaksi perubahan
Variabel yang
oksidasi-reduksi bilangan Percobaan
diamati
Pengamatan Persamaan Reaksi
serta oksidasi
1 Mereaksikan antara Larutan yang dihasilkan Cu(s) + AgNO3(aq) CuNO3(aq) + Ag (s)
menentukan unsur dalam Cu dengan AgNo3 berwarna bening, Cu
persamaan berubah menjadi
berwarna putih kehijau-
reaksi hijauan
redoks.
2
Mereaksikan antara Awalnya larutan Na2S2O3(aq) + 2 HCl(aq) 2NaCl(s) + H2S2O3(aq)
Na2S2O3 dengan berwarna bening setelah
HCl ditambahkan HCl, larutan
berubah menjadi putih
susu
bertindak sebagai oksidator dan reduktor?
Penilaian tes kognitif berupa tes kemampuan berkomunikasi sains siswa secara tulisan. Penilaian ini diberikan melalui latihan soal yang
terdapat didalam LKS.
Nilai = __Jumlah Skor__ x 100 Skor maksimal=100
Skor maksimal
MGMP KIMIA Page 19
LAMPIRAN 2
KISI-KISI INSTRUMEN PENILAIAN SIKAP
Indikator penilaian sikap dilakukan selama proses pembelajaran, yaitu pada saat
peserta didik melakukan praktikum dan mengomunikasikan hasil diskusi kelompoknya dan
juga saat mengomentari penampilan kelompok lain terkait praktikum dan data pengamatan.
Berikut rubrik penilaiannnya:
Sikap yang Dinilai Total Skor
Rasa Tanggung Jujur Komunikatif
No. Nama
Ingin Jawab
Tahu
1.
Dst
Indikator setiap sikap yang dinilai:
Sikap Indikator
Memperhatikan penjelasan guru
Mengumpulkan sumber informasi lain dari buku ajar dan
Rasa Ingin Tahu
penjelasan guru
Mengajukan pertanyaan kepada teman atau guru
Mengerjakan tugas individu dengan baik
Tanggung Jawab Mengerjakan tugas kelompok dengan sungguh-sungguh
Mengerjakan dan mengumpulkan tugas tepat waktu
Mencantumkan sumber rujukan
Mencatat data hasil pengamatan sesuai dengan yang
Jujur
diperoleh
Melaporkan hasil praktikum apa adanya
Mempresentasikan hasil percobaan dengan benar
Komunikatif Menyampaikan pendapat dengan jelas
Tidak memotong pembicaraan teman maupun guru
Rubrik penilaian:
Skala penilaian sikap dibuat dengan rentang nilai 1s.d 3
1= Hanya satu indikator yang muncul
2= Dua indikator yang muncul
3= Ketiga indikator muncul
Nilai = __Jumlah Skor__ x 100 Total skor maksimal=9
Total skor maksimal
MGMP KIMIA Page 20
LAMPIRAN 3
KISI-KISI INSTRUMEN PENILAIAN KETERAMPILAN
INSTRUMEN PENILAIAN KETERAMPILAN
INDIKATOR
1.9.1. Merancang percobaan reaksi oksidasi-reduksi berdasarkan konsep keterlibatan elekron.
1.9.2. Melakukan percobaan reaksi oksidasi-reduksi berdasarkan konsep keterlibatan elektron.
1.9.3. Mengemukakan kesimpulan hasil percobaan reaksi oksidasi-reduksi berdasarkan konsep keterlibatan elektron.
SKOR
No. ASPEK KINERJA YANG DINILAI JUMLAH
4 3 2 1
A. Tahap Persiapan Praktikum
1. Memeriksa kelengkapan alat yang diperlukan pada kegiatan praktikum
2. Memeriksa kelengkapan bahan yang diperlukan pada kegiatan praktikum
3. Menyiapkan peralatan yang digunakan dalam keadaan kering
B. Tahap Pelaksanaan Praktikum
4. Mengamati dan mencatat kedaan fisik bahan yang digunakan
5. Membersihkan permukaan logam Zn sebelum digunakan dengan baik
6. Mencelupkan ½ bagian logam Zn kedalam larutan CuSO4 dengan baik
7. Mengamati permukaan logam Zn yang tercelup selama reaksi berlangsung
C. Tahap Akhir Praktikum
8. Membersihkan alat yang telah digunakan pada saat praktikum
9. Mengembalikan alat dan bahan yang digunakan pada tempat semula
10. Membuang limbah praktikum pada tempatnya
11. Membuat jurnal praktikum
12. Melaporkan data hasil pengamatan praktikum reaksi redoks
13. Membuat kesimpulan tentang konsep reaksi oksidasi dan reduksi berdasarkan keterlibatan elektron
JUMLAH
MGMP KIMIA Page 21
KRITERIA PENSKORAN
4. = Sangat Baik 2. = Sedang
3 .= Baik 1. = Kurang
PEDOMAN PENILAIAN
Jumlah skor yang diperoleh
Nilai = x 100
52
RUBRIK PENILAIAN LAPORAN PRAKTIKUM
KRITERIA
SKOR
4 3 2 1
Ditulis dengan kalimat baku, Ditulis dengan kalimat Ditulis kurang fokus, Ditulis kurang spesifik,
rinci, terkait dengan topik baku, terkait dengan topik kalimat tidak baku, sebagian kalimat tidak baku, tidak
Tujuan
yang ditugaskan yang ditugaskan tidak terkait dengan topik terkait dengan topik yang
yang ditugaskan ditugaskan
Mencantumkan semua alat Mencantumkan sebagian Mencantumkan sebagian Tidak mencantumkan alat
Alat dan Bahan dan bahan yang diperlukan besar alat dan bahan yang kecil alat dan bahan yang dan bahan yang digunakan
dalam percobaan diperlukan dalam percobaan diperlukan dalam percobaan
Langkah Langkah kegiatan lengkap, Langkah kegiatan lengkap Langkah kegiatan tidak urut Tidak ada langkah kegiatan
kegiatan urut, dan rinci dan urut dan/atau tidak lengkap
Data ditabulasi secara logis Data ditabulasi secara logis Data ditabulasi Data tidak ditabulasi dan
Data dan
dan dianalisis dengan tepat dan dianalisis dengan tepat sembarangan dan dianalisis tidak dianalisis
Analisis Data
dan rinci kurang tepat
Ditulis berdasarkan hasil Ditulis berdasarkan hasil Ditulis tidak berdasarkan Tidak ada kesimpulan
Kesimpulan
analisis dan akurat analisis hasil analisis
PEDOMAN PENILAIAN
Jumlah skor yang diperoleh
Nilai = x 100
20
MGMP KIMIA Page 22
Anda mungkin juga menyukai
- RPP Sifat KoligatifDokumen19 halamanRPP Sifat KoligatifNadia Novita100% (1)
- RPP 4 SpuDokumen14 halamanRPP 4 SpueskawatiBelum ada peringkat
- KESETIMBANGAN KIMIADokumen4 halamanKESETIMBANGAN KIMIANana Dian LestariBelum ada peringkat
- Evaluasi KD 3.7Dokumen8 halamanEvaluasi KD 3.7Desi Purnama SariBelum ada peringkat
- KESETIMBANGAN KIMIADokumen3 halamanKESETIMBANGAN KIMIAGede WidnyanaBelum ada peringkat
- KIMIA XIDokumen2 halamanKIMIA XIDewi IkmahBelum ada peringkat
- RPP Kesetimbangan KimiaDokumen7 halamanRPP Kesetimbangan KimiaAfree Awan Mohamed100% (1)
- Kimia F11 - Hidrolis GaramDokumen21 halamanKimia F11 - Hidrolis GaramDina Ma'rifahBelum ada peringkat
- RPP HariyantoDokumen56 halamanRPP HariyantoGuruh Setiawan100% (4)
- Analisis Alokasi Waktu Kelas XII KimiaDokumen2 halamanAnalisis Alokasi Waktu Kelas XII KimiaIsmirawatyBelum ada peringkat
- Analisis Konsep StoikiometriDokumen4 halamanAnalisis Konsep StoikiometriHarunAsyakiriBelum ada peringkat
- RPP Kimia Spu KD 3.4 Dan 4.4Dokumen17 halamanRPP Kimia Spu KD 3.4 Dan 4.4riskaBelum ada peringkat
- GAYA ANTARMOLEKULDokumen5 halamanGAYA ANTARMOLEKULIrmaWati100% (1)
- Analisis Silabus Materi Faktor Laju ReaksiDokumen4 halamanAnalisis Silabus Materi Faktor Laju ReaksiRetno WahyuuBelum ada peringkat
- Contoh RPP TermokimiaDokumen12 halamanContoh RPP TermokimiaindriyaniBelum ada peringkat
- Miskonsepsi KoloidDokumen7 halamanMiskonsepsi KoloidSherly Aulia 2110246898Belum ada peringkat
- Korelasi DataDokumen11 halamanKorelasi DataAyulia AnnisaBelum ada peringkat
- Silabus Asam BasaDokumen2 halamanSilabus Asam BasaRyesz'z SaeryBelum ada peringkat
- RPP LAJU REAKSI 1. Fixxx ...Dokumen22 halamanRPP LAJU REAKSI 1. Fixxx ...Syachnia RaniBelum ada peringkat
- KESETIMBANGAN KIMIADokumen7 halamanKESETIMBANGAN KIMIAHerlina LinaBelum ada peringkat
- RPP - XI - 3.12 - Larutan PenyanggaDokumen5 halamanRPP - XI - 3.12 - Larutan PenyanggakunyBelum ada peringkat
- Persamaan Reaksi Kimia - Elfina SalsabilaDokumen15 halamanPersamaan Reaksi Kimia - Elfina SalsabilaElfina SalsabilaBelum ada peringkat
- RPP Materi Kesetimbangan Kimia Berbasis - PJBLDokumen16 halamanRPP Materi Kesetimbangan Kimia Berbasis - PJBLfidzaBelum ada peringkat
- RPP Senyawa Hidrokarbon (Kelas X-2)Dokumen6 halamanRPP Senyawa Hidrokarbon (Kelas X-2)zahraBelum ada peringkat
- Modul Ajar Xi Kimia 2023Dokumen44 halamanModul Ajar Xi Kimia 2023Heryanto TahirBelum ada peringkat
- RPP KD 3.15 Sistem KoloidDokumen27 halamanRPP KD 3.15 Sistem KoloidTUTIK KHARISMAYANTIBelum ada peringkat
- LKPD Hukum Dasar KimiaDokumen6 halamanLKPD Hukum Dasar KimiaDhiya Nabilah JanwarBelum ada peringkat
- LKS BiloksDokumen14 halamanLKS BiloksSetyaniBelum ada peringkat
- RPP Bilangan Kuantum 3Dokumen15 halamanRPP Bilangan Kuantum 3Aynie Chem'sBelum ada peringkat
- ENERGI KISI EKSPERIMENDokumen13 halamanENERGI KISI EKSPERIMENFaizal Muhammad ZubairBelum ada peringkat
- Silabus Kimia (KTSP)Dokumen76 halamanSilabus Kimia (KTSP)Anggi Fahrunnisa100% (1)
- Karakteristik Unsur Boron &Dokumen11 halamanKarakteristik Unsur Boron &Adinda SarahBelum ada peringkat
- RPP Bilangan OksidasiDokumen6 halamanRPP Bilangan OksidasiAnis Ma'rifatul MBelum ada peringkat
- KISI KISI SOAL HIDROKARBON Mata PelajaraDokumen6 halamanKISI KISI SOAL HIDROKARBON Mata PelajaraAmeliana FitriyantiBelum ada peringkat
- RPP Microteaching TermokimiaDokumen18 halamanRPP Microteaching TermokimiaShihhiya Noor MaliyaBelum ada peringkat
- RPP Hitungan Hub KC Dan KP 2Dokumen9 halamanRPP Hitungan Hub KC Dan KP 2NIFFI NEDIA SARIBelum ada peringkat
- RPP Kimia KesetimbanganDokumen15 halamanRPP Kimia Kesetimbangansuci hadi rahmawatiBelum ada peringkat
- RPP Larutan Elektrolit Dan NonelektrolitDokumen12 halamanRPP Larutan Elektrolit Dan NonelektrolithanifsarahBelum ada peringkat
- Kd. 3.3Dokumen19 halamanKd. 3.3Nay NaylaBelum ada peringkat
- JUDULDokumen14 halamanJUDULSanta TheresiasitinjakBelum ada peringkat
- RPP & LKPD PJBL Identifikasi Unsur C Dan H Dalam Senyawa HidrokarbonDokumen18 halamanRPP & LKPD PJBL Identifikasi Unsur C Dan H Dalam Senyawa HidrokarbonSMAN 1 LangkaplancarBelum ada peringkat
- RPP Unsur Golongan UtamaDokumen21 halamanRPP Unsur Golongan UtamaTats PropeNzBelum ada peringkat
- LK 2 KD 3.4Dokumen24 halamanLK 2 KD 3.4Mirwan Abu WiqyBelum ada peringkat
- RPP Kesetimbangan Kimia InkuiriDokumen98 halamanRPP Kesetimbangan Kimia InkuiriLailatul BadriyahBelum ada peringkat
- Analisis KonsepDokumen17 halamanAnalisis KonsepBatika KencanaBelum ada peringkat
- Silabus Kimia XI MIPADokumen9 halamanSilabus Kimia XI MIPAAnisa RiyaniBelum ada peringkat
- RPP 3 TermokimiaDokumen21 halamanRPP 3 TermokimiaSarmilah MhylaBelum ada peringkat
- Analisis Konsep Materi Koloid Dan MiskonsepsiDokumen10 halamanAnalisis Konsep Materi Koloid Dan MiskonsepsizaidahBelum ada peringkat
- RPP KURMA - STRUKTUR ATOM - Sry HAryani-2Dokumen6 halamanRPP KURMA - STRUKTUR ATOM - Sry HAryani-2Elsi PritamiBelum ada peringkat
- Senyawa HidrokarbonDokumen2 halamanSenyawa HidrokarbonAny SofyaniBelum ada peringkat
- RPP Konsep Mol Dan StoikiometriDokumen12 halamanRPP Konsep Mol Dan StoikiometriTonyBelum ada peringkat
- Soal UH Bab 2Dokumen7 halamanSoal UH Bab 2tyasBelum ada peringkat
- Tabel Periodik Unsur (KD 3.4, 4.4) : Rencana Pelaksanaan PembelajaranDokumen6 halamanTabel Periodik Unsur (KD 3.4, 4.4) : Rencana Pelaksanaan PembelajaranROHINIBelum ada peringkat
- LKPD Laju ReaksiDokumen9 halamanLKPD Laju ReaksiJOICE BUNGABelum ada peringkat
- KIMIADokumen66 halamanKIMIAMelisa AdrianBelum ada peringkat
- Rpp-Rizki Anggi Suhairah Nasution-16035035Dokumen10 halamanRpp-Rizki Anggi Suhairah Nasution-16035035Rizky Anggi SuhairaBelum ada peringkat
- Peer Teaching/RPP KD 3.9 Kelas X TerbaruDokumen16 halamanPeer Teaching/RPP KD 3.9 Kelas X Terbarusuci hadi rahmawatiBelum ada peringkat
- RPP Konsep Redoks PDFDokumen13 halamanRPP Konsep Redoks PDFAgni Budiarti50% (2)
- RPP_REDOKSDokumen23 halamanRPP_REDOKSsuci hadi rahmawatiBelum ada peringkat
- RPP Reaksi RedoksDokumen15 halamanRPP Reaksi RedoksGesti Hamdani HaeriahBelum ada peringkat
- Pengumuman Hasil Tes AKademik GMF 2016Dokumen9 halamanPengumuman Hasil Tes AKademik GMF 2016Debbylia AnggrainyBelum ada peringkat
- ENTAHLAHDokumen1 halamanENTAHLAHDebbylia AnggrainyBelum ada peringkat
- Khutbah BapakDokumen8 halamanKhutbah BapakDebbylia AnggrainyBelum ada peringkat
- Kartu SoalDokumen4 halamanKartu SoalDebbylia AnggrainyBelum ada peringkat
- Shalat TasbihDokumen3 halamanShalat TasbihDebbylia AnggrainyBelum ada peringkat
- ABK Guru Matematika SMAN 17 PLGDokumen5 halamanABK Guru Matematika SMAN 17 PLGDebbylia AnggrainyBelum ada peringkat
- OPTIMASI TES KIMIADokumen5 halamanOPTIMASI TES KIMIADebbylia AnggrainyBelum ada peringkat
- Program Semester 2017-2018Dokumen2 halamanProgram Semester 2017-2018Debbylia AnggrainyBelum ada peringkat
- Anjab GuruDokumen6 halamanAnjab GuruYoe ZakieBelum ada peringkat
- Bahan AjarDokumen6 halamanBahan AjarDebbylia AnggrainyBelum ada peringkat
- DUPAK - Tatik Fix1Dokumen42 halamanDUPAK - Tatik Fix1Debbylia AnggrainyBelum ada peringkat
- TatikDokumen5 halamanTatikDebbylia AnggrainyBelum ada peringkat
- RPP Struktur Pertemuan 1Dokumen4 halamanRPP Struktur Pertemuan 1Debbylia AnggrainyBelum ada peringkat
- Instrumen Penilaian Observasi PresentasiDokumen3 halamanInstrumen Penilaian Observasi PresentasiDebbylia AnggrainyBelum ada peringkat
- Instrumen PengetahuanDokumen3 halamanInstrumen PengetahuanDebbylia AnggrainyBelum ada peringkat
- KONSENTRASI LARUTANDokumen6 halamanKONSENTRASI LARUTANDebbylia AnggrainyBelum ada peringkat
- Instrumen Assesmen Kinerja ProdukDokumen4 halamanInstrumen Assesmen Kinerja ProdukDebbylia AnggrainyBelum ada peringkat
- RPP K 3.2 Debby PBLDokumen28 halamanRPP K 3.2 Debby PBLDebbylia Anggrainy100% (3)
- Struktur AtomDokumen26 halamanStruktur AtomDebbylia AnggrainyBelum ada peringkat
- Debby PrintDokumen1 halamanDebby PrintDebbylia AnggrainyBelum ada peringkat
- Bahan AjarDokumen20 halamanBahan AjarDebbylia AnggrainyBelum ada peringkat
- LKPD Hakikat & Peran Ilmu KimiaDokumen2 halamanLKPD Hakikat & Peran Ilmu KimiaDebbylia AnggrainyBelum ada peringkat
- Bahan AjarDokumen20 halamanBahan AjarDebbylia AnggrainyBelum ada peringkat
- Baru Reaksi Redoks 2Dokumen3 halamanBaru Reaksi Redoks 2Debbylia AnggrainyBelum ada peringkat
- RPP Struktur Pertemuan 1Dokumen10 halamanRPP Struktur Pertemuan 1Debbylia AnggrainyBelum ada peringkat
- RPP Struktur Pertemuan 2Dokumen9 halamanRPP Struktur Pertemuan 2Debbylia AnggrainyBelum ada peringkat
- SOAL KIMIA SMADokumen3 halamanSOAL KIMIA SMADebbylia AnggrainyBelum ada peringkat
- Cover CDDokumen1 halamanCover CDDebbylia AnggrainyBelum ada peringkat
- LKPD Hakikat & Peran Ilmu KimiaDokumen3 halamanLKPD Hakikat & Peran Ilmu KimiaSusy Harahap33% (3)
- Periode Ke 3Dokumen5 halamanPeriode Ke 3deedee0306100% (2)