OPTIMAL] Metode Aseptis dan Sterilisasi
Diunggah oleh
Aulia AmienDeskripsi Asli:
Judul Asli
Hak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
OPTIMAL] Metode Aseptis dan Sterilisasi
Diunggah oleh
Aulia AmienHak Cipta:
Format Tersedia
PETUNJUK PRAKTIKUM
MIKROBIOLOGI PANGAN
NAMA :
NIM :
JURUSAN :
LABORATORIUM MIKROBIOLOGI
PROGRAM STUDI TEKNOLOGI INDUSTRI PERTANIAN
FAKULTAS TEKNOLOGI INDUSTRI DAN AGROINDUSTRI
UNIVERSITAS INTERNASIONAL SEMEN INDONESIA
2015
KATA PENGANTAR
Assalamualaikum Wr.Wb.
Puji syukur kehadirat Allah SWT, karena atas segala rahmat dan karunia yang telah
kita terima sehingga pelaksanaan kegiatan praktikum Mikrobiologi Pangan untuk
mahasiswa tingkat pertama UISI tahun 2015/2016 dapat segera dilaksanakan.
Dalam pelaksanaan praktikum Mikrobiologi Industri akan menggabungkan topik
dalam kurikulum Mikrobiologi Pangan Program Studi Teknologi Industri Pertanian yang
berhubungan aplikasinya di dunia industri dalam sektor pangan.
Agar dalam pelaksanaannya praktikum ini dapat mencapai tujuan yang telah
ditetapkan, maka kepada praktikan, asisten, dosen pengampu diwajibkan melaksanakan
tugas dan kewajiban sesuai dngan tanggung jawab masing-masing.
Wassalamualaikum Wr. Wb.
Gresik, September 2015
Praktikum Mikrobiologi Pangan-TIP-FTIA 1
DAFTAR ISI
KATA PENGANTAR ...................................................................................................................... 01
DAFTAR ISI .................................................................................................................................. 02
Tata Tertib Praktikum Mikrobiologi Pangan .................................................................................. 03
I. Dokumentasi Kerja Laboratorium (Log Book) .................................................................... 04
II. Metode Aseptis dan Sterilisasi ............................................................................................. 05
III. Faktor Intrinsik & Ekstrinsik yang Mempengaruhi Pertumbuhan Mikroba ........................ 17
IV. Uji Sanitasi Ruangan & Alat Pengolahan ............................................................................ 26
V. Produk Pangan Berbasis Susu .............................................................................................. 29
VI. Produk Pangan Berbasis Serealia ........................................................................................ 33
VII. Produk Pangan Berbasis Buah dan Sayur ............................................................................ 35
Praktikum Mikrobiologi Pangan-TIP-FTIA 2
TATA TERTIB PRAKTIKUM MIKROBIOLOGI PANGAN
1) Selama praktikum wajib memakai jas lab untuk menghindari kemungkinan
terjadinya kontaminasi, infeksi dan sebagainya.
2) Selama praktikum wajib memakai sepatu dan dilarang memakai kaos oblong.
3) Selama praktikum dilarang makan, minum, atau merokok di dalam laboratorium.
4) Dilarang makan/minum dengan menggunakan alat laboratorium, kecuali hal
tersebut berkaitan dengan acara praktikum, pengujian organoleptik dan
sebagainya.
5) Alat-alat yang akan digunakan dalam praktikum harus dalam keadaan bersih .
6) Praktikan harus mengetahui cara pemakaian peralatan laboratorium sebelum
menggunakannya, bila perlu menanyakan ke petugas.
7) Sebelum praktikum dimulai, meja kerja harus dibersihkan dengan disinfektan (detol)
atau alkohol 70% atau 200 ppm klorin.
8) Selama praktikum, meja atau peralatan yang terkena kultur mikrobia harus
dibersihkan dengan disinfektan (detol) atau alkohol 70%.
9) Selama bekerja di laboratorium sebaiknya dihindari untuk mengusap (menyentuh)
mulut, telinga, hidung, mata ataupun muka.
10) Dilarang menggunakan pipet dengan mulut untuk menghindari kemungkinan
masuknya bahan yang berbahaya (bahan kimia atau mikrobia) ke dalam tubuh.
11) Dilarang membuang biakan yang masih hidup atau media ke dalam bak pencuci
atau sembarang tempat pembuangan, tetapi dibuang di tempat khusus yang
telah disediakan.
12) Biakan mikrobia yang tidak terpakai lagi, harus dibuang/diletakkan di tempat
khusus yang telah disediakan atau disterilkan dengan otoklaf kemudian segera
dicuci.
13) Apabila terjadi kecelakaan (tertusuk, terluka, mata kemasukan sesuatu) segera
lapor ke petugas.
14) Setelah praktikum selesai, semua alat-alat harus dibersihkan dan dikembalikan
sesuai dengan ketentuan yang ditetapkan.
15) Setelah praktikum selesai, meja harus dibersihkan dengan desinfektan.
16) Sebelum meninggalkan laboratorium, praktikan dianjurkan untuk mencuci tangan
dengan bersih.
17) Secara umum dianjurkan bahwa tata tertib yang ditentukan di atas menjadi
kebiasaan praktikan terutama sewaktu bekerja dengan mikrobia.
Praktikum Mikrobiologi Pangan-TIP-FTIA 3
BAB I
DOKUMENTASI KERJA LABORATORIUM (LOG BOOK)
Praktikum Mikrobiologi Pangan-TIP-FTIA 4
BAB II
METODE ASEPTIS DAN STERILISASI
1. NUTRISI
Mikroba terdiri atas bermacam-macam jenis yang masing-masing berbeda
dalam sifat-sifat fisiologisnya, karena itu kebutuhan makanan (nutrisi) tiap-tiap
golongan atau jenis mikroba juga berbeda-beda. Meskipun demikian susunan kimia
sel untuk semua jasad kurang lebih tetap; air merupakan bagian terbesar dari sel yaitu
80 – 90%, sedangkan sisanya merupakan bagian sel yang lain (protoplasma, dinding sel
cadangan makanan yang berupa lipida, polisakarida, polifosfat, dll) yang berat
keringnya 10 – 20%.
Dari hasil analisis kimia ditunjukkkan bahwa karbon, oksigen, nitrogen, hidrogen
dan fosfor merupakan 5 unsur yang jumlahnya ± 95% dari berat kering sel sedangkan
unsur lainnya merupakan sisanya.
Tabel 1. Susunan unsur-unsur penyusun Sel Bakteri
UNSUR % berat kering
Karbon (C ) 50
Oksigen (Oleh) 20
Nitrogen (N) 14
Hidrogen (H) 8
Fosfor (P) 3
Sulfur (S), Kalium (K), dan Natrium (Na) masing-masing 1
Kalsium (Ca), Magnesium (Mg), Khlor (Cl) masing-masing 0,5
Besi (Fe) 0,2
Lainnya 0,3
2. MEDIUM
Medium ialah suatu bahan yang terdiri dari campuran nutrisi yang dipakai untuk
menumbuhkan mikroba. Selain untuk menumbuhkan mikroba, medium dapat pula
digunakan untuk isolasi, memperbanyak, pengujian sifat-sifat fisiologi dan perhitungan
jumlah mikroba. Supaya mikroba dapat tumbuh baik dalam suatu medium, perlu
dipenuhi syarat-syarat sebagai berikut :
1. Medium harus mengandung semua nutrisi yang mudah digunakan oleh mikroba
2. Medium harus mempunyai tekanan osmose, tegangan muka, dan pH yang sesuai
3. Medium harus steril
Praktikum Mikrobiologi Pangan-TIP-FTIA 5
4. Medium tidak mengandung zat-zat penghambat.
Medium dapat diklasifikasikan berdasar atas susunan kimia, konsistensi dan fungsinya.
Klasifikasi medium berdasar susunan kimia :
a. Medium anorganik yaitu medium yang tersusun dari bahan-bahan anorganik
b. Medium organik yaitu medium yang tersusun dari bahan-bahan organik
c. Medium sintetik yaitu medium yang susunan kimianya dapat diketahui dengan
pasti; medium ini biasanya digunakan untuk mempelajari kebutuhan makanan
mikroba.
d. Medium non sintetik yaitu medium yang susunan kimianya tidak dapat ditentukan
dengan pasti, medium ini banyak digunakan untuk menumbuhkan dan
mempelajari taksonomi mikroba.
Klasifikasi medium berdasarkan konsistensinya :
a. Medium cair (liquid medium) yaitu medium yang berbentuk cair.
b. Medium padat (solid medium) yaitu medium yang berbentuk padat, medium ini
dapat berupa medium organik (alamiah) misalnya medium wortel, medium
kentang dan lain-lain atau medium anorganik misalnya silika gel.
c. Medium padat yang dapat dicairkan (semi solid medium) yaitu medium yang
dalam keadaan panas (dipanasi) berbentuk cair tetapi dalam keadaan dingin
berbentuk padat, sebab medium ini mengandung agar-agar atau gelatin.
Berdasarkan atas keperluannya medium ini dapat dibuat tegak atau miring
(misalnya medium agar tegak, medium agar miring)
Klasifikasi medium berdasarkan fungsinya :
a. Medium diperkaya (enriched medium)
yaitu medium yang ditambah zat-zat tertentu misalnya (serum, darah, ekstrak
tumbuh-tumbuhan dan lain-lain), sehingga dapat digunakan untuk menumbuhkan
mikroba heterotrof tertentu.
b. Medium selektif (selektive medium)
yaitu medium yang ditambah zat kimia tertentu yang bersifat selektif untuk
mencegah pertumbuhan mikroba lain, misalnya medium yang mengandung kristal
violet pada kadar tertentu dapat mencegah pertumbuhan bakteri Gram positif
tanpa mempengaruhi bakteri Gram negatif.
Praktikum Mikrobiologi Pangan-TIP-FTIA 6
c. Medium diferensial (differensial medium)
yaitu medium yang ditambah reagensia atau zat kimia tertentu yang
menyebabkan suatu mikroba membentuk pertumbuhan atau mengadakan
perubahan tertentu sehingga dapat untuk membedakan bakteri himolitik dan non
himolitik.
d. Medium penguji (assay medium)
yaitu medium dengan susunan tertentu yang digunakan untuk pengujian vitamin-
vitamin, asam-asam amino, antibiotik dan lain-lain.
e. Medium untuk perhitungan jumlah mikroba yaitu medium spesifik yang digunakan
untuk menghitung jumlah mikroba dalam suatu bahan misalnya medium untuk
menghitung jumlah bakteri Actinomycetes dan lain-lain.
f. Medium khusus
yaitu medium untuk menentukan tipe pertumbuhan mikroba dan kemampuannya
untuk mengadakan perubahan-perubahan kimia tertentu.
Untuk membuat medium yang tersusun atas beberapa bahan dapat dilakukan cara
berikut :
1. Mencampur bahan – bahan
Garam-garam dan bahan-bahan lain dilarutkan dalam aquadest kemudian
dipanaskan dalam pemanas air agar larutannya homogen.
2. Menyaring medium
Beberapa jenis medium kadang-kadang perlu disaring, sebagai penyaring
dapat digunakan kertas filter, kapas atau kain. Untuk medium agar atau gelatin
penyaringannya dilakukan sewaktu medium panas.
3. Menentukan dan mengatur pH
Penentuan pH suatu medium cair dapat dilakukan menggunakan kertas
indikator universal ataupun pH meter. pH diatur sesuai dengan yang diharapkan.
4. Memasukkan medium ke dalam tempat tertentu
Sebelum disterilkan medium dimasukkan ke dalam tabung steril atau tempat –
tempat lain yang steril kemudian ditutup kapas dan bagian kapasnya dibungkus
kertas sampul (kertas perkamen) agar tidak basah sewaktu disterilkan.
5. Sterilisasi medium
Sterilisasi tergantung macam mediumnya, umumnya dilakukan sterilisasi cara
basah.
Praktikum Mikrobiologi Pangan-TIP-FTIA 7
3. PEMBUATAN MEDIA
1) Pembuatan larutan pengencer (pepton water) 0,1%
(i) Timbang 0,1 g peptone water dan larutkan dalam 100 ml air aquadest sambil
dipanaskan (sampai semua bahan terlarut sempurna)
(ii) Masukkan masing-masing 9 ml larutan pepton ke dalam 10 tabung reaksi
(iii) Sumbatlah dengan kapas dan sterilkan pada suhu 121C selama 15 menit.
2) Pembuatan media racik PGYA
(i) Media PGY memiliki komposisi 10,0 g pepton, 40,0 g glukosa dan 5,0 g yeast
ekstrak, Bacteriological Agar 15 g, Aquadest
(ii) Hitunglah kebutuhan bahan media PGYA untuk pembuatan 100 ml media
sesuaikan dengan komposisi pada butir (i)
(iii) Timbanglah bahan-bahan yang diperlukan sesuai hasil perhitungan butir (ii), serta
CaCO3 0,5% (0,5 g untuk 100 ml media)
(iv) Campurkan dan larutkan semua bahan tersebut
(v) Masukkan media tersebut pada erlenmeyer 200 ml dan sumbatlah dengan kapas
(vi) Sterilisasi media tersebut pada suhu 121C selama 15 menit.
3). Pembuatan media buatan PDA dan APDA dari ekstrak kentang
(i) Komposisi 1000 ml media PDA terdiri dari Potato infusion(ekstrak kentang) 200 ml,
Glukosa 20 g, Agar 15 g, Aquadest 800 ml, dan untuk membuat APDA tambahkan
larutan 10% asam tartarat untuk mengatur pHnya menjadi 3,5 – 4,0.
(ii) Ekstrak kentang (Potato Infusion) sebanyak 200 ml dibuat dengan cara merebus
200 g kentang yang telah dikupas, dicuci dan dipotong(dibelah) dalam 1 liter air
selama 1 jam, saring filtrat yang diperoleh sebanyak 200 ml (sehingga diperoleh
200 ml sari kentang)
(iii) Tambahkan bahan-bahan lainnya ke dalam 200 ml ekstrak kentang tersebut (lihat
poin (i))
(iv) Larutkan semua bahan tersebut dan masukkan ke dalam erlenmeyer dan
sumbatlah dengan kapas.
(v) Sterilisasi media tersebut pada suhu 121C selama 15 menit.
4). Pembuatan media jadi/siap pakai : VRBA EMBA, TCBSA, SSA, PCA, NA, Rogosa Agar
(i) Bacalah komposisi dan cara pembuatan media tersebut yang tertera pada
kemasan masing-masing media.
(ii) Timbanglah bahan sesuai dengan kebutuhan.
Praktikum Mikrobiologi Pangan-TIP-FTIA 8
(iii) Larutkan media dan tempatkan pada wadah yang sesuai (erlenmeyer atau
tabung reaksi), dan sumbat dengan kapas
(iv) Sterilisasi media pada suhu dan waktu tertentu sesuai petunjuk pada kemasan
dan perhatikan bila ada catatan khusus untuk media tertentu.
5). Pembuatan media Lactose Broth untuk penghitungan MPN
(i) Setiap kelompok membuat seri pengenceran MPN 4 tingkat pengenceran
dengan menggunakan sistem 3 seri tabung (4 x 3 tabung, setiap tabung berisi 9
ml media Lactose Broth)
(ii) Timbanglah bahan untuk keperluan tersebut.
(iii) Larutkan semua bahan dan masukkan ke dalam tabung reaksi serta masukkan
satu tabung Durham pada setiap tabung reaksi tersebut, sumbatlah dengan
kapas.
(iv) Sterilisasi media tersebut pada suhu 121C selama 15 menit.
6). Pembuatan Media Agar Miring, Agar Tegak dan Agar Cawan
- Untuk pembuatan media agar miring, campurkan bahan/media yang digunakan
dengan aquades (sesuai ketentuan masing-masing media), kemudian dipanaskan
dalam beaker glass. Setelah itu, tuangkan pada tabung reaksi sebanyak 5 mL – 7
mL, tutup dengan kapas dan kertas payung, dan disterilisasi dalam autoklaf.
- Setelah selesai disterilisasi, letakkan tabung reaksi dalam posisi miring (kemiringan
45°C) hingga benar-benar memadat dan agar miring siap untuk digunakan.
- Untuk pembuatan media agar tegak, cara yang digunakan sama dengan agar
miring. Perbedaannya adalah setelah dimasukkan dalam tabung reaksi dan
disterilisasi, tabung reaksi diletakkan dalam posisi tegak (pada rak tabung reaksi)
hingga benar-benar memadat dan agar miring siap untuk digunakan.
- Untuk pembuatan media agar cawan, campurkan bahan/media yang digunakan
dengan aquades (sesuai ketentuan masing-masing media), kemudian dipanaskan
dalam erlenmeyer, tutup dengan kapas dan kertas payung. Setelah itu, media
dalam erlenmeyer tersebut disterilisasi dalam autoklaf. Setelah sterilisasi, tuangkan
media dalam cawan petri secara aseptis sebanyak 10 mL sampai 15 mL, tutup, dan
biarkan hingga memadat dan siap digunakan .
Praktikum Mikrobiologi Pangan-TIP-FTIA 9
7). Untuk keperluan praktikum pembuatan media, simpanlah selama 3 hari – 1 minggu
pada suhu kamar satu cawan agar padat atau satu tabung reaksi untuk media cair
dan larutan pengencer yang sudah disterilisasi. Kemudian amati apakah terdapat
kontaminan atau tidak. Hal ini dilakukan untuk menguji kondisi sterilisasi media yang
telah saudara lakukan apakah sudah dilakukan dengan benar, dilakukan secara
aseptis (terutama pada pembuatan media agar cawan) dan terhindar kontaminasi
pada saat penyimpanan.
Tabel 2. Karakteristik pertumbuhan bakteri enteropatogenik pada medium selektif
(Fardiaz, 1993 ; Fardiaz dan Jenie, 1989)
Organisme Medium Inkubasi Penampakan
selektif
Salmonella SS Agar 35C, 18- Keruh atau bening, tidak berwarna (bagian tengahnya
24 jam mungkin berwarna hitam)
Shigella SS Agar 35C, 18- Keruh atau bening, tidak berwarna
24 jam
Yersinia SS Agar 35C, 40- Keruh atau bening, tidak berwarna
48 jam
Salmonella – BG Agar 35C, 18- Koloni berwarna merah
Shigella 24 jam Salmonella–Shigella tidak memfermentasi laktosa
Vibrio cholerae TCBS Agar 35C, 18- Kuning, permukaan agak datar, bagian tengah keruh
24 jam dan bagian pinggir bening
V. TCBS Agar 35C, 18- Hijau kebiruan, bulat agak keruh
parahaemolyticus (+3%NaCl) 24 jam
Koliform koloni EMB agar 32C, 24- berwarna gelap dengan sinar hijau metalik, diameter
fekal 48 jam 0,5 – 1,5 mm
Koliform koloni EMB Agar 32C, 24- berwarna merah muda, diameter 1,0 – 3,0 mm dan
non fekal 48 jam tengahnya berwarna gelap seperti mata ikan
Escherichia coli VRB Agar 37C, 24- Berwarna merah gelap
48 jam
Staphylococcus VJ Agar 37C, 24- berwarna hitam dikelilingi arealwarna kuning
48 jam (karenaterjadinya fermentasi mannitol)
Staphylococcus Staphylococc 37C, 24- Koloni berwarna kuning oranye, jika ditetesi indikator
us 110 Agar 48 jam BCP (Bromcresol purple)akan menunjukkan
perubahan warna karena terjadi fermentasi mannitol
Praktikum Mikrobiologi Pangan-TIP-FTIA 10
4. METODE ASEPTIS
Kultur disebut murni apabila kultur ini hanya terdiri dari satu spesies mikrobia saja.
Pekerjaan di laboratorium mikrobiologi pada umumnya melibatkan berbagai kultur
murni. Jika spesies mikrobia yang lain masuk secara tidak sengaja ke dalam kultur
murni, kultur tersebut dikatakan telah terkontaminasi, dan tidak lagi dikatakan sebagai
kultur murni tetapi kultur campuran. Kemungkinan terjadinya kontaminasi ini
merupakan hal yang harus diperhatikan karena kontaminan ini akan mempengaruhi
hasil pengujian yang sedang dilakukan, atau akan terjadi kesalahan hasil. Oleh karena
itu, untuk mempertahankan kultur tetap murni, medium pertumbuhan yang digunakan
harus steril dan kontaminasi harus dicegah.
Pada saat telah diperoleh kultur yang murni, maka hal-hal yang harus
diperhatikan :
1. Seluruh material yang akan berhubungan langsung dengan mikrobia harus steril.
2. Seluruh media yang digunakan untuk menumbuhkan sel juga harus steril.
3. Tidak ada kontaminan yang masuk dan tumbuh.
Metoda yang digunakan untuk memelihara kultur murni atau bekerja dengan kultur
murni disebut metoda aseptis. Prosedur umum yang harus diikuti setiap bekerja
dengan kultur murni adalah:
1. Medium pertumbuhan dan tempatnya harus steril
2. Tempat pertumbuhan harus selalu ditutup untuk mencegah masuknya debu yang
membawa mikrobia dan aerosol. Apabila penutup harus dibuka, harus dalam
waktu yang sesingkat mungkin, dilarang meletakkan penutup pada sembarang
tempat.
3. Peralatan (ose dan pipet) dan larutan yang digunakan untuk pekerjaan harus steril.
Apabila tidak steril, ose atau pipet ini akan mentransfer kontaminan pada kultur
murni.
4. Ose yang telah selesai digunakan harus disterilkan dan pipet yang telah digunakan
untuk memindahkan kultur harus ditempatkan pada larutan disinfektan sesegera
mungkin.
5. Area tempat bekerja juga harus dijaga agar tidak terkontaminasi dengan kultur
yang digunakan.
Sebelum memulai acara-acara praktikum mikrobiologi terlebih dahulu harus
diketahui cara memindahkan sel secara aseptis. Beberapa hal yang perlu diperhatikan
adalah:
Praktikum Mikrobiologi Pangan-TIP-FTIA 11
1. Jangan digunakan ose yang belum steril untuk menyentuh kultur. Hal ini bertujuan
untuk mencegah terjadinya kontaminasi.
2. Mulut tabung harus dipanasi baik pada saat ose dimasukkan atau saat dikeluarkan
dari tabung. Pemanasan pertama ditujukan untuk mencegah masuknya udara luar
yang membawa partikel debu masuk ke dalam tabung, sedang pemanasan
kedua ditujukan untuk membakar sel-sel yang jatuh atau menempel pada mulut
tabung saat ose dimasukkan atau ditarik.
3. Diusahakan tabung dalam kondisi terbuka dalam waktu yang sesingkat-singkatnya.
4. Dihindari menempatkan tutup tabung pada permukaan area pekerjaan atau
menyentuhnya. Diusahakan agar tutup tabung tidak bersinggungan dengan
sumber kontaminan.
5. Ose yang telah digunakan harus disterilkan untuk mencegah kontaminasi.
Untuk mengembangkan ketrampilan memindahkan kultur secara aseptis, maka
praktikan harus memahami dan menguasai cara kerja atau langkah-langkah dalam
metoda aseptis pemindahan kultur. Berikut ini akan disajikan langkah-langkah yang
harus diikuti oleh praktikan.
a. memindahkan kultur dari tabung reaksi ke tabung reaksi
1. Siapkan tabung reaksi dan ose yang akan digunakan pada rak.
2. Pegang ose seperti saat memegang pensil.
3. Pijarkan ose di atas api spirtus sampai merah membara.
4. Biarkan ose dingin sebelum menyentuh kultur yang akan dipindahkan.
5. Buka tutup kapas pada tabung reaksi tempat kultur yang akan dipindah dengan
jari kelingking.
6. Bakar mulut tabung reaksi dengan api spirtus, kemudian masukkan ose dan ambil
satu ose kultur yang tumbuh dalam tabung reaksi.
7. Bakar mulut tabung sekali lagi dan tutup dengan kapas, selanjutnya diletakkan
kembali pada rak.
8. Ambil tabung yang baru, buka tutupnya dan bakar mulutnya di atas api, masukkan
ose tempat kultur menempel dan goreskan pada media yang baru.
9. Bakar kembali mulut tabung, tutup dengan kapas dan letakkan kembali pada rak.
10. Panaskan ose setelah selesai dipakai atau sebelum diletakkan kembali.
11. Untuk yang sudah mahir dua tabung reaksi bisa langsung dipegang sekaligus.
12. Inkubasikan tabung reaksi yang sudah diinokulasi pada inkubator.
Praktikum Mikrobiologi Pangan-TIP-FTIA 12
b. Memindahkan kultur dari tabung reaksi ke cawan Petri
1. Pijarkan ose di atas api spirtus sampai merah membara.
2. Biarkan ose dingin sebelum menyentuh kultur yang akan dipindahkan.
3. Bakar mulut tabung reaksi dengan api spirtus, kemudian masukkan ose dan ambil
satu ose kultur yang tumbuh dalam tabung reaksi.
4. Bakar mulut tabung reaksi sekali lagi dan tutup dengan kapas, selanjutnya
diletakkan kembali pada rak.
5. Buka cawan Petri tempat kultur yang akan dipindahkan dengan tangan kiri.
6. Goreskan ose pada media agar dan tutup kembali cawan Petri.
7. Inkubasikan cawan Petri pada inkubator.
Gambar 1. Cara memindahkan kultur pada agar miring
Praktikum Mikrobiologi Pangan-TIP-FTIA 13
Gambar 2. Cara memindahkan kultur pada tabung reaksi
C. Memindahkan kultur cair dari tabung reaksi ke Erlenmeyer
1. Pegang tabung reaksi tempat kultur cair dengan tangan kanan dan buka tutup
kapasnya dengan menjepitnya pada jari kelingking tangan kiri, secara aseptis.
2. Pegang Erlenmeyer dengan tangan kiri dan buka tutup kapasnya dengan
menjepitnya pada jari kelingking tangan kanan, secara aseptis.
3. Pindahkan kultur cair dari tabung reaksi ke dalam Erlenmeyer.
4. Sebelum tutup kapas dimasukkan, panasi terlebih dahulu mulut Erlenmeyer.
5. Inkubasikan Erlenmeyer pada inkubator.
5. STERILISASI
Sterilisasi merupakan destruksi atau penghilangan mikrobia yang hidup. Obyek
yeng terbebas dari kehidupan mikrobia disebut steril. Sterilisasi merupakan salah satu
cara untuk mengontrol mikrobia, sedang cara yang lain adalah dengan menghambat
pertumbuhan mikrobia. Namun sterilisasi berbeda dengan cara yang kedua, dalam
hal, bahwa pada sterilisasi seluruh mikrobia yang ada dimatikan atau dihilangkan dan
obyek menjadi steril.
Sterilisasi adalah hal yang penting dalam melakukan aktivitas laboratorium
terutama yang melibatkan mikrobia. Karena pada umumnya percobaan dilakukan
menggunakan kultur murni. Bekerja dengan kultur murni memerlukan beberapa
Praktikum Mikrobiologi Pangan-TIP-FTIA 14
persyaratan, yaitu media nutrien serta tempat untuk pertumbuhan harus steril,
demikian pula segala peralatan yang terkait. Seandainya sterilisasi tidak dikerjakan,
mikrobia kontaminan akan tumbuh dan hasil yang seharusnya diperoleh dari
percobaan menggunakan kultur murni akan menyimpang.
Sejumlah metode sterilisasi dapat dipilih oleh ahli mikrobiologi karena tidak ada
satu metode pun yang cocok untuk berbagai bahan yang harus disterilkan. Sebagai
contoh metode dengan suhu tinggi tidak dapat digunakan untuk sterilisasi larutan
vitamin.
Sterilisasi dengan panas
a. Api langsung (direct flame). Cara yang paling sederhana untuk sterilisasi panas
adalah dengan api langsung, yaitu dengan membakar obyek yang akan
disterilkan pada nyala api. Nyala api dengan suhu tinggi ini akan membunuh
seluruh mikrobia yang ada pada obyek. Metode api langsung ini biasanya
digunakan untuk sterilisasi ose, forceps, mulut tabung reaksi saat memindahkan
kultur secara aseptis.
b. Panas kering (oven udara kering). Panas kering ini biasanya digunakan untuk
sterilisasi pipet, tabung reaksi, Erlenmeyer, gelas piala dan instrumen kedokteran
(untuk operasi). Obyek yang akan disterilkan ditempatkan pada oven udara panas
dan dibakar sampai seluruh mikrobia terbunuh. Panas kering dapat membunuh
mikrobia karena terjadi oksidasi struktur sel dan makromolekul. Panas kering tidak
dapat digunakan untuk sterilisasi cairan (seperti media cair) karena kebanyakan
cairan akan mendidih pada suhu 100oC, dan selama mendidih temperaturnya
tidak akan naik. Pendidihan belum tentu dapat mensterilkan obyek, karena
bebrapa spora bakteri tetap bertahan dengan pendidihan selama berjam-jam
pada suhu 100oC.
c. Autoklaf (uap panas). Proses sterilisasi ini menggunakan uap panas dan tekanan
sehingga obyek yang disterilkan dapat mencapai suhu 121oC, selama 15 menit.
Sterilisasi cara ini sering digunakan. Berbagai jenis media yang digunakan untuk
kegiatan di laboratorium mikrobiologi disterilkan dengan cara ini.
Sterilisasi tanpa panas
a. Filtrasi. Untuk liquid yang sensitif dengan panas, misalnya vitamin, antibiotik, metoda
sterilisasi yang digunakan adalah filtrasi. Pada cara ini mikrobia tidak dimatikan
tetapi dihilangkan. Liquid yang akan disterilkan dilewatkan pada filter yang pori-
porinya sangat kecil sehingga tidak bisa lewat. Filter yang digunakan untuk
Praktikum Mikrobiologi Pangan-TIP-FTIA 15
sterilisasi ada beberapa macam, tetapi yang paling sering digunakan adalah filter
membran. Filter membran adalah material yang sangat tipis terbuat dari selulosa
asetat atau polikarbonat dengan ukuran pori-pori yang bervariasi. Sebelum
sterilisasi, filter membran dan peralatannya disterilkan terlebih dahulu (biasanya
menggunakan autoklaf).
b. Sterilisasi Kimia. Sterilisasi kimia adalah metode yang biasa digunakan untuk
sterilisasi obyek padat yang sensitif terhadap panas. Pada metode ini, mikrobia
dibunuh menggunakan bahan kimia yang toksik. Sedang mekanisme kematiannya
sangat tergantung dari bahan kimia yang digunakan. Bahan kimia yang
digunakan untuk sterilisasi harus dapat membunuh seluruh mikrobia, oleh karena itu
harus dibedakan dengan disinfektan ataupun antiseptik, yang biasanya digunakan
untuk mengontrol mikrobia tetapi tidak mensterilkan. Bahan kimia yang sering
digunakan adalah etilen oksida (EtO). Etilen oksida biasanya digunakan untuk
sterilisasi berbagai material yang sensitif terhadap panas, misalnya cawan Petri,
pipet, alat suntik yang terbiuat dari plastik.
c. Sterilisasi dengan sinar radiasi. Radiasi pengion merupakan alternatif lain untuk
sterilisasi, khususnya untuk bahan yang peka terhadap panas. Hal ini disebabkan
karena kenaikan suhu yang terjadi akibat perlakuan iradiasi hanya 4oC. Selain itu
radiasi pengion memiliki daya tembus yang besar. Radiasi pengion ini mampu
mengionkan molekul yang diterpanya. Molekul air bila kena radiasi pengion ini
akan mengalami radiolisis, dan dihasilkan radikal-radikal bebas, diantaranya radikal
bebas hidrogen dan radikal bebas hidroksil. Senyawa radikal bebas ini sifatnya
sangat reaktif dan sangat mudah bereaksi satu sama lainnya dan juga dapat
mempengaruhi dan merusak molekul di dalam sel, termasuk ensim dan asam
nukleat. Yang perlu diperhatikan dalam menggunakan sinar radiasi untuk tujuan
sterilisasi ini adalah dosis yang digunakan harus tepat. Jika tidak, akibatnya sangat
berbahaya, karena akan menyebabkan terjadinya mutasi atau resistensi terhadap
radiasi. Kelemahan sterilisasi dengan radiasi ini adalah biaya mahal, dan butuh
kehati-hatian untuk mengoperasikannya.
Praktikum Mikrobiologi Pangan-TIP-FTIA 16
BAB III
FAKTOR INTRINSIK & EKSTRINSIK YANG MEMPENGARUHI PERTUMBUHAN MIKROBA
A. FAKTOR PERTUMBUHAN MIKROBA
1. Pengaruh Suhu
Bakteri sebagai organisme hidup mampu untuk tumbuh dan berkembang pada
kisaran suhu 5°C sampai 80°C. Masing-masing spesies bagaimanapun juga
memerlukan kisaran yang lebih rendah, yang ditentukan oleh sensitivitas panas sistem
enzimnya. Kisaran suhu spesifik terdiri dari beberapa poin berikut :
a) Suhu pertumbuhan minimum : suhu terendah dimana mikroba bisa tumbuh.
Dibawah suhu ini, aktivitas enzim dihambat, dan metabolisme sel menjadi inaktif
sehingga tidak terjadi pertumbuhan
b) Suhu pertumbuhan maksimum : suhu tertinggi dimana mikroba bisa tumbuh. Diatas
suhu ini, umumnya enzim sel akan rusak dan mikroba akan mati
c) Suhu pertumbuhan optimum : suhu dimana kecepatan pertumbuhan mikroba
adalah paling tinggi, akan tetapi untuk aktivitas sel yang lain tidak memerlukan
suhu optimum.
Semua bakteri bisa diklasifikasikan kedalam satu dari tiga kelompok besar, tergantung
dari suhu pertumbuhannya.
1. Psikrofilik : Spesies bakteri yang akan tumbuh pada kisaran suhu -5° C sampai 20° C.
Karakteristik khusus dari semua mikroba psikrofilik adalah kemampuannya untuk
tumbuh antara suhu 0 sampai 5° C.
2. Mesofilik : Spesies bakteri yang akan tumbuh pada kisaran suhu 20° C sampai 45° C.
Karakteristik khusus dari semua mikroba mesofilik adalah kemampuannya untuk
tumbuh pada suhu tubuh (37° C) serta tidak mampu untuk tumbuh pada suhu
diatas 45° C. Yang termasuk dalam kelompok mesofilik dibagi menjadi 2 grup yang
berbeda :
a) Plant saprophytes, yaitu organisme yang memiliki suhu pertumbuhan optimum
antara 20° C sampai 30° C
b) Organisme yang lebih bisa tumbuh pada tubuh yang berdarah panas, dengan
suhu pertumbuhan optimum antara 35°C sampai 40° C
3. Termofilik : Spesies bakteri yang akan tumbuh pada suhu diatas 35° C. Ada 2 grup
termofilik, yaitu :
a) Termofilik Fakultatif : organisme yang akan tumbuh pada suhu 37° C, dengan
suhu pertumbuhan optimum antara 45° C sampai 60° C
Praktikum Mikrobiologi Pangan-TIP-FTIA 17
b) Termofilik Obligat : organisme yang hanya bisa tumbuh pada suhu diatas 50° C,
dengan suhu pertumbuhan optimum diatas 60° C
A. Tujuan praktikum : Mempelajari dan mengetahui suhu pertumbuhan optimum
mikroorganisme
B. Bahan dan Alat yang digunakan :
1. kultur Escherichia coli, Staphylococcus aureus, Lactobacillus casei umur 24 – 48
jam dalam media NB
2. Media Nutrien agar miring
3. Inkubator dengan suhu 15° C, 30° C, dan 55° C
4. Bunsen dan ose
C. Cara Kerja :
1. Berilah label pada setiap NA miring dengan nama mikroba yang akan
diinokulasikan serta suhu inkubasinya (15°C, 30°C, dan 55°C)
2. Kemudian inokulasikan NA miring tersebut dengan menggoreskan
permukaannya dengan E.coli.
3. Ulangi langkah no 2 untuk menginokulasikan S. aureus dan L. casei.
4. Inkubasikan masing-masing kultur pada 3 suhu yang berbeda (15°C, 30°C, dan
55°C) selama 24-48 jam.
2. Kerusakan Mikroorganisme Karena Pemanasan
Panas merupakan metode yang paling sering digunakan untuk menginaktivasi
mikroorganisme dalam produksi makanan. Paparan panas pada mikrobia memiliki dua
parameter, yakni suhu dan waktu paparan. Berdasarkan ketahanannya terhadap
panas, mikroorganisme dapat dibagi menjadi dua kelompok besar yakni sel - sel
vegetatif dan spora – spora dari jamur. Ketahanan panas mikroorganisme biasanya
dinyatakan dengan istilah waktu kematian karena panas (thermal death time), yakni
waktu yang dibutuhkan pada suhu tertentu untuk membinasakan secara sempurna
organisme atau sporanya. Kematian sel – sel vegetatif atau spora yang disebabkan
oleh panas mempunyai hubungan logaritmis dengan waktu. Jika suatu suspensi
mikroorganisme dipanaskan pada suatu suhu tertentu, maka hubungan berikut dapat
diturunkan:
Praktikum Mikrobiologi Pangan-TIP-FTIA 18
t = D (log a – log b)
dimana: t = waktu pemanasan pada suhu konstan yang bisa mematikan
mikroorganisme (menit)
D = waktu (menit) yang bisa menurunkan jumlah sel mikroorganisme
sampai 90% dari awalnya
a = jumlah sel awal
b = jumlah sel akhir
A. Tujuan Praktikum :
1. Mengetahui bahwa proses pemanasan dapat menyebabkan kerusakan
pada mikroorganisme
2. Mempelajari dan mengetahui waktu yang bisa menurunkan jumlah sel
mikroorganisme sampai 90% dari awalnya
B. Bahan dan Alat yang digunakan
1. Kultur Escherichia coli
2. Media tryptic soy broth dengan pH 7,0
3. Waterbath dengan suhu 54, 58, dan 62oC
4. Petridish dan tabung
5. Bunsen
C. Cara Kerja :
1. Berilah label pada setiap tabung dengan nomer kelompok, suhu (54, 58, dan
62oC), waktu (15, 30, 45, dan 60 menit), dan pengenceran (Tabel 1)
Tabel 1. Pengenceran pada setiap suhu
Waktu Pengenceran
Sampling
54oC 58oC 62oC
(menit)
0 10-5, 10-6, 10-7, 10-8 10-5, 10-6, 10-7, 10-8 10-5, 10-6, 10-7, 10-8
15 10-5, 10-6, 10-7, 10-8 10-2, 10-3, 10-4, 10-5 10-1, 10-2, 10-3, 10-4
30 10-3, 10-4, 10-5, 10-6 10-0, 10-1, 10-2, 10-3 10-0, 10-1, 10-2, 10-3
45 10-2, 10-3, 10-4, 10-5 10-0, 10-1, 10-2, 10-3 10-0, 10-1, 10-2, 10-3
60 10-1, 10-2, 10-3, 10-4 10-0, 10-1, 10-2, 10-3 10-0, 10-1, 10-2, 10-3
Praktikum Mikrobiologi Pangan-TIP-FTIA 19
2. Pindahkan bakteri yang sudah tumbuh selama semalam sebanyak 10 ml ke 100 ml
media uji (TSB pH 7), dan homogenkan.
3. Tambahkan 5 ml broth yang telah diinokulasi pada empat tabung. Perlakuan ini
akan menjadi sampel 100
4. Tempatkan tabung yang berlabel 15, 30, 45, dan 60 menit ke water bath dan mulai
penghitungan waktu
5. Lakukan pengenceran sesuai dengan Tabel 1. Untuk pengenceran sampel yang
telah mengalami pemanasan, tempatkan terlebih dahulu ke dalam es hingga
dingin. Kemudian homogenkan dan encerkan
6. Pour plate dalam duplo sesuai dengan Tabel 1
7. Inkubasi plates terbalik pada 37oC selama 48 jam
8. Buat thermal destruction curve (TDC)
9. Tentukan nilai D
3. Pengaruh pH
Pertumbuhan dan ketahanan mikroba sangat dipengaruhi oleh pH lingkungan,
dimana untuk semua mikroba memiliki kebutuhan pH yang berbeda-beda. Masing-
masing spesies memiliki kemampuan untuk tumbuh pada kisaran pH yang spesifik, bisa
luas ataupun terbatas, dan pertumbuhan yang paling cepat berada pada kisaran pH
optimum. Kebutuhan pH ini menggambarkan kemampuan adaptasi organisme pada
lingkungannya. Contohnya, bakteri enterik mampu bertahan hidup pada kisaran pH
yang luas, yang merupakan habitat aslinya yaitu sistem pencernaan.
Kisaran pH spesifik untuk bakteri adalah antara 4 sampai 9, dengan pH
optimumnya 6,5 sampai 7,5. Jamur, kapang dan khamir menyukai lingkungan yang
asam, dengan aktivitas optimum pada pH 4 sampai 6. Lingkungan yang netral atau
hampir netral, secara umum menguntungkan pertumbuhan mikroorganisme, dan juga
pH medium diatur sekitar 7. Aktivitas metabolisme mikroba akan menghasilkan asam
hasil degradasi karbohidrat dan basa hasil pemecahan protein, dan hal ini akan
menyebabkan perubahan pH yang akan mengganggu pertumbuhan mikroba. Untuk
memperlambat perubahan ini, senyawa kimia, yaitu buffer, seringkali digunakan ketika
menyiapkan medium.
Praktikum Mikrobiologi Pangan-TIP-FTIA 20
B. KURVA PERTUMBUHAN
Apabila seberkas cahaya dilewatkan pada suatu suspensi, maka cahaya itu
akan disebar ke berbagai arah yang nampak dimata kita sebagai suatu cairan yang
keruh. Suspensi sel mikroba mengalami hal yang sama bila dikenai cahaya. Semakin
besar konsentrasi sel mikroba dalam suspensi semakin keruh kenampakan suspensi
tersebut. Sifat ini dimanfaatkan dalam memonitor pertumbuhan mikroba dalam
medium cair. Pada pertumbuhan sel, jumlah sel meningkat dapat diamati dengan
meningkatnya kekeruhan. Bila perubahan kekeruhan ini dapat diukur maka hal ini
sangat berguna dalam mempelajari kinetika pertumbuhan mikroba.
Pengukuran kekeruhan ini dapat dikerjakan dengan menggunakan instrumen
yang disebut spektrofotometer, alat ini mengukur intensitas suatu cahaya yang
diteruskan setelah melewati suatu medium (cairan atau suspensi) yang ditempatkan
dalam kuvet. Bila cahaya melewati suatu suspensi, sebagian cahaya akan tersebar
dan sebagian lagi diteruskan sesuai dengan arah cahaya semula (Gambar 7)
Gambar 1. Skema Pengukuran dengan spektrofotometer
Rasio intensitas cahaya yang diteruskan (I) dengan intensitas cahaya mula-mula
(Io) disebut % transmitansi (%T). Semakin keruh suatu suspensi maka semakin kecil %T.
fenomena ini dijabarkan secara matematis yang menghasilkan hukum Beer-Lambert,
yaitu :
-log (Io/I) = - log (%T) = b c
Dimana I : intensitas cahaya yang diteruskan
Io : intensitas cahaya yang masuk
I/Io : %T = % transmitansi
: konstanta yang besarnya tergantung dari jenis medium dan
panjang gelombang yang digunakan
b : Panjang medium yang dilewati cahaya
c : Konsentrasi partikel (misal, sel mikroba)
Praktikum Mikrobiologi Pangan-TIP-FTIA 21
Untuk memudahkan – log (I/Io) atau – log (%T) disebut ‘optical density” (OD) atau
absorbansi (A), sehingga diperoleh hubungan sebagai berikut :
A = b c = kc
Bila dan b konstanta, maka absorbansi atau optical density berbanding lurus dengan
konsentrasi sel dengan konstanta k (gabungan konstanta dan b). Karena itu
konsentrasi sel mikroba dalam suspensi dapat dinyatakan sebagai absorbansi atau
optical density.
Bila konsentrasi sel mikroba ingin dinyatakan dalam besaran konsentrasi yang
lazim misalnya, berat kering sel per satuan volume (mg/l atau g/l) maka diperlukan
hubungan antara absorbansi dan konsentrasi sel mikroba yang dilukiskan sebagai
kurva standar. Kurva standar ini harus dibuat dengan mengukur absorbansi suspensi
dengan berbagai konsentrasi sel yang diketahui, dan selanjutnya dibuat grafik A vs c.
Grafik yang diperoleh pada kisaran absorbansi tertentu membentuk garis lurus dengan
slope yang tidak lain adalah k
Kurva standar biasanya berupa garis lurus pada pembacaan absorbansi kurang
dari 0,3 – 0,4. diatas angka tersebut mulai terjadi penyimpangan dari hukum Beer-
Lambert, absorbansi terbaca pada konsentrasi tertentu lebih rendah dari pada yang
seharusnya (Gambar 8)
A kurva menyimpang
0.4
garis lurus
C kadar sel (g/l)
Gambar 2. Hubungan antara absorbansi dan kadar sel, ditunjukkan garis linier terjadi
pada pembacaan absorbansi kurang dari 0,4
Oleh karena itu pada konsentrasi sel yang tinggi perlu dilakukan koreksi misalnya
dengan mengencerkan suspensi sehingga absorbansi terbaca berada dalam kisaran
yang linier. Penyimpangan ini akan semakin nyata pada penggunaan panjang
gelombang yang lebih rendah dari 550 nm. Konsentrasi yang sangat rendah dapat
juga menimbulkan kesalahan akibat pembacaan oleh alat yang kurang akurat.
Praktikum Mikrobiologi Pangan-TIP-FTIA 22
Pertimbangan lain dalam memilih panjang gelombang adalah bahwa semakin
rendah panjang gelombang yang digunakan, pembacaan absorbansi semakin besar
(untuk konsentrasi yang sama), sehingga untuk kasus dimana konsentrasinya rendah
dapat diukur dengan panjang gelombang yang lebih rendah. Sebaliknya untuk
konsentrasi yang lebih tinggi digunakan panjang gelombang yang lebih tinggi
sehingga tidak perlu pengenceran. Panjang gelombang 660 nm banyak digunakan
dalam pengukuran absorbansi suspensi sel karena pada panjang gelombang ini
absorbansi kebanyakan medium (tanpa pigmen / pewarna) hampir sama dengan air.
A. Tujuan : mengetahui hubungan antara biomassa dari kultur mikroba (bakteri atau
yeast) dengan absorbansi
B. Alat dan Bahan
Bahan : kultur mikroba (bakteri atau yeast) pada akhir fase logaritmik (250 ml),
aquadest dan formalin 40%. Alat yang digunakan meliputi spektrofotometer dan
tabung kuvet, sentrifuse dan tabung sentrifuse, oven, pipet volume (5, 10 dan 25 ml),
labu ukur (25, 50 dan 100ml), pipet pasteur dan vortex mixer.
METODE I
C. Cara Kerja :
1. Tambahkan kultur mikroba pada akhir fase logaritmik dengan larutan formalin
40% sebanyak 1% volume kultur (2,5 ml).
2. Kultur diencerkan sedemikian sampai absorbansinya pada panjang gelombang
660 nm mencapai nilai sekitar 1,0 (teralah dengan spektrofotometer).
3. Selanjutnya buatlah pengenceran seperti pada Tabel 1.
4. Ukurlah absorbansi masing-masing hasil pengenceran tersebut dengan
spektrofotometer pada panjang gelombang 660 nm, catat hasilnya.
5. Ambil 50 ml kultur yang absorbansinya 1,0 (lihat pada tahap 2) dan disentrifuse
pada 3000 rpm selama 10 menit (buat 2 ulangan), setelah sentrifugasi buanglah
supernatannya (bagian bening) dengan hati-hati menggunakan pipet pasteur.
6. Cucilah massa sel dalam tabung sentrifuse dengan menyesuaikannya dengan
sejumlah aquadest, disentrifugasi pada kondisi yang sama dan supernatannya
dibuang.
7. Resusensi massa sel dengan 2 ml aquadest dan pindahkan suspensi tersebut ke
dalam botol timbang yang telah diketahui beratnya. Bilas lagi tabung sentrifuse
dengan 1 ml aquadest dan tuang ke dalam botol timbang. Atau bila
Praktikum Mikrobiologi Pangan-TIP-FTIA 23
memungkinkan, setelah supernatannya dibuang (seperti pada tahap 6), massa
sel dalam tabung sentrifuse dapat langsung dikeringkan
8. Keringkan botol timbang dalam oven pada suhu 105°C selama 24 jam
9. Pindahkan botol timbang ke dalam desikator sampai dingin dan timbang.
Pengeringan dilanjutkan sampai tercapai berat konstan, catat berat massa sel
kering
10. Hitunglah konsentrasi sel untuk masing-masing pengenceran yang dibuat (lihat
tahap 3)
11. Buat kurva hubungan antara konsentrasi biomassa (mg/l) dan absorbansi (A660)
Tabel 1. Pengenceran kultur
Volume kultur (ml) Volume akhir (ml) Pengenceran
5 100 0,05
10 100 0,10
10 50 0,20
25 100 0,25
30 100 0,30
10 25 0,40
25 50 0,50
30 50 0,60
METODE II
Cara Kerja :
A. Persiapan medium untuk pengenceran dan plating:
1. Siapkan 10 set tabung reaksi (masing-masing set terdiri dari 1-3 tabung reaksi)
yang berisi 99 ml aquades steril. Beri label tiap set tabung reaksi dengan waktu
inkubasi (t0, t30, t60, t90, t150, t210, t300, t390, t510, t630) dan pengenceran yang dilakukan
sebagai berikut :
Waktu pengambilan sampel Seri Pengenceran
(sampling) pada menit ke-
0 (t0) 10-1, 10-2, 10-3
30 (t30) 10-2, 10-3,10-4
60 (t60) 10-2, 10-3,10-4
90 (t90) 10-3, 10-4,10-5
150 (t150) 10-4, 10-5,10-6
210 (t210) 10-4, 10-5,10-6
300(t300) 10-4, 10-6,10-8
390 (t390) 10-4, 10-6,10-8
510 (t510) 10-6, 10-8,10-10
630 (t630) 10-6, 10-8,10-10
Praktikum Mikrobiologi Pangan-TIP-FTIA 24
2. Siapkan 10 set petridish yang berisi media Luria Broth +1,5% Bacto Agar (masing-
masing set terdiri dari 3 petridish) dan beri label dengan waktu inkubasi (t0, t30, ... t630)
dan pengenceran yang akan ditanam (10-2, 10-4, 10-6, 10-8). Contoh : t0.10-1, t0.10-2,
t0.10-3 , t30.10-2, t30.10-3, t30.10-4
Setiap liter media Luria-Bertani (Miller) broth/ Luria broth mengandung 10.0 g Tryptone,
5.0 g Yeast extract, dan 10.0 g Sodium chloride.
B. Kultivasi E.coli dan pengukuran pertumbuhan:
1. Ambil dengan pipet steril ± 5 ml kultur E.coli (5%) dan tambahkan ke dalam
erlenmeyer yang mengandung 100 ml Luria Broth. Pipet 2ml untuk dibaca pada
O.D660 nm (sebagai t0). Setelah nilai O.D. pada t0 sudah ditentukan, kocoklah
kultur dalam erlenmeyer. Kemudian secara aseptis, pindahkan 1 ml kultur
kedalam 99 ml aquades steril yang telah disiapkan pada point 1 (berlabel t0.10-2,
t0.10-4 dan t0.10-6).
2. Letakkan erlenmeyer yang berisi kultur dalam waterbath shaker pada suhu 37°
C, 120 rpm dan inkubasi selama 30 menit.
3. Ambil kultur sebanyak 0.1 ml (100 l) dari masing-masing tabung pengenceran
10-4 dan 10-6, kemudian tumbuhkan kultur pada petridish yang telah disiapkan
pada point A. 2. dengan metode spread plate, kemudian inkubasikan dengan
posisi terbalik pada suhu 37oC selama 24 jam. Hitung jumlah sel yang tumbuh
pada petridish.
Untuk selanjutnya, setiap 30 menit, secara aseptis, ambil 2 ml kultur pindahkan ke kuvet,
dan bacalah O.D. nya. Selain itu, ambil 1 ml kultur pindahkan ke dalam aquades steril
10-2 dengan seri waktu yang benar, lengkapi pengenceran berikutnya, dan tumbuhkan
pada petridish.
Praktikum Mikrobiologi Pangan-TIP-FTIA 25
BAB IV
UJI SANITASI RUANGAN DAN ALAT PENGOLAHAN
Dalam melakukan uji sanitasi ruangan alat-alat pengolahan dapat dilakukan
beberapa cara diantaranya adalah :
1. Metode Cawan Terbuka, dimana cawan berisi medium yang sudah beku
dibiarkan terbuka selama beberapa waktu tertentu didalam ruangan yang
akan diuji sanitasinya, kemudian cawan diinkubasikan untuk melihat adanya
pertumbuhan koloni.
2. Metode oles (swab), dilakukan seperti cara yang diterapkan untuk menghitung
jumlah mikrobe pada permukaan bahan pangan, misalnya daging dan ikan.
3. Metode Rodac, dilakukan terhadap alat-alat pengolahan terutama yang
mempunyai permukaan datar seperti piring, talenan, loyang, panci, dan
sebagainya, yaitu dengan cara mengadakan kontak langsung pada agar
cawan.
4. Metode Bilas, dilakukan dengan cara membilas alat-alat atau wadah yang
digunakan untuk mengolah atau mengepak makanan.
A. Tujuan : praktikan mampu menguji tingkat sanitasi alat dan ruangan yang akan
digunakan untuk pengolahan
B. Alat dan Bahan
Alat : 1 batang pengoles, cawan petri, pipet 1 ml, inkubator 30-32°C
Bahan : PCA, pepton
C. Cara Kerja :
1. Metode Cawan Terbuka (uji kontaminasi ruangan)
Setiap kelompok menyiapkan 2 cawan PCA yang diberi tanda nama ruangan
dan waktu kontak dengan udara yaitu 10 dan 20 menit. Secara bersamaan, bukalah
cawan-cawan tersebut didalam ruangan yang ditetapkan agar mengalami kontak
dengan udara didalam ruangan tersebut. Kemudian tutuplah cawan petri satu per
satu sesuai waktu yang ditentukan. Inkubasikan semua cawan pada suhu 30-32°C
selama 2-3 hari. Amati adanya pertumbuhan, dan hitung jumlah koloni yang tumbuh.
Jika pertumbuhan koloni tidak mungkin dilakukan karena pertumbuhan yang
menyebar, nyatakan secara relatif dengan tanda – sampai ++++.
Praktikum Mikrobiologi Pangan-TIP-FTIA 26
2. Metode Oles
Setiap kelompok menggunakan satu tabung yang berisi 5 ml larutan pengencer
dan batang oles yang telah disterilkan, serta 2 cawan petri steril yang diberi tanda
nama alat yang akan diuji kebersihannya serta jumlah contoh. Peraslah batang oles
dengan cara menekan-nekannya pada dinding tabung reaksi bagian atas sambil
diputar-putar. Kemudian batang oles tersebut digunakan untuk menyeka seluruh
permukaan alat-alat yang dalam penggunannya akan mengalami kontak langsung
dengan makanan. Penyekaan dilakukan sampai 3 kali, tetapi jangan dilakukan pada
bagian-bagian alat yang digunakan untuk memegang. Batang oles dimasukkan
kembali kedalam tabung, diaduk, dan tabung diputar-putar menggunakan kedua
tangan selama 2 menit. Batang oles diperas kembali pada dinding tabung, kemudian
dikeluarkan dari tabung. Lakukan pemupukan sebanyak 1 dan 0,1 ml masing-masing
pada satu cawan petri menggunakan PCA. Inkubasikan pada inkubator 30-32°C
selama 2-3 hari. Hitung koloni yang tumbuh dan nyatakan dalam jumlah koloni mikrobe
per permukaan alat dengan perhitungan sebagai berikut :
Jumlah Koloni per permukaan alat :
= Jumlah koloni per ml x 5 atau
= Jumlah koloni per 0,1 ml x 10 x 5
3. Metode Rodac
Setiap kelompok menyiapkan 1 agar cawan dengan diameter 5-6 cm yang
berisi PCA sampai pada permukaannya. Cawan kecil tersebut ditempatkan tanpa
tutup didalam cawan yang lebih besar yang bertutup. Bukalah tutup cawan, dan
dengan posisi terbalik, tekankan cawan kecil yang berisi agar pada permukaan yang
datar dari alat yang akan diuji kebersihannya selama 4 detik. Cawan kecil kemudian
diletakkan kembali kedalam cawan yang lebih besar, ditutup, dan diinkubasikan pada
suhu 30-32°C selama 2-3 hari. Hitung koloni yang tumbuh dan luas cawan petri, dan
nyatakan dalam jumlah koloni per 100 cm2 luas permukaan alat dengan perhitungan
sebagai berikut :
Jumlah Koloni per 100 cm2 permukaan :
= 100 x jumlah koloni per cawan
Luas cawan (cm2)
Praktikum Mikrobiologi Pangan-TIP-FTIA 27
Jika pertumbuhan koloni tidak mungkin dilakukan karena pertumbuhan yang
menyebar, nyatakan secara relatif dengan tanda – (tidak ada pertumbuhan)
sampai ++++.
4. Metode Bilas
Setiap kelompok menyiapkan 2 cawan petri steril yang diberi tanda nama botol
dan jumlah contoh. Masukkan 20 ml larutan pengencer kedalam botol yang berukuran
kecil yaitu botol limun atau botol selai, atau 100 ml larutan pengencer kedalam botol
berukuran besar yaitu botol kecap atau botol sirup. Bilaslah seluruh permukaan bagian
dalam botol dengan cara memutar-mutar botol secara horizontal sebanyak 10 kali.
Inokulasikan 2 cawan petri masing-masing dengan 1 ml dan 0,1 ml suspensi tersebut.
Tuangkan PCA cair, biarkan membeku, dan inkubasikan pada suhu 30-32°C selama 2-3
hari. Hitung koloni yang tumbuh dan nyatakan dalam jumlah koloni per wadah botol
dengan perhitungan sebagai berikut :
Jumlah Koloni per wadah :
= jumlah koloni per ml x 20
= jumlah koloni per 0,1 ml x 10 x 20
Praktikum Mikrobiologi Pangan-TIP-FTIA 28
BAB V
PRODUK PANGAN FERMENTASI BERBASIS SUSU
Fermentasi pangan merupakan suatu teknik pengolahan pangan dengan
memanfaatkan bantuan mikroorganisme ataupun enzim nya, yang akan merubah
sifat fisik, kimia dan organoleptik bahan menjadi produk pangan yang memiliki cita
rasa yang khas. Salah satu produk fermentasi pangan yang sangat banyak dibuat
adalah yoghurt, kefir, keju, dan lain-lain.
Kultur starter dapat diartikan sebagai mikroba yang digunakan untuk
memfermentasika suatu produk pangan. Jenis mikroba yang digunakan sebagai kultur
starter harus memiliki kemampuan untuk menghasilkan perubahan yang diinginkan
pada produk yang difermentasi. Faktor penting yang harus diperhatikan dalam
pemilihan kultur starter yang baik adalah pengaruh kultur starter terhadap karakter
produk akhir.
Kultur yang digunakan dalam proses fermentasi harus memiliki sifat-sifat (1) tidak
mengandung kontaminan, (2) jumlah mikroba seragam dan proporsional jika
berbentuk kultur campuran dan (3)aktif menghasilkan produk yang diharapkan. Kultur
yang digunakan juga hrs dalam keadaan aktif sehingga fase lag dalam proses
fermentasi berlangsung seminimal mungkin.
Kultur starter terbagi menjadi 2 yaitu kultur tunggal dan kultur campuran.
Ampuran kultur murni dapat dibuat dengan penumbuhan secara bersama-sama
secara kontinyu atau menambahkan secara terpisah dan dicampur pada saat
digunakan. Jika strain yang berbeda pada spesies yang sama atau spesies yang
berbeda ditumbuhkan bersama-sama, maka mikroba tersebut harus dapat tumbuh
bersama tanpa ada yang saling menghambat.
Tahapan untuk memproduksi kultur starter adalah sebagai berikut : (1)
menginokulasikan kultur pada medium yang sesuai, (2) inkubasi sampai kultur tersebut
mencapai tahap pertumbuhan yang optimum, (3) tambahkan pada medium
fermentasi dengan perbandingan 1:1
Tujuan : praktikan mampu membuat kultur starter yoghurt dan produk fermentasi
berbasis susu
a. Kultur Starter minuman susu fermentasi Dari Isolat Agar Miring
Bahan dan alat
Bahan : bakteri L casein strain shirota, medium MRS, aquades, susu skim
Praktikum Mikrobiologi Pangan-TIP-FTIA 29
Alat : tabung reaksi, jarum ose, bunsen, kapas, erlenmeyer 100 ml
C. Cara kerja :
Proses pembuatan kultur starter
1. stokkulturL casei strain shirotadari media agar miring digores,
lalukulturdipindahkandalam 10 ml medium MRS cairsteril,
diinkubasis uhuruangselama 2 hari (kultur A)
2. 10 ml medium MRS cair yang berisikulturdipindahkandalam 100 ml larutan skim 10%
steril, diinkubasisuhuruangselama 2 hari, kultur starter siapdigunakan (kultur B)
3. Lakukan pengujian aktivitas kultur yakult dengan prosedur berikut :
Sebanyak 100 ml susu pasteurisasi yang telah dihangatkan didalam penangas air
sampai suhu 37oC dimasukkan ke dalam tabung erlenmeyer dan ditambahkan 2%
kultur (B). campuran diinkubasi pada suhu 45oC selama 2 jam. Selanjutnya kultur
yang terbentuk (kultur C) di amati kekentalan, bau, pH dan total asam, lalu
disimpan dalam lemari es dan di suhu ruang selama 5 hari, kemudian diamati
kekentalan, bau, pH dan total asam. Pengukuran pH dilakukan dengan cara
mengambil sampel sebanyak 20 ml bahan dan diukur pH menggunakan pH meter.
Untuk pengukuran total asam, sebanyak 10 ml bahan dipipet dan dipindahkan ke
dalam tabung erlenmeyer 50 ml, dicampur dengan 10 ml air destilasi dan ditambah
5 tetes larutan fenolftalin 1%. Titrasi dilakukan menggunakan larutan NaOH 0,1
sampai timbul warna merah muda. Total asam dihitung sebagai persen asam laktat
dengan rumus sebagai berikut:
ml NaOH x N NaOH x 1/10 x 90
% asam laktat =
ml atau g sampel
Praktikum Mikrobiologi Pangan-TIP-FTIA 30
1. Starter susu fermentasi
Media agar miring
kulturLactibacilluscasei
digores 1 ose
Biakanmurni dicampurkan
diinkubasi suhu ruang selama 2 hari
Kultur
Kultur A A
100 ml larutan dicampurkan
skim 10% steril
diinkubasi suhu ruang selama 2 hari
Kultur
Kultur B B
Susupasteurisasi 100 ml
dihangatkan dalam penangas air sampai suhu 37oC
dimasukkan ke dalam erlenmeyer
Kultur B 2% dicampurkan
diinkubasi pada suhu 45oC selama 2 jam
Kultur Pengamatan kekentalan, bau, pH
Kultur C C dan total asam
disimpan suhu ruang selama 5 hari
Diagram Alir Pembuatan Starter Yakult
Praktikum Mikrobiologi Pangan-TIP-FTIA 31
2. Produk Yoghurt
Susu sapi segar
Susu skim 6 % (b/v)
Gulapasir 3 % (b/v)
Homogenisasi (Pengadukan)
Pemanasan 850C, 15 menit
Pendinginan sampai 370C
Starter yoghurt 2 % (v/v)
Flavor / warna (bila suka)
Inkubasi 250C, 24 jam
Yogurt
Diagram AlirPembuatan Yoghurt
3. Produk Kefir
Susu sapi segar
Gulapasir 3 % (b/v)
Homogenisasi (Pengadukan)
Pemanasan 850C, 15 menit
Pendinginan sampai 370C
Starter Kefir2 % (v/v)
Inkubasi 250C, 24 jam
Kefir
Diagram AlirPembuatanKefir
Praktikum Mikrobiologi Pangan-TIP-FTIA 32
BAB VI
PRODUK PANGAN FERMENTASI BERBASIS SEREALIA
Fermentasi pangan merupakan suatu teknik pengolahan pangan dengan
memanfaatkan bantuan mikroorganisme ataupun enzim nya, yang akan merubah
sifat fisik, kimia dan organoleptik bahan menjadi produk pangan yang memiliki cita
rasa yang khas. Bahan dasar dalam pembuatan produk fermentasi pangan juga
sangat beragam, diantaranya adalah serealia dan biji-bijian. Salah satu produk
fermentasi pangan yang dihasilkan dari bahan dasar serealia dan bijian-bijian adalah
tape, tempe, kecap, roti, natto dan lain-lain.
Tape adalah produk fermentasi yang berbahan dasar serealian (tape ketan)
atau ubi kayu (tape singkong). Prinsip dasar dari pembuatan tape adalah terjadinya
perubahan dari bahan dasar karbohidrat (substrat pati) menjadi senyawa gula, asam
dan sedikit alkohol. Mikroorganisme yang berperan dalam pembuatan tape juga
bervariasi dan tergolong dalam kultur campuran, antara lain Aspergillus niger dan
Sacharomyces cereviseae.
Tempe adalah produk olahan dari biji kedelai dengan bantuan kapang jenis
Rhizopus. Pada pembuatan tape, akan terjadi perubahan fisik seperti menyatunya biji-
biji kedelai tersebut menjadi suatu bahan yg padat dan kompak karena miselium dari
Rhizopus. Kelebihan dari tape adalah nilai gizi nya yang meningkat karena senyawa
yang terdapat didalamnya lebih sederhana dibandingkan biji kedelai, sehingga
mudah dicerna.
Tujuan : praktikan mampu membuat produk pangan fermentasi berbasis serealia dan
biji-bijian
Praktikum Mikrobiologi Pangan-TIP-FTIA 33
1. Produk Tempe
kedelai
sortasi
direbusselama 45 menit
dikupas kulit
direndamselamasemalam
dicuci
direbussampaimatang
Laru 1%
inokulasi
dibungkusdengandaunpisang / plastik
difermentasi selama 36 – 48 jam suhu ruang
TEMPE
Diagram AlirPembuatan Tempe
2. Produk Tape
Ubikayu
dikupas
dicuci
dikukus
didinginkan
Ragisecukupnya ditaburiragi
difermentasi
TAPE
Diagram AlirPembuatan Tape
Praktikum Mikrobiologi Pangan-TIP-FTIA 34
BAB VII
PRODUK PANGAN FERMENTASI BERBASIS BUAH DAN SAYUR
Fermentasi pangan merupakan suatu teknik pengolahan pangan dengan
memanfaatkan bantuan mikroorganisme ataupun enzim nya, yang akan merubah
sifat fisik, kimia dan organoleptik bahan menjadi produk pangan yang memiliki cita
rasa yang khas. Bahan dasar dalam pembuatan produk fermentasi pangan juga
sangat beragam, diantaranya adalah buah, sayur, dan bahan hasil perkebunan. Salah
satu produk fermentasi pangan yang dihasilkan dari bahan tersebut adalah sayur asin,
nata de coco, VCO (Virgin Coconut Oil) dan lain-lain.
Sayur asin merupakan produk fermentasi yang menggunakan bahan Sawi.
Sayur asin termasuk dalam proses fermentasi secara alami, dimana pada proses
pembuatannya tidak menggunakan penambahan kultur. Mikroba yang berperan
dalam proses ini adalah Lactobacillus plantarum, Pediococcus, yang berasal dari sawi
tersebut. Dalam hal ini, perlu dilakukan pengaturan lingkungan dengan menggunakan
garam, sehingga menghambat mikroorganisme pembusuk dan patogen.
Nata de coco adalah produk fermentasi berbasis air buah kelapa.
Mikroorganisme yang berperan adalah Acetobacter xylinum, yang akan mengubah
gula menjadi selulosa. Nata de coco sangat baik dikonsumsi, karena selulosa tersebut
membantu memperbaiki proses pencernaan
Tujuan : praktikan mampu membuat produk pangan fermentasi berbasis buah, sayur,
dan hasil perkebunan
a. Starter Nata
Alat dan Bahan
Bahan: air kelapa segar yang telah disaring, sukrosa, (NH4)SO4, MgSO4, K2SO4,
asam asetat glassial, kultur induk Acetobacter xylinum.
Alat: botol, kertas koran, karet, autoclave
Cara Kerja :
1. air kelapa segar (1000 ml) disaring dengan kertas saring agar terpisah dari kotoran
2. air kelapa ditambah nutrisi sukrosa 10%, (NH4)SO4 0,5% K2HPO4 0,03%, MgSO4
0,03%(b/v) dan asam asetat glasial 2% (v/v) dipanaskan sampai mencapai
Praktikum Mikrobiologi Pangan-TIP-FTIA 35
mendidih, dituang ke dalam botol steril, ditutup kertas koran dan didinginkan dalam
suhu ruang selama 24 jam.
3. setelah dingin, dilakukan inokulasi dengan starter Acetobacter xylinum sebanyak
10% (v/v) inkubasi selama 5-7 hari pada suhu ruang
4. starter siap digunakan untuk pembuatan nata
5. amati perubahan pembentukan pelikel
1. Starter Nata
Air kelapa
1000 ml
disaring kotoran
-sukrosa 10% (b/v)
- (NH4)SO4 0,5% (b/v)
- K2HPO4 0,03% (b/v) dipanaskan hingga mendidih
- MgSO4 0,03% (b/v)
- asamasetatglasial 2% (v/v)
dituang dalam wadah steril
ditutup dengan kertas koran
didinginkan pada suhu ruang selama 24 jam
atau sampai media mencapai suhu ruang
Acetobacterxylinum 10% (v/v)
diinokulasi
diinkubasi pada suhu ruang selama 5 – 7 hari
starternata Pengamatanperubahanpembentuk
anpelikel (ketebalan)
Diagram Alir Pembuatan Starter Nata
Praktikum Mikrobiologi Pangan-TIP-FTIA 36
2. Produk Nata
Air kelapa
1000 ml
disaring kotoran
-sukrosa 10% (b/v)
- (NH4)SO4 0,5% (b/v)
- K2HPO4 0,03% (b/v) dipanaskan hingga mendidih
- MgSO4 0,03% (b/v)
- asamasetatglasial 2% (v/v)
dituang dalam wadah steril
ditutup dengan kertas koran
didinginkan pada suhu ruang selama 24 jam
atau sampai media mencapai suhu ruang
Starter Nata 10 % (v/v)
diinokulasi
diinkubasi pada suhu ruang selama 5 – 7 hari
Nata de coco Pengamatanperubahanpembentuk
anpelikel (ketebalan)
Diagram Alir Pembuatan Nata de Coco
Praktikum Mikrobiologi Pangan-TIP-FTIA 37
3. ProdukSayurAsin
Sawihijau
Beras Garam
Dipisahkandaunnya, dicuci,
dandilayukan
Garam
Dimasak & diambil airnya
Diremas-remas
Air Tajin
Direndam
SayurAsin
Diagram Alir Pembuatan Sayur Asin
Praktikum Mikrobiologi Pangan-TIP-FTIA 38
4. Produk VCO (Virgin Coconut Oil)
BuahKelapaTua
Dikupasdandibelah
DagingBuahKelapa
Diparutdenganmesinparut
Air (70 0C1 0C)
Air : Kelapa parut (1 : 1) DagingKelapaParut
Pengepresan
Santan
Pemisahan
(dibiarkan 1-2 jam)
SantanKelapa (krim) Air Santan
Fermentasi spontan pada suhu kamar selama 14 jam
Pemisahan
Air danBlondo FraksiMinyak
Penyaringan Blondo
MinyakKelapaMurni
Diagram Alir Pembuatan Virgin Coconut Oil
Praktikum Mikrobiologi Pangan-TIP-FTIA 39
Anda mungkin juga menyukai
- Diktat Penuntun Praktikum MikrobiologiDokumen37 halamanDiktat Penuntun Praktikum MikrobiologiSurya FatmadewiBelum ada peringkat
- LKP 2 - Ulfah Faoziah - 1BDokumen8 halamanLKP 2 - Ulfah Faoziah - 1BUlfah FaoziahBelum ada peringkat
- BK Petjk MikroP Agrotek Agust2014 Jan15 Vita PDFDokumen43 halamanBK Petjk MikroP Agrotek Agust2014 Jan15 Vita PDFJeni AriyantiBelum ada peringkat
- Laporan Pembuatan Media Kelompok 5Dokumen23 halamanLaporan Pembuatan Media Kelompok 5tia bakriBelum ada peringkat
- Petunjuk Praktik MikrobiologiDokumen18 halamanPetunjuk Praktik MikrobiologiFafaaBelum ada peringkat
- Print Sterilisasi 1Dokumen40 halamanPrint Sterilisasi 1Rini AnggreiniBelum ada peringkat
- Laporan Pembuatan Media Agar MiringDokumen6 halamanLaporan Pembuatan Media Agar MiringAlma HadisyahBelum ada peringkat
- Vidya Putri Yuananda (194106) Laporan Uji Angka Kapang Atau Khamir MikroDokumen16 halamanVidya Putri Yuananda (194106) Laporan Uji Angka Kapang Atau Khamir MikroVidya YuanandaBelum ada peringkat
- Buku Praktikum Mikrobiologi Blok 5 Full-1Dokumen45 halamanBuku Praktikum Mikrobiologi Blok 5 Full-1ELISABETH CINDY SETYAWANBelum ada peringkat
- Laporan Praktikum Teknologi BioprosesDokumen71 halamanLaporan Praktikum Teknologi BioprosesasmaraputriBelum ada peringkat
- Modul Prak. Mikrobiologi PDFDokumen50 halamanModul Prak. Mikrobiologi PDFNonha ElsamanthaBelum ada peringkat
- ISOLASI BAKTERIDokumen15 halamanISOLASI BAKTERIIzchak Zhesoatoe100% (3)
- LAPORAN BakteriDokumen43 halamanLAPORAN BakteriHendrik_NurfitriantoBelum ada peringkat
- Laboratorium Mikrobiologi dan Pengujian MikrobiologiDokumen56 halamanLaboratorium Mikrobiologi dan Pengujian MikrobiologiNiko TanzillafitsiBelum ada peringkat
- Buku Petunjuk Praktikum Biosel - Mikro 2019 PDFDokumen39 halamanBuku Petunjuk Praktikum Biosel - Mikro 2019 PDFSyahrul MeidikaBelum ada peringkat
- Sap Kuliah & Praktikum MikrobiologiDokumen40 halamanSap Kuliah & Praktikum MikrobiologiKuntum KhoiraniBelum ada peringkat
- Laporan IsolasiDokumen20 halamanLaporan Isolasitia bakriBelum ada peringkat
- Laporan Praktikum 2Dokumen12 halamanLaporan Praktikum 2Ibnu Sitna FajarBelum ada peringkat
- Laporan Praktikum Mikro 1Dokumen17 halamanLaporan Praktikum Mikro 1Sarman DavidBelum ada peringkat
- LAPORAN RESMI PRAKTIKUM MIKROBIOLOGI andDokumen48 halamanLAPORAN RESMI PRAKTIKUM MIKROBIOLOGI andEka SaputraBelum ada peringkat
- Mikrobiologi PanganDokumen94 halamanMikrobiologi Pangansgita nzmBelum ada peringkat
- MODUL4.1Dokumen15 halamanMODUL4.1Bunga Tresna MaduriBelum ada peringkat
- Teknik Diagnosa Penyakit IkanDokumen12 halamanTeknik Diagnosa Penyakit Ikannurfitri rahimBelum ada peringkat
- Media MikrobiologiDokumen15 halamanMedia MikrobiologiDevi Epi DevirinBelum ada peringkat
- Makalah Analisis Mikro Sediaan Kosmetik-Azzahra Aulya Rahmah (15020180140) - C7Dokumen17 halamanMakalah Analisis Mikro Sediaan Kosmetik-Azzahra Aulya Rahmah (15020180140) - C7ZahraBelum ada peringkat
- Penuntun Praktikum Biokimia S1Dokumen12 halamanPenuntun Praktikum Biokimia S1Zahra SalsabilaBelum ada peringkat
- Laporan 3 AuliyaDokumen9 halamanLaporan 3 AuliyaCinta NurdiwanBelum ada peringkat
- Copy-Diktat Mikrobiologi Farmasi 2019 PDFDokumen62 halamanCopy-Diktat Mikrobiologi Farmasi 2019 PDFJungwoo NimBelum ada peringkat
- Modul MikroDokumen54 halamanModul MikroEsnaeni FitriBelum ada peringkat
- ACARA I MartheffanyDokumen18 halamanACARA I MartheffanyMuhammad Aprilian SudrajatBelum ada peringkat
- Makalah Pengelolaan Laboratorium Pengelolaan Limbah LaboratoriumDokumen21 halamanMakalah Pengelolaan Laboratorium Pengelolaan Limbah Laboratoriumsofi izatiBelum ada peringkat
- Laporan PraktikumDokumen8 halamanLaporan PraktikumChaya Stia ClaluiBelum ada peringkat
- ApatuhDokumen15 halamanApatuhBucinBelum ada peringkat
- Acc - Ufl - Syasya Nazifa (2004103010060)Dokumen21 halamanAcc - Ufl - Syasya Nazifa (2004103010060)Al FatihBelum ada peringkat
- MEDIA MIKROBIOLOGIDokumen12 halamanMEDIA MIKROBIOLOGIMuhammad AlangBelum ada peringkat
- UJI MIKROBIOLOGI LAPORAN PRAKTIKUMDokumen21 halamanUJI MIKROBIOLOGI LAPORAN PRAKTIKUMfaradillahBelum ada peringkat
- Media pertumbuhan mikroorganismeDokumen13 halamanMedia pertumbuhan mikroorganismeMarsya Diah IzdiharBelum ada peringkat
- Laporan Praktikum Mikrobiologi AwanDokumen12 halamanLaporan Praktikum Mikrobiologi AwanhafidBelum ada peringkat
- Laporan Praktikum Mikrobiologi IDokumen10 halamanLaporan Praktikum Mikrobiologi Ieko fitriansyahBelum ada peringkat
- MEDIA PEMBUATANDokumen12 halamanMEDIA PEMBUATANiinndah_Belum ada peringkat
- Acara IIDokumen17 halamanAcara IIAnindya NusaraBelum ada peringkat
- Laporan Mikro Ke-1 SesqiDokumen12 halamanLaporan Mikro Ke-1 SesqiAmallia Sesqi100% (1)
- Laporan Praktikum Pembuatan Media Dan St-with-cover-page-V2Dokumen17 halamanLaporan Praktikum Pembuatan Media Dan St-with-cover-page-V2Ahmat FajarBelum ada peringkat
- Laporan Praktikum Mikrobiologi Bab 1Dokumen30 halamanLaporan Praktikum Mikrobiologi Bab 1Reghi Aji SaputraBelum ada peringkat
- Laporan Praktikum Mikrobiologi MakananDokumen46 halamanLaporan Praktikum Mikrobiologi MakananStephanie SnowBelum ada peringkat
- Agar Darah CTHDokumen17 halamanAgar Darah CTHSeptrianiNainggolanBelum ada peringkat
- Laporan LabkesDokumen17 halamanLaporan LabkesSuhardatan HaniBelum ada peringkat
- SterilisasiDokumen19 halamanSterilisasiHildiana AprilianiBelum ada peringkat
- PENGOLAHAN LIMBAH LABDokumen19 halamanPENGOLAHAN LIMBAH LABMirandaAyuBelum ada peringkat
- LAPORAN PKM. C4.Syasya Nazifa. 2004103010060Dokumen26 halamanLAPORAN PKM. C4.Syasya Nazifa. 2004103010060Al FatihBelum ada peringkat
- Modul Mikrobiologi PanganDokumen32 halamanModul Mikrobiologi PanganDara DeyanaBelum ada peringkat
- Pembuatan Medium Dan SterilisasiDokumen26 halamanPembuatan Medium Dan SterilisasiEndah Pitaloka100% (1)
- Jamur MikroskopisDokumen17 halamanJamur MikroskopisAgung Wiriat PutraBelum ada peringkat
- Laporan Praktikum Mikrobiologi Faktor LingkDokumen16 halamanLaporan Praktikum Mikrobiologi Faktor LingkWa Ode Leni MarlinaBelum ada peringkat
- MAKALAH BIAKAN MURNIDokumen14 halamanMAKALAH BIAKAN MURNIAfif AbdullahBelum ada peringkat
- Mikrobiologi Medis I: Patogen dan Mikrobioma ManusiaDari EverandMikrobiologi Medis I: Patogen dan Mikrobioma ManusiaPenilaian: 4 dari 5 bintang4/5 (11)
- Mikrobiologi Perubatan I: Patogen dan Mikrobiologi ManusiaDari EverandMikrobiologi Perubatan I: Patogen dan Mikrobiologi ManusiaPenilaian: 2.5 dari 5 bintang2.5/5 (2)
- Teknik Asas Pembiakan Hibrid Ikan Keli Thailand (Clarias sp.)Dari EverandTeknik Asas Pembiakan Hibrid Ikan Keli Thailand (Clarias sp.)Penilaian: 5 dari 5 bintang5/5 (2)
- Coronavirus Covid-19. Membela diri. Cara menghindari penularan. Bagaimana melindungi keluarga dan pekerjaan Anda. Diperbarui edisi keempat.Dari EverandCoronavirus Covid-19. Membela diri. Cara menghindari penularan. Bagaimana melindungi keluarga dan pekerjaan Anda. Diperbarui edisi keempat.Penilaian: 5 dari 5 bintang5/5 (2)
- Buku Masakan untuk Penyembuhan Skoliosis Anda: Jadikan tulang belakang lebih sehat dengan mengatur apa yang anda makan!Dari EverandBuku Masakan untuk Penyembuhan Skoliosis Anda: Jadikan tulang belakang lebih sehat dengan mengatur apa yang anda makan!Penilaian: 3.5 dari 5 bintang3.5/5 (4)
- Brahmantio Gilang KelanaDokumen4 halamanBrahmantio Gilang KelanaAulia AmienBelum ada peringkat
- Brahmantio Gilang KelanaDokumen4 halamanBrahmantio Gilang KelanaAulia AmienBelum ada peringkat
- Masyarakar Ekonomi Asean-1Dokumen1 halamanMasyarakar Ekonomi Asean-1Aulia AmienBelum ada peringkat
- OPTIMASI PENGOLAHANDokumen8 halamanOPTIMASI PENGOLAHANDiniYuliantiBelum ada peringkat
- M Arif Afandi - 2041610016 - Manajemen KeuanganDokumen4 halamanM Arif Afandi - 2041610016 - Manajemen KeuanganAulia AmienBelum ada peringkat
- Pengawetan Dengan Suhu RendahDokumen2 halamanPengawetan Dengan Suhu RendahAulia AmienBelum ada peringkat
- Pengolahan Minimal Pada Sayur Dan BuahDokumen16 halamanPengolahan Minimal Pada Sayur Dan BuahAulia AmienBelum ada peringkat
- Analisis Kasus Bangkrutnya KodakDokumen30 halamanAnalisis Kasus Bangkrutnya Kodaklulupuspitaa90% (20)
- Rundown Kasaran Desbin - 1-1Dokumen62 halamanRundown Kasaran Desbin - 1-1Aulia AmienBelum ada peringkat
- Brahmantio Gilang KelanaDokumen4 halamanBrahmantio Gilang KelanaAulia AmienBelum ada peringkat
- ModuullDokumen4 halamanModuullAulia AmienBelum ada peringkat
- Uji BakteriDokumen7 halamanUji BakteriAulia AmienBelum ada peringkat
- Flowchart Pengumpulan Jurnal LaporanDokumen2 halamanFlowchart Pengumpulan Jurnal LaporanAulia AmienBelum ada peringkat
- OPTIMASI PENGOLAHANDokumen8 halamanOPTIMASI PENGOLAHANDiniYuliantiBelum ada peringkat
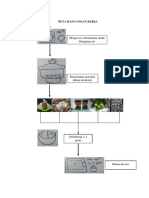
- Peta Rancangan KerjaDokumen6 halamanPeta Rancangan KerjaAulia AmienBelum ada peringkat
- Masyarakar Ekonomi Asean-1Dokumen1 halamanMasyarakar Ekonomi Asean-1Aulia AmienBelum ada peringkat
- Proses Pembuatan BanDokumen3 halamanProses Pembuatan BanAulia AmienBelum ada peringkat
- Jurnal Praktikum Pengaruh Intrinsik Dan Ekstrinsik MikrobaDokumen21 halamanJurnal Praktikum Pengaruh Intrinsik Dan Ekstrinsik MikrobaAulia AmienBelum ada peringkat
- KendelDokumen4 halamanKendelAulia AmienBelum ada peringkat
- Study Case DesBinDokumen1 halamanStudy Case DesBinAulia AmienBelum ada peringkat
- BULETINDokumen1 halamanBULETINAulia AmienBelum ada peringkat
- Masyarakar Ekonomi Asean-1Dokumen1 halamanMasyarakar Ekonomi Asean-1Aulia AmienBelum ada peringkat
- BULETINDokumen1 halamanBULETINAulia AmienBelum ada peringkat
- Karakteristik Biologi Bawang MerahDokumen5 halamanKarakteristik Biologi Bawang MerahAulia AmienBelum ada peringkat
- 01 JurnalPBAI5 Irawati Ningsih 2041610011Dokumen13 halaman01 JurnalPBAI5 Irawati Ningsih 2041610011Aulia AmienBelum ada peringkat
- AwewDokumen11 halamanAwewAulia AmienBelum ada peringkat
- Laporan Praktikum Manajemen Limbah IndusDokumen31 halamanLaporan Praktikum Manajemen Limbah IndusAulia AmienBelum ada peringkat
- Bab ViiiDokumen4 halamanBab ViiiAulia AmienBelum ada peringkat
- Yudha EssayDokumen9 halamanYudha EssayAulia AmienBelum ada peringkat