Bab 4 Data Wahyudi Saputra Sulfat
Diunggah oleh
Wahyudi Saputra0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
7 tayangan3 halamanJudul Asli
BAB 4 DATA WAHYUDI SAPUTRA SULFAT
Hak Cipta
© © All Rights Reserved
Format Tersedia
PDF, TXT atau baca online dari Scribd
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PDF, TXT atau baca online dari Scribd
0 penilaian0% menganggap dokumen ini bermanfaat (0 suara)
7 tayangan3 halamanBab 4 Data Wahyudi Saputra Sulfat
Diunggah oleh
Wahyudi SaputraHak Cipta:
© All Rights Reserved
Format Tersedia
Unduh sebagai PDF, TXT atau baca online dari Scribd
Anda di halaman 1dari 3
BAB IV
HASIL DAN PEMBAHASAN
4.1 Data
Berikut data yang didapatkan dari hasil praktikum :
4.1.1 Larutan Standar
Tabel 4.1 Tabel Larutan Standar
Konsentrasi (ppm) (X) Absorban (Y)
0 0,067
10 0,074
20 0,076
30 0,089
40 0,112
50 0,118
Sumber: Data Hasil Pratikum Kimia Lingkungan, 2022
4.1.2 Larutan Sampel
Tabel 4.2 Larutan Sampel
Jenis Larutan Absorban
Sampel 0,086
Sumber: Data Hasil Pratikum Kimia Lingkungan, 2022
4.2 Perhitungan
Untuk pengenceran menggunakan rumus:
V1 × M1 =V2 × M2
1. Volume Pembuatan Larutan Standar Konsentrasi 0 ppm:
V1 × M1 =V2 × M2
V1 × 1000 ppm =100 ml× 0 ppm
V1 = 0 ml
2. Volume Pembuatan Larutan Standar Konsentrasi 10 ppm:
V1 × M1 =V2 × M2
V1 × 1000 ppm =100 ml× 10 ppm
V1 = 1 ml
KEMENTERIAN PENDIDIKAN, KEBUDAYAAN, RISET, DAN
TEKNOLOGI
FAKULTAS TEKNIK, UNIVERSITAS ANDALAS
DEPARTEMEN TEKNIK LINGKUNGAN
LABORATORIUM AIR
Kampus Unand Limau Manis, Padang 25163
3. Volume Pembuatan Larutan Standar Konsentrasi 20 ppm:
V1 × M1 =V2 × M2
V1 × 1000 ppm =100 ml× 20 ppm
V1 = 2 ml
4. Volume Pembuatan Larutan Standar Konsentrasi 30 ppm:
V1 × M1 =V2 × M2
V1 × 1000 ppm =100 ml× 30 ppm
V1 = 3 ml
5. Volume Pembuatan Larutan Standar Konsentrasi 40 ppm:
V1 × M1 =V2 × M2
V1 × 1000 ppm =100 ml× 40 ppm
V1 = 4 ml
6. Volume Pembuatan Larutan Standar Konsentrasi 50 ppm:
V1 × M1 =V2 × M2
V1 × 1000 ppm =100 ml× 50 ppm
V1 = 5 ml
Tabel 4.3 Perhitungan Pengenceran Larutan Standar
Nomor M1 (ppm) V1 (ml)
1 1000 0
2 1000 1
3 1000 2
4 1000 3
5 1000 4
6 1000 5
Sumber: Data Hasil Praktikum Kimia Lingkungan, 2022
Berikut grafik hubungan konsentrasi terhadap absorban yang telah dilakukan:
WAHYUDI SAPUTRA 2110941003
KEMENTERIAN PENDIDIKAN, KEBUDAYAAN, RISET, DAN
TEKNOLOGI
FAKULTAS TEKNIK, UNIVERSITAS ANDALAS
DEPARTEMEN TEKNIK LINGKUNGAN
LABORATORIUM AIR
Kampus Unand Limau Manis, Padang 25163
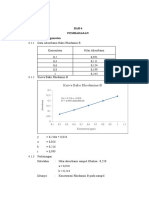
Grafik 4.1 Hubungan Konsentrasi Larutan Standar terhadap Absorban
0,14
0,12
y = 0,0011x + 0,062
R² = 0,9276
0,1
0,08
Absorban
0,06
0,04
0,02
0
0 10 20 30 40 50 60
Larutan Standar (ppm)
Persamaan untuk mendapatkan kurva regresi linear, yaitu:
y = 0,0011x+ 0,062
Keterangan:
x = konsentrasi
y = absorban
Dapat ditentukan konsentrasi sulfat pada larutan sampel sebagai berikut:
y = 0,0011x + 0,062
0,086 = 0,0011x + 0,062
x = 21,8182 mg/L
Konsentrasi sulfat yang didapatkan dari sampel praktikum adalah sebesar 21,8182
mg/L.
WAHYUDI SAPUTRA 2110941003
Anda mungkin juga menyukai
- Bab 4 Perhitungan FosfatDokumen4 halamanBab 4 Perhitungan FosfatWahyudi SaputraBelum ada peringkat
- BAB IV Data Dan PerhitunganDokumen2 halamanBAB IV Data Dan PerhitunganhannaBelum ada peringkat
- Bab 4 Perhitungan FosfatDokumen4 halamanBab 4 Perhitungan FosfatWahyudi SaputraBelum ada peringkat
- Laporan Prak Instrumen 6 Pengukuran Sediaan ObatDokumen9 halamanLaporan Prak Instrumen 6 Pengukuran Sediaan ObatAlisa AdistiaBelum ada peringkat
- 3D - Kelompok 2 - Spektrofotometri UV-VisDokumen6 halaman3D - Kelompok 2 - Spektrofotometri UV-VisWa FfaBelum ada peringkat
- Laporan Praktikum Instrumentasi Kelompok 3Dokumen9 halamanLaporan Praktikum Instrumentasi Kelompok 3Tasha AsyariBelum ada peringkat
- Laporan1 AnalyticalChemistry Kelompok4 BA46Dokumen11 halamanLaporan1 AnalyticalChemistry Kelompok4 BA46Nur Fathonah SadekBelum ada peringkat
- Jonathan Stefanus Modul 5Dokumen5 halamanJonathan Stefanus Modul 5JONATHAN STEFANUSBelum ada peringkat
- Ekstraksi Cair-Cair PDFDokumen12 halamanEkstraksi Cair-Cair PDFElta Melan FitriyaniBelum ada peringkat
- Pembahasan NitratDokumen11 halamanPembahasan NitratMonika Utami AndryasBelum ada peringkat
- SPEKTROFOTO UV-Vis "Metode Estimasi Simultan Untuk Sampel Multikomponen Prinsip Aditif Absorbansi"Dokumen12 halamanSPEKTROFOTO UV-Vis "Metode Estimasi Simultan Untuk Sampel Multikomponen Prinsip Aditif Absorbansi"MISSYE DAYANA SABILLABelum ada peringkat
- Laporan Kai P5 - B2-2Dokumen12 halamanLaporan Kai P5 - B2-2Aira Putri renansaBelum ada peringkat
- Laporan PraktikumDokumen14 halamanLaporan PraktikumchyeebiyooBelum ada peringkat
- Agung Setiadi Nugroho - F3 - Spektro GCDokumen15 halamanAgung Setiadi Nugroho - F3 - Spektro GCAGUNG SETIADI NUGROHOBelum ada peringkat
- Laporan Penentuan Tetapan Pengionan Secara Spektrofotometri 1Dokumen14 halamanLaporan Penentuan Tetapan Pengionan Secara Spektrofotometri 1Jeffry Todo JeremiaBelum ada peringkat
- Bab 4 KPT 11Dokumen10 halamanBab 4 KPT 11Defri AfBelum ada peringkat
- Bab Iv Data Dan Pembahasan: 4.1 Data 4.1.1 Data Adsorban Larutan StandarDokumen9 halamanBab Iv Data Dan Pembahasan: 4.1 Data 4.1.1 Data Adsorban Larutan StandarDICKY WAHYUDI SIMBOLONBelum ada peringkat
- Percobaan 1 SpektrofotometriDokumen15 halamanPercobaan 1 SpektrofotometriAinayya AnnihayahBelum ada peringkat
- Shinta Nurika - LP - Spektro FenolDokumen14 halamanShinta Nurika - LP - Spektro Fenolnurika shintaBelum ada peringkat
- LAPRES Percobaan V - Hidayaturrahman - 1848201110052 - A18Dokumen14 halamanLAPRES Percobaan V - Hidayaturrahman - 1848201110052 - A18HidayaturrahmanBelum ada peringkat
- Analisis Intrumentasi Cu.Dokumen9 halamanAnalisis Intrumentasi Cu.Sipaa SipaaBelum ada peringkat
- Laporan NirDokumen7 halamanLaporan NirpipitfpuspitaBelum ada peringkat
- Valeria Uji AntioksidanDokumen16 halamanValeria Uji AntioksidanValeria MaloBelum ada peringkat
- LKM Metode Penambahan Standar-1 Indahhh HaerunissaDokumen15 halamanLKM Metode Penambahan Standar-1 Indahhh HaerunissaRahul AlfariziBelum ada peringkat
- Laporan Praktikum Ekstraksi Cair - Cair Kel.1Dokumen18 halamanLaporan Praktikum Ekstraksi Cair - Cair Kel.1salma nabila putriBelum ada peringkat
- Dokumen - Tips - Laporan Praktikum AntalginDokumen16 halamanDokumen - Tips - Laporan Praktikum AntalginShasha elshaBelum ada peringkat
- FINISH Laporan SpektrofotometriDokumen66 halamanFINISH Laporan SpektrofotometriEMardinus0% (1)
- Lampiran AasDokumen8 halamanLampiran AasTamia ElindaBelum ada peringkat
- PO6 - 22 - Waridatul HasanahDokumen7 halamanPO6 - 22 - Waridatul HasanahwaridaBelum ada peringkat
- Laporan Praktikum Penetapan Ciprpfloxacin Spektrofotometri Uv-VisDokumen13 halamanLaporan Praktikum Penetapan Ciprpfloxacin Spektrofotometri Uv-VisdesyBelum ada peringkat
- Lapres P2 AnalisisDokumen12 halamanLapres P2 AnalisisRony SetiawannBelum ada peringkat
- Gadis Faradipa - PENENTUAN NO2 DENGAN SPEKTROFOTOMETER UV-VIS - AisyahDokumen8 halamanGadis Faradipa - PENENTUAN NO2 DENGAN SPEKTROFOTOMETER UV-VIS - AisyahDipsi HaechanBelum ada peringkat
- Hidrolisis Pati Dan AnalisisnyaDokumen5 halamanHidrolisis Pati Dan AnalisisnyaRama JhowryBelum ada peringkat
- Bab 1-4 Detergen - Revisi 170117Dokumen8 halamanBab 1-4 Detergen - Revisi 170117putri atmajaBelum ada peringkat
- Laporan Seminar Filtrasi (D-09)Dokumen12 halamanLaporan Seminar Filtrasi (D-09)Dekabris Avogardo GeraldBelum ada peringkat
- Bab Iii - Bab IvDokumen9 halamanBab Iii - Bab IvAnisa FitriaBelum ada peringkat
- BAB 4 Perc 4Dokumen4 halamanBAB 4 Perc 4Nurjana AndrisBelum ada peringkat
- Hasil Kadar Polifenol YosephinaDokumen4 halamanHasil Kadar Polifenol YosephinaKristian AgustinusBelum ada peringkat
- Tugas LatihanDokumen3 halamanTugas LatihanAnggita Kurnia RinjaniBelum ada peringkat
- Gadis Faradipa - p4 - AvatarDokumen7 halamanGadis Faradipa - p4 - AvatarDipsi HaechanBelum ada peringkat
- Analisa Kadar Tembaga IiDokumen10 halamanAnalisa Kadar Tembaga Iifadel rahmatBelum ada peringkat
- Kadar Total FenolDokumen6 halamanKadar Total FenolAisyah NurmafajahBelum ada peringkat
- BAB IV Dan V Kurva KalibrasiDokumen4 halamanBAB IV Dan V Kurva KalibrasiRizki AmaliaBelum ada peringkat
- Bab 1-4 Detergen - AccDokumen8 halamanBab 1-4 Detergen - Accputri atmajaBelum ada peringkat
- LAPRES FitoDokumen14 halamanLAPRES FitoHidayaturrahmanBelum ada peringkat
- Cara Membuat Kurva StandarDokumen2 halamanCara Membuat Kurva Standarfeni ariatiBelum ada peringkat
- LAPORAN PRAKTIKUM BIOKIMIA-dikonversi PDFDokumen15 halamanLAPORAN PRAKTIKUM BIOKIMIA-dikonversi PDFDewi MasitohBelum ada peringkat
- PRAKTIKUM 1 BLOK AKF II OkeDokumen14 halamanPRAKTIKUM 1 BLOK AKF II OkeAmila Dzaky RBelum ada peringkat
- F1b019037-Alzaidane Widad Taufik-Penentuan Panjang Gelombang Maksimum Metilen BiruDokumen19 halamanF1b019037-Alzaidane Widad Taufik-Penentuan Panjang Gelombang Maksimum Metilen BiruAlzaidane widad taufikBelum ada peringkat
- BismillahDokumen9 halamanBismillahlisviaBelum ada peringkat
- KFA Kerpok 3Dokumen15 halamanKFA Kerpok 3Febbio YoghatamaBelum ada peringkat
- Laporan PraktikumDokumen13 halamanLaporan PraktikumHilda KhairunnisaBelum ada peringkat
- Aprilia Kurnia P - P4. PENENTUAN COD DALAM AIR LIMBAHDokumen6 halamanAprilia Kurnia P - P4. PENENTUAN COD DALAM AIR LIMBAHaprilia kurnia putriBelum ada peringkat
- Laporan Praktikum Farfis 1Dokumen22 halamanLaporan Praktikum Farfis 1tarisa perolinBelum ada peringkat
- Modul g4 DinamikaDokumen9 halamanModul g4 DinamikaAlsha AndiniBelum ada peringkat
- Hasil Uji SuciDokumen3 halamanHasil Uji SuciAlfat IsnawansyahBelum ada peringkat
- Laporan KurvaDokumen5 halamanLaporan Kurvaine rosmala dewiBelum ada peringkat
- S5A DisolusiDokumen13 halamanS5A Disolusilala liliBelum ada peringkat
- Muliati Supandi - Vitamin CDokumen12 halamanMuliati Supandi - Vitamin CMuliatiSupandi100% (1)
- AMBANG 3 SHIFT 1-REVISI FIKS YaDokumen22 halamanAMBANG 3 SHIFT 1-REVISI FIKS YaWahyudi SaputraBelum ada peringkat
- Studi Kasus Hidro OkDokumen8 halamanStudi Kasus Hidro OkWahyudi SaputraBelum ada peringkat
- Bab 1 3 OksigenDokumen8 halamanBab 1 3 OksigenWahyudi SaputraBelum ada peringkat
- BAB II AMBANG 3 SHIFT 1 Revisi 2xDokumen14 halamanBAB II AMBANG 3 SHIFT 1 Revisi 2xWahyudi SaputraBelum ada peringkat
- AMBANG 3 SHIFT 1-REVISI FIKS YaDokumen22 halamanAMBANG 3 SHIFT 1-REVISI FIKS YaWahyudi SaputraBelum ada peringkat
- Bab 4 Dan 5 Wahyudi AccDokumen22 halamanBab 4 Dan 5 Wahyudi AccWahyudi SaputraBelum ada peringkat
- Analisis Ambang 3 Shift 1Dokumen24 halamanAnalisis Ambang 3 Shift 1Wahyudi SaputraBelum ada peringkat
- Tugas Sedimentasi 1 Dan 2 - UPFK Genap 2023 - Kelas DDokumen1 halamanTugas Sedimentasi 1 Dan 2 - UPFK Genap 2023 - Kelas DWahyudi SaputraBelum ada peringkat
- Employee EmpowermentDokumen2 halamanEmployee EmpowermentWahyudi SaputraBelum ada peringkat
- Sppma Bab 4,5,6 Kelompok 2Dokumen18 halamanSppma Bab 4,5,6 Kelompok 2Wahyudi SaputraBelum ada peringkat
- Aspek FinansialDokumen10 halamanAspek FinansialWahyudi SaputraBelum ada peringkat
- Kelompok 2 Sppma Bab 7,8,9Dokumen17 halamanKelompok 2 Sppma Bab 7,8,9Wahyudi SaputraBelum ada peringkat
- Aspek FinansialDokumen10 halamanAspek FinansialWahyudi SaputraBelum ada peringkat
- Kuliah 7 Non Linear Fungsi Cobb Dauglas)Dokumen22 halamanKuliah 7 Non Linear Fungsi Cobb Dauglas)Wahyudi SaputraBelum ada peringkat
- Laprak F - Silvi Refzunia - 2010941003Dokumen20 halamanLaprak F - Silvi Refzunia - 2010941003Wahyudi SaputraBelum ada peringkat
- Sistem Perencanaan Dan Pengendalian Manajemen BAB 7,8, Dan 9Dokumen17 halamanSistem Perencanaan Dan Pengendalian Manajemen BAB 7,8, Dan 9Wahyudi SaputraBelum ada peringkat
- Surat PernyataanDokumen1 halamanSurat PernyataanWahyudi SaputraBelum ada peringkat
- Mekanisme Perjalanan ToksisitasDokumen1 halamanMekanisme Perjalanan ToksisitasWahyudi SaputraBelum ada peringkat
- Sulfat AnggunDokumen16 halamanSulfat AnggunWahyudi SaputraBelum ada peringkat
- Primal DualDokumen12 halamanPrimal DualWahyudi SaputraBelum ada peringkat
- Silvi Refzunia - PG BAB 2Dokumen22 halamanSilvi Refzunia - PG BAB 2Wahyudi SaputraBelum ada peringkat
- BAB II KA - Annisa Fairuz Elkansha 2010943018 RevisiDokumen6 halamanBAB II KA - Annisa Fairuz Elkansha 2010943018 RevisiWahyudi SaputraBelum ada peringkat
- Bab 4&5Dokumen4 halamanBab 4&5Wahyudi SaputraBelum ada peringkat
- BAB II KA - Titan Diovanda Edde 2010941010Dokumen8 halamanBAB II KA - Titan Diovanda Edde 2010941010Wahyudi SaputraBelum ada peringkat
- Bab 3 Fosfat Fix BGTDokumen3 halamanBab 3 Fosfat Fix BGTWahyudi SaputraBelum ada peringkat
- Bab 3 Fosfat FixDokumen4 halamanBab 3 Fosfat FixWahyudi SaputraBelum ada peringkat
- Bab 3 FosfatDokumen4 halamanBab 3 FosfatWahyudi SaputraBelum ada peringkat