m.2 Galvanic
Diunggah oleh
rizky saptahadiHak Cipta
Format Tersedia
Bagikan dokumen Ini
Apakah menurut Anda dokumen ini bermanfaat?
Apakah konten ini tidak pantas?
Laporkan Dokumen IniHak Cipta:
Format Tersedia
m.2 Galvanic
Diunggah oleh
rizky saptahadiHak Cipta:
Format Tersedia
BAB III
KOROSI GALVANIK
Pada bab III ini berisikan tentang tujuan, teori dasar, alat dan bahan, metodelogi
praktikum, data pengamatan, perhitungan, persamaan reaksi, analisa dan pembahasan,
dan kesimpulan
3.1. Tujuan
1. Mengetahui dan memahami tahapan proses dari pengujian korosi galvanik.
2. Mengetahui dan memahami mekanisme terjadinya korosi galvanik.
3. Mengetahui dan memahami factor yang dapat mempengaruhi proses korosi
galvanik.
4. Mengetahui parameter yang mempengaruhi korosi galvanik.
5. Mengetahui fenomena yang terjadi pada logam yang telah diamati selama 7
hari.
3.2. Teori Dasar
Korosi galvanik adalah korosi yang ditingkatkan antara dua atau lebih banyak
logam berbeda yang terhubung secara elektrik pada awalnya, di mana yang lebih aktif
bertindak sebagai anoda dan menimbulkan korosi, sedangkan yang kurang yang aktif
adalah katoda. Ini akan meningkatkan korosi laju logam anodik dan mengurangi
paduan katodik. Logam aktif te adalah logam dengan potensial lebih negative dalam
rangkaian gaya gerak listrik logam, sedangkan yang mulia logam adalah logam
dengan potensi negatif yang lebih kecil. Terbesarnya perbedaan potensial antara yang
berbeda logam tidak dapat digunakan untuk memprediksi tingkat keparahan galvanic
korosi, karena potensial elektrokimia adalah fungsi termodinamika dan bukan
kinetika reaksi yang mungkin terjadi. Ini adalah kinetika permukaan yang
menentukan tingkat keparahan korosi galvanic. Korosi galvanic merupaka jenis
korosi yang terjadi Ketika dua buah logam mulia tau tidak mulia saling kontak dalam
Laporan Akhir Praktikum Korosi T.A 2021/2022
suatu larutan elektrolit (Standard ASTM G15). Larutn elektrolit dapat berupa larutan
garam, asam atau basa.
Proses ini melibatkan reaksi reduksi dan oksidasi (redoks). Kedua logam yang
berada dalam larutan elektrolit akan membentuk sebauh sel galvanic. Logam yang
memiliki nilai potensial elektroda yang lebih rendah, yaitu logam dengan posisi lebih
tinggi dalam daftar seri elektrokimi akan mengalami reaksi anodic atau oksidasi,
sedangkan logam yang memiliki nilai potensial elektroda lebih tinggi atau lebih mulia
akan mengalami reaksi katodik atau reduksi pada permukaannya. Perbedaan potensial
elektroda antara kedua logam yang membentuk sel galvanic tersebut merupakan
penentu daya dorong untung terjadinya korosi. Dimana keduanya mempunyai
perbedaan potensial korosi yaitu baja karbon paduan rendah akan bersifat lebih aktif
dibanding paduan seng yang pasif.
Penentuan Laju Korosi dengan Metode Berat Hilang Metode yang digunakan
untuk menghitung laju korosi adalah metode berat hilang. Metode ini melibatkan
proses pembersihan dan penimbangan sebelum korosi dan pembersihan serta
penimbangan setelah korosi. Untuk menghitung laju korosi, digunakan rumus MPY,
mils per year (mili per tahun) (Callister, 1990) :
534 ×W
CR = ( 2.8 )
ρ ×A ×t
dimana W adalah berat yang hilang selama korosi (mg), ρ adalah massa jenis
bahan uji (g/cm3), A adalah luas penampang (inchi2) dan t adalah waktu uji korosi
(jam).
3.3. Metodologi Praktikum
3.3.1. Skema Proses
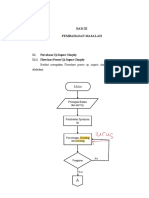
a) Pembuatan Larutan NaCl 3,5%
Siapkan alat dan bahan
Laporan Akhir Praktikum Korosi T.A 2021/2022
Timbang Garam
Masukan kedalam gelas kimia
Masukan aqua dm
Aduk larutan NaCl
Analisa pengamatan
Kesimpulan
Gambar 5.2 Pembuatan larutan NaCl 3,5%
b) Proses Pengujian Spesimen
Siapkan alat dan bahan
Bersihkan permukaan spesimen secara mekanik
Ukur, timbang dan foto dimensi spesimen
Siapkan larutan
Bersihkan spesimen uji secara kimiawi dan keringkan
Lilitkan kawat timah pada spesimen uji
Ukur pH larutan dan potensial spesimen uji mula-mula
Celupkan spesimen uji dalam larutan NaCl
Amati perubahan dan ukur pH serta potensial setiap 1 x 24 jam selama 7
hari
Angkat spesimen dari gelas kaca
Bersihkan dan keringkan spesimen uji
Laporan Akhir Praktikum Korosi T.A 2021/2022
Timbang dan ukur dimensi spesimen uji
Catat hasil pengamatan
Hitung laju korosi
Analisa dan pembahasan
Kesimpulan
Gambar 5.3 Proses pengujian spesimen
3.3.2. Penjelasan Skema Proses
3.3.3. Gambar Proses
3.4. Alat Dan Bahan
3.4.1. Alat
3.4.2. Bahan
3.5. Pengamatan Data
3.5.1 Pengumpulan Data
3.6. Pengolahan Data
3.7. Analisa Dan Pembahasan
3.8. Kesimpulan
Laporan Akhir Praktikum Korosi T.A 2021/2022
Anda mungkin juga menyukai
- m.1 Pengaruh LarutanDokumen6 halamanm.1 Pengaruh Larutanrizky saptahadiBelum ada peringkat
- m.3 SCCDokumen4 halamanm.3 SCCrizky saptahadiBelum ada peringkat
- KOROSI POTENSIODINAMIKDokumen18 halamanKOROSI POTENSIODINAMIKNurul IzzahBelum ada peringkat
- m.4 PotensiodinamikDokumen6 halamanm.4 Potensiodinamikrizky saptahadiBelum ada peringkat
- Modul 1 Pengaruh Berbagai Larutan Terhadap KorosiDokumen8 halamanModul 1 Pengaruh Berbagai Larutan Terhadap Korosidaffa ramadhanBelum ada peringkat
- Cover NuurangDokumen6 halamanCover Nuurangrizky saptahadiBelum ada peringkat
- Uji Korosi Paa BesiDokumen12 halamanUji Korosi Paa BesiAnonymous EXYGIzYpBelum ada peringkat
- Laporan KorosiDokumen56 halamanLaporan KorosiIndri DurikaBelum ada peringkat
- Bab 1Dokumen6 halamanBab 1Frans SiregarBelum ada peringkat
- Bab 5Dokumen15 halamanBab 5Frans SiregarBelum ada peringkat
- Albert Prayitno - Uji Impak - Hendrikus Avero Widarto - 2020-0451-0055Dokumen16 halamanAlbert Prayitno - Uji Impak - Hendrikus Avero Widarto - 2020-0451-0055Christian AlbertBelum ada peringkat
- GravimetriDokumen28 halamanGravimetriAgus Mangiring100% (1)
- Bab 3Dokumen22 halamanBab 3fakhru zakariaBelum ada peringkat
- Bab IvDokumen26 halamanBab IvRobymBelum ada peringkat
- Modul KINETIKA KIMIA 2022Dokumen38 halamanModul KINETIKA KIMIA 2022Dinda Ayu A.SBelum ada peringkat
- Bab 3 SCCDokumen14 halamanBab 3 SCCJamal NurdiansyahBelum ada peringkat
- Anastasia Rosari Yunita JujeDokumen94 halamanAnastasia Rosari Yunita JujeAnastasia RosariBelum ada peringkat
- Resume Analitik Penentuan Gravimetri NikelDokumen4 halamanResume Analitik Penentuan Gravimetri NikelcerryBelum ada peringkat
- PROPOSAL KERJA PRAKTEK - Niko Adi Alvredo NababanDokumen41 halamanPROPOSAL KERJA PRAKTEK - Niko Adi Alvredo NababanImajinasi berpikir kekuatan melangkahBelum ada peringkat
- Laporan Praktikum Kimia AnalisaDokumen21 halamanLaporan Praktikum Kimia AnalisazeniBelum ada peringkat
- Bab I PendahuluanDokumen6 halamanBab I PendahuluanFrans SiregarBelum ada peringkat
- Modul Analisis Mikro StrukturDokumen17 halamanModul Analisis Mikro StrukturBayu PrastioBelum ada peringkat
- Jurnal Kimia Analitik Gravimetri Bintang MeyriskaDokumen16 halamanJurnal Kimia Analitik Gravimetri Bintang MeyriskaBintang MeyriskaBelum ada peringkat
- K1a021065 - M. Dwi Jefry Ardiansyah - Laporan Praktikum Percobaan 4Dokumen17 halamanK1a021065 - M. Dwi Jefry Ardiansyah - Laporan Praktikum Percobaan 428M. Dwi Jefry ArdiansyahBelum ada peringkat
- Bab 3Dokumen19 halamanBab 3Frans SiregarBelum ada peringkat
- BAB III Dan IV Skripsi RisnaDokumen10 halamanBAB III Dan IV Skripsi RisnaDiego FerdinandBelum ada peringkat
- Buku Petunjuk Praktikum Ilmu Bahan Dan KorosiDokumen35 halamanBuku Petunjuk Praktikum Ilmu Bahan Dan KorosisyalaBelum ada peringkat
- Kimnal Acara 3 IwanDokumen16 halamanKimnal Acara 3 IwanGmliel JhoniBelum ada peringkat
- REV - (TD) - 28 - PT - Aditya Rahman - 3334190060Dokumen39 halamanREV - (TD) - 28 - PT - Aditya Rahman - 3334190060ADITYA RAHMANBelum ada peringkat
- Laporan Kimia Analisa ZulfaDokumen14 halamanLaporan Kimia Analisa Zulfayudha puspaBelum ada peringkat
- PROPOSAL ALAT UKUR RESISTIVITASDokumen8 halamanPROPOSAL ALAT UKUR RESISTIVITASRifky Zulfiar SaniBelum ada peringkat
- GravimetriDokumen20 halamanGravimetriFitri WulandariBelum ada peringkat
- SilabusDokumen4 halamanSilabussuarni panaiBelum ada peringkat
- Gravimetri ChristianDokumen17 halamanGravimetri ChristianLeni MarlinaBelum ada peringkat
- Bab3 002 RevDokumen21 halamanBab3 002 RevM Septian LubayBelum ada peringkat
- Trisna Handika - 21421488 - 2ic01 - LA Final - RemovedDokumen23 halamanTrisna Handika - 21421488 - 2ic01 - LA Final - RemovedZulfikar AFSBelum ada peringkat
- ANALISA GRAVIMETRIDokumen19 halamanANALISA GRAVIMETRIReihan FaizaldiBelum ada peringkat
- ANALISIS GRAVIMETRI TAWASDokumen12 halamanANALISIS GRAVIMETRI TAWASAchmad Afandi OktaviantoBelum ada peringkat
- SNI 06 6989 1 33 2005 Ag SSADokumen10 halamanSNI 06 6989 1 33 2005 Ag SSAadhyBelum ada peringkat
- 04.SNI 6989.4 - 2009-Fe AASDokumen10 halaman04.SNI 6989.4 - 2009-Fe AASDy ChemsBelum ada peringkat
- Seminar Penelitian - Kennard &yunitaDokumen38 halamanSeminar Penelitian - Kennard &yunitaYunita SarahBelum ada peringkat
- Kimia Unsur Gol UtamaDokumen11 halamanKimia Unsur Gol UtamaWindy Ning TiasBelum ada peringkat
- Cindy Saskia Damayanti - 19031010029 PDFDokumen122 halamanCindy Saskia Damayanti - 19031010029 PDFCindy SaskiaBelum ada peringkat
- Pendahuluan KA 1Dokumen23 halamanPendahuluan KA 1Muhammad FajrinBelum ada peringkat
- Modul Praktikum KimDas Lanjutan 2022-2023 PDFDokumen40 halamanModul Praktikum KimDas Lanjutan 2022-2023 PDFMustaqimBelum ada peringkat
- Laporan Praktikum Teknik Pengujian LogamDokumen111 halamanLaporan Praktikum Teknik Pengujian LogamYosua Banjarnahor50% (2)
- Praktikum Material Teknik-Impact-Kelompok 5Dokumen28 halamanPraktikum Material Teknik-Impact-Kelompok 5KRISTOFER SEVERIANO DINATABelum ada peringkat
- LAPORAN Kinetika Kimia (Raja Bima Pane) 2002122Dokumen15 halamanLAPORAN Kinetika Kimia (Raja Bima Pane) 2002122Marta LenaBelum ada peringkat
- METODOLOGI PENELITIANDokumen11 halamanMETODOLOGI PENELITIANhening purnamawatiBelum ada peringkat
- Laporan Impak BagasDokumen19 halamanLaporan Impak BagasNicholas DarielBelum ada peringkat
- Revisi - Modul Praktikum Kimia Anorganik IIDokumen38 halamanRevisi - Modul Praktikum Kimia Anorganik IIMutiara hasyimBelum ada peringkat
- Gravimetri BaSO4Dokumen16 halamanGravimetri BaSO4Naurah NazhifahBelum ada peringkat
- PenuntunPrak Kimia 2020Dokumen52 halamanPenuntunPrak Kimia 2020adindaBelum ada peringkat
- GALVANIC CORROSIONDokumen12 halamanGALVANIC CORROSIONNOBPDYBelum ada peringkat
- Bab IiiDokumen12 halamanBab IiiAndika DhimasBelum ada peringkat
- Spektrofotometri Serapan AtomDokumen21 halamanSpektrofotometri Serapan AtomM.Ganta KhaitamiBelum ada peringkat
- Jiptummpp GDL Ilhamansha 49855 4 BabiiiDokumen7 halamanJiptummpp GDL Ilhamansha 49855 4 BabiiiafifahBelum ada peringkat
- ElektrodaDokumen13 halamanElektrodaAllan PermanaBelum ada peringkat
- Bab III Sifat Mampu KerasDokumen16 halamanBab III Sifat Mampu Kerasrizky saptahadiBelum ada peringkat
- Cover DikaDokumen2 halamanCover Dikarizky saptahadiBelum ada peringkat
- Cover NuurangDokumen6 halamanCover Nuurangrizky saptahadiBelum ada peringkat
- Bab II Perlakuan PanasDokumen18 halamanBab II Perlakuan Panasrizky saptahadiBelum ada peringkat
- Laporan Sementara Modul 3Dokumen2 halamanLaporan Sementara Modul 3rizky saptahadiBelum ada peringkat
- Kata Pengantan & SebagainyaDokumen8 halamanKata Pengantan & Sebagainyarizky saptahadiBelum ada peringkat
- Bab Iv Uji ImpakDokumen8 halamanBab Iv Uji Impakrizky saptahadiBelum ada peringkat
- Laporan Praktikum KorosiDokumen24 halamanLaporan Praktikum KorosiWilliam DoloksaribuBelum ada peringkat
- Bab Vi Uji MulurDokumen5 halamanBab Vi Uji Mulurrizky saptahadiBelum ada peringkat
- Saluran Tuang 2DDokumen1 halamanSaluran Tuang 2Drizky saptahadiBelum ada peringkat
- BAB II Pengujian TarikDokumen8 halamanBAB II Pengujian Tarikrizky saptahadiBelum ada peringkat
- Speedometer 2 DDokumen1 halamanSpeedometer 2 Drizky saptahadiBelum ada peringkat
- Bab Vii Dye PenetrantDokumen5 halamanBab Vii Dye Penetrantrizky saptahadiBelum ada peringkat
- Isometri Gating SystemDokumen1 halamanIsometri Gating Systemrizky saptahadiBelum ada peringkat
- Isometri Gating SystemDokumen1 halamanIsometri Gating Systemrizky saptahadiBelum ada peringkat
- Bab 4 Anodisasi AlDokumen18 halamanBab 4 Anodisasi Alrizky saptahadiBelum ada peringkat
- Speedometer 2 DDokumen1 halamanSpeedometer 2 Drizky saptahadiBelum ada peringkat
- Bab 4 Anodisasi AlDokumen18 halamanBab 4 Anodisasi Alrizky saptahadiBelum ada peringkat
- Elektroplating BajaDokumen16 halamanElektroplating Bajarizky saptahadiBelum ada peringkat
- Bab Ii Perlakuan PanasDokumen20 halamanBab Ii Perlakuan Panasrizky saptahadiBelum ada peringkat
- UJI KEKERASAN LOGAMDokumen15 halamanUJI KEKERASAN LOGAMrizky saptahadiBelum ada peringkat
- Bab Vii Dye PenetrantDokumen12 halamanBab Vii Dye Penetrantrizky saptahadiBelum ada peringkat
- UJI KEKERASAN LOGAMDokumen15 halamanUJI KEKERASAN LOGAMrizky saptahadiBelum ada peringkat
- Elektroplating BajaDokumen16 halamanElektroplating Bajarizky saptahadiBelum ada peringkat
- Bab 2 LarutanDokumen22 halamanBab 2 Larutanrizky saptahadiBelum ada peringkat
- Laporan Akhir Praktikum Teknik Pemesinan LogamDokumen43 halamanLaporan Akhir Praktikum Teknik Pemesinan Logamrizky saptahadiBelum ada peringkat